Hg2+��ľ�ϵ���ø���������ü��䶯��ѧ
�����ᣬ�����࣬�����ԣ���ƽ���Ŵ��ޣ���ѧӢ��������
(��̶��ѧ ����ѧԺ������ ��̶��411105)
ժҪ��ͨ����Hg2+������ľ�ϵ���øFT-IRͼ���е������������ȥ������������ϣ����ӫ���������������ж����ṹ��������������ø���Բ�����ı䶯��ѧ���ۣ��о�ø��Hg2+��ϵĶ���ѧ���ɣ�̽��Hg2+��ľ�ϵ���ø���Ե����û������о����������Hg2+��ľ�ϵ���ø��������Ƶ�˫�����ã�Hg2+��ľ�ϵ���ø���ñ��ֳ��ʹٸ��ֵ�Hormesis����ø����Ҫȡ�������������λ������������������ͦ�-ת�ǡ���-ת�Ǻ������٣���������������ӣ�������ø����ߣ���֮ø��͡���Ũ����(10-6 mol/L)Hg2+��ľ�ϵ���ø������Ϊ�Ǿ����Բ����漤�ø������Ũ����(10-4 mol/L) Hg2+��ø�����������Ծ���������Ϊ����ø��͡�
�ؼ��ʣ�ľ�ϵ���ø��Hg2+������ѧ��ø������ṹ������������
��ͼ����ţ�TQ028.8 ���ױ�־�룺A ���±�ţ�1672-7207(2013)10-3991-07
Modification effect of Hg2+ on papain and its kinetics
CAI Xiling, ZENG Hongyan, CAI Lianhui, HE Ping, ZHANG Cunying, LIU Xueying, WU Yalan
(School of Chemical Engineering, Xiangtan University, Xiangtan 411105, China)
Abstract: The secondary structures of the papain treated by Hg2+ were determined by FT-IR in amide-I region band using Fourier deconvolution and curve-fitting technique and fluorescence emission spectra. Based on Tsou��s theory on the kinetics of irreversible modification of enzymic activity, the kinetics of the reaction of Hg2+ with papain was studied in order to explore the mechanism of Hg2+ on papain. The results show that Hg2+ has active and inhibitory effect on papain, and the effect of Hg2+ on papain in the tyrosine hydrolytic reaction shows the Hormesis effect. The activity of papain depends crucially on the active site conformation, especially of ��-turn and random. The papain activity is increased when the amounts of ��-turn decrease or with random increase in papain, and vice versa. At low Hg2+ concentration of 10-6 mol/L, Hg2+ is efficacious activator, and effect is classified as noncompetitive type. Under high concentration of 10-4 mol/L, the inhibition of Hg2+ on the enzyme is found to be largely of competitive type.
Key words: papain; Hg2+; kinetics; enzymic activity; secondary structure; irreversible modification
ø��Ϊһ������������ѹ㷺��Ӧ���ڹ�ҵ�����ĸ�������ľ�ϵ���ø��һ����õĹ�ҵ����ø����ʳƷ��ҽҩ����֯�������й㷺Ӧ��[1]���о������ؽ���ͨ����øϵͳ���Ƽ���ʹø��������ʹ���ܵ����������[2]����ǰ�о��ؽ�����ø����������Ҫ�������ؽ�����ø���Լ���ṹ�Ĺ�ϵ��[3]�����ؽ���������ø���Է����仯�Ĺ��̺ͻ������Լ�ø����ѧ�����о����١���Ҫ�ڷ���ˮƽ���˽��ؽ���������ø�Ĵ����ԣ�̽���䱾�ʣ�����õ�����ѧ�о���֧�ţ��ؽ���������ø����ѧ�����ɷ�ӳ�ؽ�����ø�Լ������Ľ��̶ܳȺ����ù��̣�����ø��Ӧ��������һ����ʾø���ؽ������������ϵ���������߿�����Hg2+��ľ�ϵ���ø�����ã��о�Hg2+��ľ�ϵ���ø�����Ӱ�죬�ӷ���ˮƽ���о�����ľ�ϵ���ø֮������û������о�Hg2+������ľ�ϵ���ø����ѧ��������ṹ����������û�������ʾľ�ϵ���ø�۽ṹ������ܵĹ�Ч��ϵ��Ϊ����ľ�ϵ���ø�Ĺ�ҵӦ���ṩ���ۻ�����
1 �����뷽��
1.1 ʵ�����������
ľ�ϵ���ø[EC 3.4.22.2] (����Sigma��˾���������ȡ�99%)�����װ��ᣬ�ҵ��� (�Ϻ���������Ƽ�����˾����)�����û�ѧ�Լ���Ϊ��������UV-2001������ֹ��ȼ�(�ձ�����˾����)��Thermo��˾Nicolet 380 FT-IR (�ֱ��� 4 cm-1��ɨ��100��)��PE��˾LS55��ӫ�������(��������288 nm��ɨ���ٶ�Ϊ500 nm/min��ɨ�跶ΧΪ310~400 nm)����1.0 mLľ�ϵ���øҺ�ֱ���1.0 mL��ͬŨ�ȵ�HgCl2��Һ(0��10�C4��10�C6 mol/L)��ϣ�����8.0 mL��PBS������Һ��45 �汣��1 h������ӫ����ײⶨ��
1.2 ʵ�鷽��
(1) ��ȷ��ȡHgCl2�������Ỻ��Һ(PBS��Ũ��0.1 mol/L��pH 7.0)���һ��Ũ�ȵ�HgCl2��Һ����ȷ��ȡľ�ϵ���ø����PBSҺ������Ũ��Ϊ1.0 mg/mL��øҺ����ȡ2.0 g�ҵ����ܽ���60 mL��PBSҺ�У�������У���ȴ��PBSҺ�������2.0 g/mL���ҵ�����Һ����HgCl2��Һ��øҺ���ҵ�����Һ��1:1:3����Ȼ�Ϸ�Ӧ������Hg2+��ľ�ϵ���ø���Ե�Ӱ�졣
(2) ø�����ⶨ�μ�����[4]��ȡ1.0 mg/mL��øҺ1 mL��1 mL��ͬŨ��Hg2+��ϣ�40 ���±���10 min���ټ���3 mLԤ��10 min���ҵ�����Һ��45 �淴Ӧ30 min������10%�������� (TCA) ��Һ3.0 mL��ֹ��Ӧ����45 �����30 min�����˺�ȡ����Һ���ⶨUV����ԭø(��ø)øҺΪ���ա�ľ�ϵ���ø��1��ø������λ(U)���壺45 �棬pH 7.0�����£���λʱ����ˮ���ҵ��ײ���l ��g�Ұ����ø�������ø����δ��Hg2+������øø��Ϊ100%�ơ�
2 ���������
2.1 Hg2+Ũ�ȶ�ø���Ӱ��
���첻ͬŨ��Hg2+��ľ�ϵ���ø��ø��Ӱ�죬�����ͼ1����ͼ1��֪����Hg2+Ũ�ȵ���10-7 mol/Lʱ��Hg2+��ø����������Ӱ�졣10-6~10-7 mol/L Hg2+��ø�м������ã�10-6 mol/L Hg2+��ʹ�����ø��ﵽ��ߣ�Ϊ111.03%����Hg2+Ũ�ȸ���10-5mol/Lʱ��Hg2+��ø���������������ã���Hg2+��Ũ�ȴ���10-4 mol/Lʱ��ø���������ôﵽ��ǿ�����ø���6%���ҡ������������֪��10-6 mol/L Hg2+��ø�����������ã�10-4 mol/L Hg2+��ø��ǿ������ЧӦ��Hg2+��ľ�ϵ���ø���ñ��ֳ�����HormesisЧӦ�ĵʹ٣���������[5]��
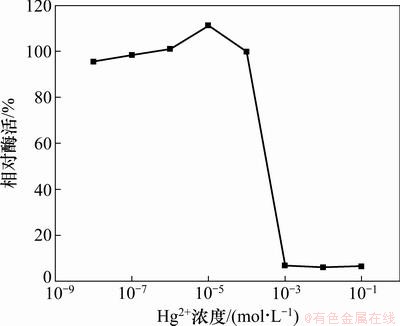
ͼ1 Hg2+��ľ�ϵ���ø��Ӱ��
Fig. 1 Effect of Hg2+ on papain activity
2.2 Hg2+������ľ�ϵ���ø�������
ø���ӻ�����ø���ӵĹ��������ء�Ϊ�˽�һ���о�Hg2+��ľ�ϵ���ø�����ƺͼ�����������IJ���10-4��10-6 mol/L��Hg2+��ľ�ϵ���ø���д������Դ�øΪ���գ�����Ʒ����FT-IR��ӫ����ױ���������̽��Hg2+��ľ�ϵ���ø�����Ӱ�졣
2.2.1 FT-IR����
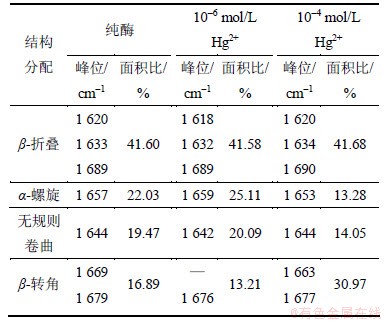
�����ʺ�����������������Ҫ���ɵ����ʹǼ��е��ʻ�������, �ܹ������ط�ӳ�����ʵĹ�����仯������I��(1 700~1 600 cm�C1)�Ե����ʶ����ṹ(��-��������-�۵����������ת�ǽṹ)�ı仯��Ϊ����[6]����������I������Hg2+������ľ�ϵ���ø�����ṹ���졣Ϊ�˸��õط��������͵õ���ϸ�Ķ����ṹ��Ϣ�����ö�������ȥ�������������(��˹���)��������Ʒ�������FT-IRͼ���д���[7]���������1��
�ɱ�1��֪����ø��10�C6 mol/L Hg2+������ø��10�C4 mol/L Hg2+������ø��-�۵�����̫����죬˵����-�۵��ṹ���ȶ���Hg2+������������ṹ��δ����̫��Ӱ�졣����ڴ�ø(41.60%)��10�C6 mol/L Hg2+������ø��-��������������13.98%��˵��ø�ķǼ��Բл����ࣻ��10�C4 mol/L Hg2+������ø��-��������������39.72%��˵��ø�ķǼ��Բл����١�����ڴ�ø(22.03%)��10�C6 mol/L Hg2+������ø��-ת�Ǻ���������21.85%����10�C4 mol/L Hg2+������ø��-ת�Ǻ���������83.34%��10�C6 mol/L Hg2+������ø�����������������3.18%����10�C4 mol/L Hg2+������ø�����������������27.84%��
��1 ľ�ϵ���ø����I�����ӷ�λ�á�����������ṹ����
Table 1 Curve fitting analyses expressed as component bands, areas and assignments in amide I infrared bands of the secondary structures from papain
�ڵ����ʵĶ����ṹ�У���-�����ͦ�-�۵��ṹ�߸߶��ȶ��ԣ��京�������ں������ṹ���ȶ��ԣ�Ϊ�����ʵ�����ṹ����-ת�Ǻ������Ϊ�����ʵ�����ṹ[8]��10�C6 mol/L Hg2+������ø��������ṹ�������(66.69%)����ø��֮(63.63%)��10�C4 mol/L Hg2+������ø�������(54.96%)��˵��10�C6 mol/L Hg2+������ø�ȶ������ӣ���10�C4 mol/L Hg2+������ø�ȶ��Խ��ͣ�����Щ�仯�����ڦ�-�����ṹ�ĸı����¡����⣬10�C6 mol/L Hg2+������ø�����ṹ�ĸ�������ռ�ĺ����봿ø����Ӧ���������IJ�����С��10�C6 mol/L Hg2+������ø�봿ø�IJ��졣���������������ø�Ļ��Բ�λ[9]����-ת����ø�Ļ����������[10]�����Ƕ�ø���������������Ҫ�����á�10�C6 mol/L Hg2+��ľ�ϵ���ø�д̼����ã���������������������ӣ���-ת�Ǽ��٣�ʹ��ø��������λ�ṹ���������ԡ����������Ӷ�ʹ���������ߡ���֮��Ȼ��10�C4 mol/L Hg2+��ľ�ϵ���ø���������á�10�C4 mol/L Hg2+��������ṹ��-ת�Ǻ����������Ӱ�������10�C6 mol/L Hg2+�ģ�����Ϊ10�C4 mol/L Hg2+������ЧӦ������10�C6 mol/L Hg2+�ļ���ЧӦ���ڵ�Ũ����Hg2+��ø�ɲ������Ȳ���ЧӦ��������ЧӦ����Ũ����Ϊ����ЧӦ��Hormesis����[11]��������������-�����ṹ��ľ�ϵ���ø���ȶ�����أ��京��Խ�ߣ��ṹԽ�ȶ���ľ�ϵ���ø�Ħ�-ת�Ǻ����������ø�Ļ���������أ���ø�Ļ�������λ�������ɦ�-ת�Ǻ����������������-ת�Ǻ������٣���������������ӣ�������ø����ߣ���֮ø��͡�
2.2.2 ľ�ϵ���øӫ�������
ӫ��������о���������������������õļ�Ϊ��Ч�ķ���֮һ�������ṩ���������ʵĹ���仯��Ϣ[12]��ͼ2��ʾΪľ�ϵ���øӫ����ס���ͼ2��֪��10�C6��10�C4 mol/L Hg2+������øӫ�ⷢ����Ϊ���壬���λ�����ͬ�������ӫ��ǿ��(Imax)�ͷ�λ(��max)���졣�봿ø��ȣ�10�C6 mol/L Hg2+����ø��max����2 nm��������������ø�����Ц�-������������(��1)��ø����������Ͷ�����ȶ���ǿ[13]��Imax������������Hg2+ʹø�����е�ɫ���ᡢ�Ұ���л����ڸ���ļ�������ø�����������ǿ��ø������ǿ����10�C4 mol/L Hg2+������ø��max����14 nm��������ø�����Ц�-������������(��1)��ø�����ṹ�ȶ��Խ��ͣ�����ӫ�������Imax��������Ϊ��ø��35.05%����������Ϊɫ���ᡢ�Ұ���л����ڷǼ�������ø���������������ø���Խ��͡���ͼ2��֪��10�C4 mol/L��Hg2+ʹø��max��λ�̶����Դ���10�C6 mol/L��Hg2+��˵�����ߵ��������ô�����ǰ�ߵ��������á���Щ�ṹ����FT-IR�������һ��(��1)��
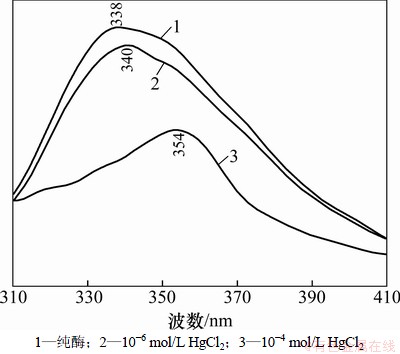
ͼ2 ľ�ϵ���øӫ�����
Fig. 2 Fluorescence emission spectra of papain
2.3 Hg2+������ľ�ϵ���ø�ķ�Ӧ����ѧ�о�
2.3.1 ľ�ϵ���ø���Բ����涯��ѧ
Hg2+��ľ�ϵ���ø���ֳ��ʹٸ��ֵ�Hormesis����Hg2+������ø���Բ�λʹø�Ĺ������ı䣬Hg2+��ø�Ľ��Ϊ�����淴Ӧ���������·�Ӧ���ƣ�
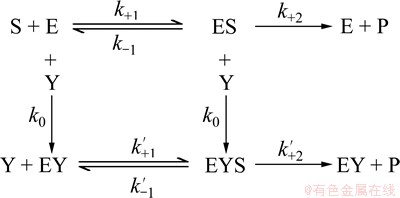
ʽ�У�E��S��Y��P��EY��ES��EYS�ֱ��ʾø�����Hg2+�����P����Ӧ������k0��k0��ֱ�ΪHg2+����������ø��ʧ�����ʳ����ͽ��øES��ʧ�����ʳ��������ݵ�����ø��Ӧ������ø���Բ����涯��ѧ����[14]�������Ũ��[S]����ʱ��ı䣬ø��Hg2+��Ϻ��Դ��ڲ���ø���ʱk+2��k+2�䲻Ϊ0����tʱ�̵IJ���Ũ�ȱ�ʾΪ��
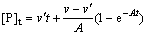 (1)
(1)
����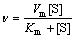 ��
��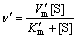 ��
��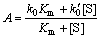 ��
��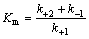 ��
��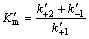 ��
��
ʽ�У�A��ʾø��Hg2+��ϵı����ٶȳ�����v��v��ֱ����ø��Hg2+���ǰ��ķ�Ӧ�ٶȣ�v��v��ʱ���÷�ӦΪ���ƹ��̣�v��v��ʱ��Ϊ������̣�Km��Km��Ϊ���ϳ�����Vm��Vm��Ϊ���Ӧ�ٶȡ���t���ޣ�����Ӧ�ﵽƽ��ʱ���ղ���Ũ�Ȳ�����ʱ��t�仯���仯���ﵽ���ֵ����Ϊ[Pe][15]����
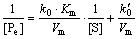 (2)
(2)
2.3.2 ���ϳ����IJⶨ
���¶�45 �棬pH 7.0��øŨ��Ϊ1.0 mg/mL�������£��ֱ���0��10�C4��10�C6 mol/L��Hg2+����ľ�ϵ���ø���ⶨ��ͬ�ҵ�������Ũ��(0.2��0.4��0.6��0.8��1.0��1.6��2.0 mg/mL)��ľ�ϵ���ø��ø�ٳ��ٶȡ�ľ�ϵ���ø����Ӧ��ѭ�����Ϸ��̣���Lineweaver -Burk˫����ͼ������ͼ�������ͼ3��ʾ���봿ø��ȣ�10�C6 mol/L Hg2+������øKm��С��Ϊ��ø��0.39������������Vm������9.2%��10�C4 mol/L Hg2+������øKm�������ӣ�Ϊ��ø��1.05��������������Vm������32.44%����Vm�ı仯�̶ȿ���10�C4 mol/L Hg2+������øVm�����½�(32.44%)����10�C6 mol/L Hg2+�Ľ���������(9.2%)��˵��10�C6 mol/L Hg2+������ø�ļ���ЧӦԶԶ����10�C4 mol/L Hg2+������ЧӦ����Km�ı仯������10�C6 mol/L Hg2+������øKm�����½�(0.39��)����10�C4 mol/L Hg2+��ֻ��Km��������(1.05��)����Ȼ10�C6 mol/L Hg2+��Km�ı仯���ȱ�10�C4 mol/L Hg2+�Ĵ�ǰ�߶�ø���Ե�Ӱ�������Ⱥ��ߵ͡��ۺ�����Hg2+��ø��Ӱ��(ͼ1)��������ø�Ч��ϵ�о�����(��1��ͼ2)���ɵó���ø����������ø����Ӱ�죬��ø��ĸı���Ҫȡ�������������λ����ı仯����������������ͦ�-ת�ǵı仯��
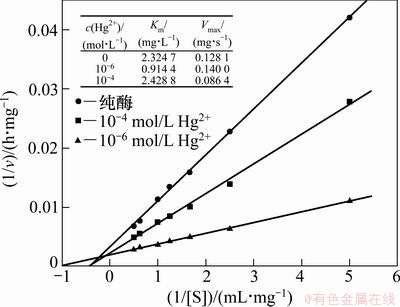
ͼ3 ľ�ϵ���ø�Ķ���ѧ����
Fig. 3 Kinetic parameters of papain
2.3.3 Hg2+��ľ�ϵ���ø����ѧ������Ӱ��
ͼ4��ʾΪ��ͬ�ҵ�������Ũ���£���ø�Լ�10�C4��10�C6 mol/L Hg2+������ø�������ˮ�ⷴӦ����ͼ4��֪�����ŷ�Ӧʱ����ӳ�������Ũ������һ����ֵ��ľ�ϵ���øøˮ���ѧ������³���ڵ�����ø������ı�Ķ���ѧ����[14]����ʽ(1)����øˮ�ⷴӦ�в���Ũ������ʱ������ӳʽ������Ա仯��10�C6 mol/L Hg2+������øˮ�ⷴӦ�ʼ���ø�ٷ�Ӧģʽ(ͼ4(b))����10�C4 mol/L Hg2+������ľ�ϵ���øˮ�ⷴӦ������ø�ٷ�Ӧģʽ(ͼ4(c))��ľ�ϵ���ø��ˮ���ѧ����ʽ(1)����ʵ�����ݽ��з�������С���˷���Exponential Linear������ϣ�ģ��������2��
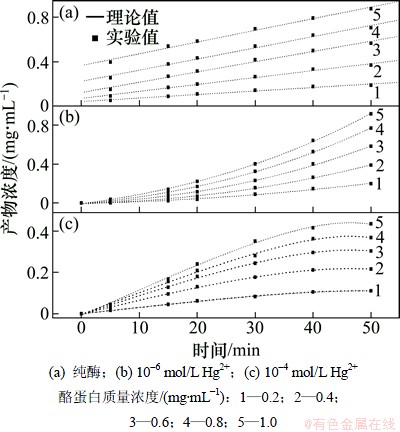
ͼ4 ����Ũ����ʱ��Ĺ�ϵ
Fig. 4 Relationship between product concentration and time
�Ӷ���ѧ����(��2)��֪��ʽ(1)�IJ�����ı䶯��ѧģ�͵�����������������������������Ժ�(R��0.99)����ģ�Ϳ��Ժܺõؽ���Hg2+��ø��ϵĶ���ѧ���ɡ���ʽ(2)����1/[Pe]��1/[S]��ͼ(ͼ5)����10�C6 mol/L Hg2+����ø�����ٶȳ���(R=0.999 9)k0=0.150 9��k0��=0.015 0��k0���k0����k0��k0���10����10�C4 mol/L Hg2+����ø���ٶȳ���(R= 0.999 4)k0=0.063 4��k0��=0.034 4����k0���0����k0��k0���1������������ģ��(��2)������ͬ����Ũ����Hg2+Ũ��Խ�ߣ�ø�ı��۷�Ӧ�ٶȦͺͦ͡�Խ��˵��Hg2+��ЧӦ����Ũ�ȵ���߶��������μ���ø�ľ����ԡ��Ǿ������Լ��������ԵĹ�ϵ���Ը��ݵ���Ա����ٶȳ���A��Ӱ�����[16]���ɱ�2��֪��10�C6 mol/L Hg2+������ø���ͣ��͡䣬˵��10�C6 mol/L Hg2+��ľ�ϵ���ø��������ЧӦ��A��[S]�أ���1/A��Km/(Km+[S])�����Թ�ϵ������10�C6 mol/L Hg2+��ľ�ϵ���ø���ڷǾ����Բ����漤���ϵ�����Ũ����k0���k0��k0��k0���10��������Hg2+(Y)��øE�������EY����ԶԶ����Hg2+��ES�������EYS�ġ���Щ���˵������Ũ����10�C6 mol/L Hg2+��ľ�ϵ���øΪ�Ǿ����Բ����漤�����ã�Y��E��ϲ�Ӱ��E�����S��ϣ���Hg2+��ø�Ļ�������λ����ı�����ŵļ���λ���ϣ���ʹø��������λ�ṹ����������S��ϣ�ø�Ļ������ӡ�����Hg2+Ϊ��רһ�����μ�������Hg2+��ø�Ļ�������λ���������λ���ϣ��̶���ES����γ�EYS���ܽ�һ���ͷų�����ʱ��ֳ�k0���k0����Hg2+�������ŵļ���λ����ԶԶ��������λ��(k0��10k0��)���Ӷ����ֳ�����ЧӦ��10�C4 Hg2+������ø�ͣ��͡䣬˵��10�C4 mol/L Hg2+��ľ�ϵ���øΪ����ЧӦ��A��[S]�����Ӷ�����1/A��Km/(Km+[S])�������Թ�ϵ(R=0.993 8)������10�C4 mol/L Hg2+��ľ�ϵ���ø�����Բ��������Ƽ�����Ũ����k0���0����k0��2k0�䣬����Hg2+(Y)��øE�������EY�����ʴ���Hg2+��ES�������EYS����Щ���˵������Ũ����10�C4 mol/L Hg2+��ľ�ϵ���ø�����Բ��������Ƽ���Y��E�������EY������Hg2+��ø�Ļ�������λ��ϣ���S����ø�Ļ������ģ��Ӷ��谭E��S�Ľ�ϡ�ͬʱ����Hg2+��ø�Ļ�������λ����ı������λ���ϣ��̶���ES����γ�EYS�����ܽ�һ���ͷų�����ʱ��ֳ�k0���0�����ԣ�10�C4 mol/L Hg2+��ľ�ϵ���ø���Ծ����Բ���������Ϊ���Ļ�������ơ�
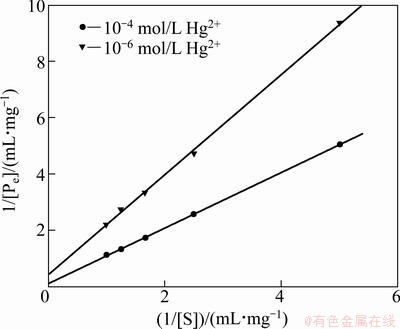
ͼ5 1/[Pe]��1/[S]��ϵͼ
Fig. 5 1/[Pe] versus 1/[S]
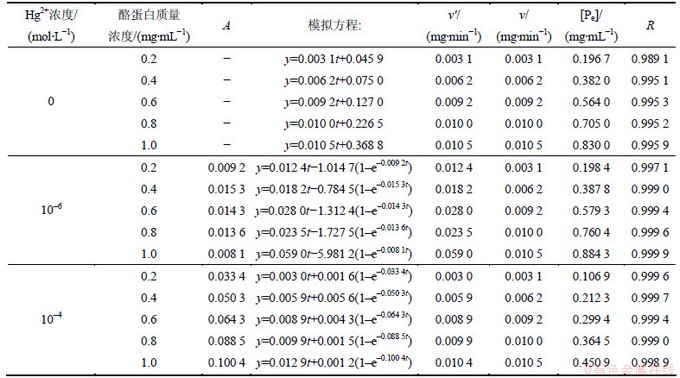
��2 ľ�ϵ���ø�Ķ���ѧ����
Table 2 Kinetics equations of papain
3 ����
(1) ��Ũ��(10-6 mol/L)��Hg2+��ø�м������ã���Ũ��(10-4 mol/L)��Hg2+��ø������ЧӦ��Hg2+��ľ�ϵ���ø���ñ��ֳ��ʹٸ��ֵ�Hormesis����ľ�ϵ���ø�Ħ�-ת�Ǻ����������ø�Ļ���������أ���ø�Ļ�������λ�������ɦ�-ת�Ǻ����������������-ת�Ǻ������٣���������������ӣ�������ø����ߣ���֮ø��͡�
(2) ͨ���о�Hg2+������ľ�ϵ���øˮ���ҵ��IJ����淴Ӧ����ѧ��̽��Hg2+��ľ�ϵ���ø��϶���ѧ���ɡ�����ø���Բ�����ı䶯��ѧģ�͵�������������뱾�����������Ǻϣ���ģ�Ϳ�ȷ����Hg2+��ø��ϵĶ���ѧ���ɡ���Ũ���£�10�C6 mol/L Hg2+��ľ�ϵ���ø�ķǾ����Բ����漤�������Hg2+��ø�Ļ�������λ����ı�����ŵļ���λ���ϣ���ʹø��������λ�ṹ��������������ϣ�ø�Ļ������ӡ���Ũ���£�10�C4 mol/L Hg2+��ľ�ϵ���ø�����Բ��������Ƽ�������Hg2+��ø�Ļ�������λ��ϣ�����ᄎ��ø�Ļ������ģ��Ӷ��谭ø�����Ľ�ϡ�����Hg2+��ø�Ļ�������λ����ı������λ���ϣ��̶���ES����γ�EYS�����ܽ�һ���ͷų��������10�C4 mol/L Hg2+��ľ�ϵ���ø���Ծ����Բ���������Ϊ���Ļ�������ơ�����ͨ���о�Hg2+������ľ�ϵ���øˮ���ҵ��IJ����淴Ӧ����ѧ���ӷ���ˮƽ�ϲ���Hg2+��ľ�ϵ���ø֮������û�������ʾľ�ϵ���ø�۽ṹ������ܵĹ�Ч��ϵ����������Ϊľ�ϵ���ø�Ĺ�ҵʵ��Ӧ���ṩ���ݡ�
�ο����ף�
[1] �ط�, ����, ������, ��. �̶���ľ�ϵ���ø���Ʊ��������о�[J]. �߷���ѧ��. 2000(5): 637-640.
HE Feng, ZHUO Renxi, LIU Lijian, et al. Studies on the preparation and characterization of immobilized papain[J]. Acta Polymerica Sinica, 2000(5): 637-640.
[2] Zhao Y, Wang X, Qin Y, et al. Mercury(Hg2+) effect on enzyme activities and hepatopancreas histostructures of juvenile Chinese mitten crab Eriocheir sinensis[J]. Chinese Journal of Oceanology and Limnology, 2010, 28(3): 427-434.
[3] �鷨ˮ, ��ѩ��, �⿵, ��. �ؽ������Ӷ����Ȧ�-����ø����Ӱ������û����о�[J]. �ߵ�ѧУ��ѧѧ��, 2001, 22(12): 1979-1983.
HONG Fashui, WANG Xuefeng, WU Kang, et al. Mechanism of heavy metal ions on ��-amylase activity from porcine pancreas[J]. Chemistry Journal Chinese Universities, 2001, 22(12): 1979-1983.
[4] ��ƽ, ����, ��־ս, ��. �����ľ�ϵ���ø�����빹���Ӱ��[J]. �Ϻ���ͨ��ѧѧ��, 2006, 24(3): 245-249.
HE Ping, HUANG Zhuolie, CHU Zhizhan, et al. Effect of a cetonitrile on activity and conformation of papain[J]. Journal of Shanghai Jiaotong University, 2006, 24(3): 245-249.
[5] ¬��ΰ, ��ΰ��, �Դ���. ���С������м���ø���Ե�Ӱ��[J]. ��ѧ�о�, 2002, 13(2): 1-4.
LU Zhenwei, LI Weiguo, ZHAO Dajqing. Effect of La3+ on the activity of several enzymes in mice liver[J]. Chemical Research, 2002, 13(2): 1-4.
[6] Zhao X , Chen F, Xue W, et al. FTIR spectra studies on the secondary structures of 7S and 11S globulins from soybean proteins using AOT re��erse micellar extraction[J]. Food Hydrocolloids, 2008, 22(4): 568-575.
[7] Choi E S M, Ma C Y. Structural characterization of globulin from common buckwheat (Fagopyrum esculentum Moench) using circular dichroism and Raman spectroscopy[J]. Food Chem, 2007, 102(1): 150-160.
[8] ������, ��Ⱥ, ����, ��. ��������ͬ���������µ����ʶ����ṹ��Fourier�任��������о�[J]. ����ѧ�������, 2009, 29(1): 82-87.
WU Liming, ZHOU Qun, ZHOU Xiao, et al. FTIR assessment of the secondary structure of proteins in royal jelly under different storage conditions[J]. Spectroscopy and Spectral Analysis, 2009, 29(1): 82-87.
[9] ������, ��ʥ��, �쳤��. ���ﻯѧ[M]. ����: �ߵȽ���������, 1989: 212.
WANG Jingyan, ZHU Shenggeng, XU Changfa. Biological chemistry[M]. Beijing: Higher Education Press, 1989: 212.
[10] �����, ����Ӣ, ���ݳ�, ��. ��-ת������øͻ����Ĺ�������������ʷ���[J]. ���﹤��ѧ��, 1998, 14(1): 39-45.
LI Hongye, ZHANG Yuying, DONG Yicheng, et al. Construction, expression and characterization of calf chymosin ��-turn mutants[J]. Chinese Journal of Biotechnology, 1998, 14(1): 39-45.
[11] Calabrese E J. Over compensation stimulation: A mechanism for hormetic effects[J]. Critical Reviews in Toxicology, 2001, 31(4/5): 425-470.
[12] ������, ���ƻ�. ӫ������о�ţѪ�嵰������������ϵ�еı���[J].��������ѧ��. 2011, 30(9): 1039-1043.
LI Xiangrong, YAN Yunhui. Denaturation study of bovine serum albumin indunced by guanidine ghloride with fluorescence spectroscopy[J]. Journal of Instrumental Analysis, 2011, 30(9): 1039-1043.
[13] ����, ����Ȩ, ���ӱ. �ؽ����������˹��ϳɿ�ԭ��ӫ�����Է���[J]. ������ѧ�о�����, 2009, 37(7): 1009-1013.
GUO Ming, PANG Shuoquan, ZHANG Luying. Detection of artifical antigen for Cd(��) by fluorescence spectroscopy[J]. Chinese Journal of Analytical Chemistry, 2009, 37(7): 1009-1013.
[14] ��³, �Կ�Դ. ø���Բ�����ı䶯��ѧ�����о�[J]. ��Ȼ��ѧ��չ, 1991, 1(1): 26-39.
TSOU Chenlu, ZHAO Kangyuan. Theory on the kinetics of irreversible modification of enzymic activity[J]. Progress in Natural Science, 1991, 1(1): 26-39.
[15] ������, ����, ����Ӣ, ��. ø���Բ�����ı�ĵ��ﱣ������ѧ[J]. ���Ŵ�ѧѧ��: ��Ȼ��ѧ��, 1992, 31(1): 425-429.
HUANG Shouqin, YAN Qing, LIN Qingying, et al. Kinetic studies on the protection of enzyme activity by substrate during irreversible modification[J]. Journal of Xiamen University: Natural Science, 1992, 31(1): 425-429.
[16] ��³. ø���Բ�����ı�Ķ���ѧI[J]. ���ﻯѧ����������ѧ��, 1965, 5(4): 398-408.
TSOU Chenlu. Kinetic of irreversible modification of enzyme activity. I: The effect of substrate on the rate of binding between an enzyme and a modifier[J]. Acta Biochimica et Biophysica Sinica, 1965, 5(4): 398-408.
(�༭ ����ƽ)
�ո����ڣ�2012-12-05�������ڣ�2013-03-17
������Ŀ������ʡ�Ƽ����ƻ���Ŀ(2011SK3138); ����ʡ�о������д�����Ŀ(CX2011B265); ��̶��ѧ��ѧ��������Ŀ(2012��)
ͨ�����ߣ�������(1963-)��Ů�����������ˣ���ʿ�����ڣ���ʿ����ʦ���������ﻯ���о����绰��0731-58298175��E-mail��hyzeng@xtu.edu.cn