DOI: 10.11817/j.ysxb.1004.0609.2021-37760
������YL15�Ի�ͭ��Ͱ�ͭ���Эͬ��������绯ѧ�о�
���_Ƽ1, 2�����ü�1, 2����ΰ��1, 2
(1. ���ϴ�ѧ ��Դ�ӹ������﹤��ѧԺ����ɳ 410083��
2. ���ϴ�ѧ ����ұ��������ص�ʵ���ң���ɳ 410083)
ժ Ҫ�������о���10 �������AcidithiobacillusferrivoransYL15�Ի�ͭ��Ͱ�ͭ���Эͬ�������̣���ϲ�ͬ�ĵ绯ѧ�����ֶ�̽����绯ѧ�ܽ�ͱ���ۻ���Ϊ�������������ͬ������ϵ����������͵绯ѧ��Ϊ���ڼ�����졣Эͬ������Ľ�������ߣ��ﵽ��48.4%����ͭ���֮�����߶�Զ���ڻ�ͭ���16.4%����ͭ��ļ��뽵����������ԭ��λ��ά�ֵ�һ�����˵ķ�Χ(400~420 mV)���ӿ��˿�������������⣬ͨ���绯ѧ���ԣ�����Эͬ�������λ���͡��������ߺ��迹��С�ĵ绯ѧ����ӳ�˿����������ʵļ�����ߡ�
�ؼ��ʣ���ͭ��ͭ��Эͬ���������£��绯ѧ���ۻ�
���±�ţ�1004-0609(2021)-xx--���� ��ͼ����ţ�TF18���� ���ױ�־�룺A
���ĸ�ʽ�����_Ƽ, ���ü�, ��ΰ��. ������YL15�Ի�ͭ��Ͱ�ͭ���Эͬ��������绯ѧ�о�[J]. �й���ɫ����ѧ��, 2021, 31(x): xxxx-xxxx. DOI: 10.11817/j.ysxb.1004.0609.2021-37760
PENG Yu-ping, PENG Tang-jian, ZENG Wei-min. Electrochemical studies and synergistic bioleaching of chalcopyrite and bornite in presence of Acidithiobacillus ferrivorans YL15 at low temperature[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(x): xxxx-xxxx. DOI: 10.11817/j.ysxb.1004.0609.2021-37760
��ͭ����������Ϊ�ḻ��ͭ��Դ[1-2]��Ҳ�����Ѵ�����ͭ����Դ��Ŀǰ������ұ����Ծ��ú����ش�ͭ�����л��ս������ҶԻ����Ѻ�[3-4]�����ֳ������е���Խ�ԡ�Ȼ�������������ͭ�������ʪ��ұ������Ȼ������ս�ԡ����У�����������ϸ������ʱ�ۻ���[5-6]�����ɵ�����ϵ͵Ľ������ʡ�һЩ����ָ��[7-9]������ͨ������Һ��λ������һ����Խϵ͵�λ�������ͭ��Ľ����ʡ������кࣺܶ�������������������������������������ӻ�ѧ�Լ������Dz��ö��ֿ����Эͬ������
��ͭ����Ϊ������Эͬ���������л�����[8]�Ͱ�ͭ�����ְ�ͭ��ͻ�ͭ��һ���γɻ�Ͽ�[10-11]�����ǵ�ʵ�ʹ�ҵӦ�ã������ߵ�Эͬ������Ϊ���С���һЩ�о�[12]���������и��»����µİ�ͭ��ͻ�ͭ����ܽ���Ϊ�������ͭ����Խ��ͻ����ϵ��Һ�ĵ��Ƽ��ٺ����ܽ⡣���ǣ��ڵ�������£���ͭ������ܽ�Ͷۻ����о����١���ˣ������о�10 ���°�ͭ��ͻ�ͭ������Эͬ������Ӧ������������ĵ绯ѧ�ܽ�Ͷۻ����̡�
1 �����뷽��
1.1 ��������Ϳ���
ʵ���������������Acidithiobacillus ferrivoransYL15�������ϴ�ѧ����ұ���ص�ʵ���ң����й�����ͭ��ɽ���ˮ��[13]���������봿���õ���ϸ�������Ļ��������������Ϊ(NH4)2SO4 (3.0 g/L)��MgSO4.7H2O(0.5 g/L)��K2HPO4(0.5 g/L)��KCl(0.1 g/L)��Ca(NO3)2(0.01 g/L)��
ʵ�������ͭ��Ͱ�ͭ�Ƚϸߣ��ֱ�Ϊ96.0%��97.6%���������й�������ұͭ��ɽ�����������鵽ϸ�����پ�ĥ��ʽɸ��(��С��75 ��m)�����ڽ���ʵ��͵绯ѧʵ�顣������Ʒ��Ԫ����������Ϊ���1��ʾ����X������(XRD)����ͼ1��ʾ��
��1 ����Ļ�ѧ���
Table 1 Chemical compositions of mineral samples (%)
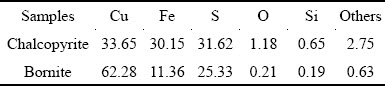
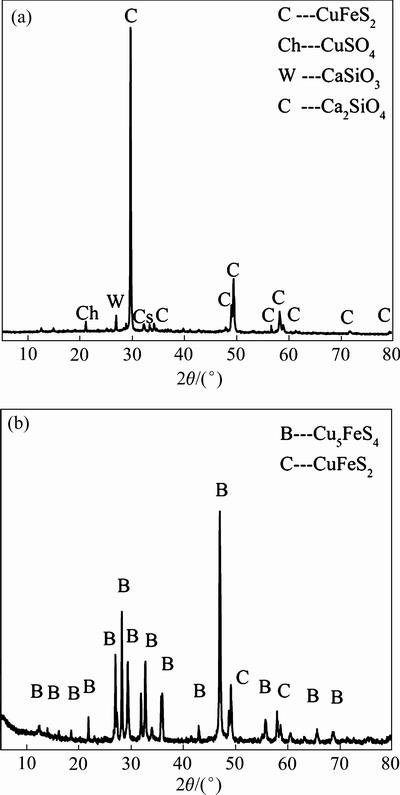
ͼ1 ��ͭ��Ͱ�ͭ���XRD��
Fig. 1 XRD patterns of chalcopyrite(a) and bornite(b) samples
1.2 �������ʵ��
�������ʵ����250 mL��ϸ��ҡƿ�н��С�ȡ120 mL�Ļ������������Ͳ�ͬ�����ȵĿ���6 g��ҡƿ�У�115�����������30 min����49%��ϡ�������pH��2.0�������ֶ�����ϸ��ʹ��ʼϸ���ܶ�ԼΪ1��107 cells/mL����ҡƿ���ں��¿���������������������������Ϊת��160 r/min���¶�10 �档������ǰ���о�[14]������ʵ��������A-C 3����ͬ�����Ļ�ͭ��Ͱ�ͭ���������2��ÿ��������ƽ�к�һ����������(AS��BS��CS)��
��2 ��ͬ�Ŀ�����ϵ
Table 2 Different mineral systems

������60 d�Ľ��������У�ÿ2 d������Һ��ͭ��Ũ�ȣ���������Һ��ϵ��������ԭ��λ(ORP)��pHֵ��ͭ����Ũ�Ȳ��õ����ϵ������������(ICP)�����Բⶨͭ�����ʡ�pHֵ�IJⶨ����PHS-3C��pH�Ʋ�������ORP���ò��缫�ڸ�pH�Ƶĵ�λ���ⶨ���ⶨ�ĵ�λ������ڸʹ��缫(SCE��0.242 V vs. SHE)��������ɺ�Ŀ��������ġ��ữˮƯϴ���Σ�������ո������и���24 h������XRD��⡣
1.3 �缫�Ʊ�
�绯ѧ�������ù����缫Ϊ����̼���缫[15]������������Ϊ���������1.4 g���״�ʯī��0.2 g�����в��ھ��Ȼ�ϣ��ӵ��ۻ���0.4 gʯ���У��㹻���Ⱥ���������ѹƬ���У���ѹƬ���Ƴɸ�4 mm��ֱ��Լ13 mm��Բ���塣����Ƕ�붨�Ƶĵ缫���У�ʹ�缫��һ����(Լ1 cm2)��¶����Һ�У��Ա���缫�ǹ����汻��ʴ������ǰ����3000Ŀɰ����̼���缫��¶������⣬�Եõ�һ���µĹ����档
1.4 ���½��������еĵ绯ѧʵ��
�绯ѧ����װ��Ϊ����Gamry�绯ѧ����վ������������ӣ���������ΪGamry Framework���缫ϵͳΪ���������缫ϵͳ�����ƵIJ�ͬ�����Ŀ���̼���缫���������缫��Hg/Hg2SO4�缫(MSE��0.640 V vs. SHE)Ϊ�αȵ缫��ʯī�缫�����Ե缫�������Ϊ50 mL�Ļ�����������(pH=2.0)�������е�λ��������˵�������Hg/Hg2SO4�αȵ缫�ı���ѹֵ0.640 V��Ϊ�˼���ʵ����ά�ֹ����缫�Ͳαȵ缫�ľ��벻�䣬�������ܵĽ���ѭ��������(CV)��ɨ������Ϊ20 mV/s��ɨ�跶Χ��-1.0~0.4 V����λ-0.3 V(vs. ��·��λOCP)�ӵ�0.3 V(vs. ��·��λOCP)�仯�õ���λ��̬�������ߡ������迹��(EIS)ʵ���Ƶ��Ϊ10-1~105 Hz������ѭ���������о��˿���ĵ绯ѧ�ܽ���Ϊ���������˵�λ��̬�����ͽ����迹��ʵ�顣
2 ���������
2.1 �������ʵ��
ͼ2��ʾΪ60 d��YL15�Բ�ͬ������ϵ�Ľ����������ͼ2(a)��ʾ��ͭ�Ľ������ɸߵ��ͷֱ�ΪC��B��A��CS��BS��AS����C��ϵ�У���Ͽ���Эͬ��������������Ϊ48.4%�������䵥������ϵA(16.4%)��B(43.7%)�У������ʽ�С��˵����ͭ��Ͱ�ͭ��ļ����ܹ���ٽ���ͭ�Ľ��������ϵ�����ͬ�����������������У�����ͭ�Ľ�����Զ����ʵ���飬˵��ϸ��YL15�ļ������Դٽ��˿���Ľ�������ͼ2(b)�У���ͭ��Ͱ�ͭ��ĵ����������ʱ��Ũ�ں��ڻ����һ��ƽ̨�ڣ�Ȼ��Эͬ����ʱϸ�����Խ�ǿ����Ũ���ڲ��������������������ͭ���ܳ���
������ʼ��ͬ������ϵ�Ľ���ҺpHֵ�����ߡ��������ڻ�ͭ��Ͱ�ͭ����ܽ���һϵ�к��ᷴӦ����(1)[16]ʽ��(2)[17]ʽ��ʾ��
CuFeS2+4H++O2��Cu1-xFe1-yS2-z+xCu2++yFe2++zS0+2(x+y)e+2H2O (1)
Cu5FeS4+4H++O2��5Cu2++Fe2++2H2O (2)
ʵ����pHֵ�ֳ����½������ܹ�����ϸ��������������������ķ�Ӧ[18-19]������ʽ��
2S0+3O2+2H2O�� +4H+ (3)
+4H+ (3)
���У���ϵA������Ժ�����ߣ������pHֵ��С��
ͨ���Ƚ�ͼ2(c)��2(d)��֪���о������pHֵ�½�����������������ԭ��λ��������ǰ���ṩ��H+�ٽ��˷�Ӧ(4)[20]ʽ�ķ��������˺��ߡ���ˣ�pHֵ�Կ����ܽ��Ӱ���Ǹ��ӵģ� pHֵ�½�һ�����������������̣���һ����Ҳ������ORP���߲����ڻ�ͭ��Ŀ����ܽ⡣
4Fe2++4H++O2��4Fe3++2H2O (4)
��ͼ2(d)�У���ͭ��Ͱ�ͭ��Эͬ������ORP���ڻ�ͭ��ģ���ͭ��ļ���ȷʵ��С�˻�ͭ���ORPֵ������ǰ���о���������ϡ�

ͼ2 �����������������ͭ�����ʣ���Ũ��pHֵ��������ԭ��λ�ı仯����
Fig. 2 Variation of copper extraction rate(a), cell density(b), pH(c) and ORP(d) with time during bioleaching
2.2 �绯ѧ����
2.2.1 ��·��λ����
Ϊ�˲����缫�ı�����ԣ��ڿ�ʼÿ���绯ѧ����֮ǰ[21]���缫������Һ�н���20 min�����п�·��λ���ԡ�OCP����CV�����Ѷ�����(Tafel)��EIS�ȼ�����Ӧ��������Ҫ����ͬ����缫��OCP������ʱ��仯��ͼ3��ʾ�������е������У��缫��λ��20 min��������������Ȼ��ﵽ��̬��·��λ��

ͼ3 ��ͬ�Ŀ�����ϵ�Ŀ�·��λ
Fig. 3 Open circuit potential (OCP) of different mineral systems
��һ���棬��·��λҲ��ϵ�������������������������ǰ뵼�壬��������ܽ�ʵ���ǰ뵼������Һ������ӻ��Ѩת�ƵĹ���[22]�����ߵĻ�ѧ��ͨ���÷����ܼ�(EF)����ʾ�����ݰ뵼��-��Һ����ģ��[23]���������¹�ϵ��
EF-Eref=-eVm (5)
���У�ErefΪ�αȵ缫�ķ����ܼ���VmΪ�뵼��ľ���λ�������OCP��
������缫�ľ���λת��Ϊ����ڱ���缫(SHE�������ܼ�Ϊ0)���ٴ��뷽�̵õ������ܼ����3��ʾ��һ����˵�������ܼ��ϸߵİ뵼����Ͻ�����ʧ�����Ӷ�������������[24-25]�����ֿ���ķ����ܼ���ߵ��ͷֱ�ΪB��C��A����ʾ��ͭ���Эͬ��������������������۽����ʸ��ߡ��෴����ͭ����ѽ��������뾲��λ�͵İ�ͭ��ȷʵ�ή�;���λ�Ӷ����ٻ�ͭ����ܽ⣬����ǰ�����ʵ��ͼ2(a)��2(d)�Ľ��һ�¡�
��3 ��ͬ�Ŀ�����ϵ�Ŀ�·��λ�ͷ����ܼ�����
Table 3 Open circuit potential and Fermi level parameters of different mineral systems

2.2.2 ѭ������
ͼ4��ʾΪOCP�ȶ���ͬ��ϵ�缫��CV���ߡ��������ȴ�OCP����ɨ����0.4 V��Ȼ��ɨ����-1.0 V���ٻص�OCP��������ͼ4������3��������a1-3��2����ԭ��c1-2��
����a1��Ϊ��Ҫ��������Ӧ����ʾ��ͭ����ͭ�����ɷǻ�ѧ�������м����緽��ʽ(1)��(6)[26-27]��ʾ��
Cu5FeS4+6H+��CuS +(4-x)Cu2++Fe3++3H2S+(5-x)e (6)
����ɨ���У�����λ��-0.2 V��0 V���䣬�л�ԭ��c1���֣���[20, 28]��Ϊ�����漰��Fe3+��Fe2+��Cu2+��S0�Ļ�ԭ(�緽��ʽ(7)~(10))
Fe3++e Fe2+ (7)
Fe2+ (7)
Fe2++2e Fe0 (8)
Fe0 (8)
Cu2++S0+2e CuS (9)
CuS (9)
Cu2++2e Cu0 (10)
Cu0 (10)
��ԭ��c2���Ӧ�ڻ�ͭ���ͭ��[28-29]��ԭ��Ӧ���ֱ�����Cu5FeS4��Cu2S������緽��ʽ(11)~(12)��
5CuFeS2+12H++2e Cu5FeS4+4Fe2++6H2S (11)
Cu5FeS4+4Fe2++6H2S (11)
2CuS+2H++2e Cu2S+H2S (12)
Cu2S+H2S (12)
��-0.6~-0.4 V����������������a2��a3���練Ӧ����ʽ(13)��(14)��ʾ[30]����a2����Ϊ�ǵ���ͭ�����������ɻ�ͭ��a3���ǻ�ͭ�������������һ��Cu-S�м����Cul.92S��
2Cu+HS-+OH- Cu2S+H2O+2e (13)
Cu2S+H2O+2e (13)
Cu2S Cu1.92S+0.08Cu2++0.16e (14)
Cu1.92S+0.08Cu2++0.16e (14)
��ͼ4��ʾ����ͬ������ϵ�缫��CV�����з��ѹֵ(��)����Ӧ����(J)���в�ͬ����״����ʮ�����ƣ�˵����ͬ��������ϵ�µ������ܽ����������ͬ���Աȷ��֣���ͭ��Ͱ�ͭ���ϵ缫�ĵ����ܶ�ԶԶ���ڻ�ͭ��ģ�˵����ʱ�и�����������ʸ������ڿ���������ֽ⣻�����ͭ���ĵ缫�����˵�λ���Ƶ�����ʾ�併���˷�Ӧ����ĵ�ѹʹ�ܽ��������
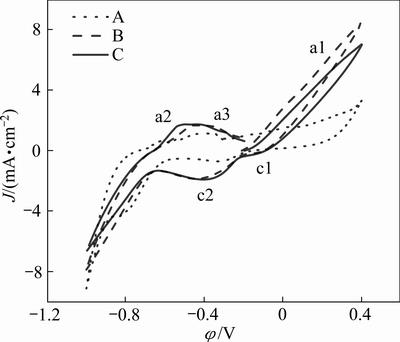
ͼ4 �缫��ѭ������ͼ
Fig. 4 Cyclic voltammograms of electrodes
2.2.3 ���ƶ�����
����Tafel���Կ���ĸ�ʴ����ѧ�����˷�������ʴ��λ(��corr)��ʴ����(Jcorr)���Ƿ�ӳ�����ʴ�����IJ�������ʴ��λֵԽ�ͣ���ʴ�����ܶ�Խ����Խ���ױ���ʴ���������Բ�ͬ��ϵ�缫������һϵ�е�λ��̬����ʵ��(��ͼ5)����4�г�������Tafel������ϼ����õĵ绯ѧ��ʴ����ѧ����������Tafel��ʽ������б��(ba)������б��(bc)�����º��壻
ba=2.303RT/n��F (15)
bc=2.303RT/n��F (16)
��ͼ5��֪����Ͽ�����ϵ��C�Ħ�corr�ϵͣ�Jcorr�ܶȽϴ��ټ��ϣ��缫б��ba��bc����С(��ʽ(15)~(16)�����Ӵ���ϵ���ºͦ���)����Щ���ݶ���������ĸ�ʴ��Ӧ�����������ױ���ʴ����֮�����Ļ�ͭ��Jcorr�ܶȽ�С����corr�߿��ܱ����������[31]�����в��︲���˻�ͭ����棬��������������Ӧ�����ѷ��֣�-218.7 mV vs. MSE�İ�ͭ��ĸ�ʴ��λ���ڻ�ͭ��(-191.4 mV vs. MSE)��������������ֿ���һ���Ͽ��γɼӷ���˵��(ԭ���)[32-33]����ˣ��ӷ����ЧӦ�ǻ�ͭ���м����ͭ����Դﵽ�ܸߵ�ͭ��ȡ�����е�ԭ��֮һ������Ȼ��ʴ�Ѷ��ϱȽϣ�A��C��B������OCP�Ľ��һ�¡�

ͼ5 �缫�����ƶ����ߡ�
Fig. 5 Tafel curves of electrodes
��4 �缫��������ѧ����
Table 4 Polarization dynamic parameters of different electrodes

2.2.4 �����迹
�����迹�о��У��κ�ģ���·���ɿ�������͵��ݵļ�����·��������ϡ����迹��ƽ��(Nyquist)ͼ����һ��Բ����һ��������·ʱ���У�
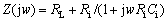 (17)
(17)
 (18)
(18)
ʽ�У�ZΪ�迹��ZreΪʵ�裻ZimΪ���裻RLΪ��Һ���裻RiΪ��ɴ�����Ե����������裻CiΪ���ݡ�
ͼ6�е�Nyquistͼ�������������: ��Ƶ��2��ʵ�����ϵ�Բ������ʾ�缫�����ɵ绯ѧ���̿��ƣ�����Ϊ�ݿ�������Ƶ��һ��ֱ�ߣ���ʾ�缫��������ɢ�������Warburg�迹�ij��֡��������˵�ɴ��ݹ��̺ʹ��ʹ��̹�ͬ���Ƶĵ缫��Ч��·ͼ7��

ͼ6 ��ͬ�缫�Ľ����迹��
Fig. 6 Ac impedance spectra of different electrodes

ͼ7 �缫�ĵ�Ч��·ͼ
Fig. 7 Equivalent circuit diagram of electrodes
����RS��ʾ����ʵĵ��裻R2��R1Ϊ��ɴ��ݵ��迹��CPE1�� CPE2�ǵ���Ԫ����W1��WarburgԪ�أ���缫�͵���ʽ�������ɢ�йء�
��Ƶ�İ�Բ��Ӧ�ڿ���ij�ʼ�绯ѧ�ܽ⡣�ڵ�Ƶ�������ֵ�����һ���ݿ�Բ�������ڿ�������γɵĶۻ�Ĥ����Ƶ��ֱ�߶�Ӧ��������(Fe3+)����������(Cu2+��Fe2+��S0)ͨ���缫����ʽ������ɢ���á���ˣ�����缫������迹��Ҫ��Դ�����ӽ����ͱ���ۻ��㡣
����ʽ(18)��Nyquistͼ��Բ����ֱ������Ri��������ɴ��ݵ���������ͼ6��ʾΪ��·��ѹ�µ缫��ʵ��Nyquistͼ����ϵC��EIS����Բ��ֱ��ҪԶС�ڴ���ͭ��A�ģ�˵����ͭ��ļ��뽵���˷�Ӧ���衣Эͬ����ʱ���ܽ���ͭ��ĵ�λ���������ٱ���ۻ���[34]�������ǵ��µ缫�迹���͵Ĺؼ�ԭ��
3 ����
1) �����������ʱ��ͭ��Ͱ�ͭ������ʷֱ�Ϊ16.4%��43.7%������Эͬ����ʱ������(48.4%)���ߡ�һ���棬���ڼӷ����ЧӦ�ٽ��˰�ͭ�����������һ���棬ͨ��ORP��OCP��CV��Tafel���Է��ְ�ͭ��ļ��뽵������ϵ�ĵ�λ����ʱ���ϸߵķ����ܼ�����Ӧ������ʴ������ֱ��������Эͬ������ϵ������������ʡ�
2) ͬʱ��EIS�������ֻ�ͭ��Ͱ�ͭ��缫�ı����迹�ܴ����Ƕ�����͵������γɵĶۻ�Ĥ��ɵģ����������»����������ɵĻƼ�������
REFERENCES
[1] CORDOBA E M, MUNOZ J A, BLAZQUEZ M L, et al. Leaching of chalcopyrite with ferric ion. Part ��: General aspects[J]. Hydrometallurgy, 2008, 93(3/4): 81-87.
[2] LI Yu-biao, KAWASHIMA N, LI Jun, et al. A review of the structure, and fundamental mechanisms and kinetics of the leaching of chalcopyrite[J]. Advances in Colloid and Interface Science, 2013, 197/198: 1-32.
[3] PRADHAN N, NATHSARMA K C, RAO K S, et al. Heap bioleaching of chalcopyrite: A review[J]. Minerals Engineering, 2008, 21(5): 355-365.
[4] OLSON G J, BRIERLEY J A, BRIERLEY C L. Bioleaching review part B: progress in bioleaching: applications of microbial processes by the minerals industries[J]. Applied Microbiology & Biotechnology, 2003, 63(3): 249-257.
[5] KLAUBER C. A critical review of the surface chemistry of acidic ferric sulphate dissolution of chalcopyrite with regards to hindered dissolution[J]. International Journal of Mineral Processing, 2008, 86(1/4): 1-17.
[6] MAJUSTE D, CIMINELLI V S T, ENG P J, et al. Cheminform abstract: Applications of in situ synchrotron XRD in hydrometallurgy: literature review and investigation of chalcopyrite dissolution[J]. ChemInform, 2013, 44(28): no-no.
[7] AHMADI A, SCHAFFIE M, MANAFI Z, et al. Electrochemical bioleaching of high grade chalcopyrite flotation concentrates in a stirred bioreactor[J]. Hydrometallurgy, 2010, 104(1): 99-105.
[8] NATARAJAN K A. Bioleaching of sulphides under applied potentials[J]. Hydrometallurgy, 1992, 29(1/3): 161-172.
[9] QIN Wen-qing, YANG C, LAI Shao-shi, et al. Bioleaching of chalcopyrite by moderately thermophilic microorganisms[J]. Bioresource Technology, 129(Complete): 200-208.
[10] DUTRIZAC J E, MACDONALDR J C, INGRAHAM T R. The kinetics of dissolution of bornite in acidified ferric sulfate solutions[J]. Metallurgical Transactions, 1970, 1: 225-231.
[11] WANG Jun, TAO Lang, ZHAO Hong-bo, et al. Cooperative effect of chalcopyrite and bornite interactions during bioleaching by mixed moderately thermophilic culture[J]. Minerals Engineering, 2016, 95: 116-123.
[12] ZHAO Hong-bo, WANG Jun, HU Ming-hao, et al. Synergistic bioleaching of chalcopyrite and bornite in the presence of Acidithiobacillus ferrooxidans[J]. Bioresource Technology, 2013, 149(4): 71-76.
[13] PENG Tang-jian, MA Li-yuan, FENG Xue, et al. Genomic and transcriptomic analyses reveal adaptation mechanisms of an Acidithiobacillus ferrivorans strain YL15 to alpine acid mine drainage[J]. Plos One, 2017, 12(5): e0178008.
[14] ���ü�. ���������Acidithiobacillus ferrivorans�Ļ�����Ӧ���Ƽ������Ľ����о�[D]. ��ɳ: ���ϴ�ѧ, 2017: 68-70.
PENG Tang-jian. Insights into the environmental adaptation mechanisms of cold-adapted acidophile Acidithiobacillus ferrivorans and its application in bioleaching of sulfide minerals[D]. Changsha: Central South University, 2017: 68-70.
[15] LAZARO I, MARTINEZ-MEDINA N, RODRIGUEZ I, et al. The use of carbon paste electrodes with non-conducting binder for the study of minerals: chalcopyrite[J]. Hydrometallurgy, 1995, 38(3): 277-287.
[16] ZENG Wei-min, QIU Guan-zhou, CHEN Miao. Investigation of Cu-S intermediate species during electrochemical dissolution and bioleaching of chalcopyrite concentrate[J]. Hydrometallurgy, 2013, 134/135(3): 158-165.
[17] BEVILAQUA D, GARCIA-JR O, TUOYINEN O H. Oxidative dissolution of bornite by Acidithiobacillus ferrooxidans[J]. Process Metallurgy, 2010, 45(1): 101-106.
[18] LEAHY M J, SCHWARZ M P. Modelling jarosite precipitation in isothermal chalcopyrite bioleaching columns[J]. Hydrometallurgy, 2009, 98(1/2): 181-191.
[19] ZHOU Hong-bo, ZENG Wei-min, YANG Zhi-feng, et al. Bioleaching of chalcopyrite concentrate by a moderately thermophilic culture in a stirred tank reactor[J]. Bioresource Technology, 2009, 100(2): 515-520.
[20] GOMEZ C, FIGUEROA M, MUNOZ J, et al. Electrochemistry of chalcopyrite[J]. Hydrometallurgy, 1996, 43(1/3): 331-344.
[21] GHAHREMANINEZHAD A, ASSELIN E, DIXON D G. Electrochemical evaluation of the surface of chalcopyrite during dissolution in sulfuric acid solution[J]. Electrochimica Acta, 2010, 55(18): 5041-5056.
[22] �����, ������.��ϸ�������İ뵼���ܴ����۷���[J]. ��ɫ��������, 2004, 56(3): 36-38, 49.
LI Hong-xu, WANG Dian-zuo. Fundamental analysis of sulfide bioleaching process based on semiconductor electrochemistry[J]. Nonferrous Metals Engineering, 2004, 56(3): 35-37, 48.
[23] �½���, ������, ¬����. �绯ѧ���ظ�ѡ�ܴ�ģ�ͼ�Ӧ��(��)�١��� �뵼���ܴ����ۼ�ģ��[J]. �й���ɫ����ѧ��, 2000, 2: 240-244.
CHEN Jian-hua, FENG Qi-ming, LU Yi-ping. Energy band model of electrochemical flotation and its application(��)��Theory and model of energy band of semiconductor-solution interface[J]. The Chinese Journal of Nonferrous Metals, 2000, 2: 240-244.
[24] CRUNDWELL F K. The influence of the electronic structure of solids on the anodic dissolution and leaching of semiconducting sulphide minerals[J]. Hydrometallurgy, 1988, 21(2):155-190.
[25] MORRISON S R. Electrochemistry at semiconductor and oxidized metal electrodes[M]. New York: Plenum Press, 1980: 401.
[26] ARCE E M, GONZALEZ I. A comparative study of electrochemical behavior of chalcopyrite, chalcocite and bornite in sulfuric acidsolution[J]. International Journal of Mineral Processing, 2002, 67(1): 17-28.
[27] LIANG Chang-li, XIA Jin-lan, NIE Zhen-yuan, et al. Comparison of electrochemical behaviors of chalcopyrite, bornite, chalcocite and covellite in 9K medium[J]. Advanced Materials Research, 2013, 634: 68-71.
[28] LU Z Y, JEFFREY M I, LAWSON F. An electrochemical study of the effect of chloride ions on the dissolution of chalcopyrite in acidic solutions[J]. 2000, 56(2):145-155.
[29] BIEGLER T, SWIFT D A. Anodic electrochemistry of chalcopyrite[J]. Journal of Applied Electrochemistry, 1979, 9(5): 545-554.
[30] VELASQUEZ P, LEINEN D, PASCUAL J, et al. XPS, SEM, EDX and EIS study of an electrochemically modified electrode surface of natural chalcocite (Cu2S)[J]. Journal of Electroanalytical Chemistry, 2001, 510(1): 20-28.
[31] O'CONNOR G M, LEPKOVA K, EKSTEEN J J, et al. Electrochemical behaviour of copper in alkaline glycine solutions[J]. Hydrometallurgy, 2018, 181: 221-229.
[32] ATTIA Y A. Effects of galvanic interactions of sulfides on extraction of precious metals from refractory complex sulfides by bioleaching[J]. International Journal of Mineral Processing, 1990, 30(1): 99-111.
[33] LI Hong-xu, QIU Guan-zhou, HU Yue-hua, et al. Galvanic effect on mixed sulfidebioleaching[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(5): 1287-1290.
[34] WANG Jun, GAN Xiao-wen, ZHAO Hong-bo, et al. Dissolution and passivation mechanisms of chalcopyrite during bioleaching: DFT calculation, XPS and electrochemistry analysis[J]. Minerals Engineering, 2016, 98: 264-278.
Electrochemical studies and synergistic bioleaching of chalcopyrite and bornite in presence of Acidithiobacillus ferrivorans YL15 at low temperature
PENG Yu-ping1, 2, PENG Tang-jian1, 2, ZENG Wei-min1, 2
(1. School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China;
2. Key Laboratory of Biometallurgy, Ministry of Education, Changsha 410083, China)
Abstract: In this paper, the synergistic leaching process of chalcopyrite and bornite by Acidithiobacillus ferrivoransYL15 was studied at a low temperature of 10��. And its electrochemical dissolution and surface passivation behaviors were investigated by combining different electrochemical test methods. The results showed that the bioleaching and electrochemical behavior of various mineral systems were extremely different. The optimal extraction rate of 48.4% in synergetic leaching group was obtained, followed by bornite, both of which were much higher than 16.4% of chalcopyrite. The redox potential was reduced and maintained to a suitable range (400-420 mV) as the addition of bornite to accelerate the oxidation of minerals. In addition, results of electrochemical tests indicated that the reduced potential, increased current, and decreased impedance corporately reflected the significant increase of oxidation rate during synergistic leaching.
Key words: chalcopyrite; bornite; synergistic bioleaching; low temperature; electrochemical; passivation
Foundation item: Projects(51934009, 51604308, 31900108) supported by the National Natural Science Foundation of China; Project(2018JJ2486) Natural Science Foundation of Hunan Province of China; Project(2017RS3003) supported by the Youth Talent Foundation of Hunan Province of China; Project(207159) supported by the Postdoctoral Research Funding plan in Hunan Province, China; Project(2019M662802) supported by China Postdoctoral Science Foundation; Project(2018DCYJ058) supported by Post-graduate Investigate and Research Projects of Central South University, China
Received date: 2020-03-30; Accepted date: 2021-05-06
Corresponding author: ZENG Wei-min; Tel: +86-10-88877472; E-mail: zengweimin1024@sina.com
(�༭ )
������Ŀ��������Ȼ��ѧ����������Ŀ(51934009��51604308��31900108)������ʡ��Ȼ��ѧ����������Ŀ(2018JJ2486)������ʡ�����˲Ż���������Ŀ(2017RS3003)������ʡ��ʿ����������ƻ���Ŀ(207159)�����Ҳ�ʿ���ѧ����������Ŀ(2019M662802)�����ϴ�ѧ�о��������о���Ŀ(2018DCYJ058)
�ո����ڣ�2020-03-30�������ڣ�2021-05-06
ͨ�����ߣ���ΰ���ڣ���ʿ���绰��010-88877472��E-mail��zengweimin1024@sina.com