≥¨ľ∂ĶÁ»›∆ų—–ĺŅľį∆š”¶”√
ņī‘ī∆ŕŅĮ£ļŌ°”–Ĺū Ű2003ńÍĶŕ3∆ŕ
¬Řőń◊ų’Ŗ£ļŃű√ų“Ś ≥¬ÍÕ ľÚ–Ů”Ó ő‚≤ģ»Ŕ ņÓ÷ĺ«Ņ ÷žņŕ
ĻōľŁī £ļ≥¨ľ∂ĶÁ»›∆ų; ĶÁĽĮ—ßĶÁ»›∆ų; ĶÁ∂Į≥Ķ; łŖĪ»Ļ¶¬ ;
’™ “™£ļ≥¨ľ∂ĶÁ»›∆ų «ĹŁńÍņī∑Ę’Ļ∆ūņīĶń“Ľ÷÷–¬–ÕĶńīĘń‹◊į÷√,ĺŖ”–Ļ¶¬ √‹∂»łŖ°Ę Ŕ√Ł≥§°Ę Ļ”√ő¬∂»ŅŪľį≥šĶÁ—łňŔĶ»”Ň“žŐō–‘,∂‘∆šĶń—–ĺŅľį”¶”√“≤»’“śĽÓ‘ĺ.ĪĺőńĹť…‹Ńň≥¨ľ∂ĶÁ»›∆ųĶń‘≠ņŪļÕ∑÷ņŗ,“‘ľįĹŁńÍņī≥¨ľ∂ĶÁ»›∆ųĶń∑Ę’ĻļÕ…Ő“ĶĽĮĹÝ≥Ő.Õ¨ Ī,“≤Ĺť…‹Ńň≥¨ľ∂ĶÁ»›∆ųĶń”¶”√«ťŅŲ. ňś◊ŇĶÁ∂Į≥Ķ—–ĺŅĶń–ň∆ū,≥¨ľ∂ĶÁ»›∆ų÷ō“™Ķń—–ĺŅ∑ĹŌÚ÷ģ“Ľ «Ĺę∆š”ŽłŖĪ»ń‹ŃŅĶń–ÓĶÁ≥ōѨ”√,‘ŕ≥ĶŃĺľ”ňŔ°Ę…≤≥ĶĽÚŇņ∆¬Ķń ĪļÚŐŠĻ©≥ĶŃĺňý–ŤĶńłŖĻ¶¬ ,īÔĶĹľű…Ŕ–ÓĶÁ≥ōĶńŐŚĽżļÕ—”≥§–ÓĶÁ≥ō Ŕ√ŁĶńńŅĶń.ń…√◊Őľ≤ńŃŌĶń≥ŲŌ÷ļÕ∑Ę’Ļő™≥¨ľ∂ĶÁ»›∆ųĶÁľę≤ńŃŌ—–ĺŅŐŠĻ©Ńň–¬Ķń∑Ę’Ļ∑ĹŌÚ,ĹęłÝ≥¨ľ∂ĶÁ»›∆ų–‘ń‹ŐŠłŖŐŠĻ©Ļ„ņęĶń∑Ę’Ļňľ¬∑ļÕŅ’ľš.
Ō°”–Ĺū Ű 2003,(03),385-390 DOI:10.13373/j.cnki.cjrm.2003.03.017
ő‚≤ģ»Ŕ ≥¬ÍÕ Ńű√ų“Ś ľÚ–Ů”Ó ņÓ÷ĺ«Ņ
ĪĪĺ©”–…ęĹū Ű—–ĺŅ◊‹‘ļń‹‘ī≤ńŃŌ”Žľľ ű—–ĺŅ÷––ń,ĪĪĺ©”–…ęĹū Ű—–ĺŅ◊‹‘ļń‹‘ī≤ńŃŌ”Žľľ ű—–ĺŅ÷––ń,ĪĪĺ©”–…ęĹū Ű—–ĺŅ◊‹‘ļń‹‘ī≤ńŃŌ”Žľľ ű—–ĺŅ÷––ń,ĪĪĺ©”–…ęĹū Ű—–ĺŅ◊‹‘ļń‹‘ī≤ńŃŌ”Žľľ ű—–ĺŅ÷––ń,ĪĪĺ©”–…ęĹū Ű—–ĺŅ◊‹‘ļń‹‘ī≤ńŃŌ”Žľľ ű—–ĺŅ÷––ń,ĪĪĺ©”–…ęĹū Ű—–ĺŅ◊‹‘ļń‹‘ī≤ńŃŌ”Žľľ ű—–ĺŅ÷––ń ĪĪĺ©100088 ,ĪĪĺ©100088 ,ĪĪĺ©100088 ,ĪĪĺ©100088 ,ĪĪĺ©100088 ,ĪĪĺ©100088
≥¨ľ∂ĶÁ»›∆ų «ĹŁńÍņī∑Ę’Ļ∆ūņīĶń“Ľ÷÷–¬–ÕĶńīĘń‹◊į÷√ , ĺŖ”–Ļ¶¬ √‹∂»łŖ°Ę Ŕ√Ł≥§°Ę Ļ”√ő¬∂»ŅŪľį≥šĶÁ—łňŔĶ»”Ň“žŐō–‘ , ∂‘∆šĶń—–ĺŅľį”¶”√“≤»’“śĽÓ‘ĺ°£ĪĺőńĹť…‹Ńň≥¨ľ∂ĶÁ»›∆ųĶń‘≠ņŪļÕ∑÷ņŗ , “‘ľįĹŁńÍņī≥¨ľ∂ĶÁ»›∆ųĶń∑Ę’ĻļÕ…Ő“ĶĽĮĹÝ≥Ő°£Õ¨ Ī , “≤Ĺť…‹Ńň≥¨ľ∂ĶÁ»›∆ųĶń”¶”√«ťŅŲ°£ňś◊ŇĶÁ∂Į≥Ķ—–ĺŅĶń–ň∆ū , ≥¨ľ∂ĶÁ»›∆ų÷ō“™Ķń—–ĺŅ∑ĹŌÚ÷ģ“Ľ «Ĺę∆š”ŽłŖĪ»ń‹ŃŅĶń–ÓĶÁ≥ōѨ”√ , ‘ŕ≥ĶŃĺľ”ňŔ°Ę…≤≥ĶĽÚŇņ∆¬Ķń ĪļÚŐŠĻ©≥ĶŃĺňý–ŤĶńłŖĻ¶¬ , īÔĶĹľű…Ŕ–ÓĶÁ≥ōĶńŐŚĽżļÕ—”≥§–ÓĶÁ≥ō Ŕ√ŁĶńńŅĶń°£ń…√◊Őľ≤ńŃŌĶń≥ŲŌ÷ļÕ∑Ę’Ļő™≥¨ľ∂ĶÁ»›∆ųĶÁľę≤ńŃŌ—–ĺŅŐŠĻ©Ńň–¬Ķń∑Ę’Ļ∑ĹŌÚ , ĹęłÝ≥¨ľ∂ĶÁ»›∆ų–‘ń‹ŐŠłŖŐŠĻ©Ļ„ņęĶń∑Ę’Ļňľ¬∑ļÕŅ’ľš
≥¨ľ∂ĶÁ»›∆ų;ĶÁĽĮ—ßĶÁ»›∆ų;ĶÁ∂Į≥Ķ;łŖĪ»Ļ¶¬ ;
÷–Õľ∑÷ņŗļŇ£ļ TM53
’łŚ»’∆ŕ£ļ2002-09-23
ĽýĹū£ļĻķľ“ 8 63ľ∆ĽģĶÁ∂Į≥Ķ◊®ŌÓ◊ ÷ķŌÓńŅ (2 0 0 1AA5 0 12 3 4);
Abstract£ļ
The supercapacitor is a new type of energy-storage device with excellent performance of high power density, long cycle life, quick charging and wide using temperature, which has been widely developed these days. The principle and classification of supercapacitor were described, together with its development, commercialization and application. Making a comprehensive view, with the development of the electric vehicle, supercapacitor will be used together with the battery to provide high power for acceleration, braking or climbing of the electric vehicle, which will be helpful for reducing the volume and lengthening the life of the battery. With the appearance of nano carbon materials, the study of supercapacitor will be promoted greatly, and the performance of supercapacitor will be greatly improved.
Keyword£ļ
supercapacitor; electrochemical capacitor; electric vehicle; high specific power;
Received£ļ 2002-09-23
≥¨ľ∂ĶÁ»›∆ų“≤≥∆ĶÁĽĮ—ßĶÁ»›∆ų, ňŁĺŖ”–”ŇŃľĶń¬Ų≥Ś≥š∑ŇĶÁ–‘ń‹ļÕīů»›ŃŅīĘń‹–‘ń‹, “Ú∆šīśīĘń‹ŃŅīů, ÷ ŃŅ«Š, Ņ…∂ŗīő≥š∑ŇĶÁ∂Ý≥…ő™“Ľ÷÷–¬–ÕĶńīĘń‹◊į÷√, ĹŁńÍņī ‹ĶĹŅ∆—ß—–ĺŅ»ň‘ĪĶńĻ„∑ļ÷ō ”°£ ňś◊ŇĽ∑Ī£–ÕĶÁ∂Į∆Ż≥Ķ—–ĺŅĶń–ň∆ūļÕ∑Ę’Ļ, ≥¨ľ∂ĶÁ»›∆ų”Žłųņŗ∂ĮѶĶÁ≥ōŇšļŌ Ļ”√◊ť≥…łīļŌĶÁ≥ō, ”¶”√”ŕĶÁ∂Į∆Ż≥ĶĶńĶÁ‘ī∆Ű∂ĮŌĶÕ≥, ‘ŕ≥ĶŃĺĶń∆ū≤Ĺ°Ę ľ”ňŔ°Ę ÷∆∂ĮĻż≥Ő÷–∆ūĶĹĪ£Ľ§–ÓĶÁ≥ōļÕĹŕń‹Ķń◊ų”√, ĽÚ’Ŗ÷ĪĹ”◊ųő™ĶÁ∂Į≥ĶĶńĶÁ‘ī°£ “≤Ņ…“‘ő™ń໾Ľķ“‘ľį∆šňŁ÷ō–Õ∆Ż≥Ķ∑Ę∂ĮĽķĶń∆Ű∂ĮŌĶÕ≥ŐŠĻ©ň≤ľšĶńīůĶÁŃų°£
≥¨ľ∂ĶÁ»›∆ų‘ŕīĘīśīůŃŅń‹ŃŅĶń ĪļÚĶÁ—ĻĹŌĶÕ, ļÕ–ÓĶÁ≥ōĶńĶÁ—ĻĪ»ĹŌ∆•Ňš°£ ”…”ŕ≥¨ľ∂ĶÁ»›∆ų◊Óīů≥š∑ŇĶÁ–‘ń‹”…ĽÓ–‘őÔ÷ ĪŪ√śĶńņŽ◊”»°ŌÚļÕĶÁļ…◊™“∆ňŔ∂»Ņō÷∆, “Úīň, Ņ…‘ŕ∂Ő ĪľšńŕĹÝ––ĶÁļ…Ķń◊™“∆, “ÚīňŅ…Ķ√ĶĹłŁłŖ∑ŇĶÁĪ»Ļ¶¬ (Ņ…īů”ŕ500 W°§kg-1) ; Õ¨ Ī, ”…”ŕĶÁľę…Ō√Ľ”–∑Ę…ķĺŲ∂®∑ī”¶ňŔ∂»”ŽŌř÷∆ĶÁľę Ŕ√ŁĶńĽÓ–‘őÔ÷ ĶńŌŗ”¶ĪšĽĮ, “ÚīňňŁĺŖ”–ļ‹ļ√Ķń—≠Ľ∑ Ŕ√Ł (Ņ…īů”ŕ105īő—≠Ľ∑) °£
1 ≥¨ľ∂ĶÁ»›∆ų∑÷ņŗ [1,2]
įī≤…”√ĶńĶÁľę≤ĽÕ¨, ≥¨ľ∂ĶÁ»›∆ųŅ…∑÷ő™“‘Ō¬ľł÷÷: (1) ŐľĶÁľęĶÁ»›∆ų; (2) ĻůĹū Ű—űĽĮőÔĶÁľęĶÁ»›∆ų; (3) ĶľĶÁĺŘļŌőÔĶÁ»›∆ų°£
įīīĘīśĶÁń‹ĶńĽķņŪ≤ĽÕ¨, ≥¨ľ∂ĶÁ»›∆ųŅ…∑÷ő™ŃĹ÷÷ņŗ–Õ: “Ľ÷÷ «°įňęĶÁ≤„ĶÁ»›∆ų°Ī, ∆šĶÁ»›Ķń≤ķ…ķ÷ų“™Ľý”ŕĶÁľę/ĶÁĹ‚“ļ…ŌĶÁļ…∑÷ņŽňý≤ķ…ķĶńňęĶÁ≤„ĶÁ»›, »ÁŐľĶÁľęĶÁ»›∆ų; ŃŪ“Ľ÷÷‘ÚĪĽ≥∆ő™°į∑®ņ≠Ķŕ◊ľĶÁ»›°Ī, ”…ĻůĹū ŰļÕĻůĹū Ű—űĽĮőÔĶÁľęĶ»◊ť≥…, ∆šĶÁ»›Ķń≤ķ…ķ «Ľý”ŕĶÁĽÓ–‘ņŽ◊”‘ŕĻůĹū ŰĶÁľęĪŪ√ś∑Ę…ķ«∑ĶÁőĽ≥ŃĽż, ĽÚ‘ŕĻůĹū Ű—űĽĮőÔĶÁľęĪŪ√śľįŐŚŌŗ÷–∑Ę…ķĶń—űĽĮĽĻ‘≠∑ī”¶∂Ý≤ķ…ķĶńőŁłĹĶÁ»›, ł√ņŗĶÁ»›Ķń≤ķ…ķĽķ÷∆”ŽňęĶÁ≤„ĶÁ»›≤ĽÕ¨, ≤ĘįťňśĶÁļ…īęĶ›Ļż≥ŐĶń∑Ę…ķ, Õ®≥£ĺŖ”–łŁīůĶńĪ»ĶÁ»›°£
łýĺ›≥¨ľ∂ĶÁ»›∆ųĶńĹŠĻĻľįĶÁľę…Ō∑Ę…ķ∑ī”¶Ķń≤ĽÕ¨, ”÷Ņ…∑÷ő™∂‘≥∆–ÕļÕ∑«∂‘≥∆–Õ°£ »ÁĻŻŃĹłŲĶÁľęĶń◊ť≥…ŌŗÕ¨«“ĶÁľę∑ī”¶ŌŗÕ¨, ∑ī”¶∑ĹŌÚŌŗ∑ī, ‘ÚĪĽ≥∆ő™∂‘≥∆–Õ°£ ŐľĶÁľęňęĶÁ≤„ĶÁ»›∆ų, ĻůĹū Ű—űĽĮőÔĶÁ»›∆ųľīő™∂‘≥∆–ÕĶÁ»›∆ų°£ »ÁĻŻŃĹĶÁľę◊ť≥…≤ĽÕ¨ĽÚ∑ī”¶≤ĽÕ¨, ‘ÚĪĽ≥∆ő™∑«∂‘≥∆–Õ, ”…Ņ…“‘ĹÝ––n–ÕļÕp–Õ≤Ű‘”ĶńĶľĶÁĺŘļŌőÔ◊ųĶÁľęĶńĶÁ»›∆ųľīő™∑«∂‘≥∆–ÕĶÁ»›∆ų, ∆š–‘ń‹ĪŪŌ÷–ő ĹłŁĹ”ĹŁ–ÓĶÁ≥ō, ĪŪŌ÷≥ŲłŁłŖĶńĪ»ń‹ŃŅļÕĪ»Ļ¶¬ °£
≥¨ľ∂ĶÁ»›∆ųĶń◊ÓīůŅ…”√ĶÁ—Ļ”…ĶÁĹ‚÷ Ķń∑÷Ĺ‚ĶÁ—ĻňýĺŲ∂®°£ ĶÁĹ‚÷ Ņ…“‘ «ňģ»‹“ļ (»Á«ŅňŠĽÚ«ŅľÓ»‹“ļ) “≤Ņ… «”–Ľķ»‹“ļ (»Á—őĶń÷ ◊”∂Ť–‘»‹ľŃ»‹“ļ) °£ ”√ňģ»‹“ļŐŚŌĶŅ…ĽŮĶ√łŖ»›ŃŅľįłŖĪ»Ļ¶¬ (“Úő™ňģ»‹“ļĶÁĹ‚÷ ĶÁ◊ŤĹŌ∑«ňģ»‹“ļĶÁĹ‚÷ ĶÕ, ňģ»‹“ļĶÁĹ‚÷ ĶÁĶľő™10-1°ę10-2 S°§cm-1, ∂Ý∑«ňģ»‹“ļŐŚŌĶĶÁĶľ‘Úő™10-3°ę10-4 S°§cm-1) ; —°”√”–Ľķ»‹“ļŐŚŌĶ‘ÚŅ…ĽŮĶ√łŖĶÁ—Ļ (“Úő™∆šĶÁĹ‚÷ ∑÷Ĺ‚ĶÁ—ĻĪ»ňģ»‹“ļĶńłŖ, ”–Ľķ»‹“ļ∑÷Ĺ‚ĶÁ—Ļ‘ľ3.5 V, ňģ»‹“ļ‘Úő™1.2 V) , ī”∂Ý“≤Ņ…ĽŮĶ√łŖĶńĪ»ń‹ŃŅ°£
1.1 ŐľĶÁľęĶÁ»›∆ų [1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16]
ŐľĶÁľęĶÁ»›∆ųĶń—–ĺŅņķ ∑ĹŌ≥§°£ 1962ńÍ, ĪÍ◊ľ Į”ÕĻęňĺ (SOHIO) »Ō ∂ĶĹ»ľŃŌĶÁ≥ō÷– ĮńęĶÁľęĪŪ√śňę≤„ĶÁ»›ĶńĺřīůņŻ”√ľŘ÷Ķ, ≤Ę…ķ≤ķ≥ŲŃňĻ§◊ųĶÁ—Ļő™6VĶń“‘Őľ≤ńŃŌ◊ųő™ĶÁľęĶńĶÁ»›∆ų°£ ĶÁ»›∆ųĶńīů–°ļÕ∆Ż≥Ķ–ÓĶÁ≥ōĶńīů–°≤Ó≤Ľ∂ŗ, Ņ…“‘«ż∂Į–°÷Ř‘ŕļĢ√ś…Ō–– Ľ ģ∑÷÷”◊ů”“°£ …‘ļů, ’‚ŌÓľľ ű◊™»√łÝŃň»’ĪĺNECĶÁ∆ÝĻęňĺ, ł√Ļęňĺī”1979ńÍŅ™ ľ“Ľ÷Ī…ķ≤ķ≥¨ľ∂ĶÁ»›∆ų, ≤ĘĹę’‚ŌÓľľ ű”¶”√”ŕĶÁ∂Į∆Ż≥ĶĶńĶÁ≥ō∆Ű∂ĮŌĶÕ≥, Ņ™ ľŃňĶÁĽĮ—ßĶÁ»›∆ųĶńīůĻśń£Ķń…Ő“Ķ”¶”√°£ ľłļű”ŽīňÕ¨ Ī, »’Īĺň…Ō¬Ļęňĺ…Ťľ∆Ńň“‘ĽÓ–‘ŐŅő™ĶÁľę≤ńŃŌ, “‘”–Ľķ»‹“ļő™ĶÁĹ‚÷ Ķń≥¨ľ∂ĶÁ»›∆ų°£
ŐľĶÁľęĶÁ»›∆ų∆šĶÁ»›Ķńīů–°ļÕĶÁľęĶńľęĽĮĶÁőĽľįĶÁľęĪ»ĪŪ√śĽżīů–°”–Ļō, Ļ Ņ…“‘Õ®ĻżľęĽĮĶÁőĽĶń…żłŖļÕ‘ŲīůĶÁľęĪ»ĪŪ√śĽżīÔĶĹŐŠłŖĶÁ»›īů–°ĶńńŅĶń°£ ĶÁľę/ĶÁĹ‚÷ ňęĶÁ≤„…ŌŅ…÷ŁīśĶńĶÁŃŅ∆šĶš–Õ÷Ķ‘ľő™15°ę40 ¶ŐF°§cm-2°£ —°”√ĺŖ”–łŖĪŪ√śĽżĶńłŖ∑÷…ĘĶÁľę≤ńŃŌŅ…“‘ĽŮĶ√ĹŌłŖĶńĶÁ»›°£ ∂‘ņŪŌŽŅ…ľęĽĮŐŚŌĶ∂Ý—‘, Ņ…Õ®ĻżőřŌřŐŠłŖ≥šĶÁĶÁ—Ļ∂ÝīůŃŅīĘīśń‹ŃŅ°£ Ķę «, ∂‘”ŕ Ķľ ŐŚŌĶ»ī ‹ĶÁľę≤ńŃŌļÕĶÁĹ‚“ļ◊ť≥…ĶńĶÁľęŌĶÕ≥ĶńŅ…ľęĽĮ–‘ļÕ»‹ľŃ∑÷Ĺ‚ĶńŌř÷∆, Ņ…Õ®Ļżľ”īůĶÁľęĪ»ĪŪ√śĽżņī‘Ųľ”ĶÁ»›÷Ķ°£
ĶÁ»›CŅ…”…Ō¬ ĹłÝ≥Ų
Ĺ÷–: ¶Ň0ő™◊‘”…Ņ’ľšĶńĺÝ∂‘ĹťĶÁ≥£ ż, ¶Ňő™ĶÁĶľŐŚļÕńŕ≤Ņļ’ń∑ĽŰ◊»√śľš«Ý”ÚĶńŌŗ∂‘ĹťĶÁ≥£ ż, Aő™ĶÁľęĪŪ√śĽż, dő™ĶľŐŚ”Žńŕļ’ń∑ĽŰ◊»√ś÷ģľšĶńĺŗņŽ°£ ÷∆◊ų Ķ”√≥¨ľ∂ĶÁ»›∆ų◊Ó”––ßĶń∑Ĺ∑® «—°”√łų÷÷ĻśłŮņŗ–ÕĶńŐľ∑Řń©°£ ņż»Á, Ņ…“‘‘ŕ800°ę1100 °ś∑÷Ĺ‚∑”»© ų÷¨ņī÷∆◊ų Ķ”√ĶńŐľĶÁľę, įī’‚÷÷Ļ§“’∆šĽÓ–‘ĪŪ√śĽż (ľī…Ō Ĺ÷–ĶńA) Ņ…“‘‘Ųľ”ĶĹ‘≠ņīĶń250Ī∂, ∆šňŁņŗ–ÕŐľĶÁľęŅ…”√Őľ/Ĺū ŰĽžļŌŌňő¨…’ĹŠ÷∆≥…, ’‚Ņ… ĻĶÁľęľ»ĺŖ”–łŖĪŪ√śĽż∂ÝĶÁ◊Ť”÷ĹŌĶÕ, ī”∂Ý ĻĶÁľęľ»ĺŖ”–łŖĶń»›ŃŅĶńÕ¨ Ī”÷ĺŖ”–łŖĻ¶¬ °£ ňęĶÁ≤„≥¨ľ∂ĶÁ»›∆ų≤…”√ĶńŐľĶÁľęĪŪ√śĽżńŅ«įŅ…īÔĶĹ1000°ę2000 m2°§g-1°£
ĹŁńÍņī—–ĺŅ÷ų“™ľĮ÷–‘ŕŐŠłŖŐľ≤ńŃŌĶńĪ»ĪŪ√śĽżļÕŅō÷∆Őľ≤ńŃŌĶńŅ◊ĺ∂ľįŅ◊ĺ∂∑÷≤ľ, ≤ĘŅ™∑Ę≥Ų–Ū∂ŗ≤ĽÕ¨ņŗ–ÕĶńŐľ≤ńŃŌ, ÷ų“™”–: ĽÓ–‘Őľ∑Ř°Ę ĽÓ–‘ŐŅŌňő¨°Ę Őľ∆ÝńżĹļ°Ę Őľń…√◊Ļ‹Ķ»°£
1.2 ĻůĹū Ű—űĽĮőÔĶÁľęĶÁ»›∆ų [1,2]
∂‘ĻůĹū Ű—űĽĮőÔĶÁľęĶÁ»›∆ųĶń—–ĺŅ, ÷ų“™≤…”√RuO2, IrO2 Ķ»ĻůĹū Ű—űĽĮőÔ◊ųő™ĶÁľę≤ńŃŌ°£ ”…”ŕRuO2ĶÁľęĶńĶľĶÁ–‘Ī»ŐľĶÁľęļ√, ĶÁľę‘ŕŃÚňŠ÷–ő»∂®, Ņ…“‘ĽŮĶ√łŁłŖĶńĪ»ń‹ŃŅ, ÷∆ĪłĶńĶÁ»›∆ųĪ»ŐľĶÁľęĶÁ»›∆ųĺŖ”–łŁļ√Ķń–‘ń‹, “ÚīňĺŖ”–ļ‹ļ√Ķń∑Ę’Ļ«įĺį, Ķę «, ”…”ŕĻůĹū ŰĶń◊ ‘ī”–Ōř°Ę ľŘłŮįļĻůŌř÷∆ŃňňŁĶń Ļ”√°£ “‘RuO2°§nH2Oőř∂®–ÕňģļŌőÔ◊ųĶÁľę, 5.3 mol°§L-1 H2SO4◊ųĶÁĹ‚“ļňý÷∆Ķ√ĶńĶÁ»›∆ųĪ»ĶÁ»›ń‹īÔĶĹ700 F°§g-1; ∂Ý“‘őř∂®–ÕňģļŌőÔMnO2°§nH2O◊ųĶÁľę, 2 mol°§L-1 KClňģ»‹“ļ◊ųĶÁĹ‚“ļňý÷∆Ķ√ĶńĶÁ»›∆ųĪ»ĶÁ»›“≤Ņ…īÔĶĹ200 F°§g-1°£ ĶęĪ»ĹŌ∂Ý—‘, “Úő™‘ŕ÷––‘KClňģ»‹“ļ÷–≤ńŃŌĪ»ĹŌő»∂®, ≤Ľ∑Ę…ķĽĮ—ßłĪ∑ī”¶, “‘KClňģ»‹“ļ◊ųĶÁĹ‚“ļ ”√”ŕ∂ŗ÷÷ĶÁľę≤ńŃŌ°£
“‘RuO2◊ųő™ĶÁľę≤ńŃŌĶń—–ĺŅ÷ų“™ľĮ÷–‘ŕĶÁľę÷∆Īł∑Ĺ∑®…Ō°£ RuO2Ķń÷∆Īł÷ų“™≤…”√»»∑÷Ĺ‚—űĽĮRuCl3°§xH2OĶńňģ»‹“ļĽÚ’Ŗ““īľ»‹“ļ (ő¬∂»300°ę800 °ś) °£ ő™ŐŠłŖĶÁľęĶńĪ»ĪŪ√ś, ≤…»°Ńň‘ŕī÷≤ŕĶńĽýŐŚ≤ńŃŌ…ŌĽÚ‘ŕłŖĪ»ĪŪ√śĶńŐľŌňő¨ĪŪ√ś…Ō÷∆ĪłRuO2, ÷∆Īł∂Ģ‘™Ĺū Ű—űĽĮőÔĽÚ‘ŕĶÕő¬Ō¬÷∆ĪłĶÁľęĶ»∑Ĺ∑®°£ “≤Ņ…”√Ň®Ĺļ∑®÷∆Īłőř∂®–ÕňģļŌRuO2ĶÁľę≤ńŃŌ, ľ”»Ž’≥ĹŠľŃ÷∆ĪłĶÁľę, ňý÷∆ĶÁľęĽÓ–‘őÔ÷ ĶńĪ»ĶÁ»›ő™720 F°§g-1, Ī»…Ō Ų∑Ĺ∑®÷∆Ķ√ĶÁľęĶńĪ»ĶÁ»›łŖ≥Ų2Ī∂°£ ”√»»∑÷Ĺ‚—űĽĮ∑Ĺ∑®÷∆ĪłĶńĶÁľęĽÓ–‘őÔ÷ RuO2≤Ľļ¨ĹŠĺßňģ, ňýĶ√ĶÁľęĪ»ĶÁ»›ŃŅĪ»ņŪ¬Ř÷Ķ–°Ķ√∂ŗ°£ ∂Ý”√–¬∑Ĺ∑®÷∆ĪłĶńļ¨ňģĽÓ–‘őÔ÷ RuO2°§2H20, H+ļ‹»›“◊‘ŕŐŚŌŗ÷–īę š, ∆šŐŚŌŗ÷–ĶńRu4+“≤ń‹∆ū◊ų”√, ī”∂ÝīůīůŐŠłŖŃňĶÁľęĶńĪ»ĶÁ»›°£ ‘ň”√’‚÷÷∑Ĺ∑®÷∆ĪłĶńĶÁ»›∆ų∆š—≠Ľ∑ Ŕ√Ł≥š∑ŇĶÁ–‘ń‹Ķ»“≤ŌŗĶĪļ√, ī”∂Ý»Ōő™őř∂®–ÕňģļŌRuO2 «ļ‹ļ√ĶńĽÓ–‘őÔ÷ –őŐ¨°£ ĺ›Ī®Ķņ, ĶÕ≥…Īĺ°Ę łŖĪ»ĪŪ√śĶńR-Mo2N◊ųő™“Ľ÷÷–¬–ÕĶÁľę≤ńŃŌ, ‘ŕľÓ–‘ĶÁĹ‚“ļ÷–Ņ…ĽŮĶ√125 F°§g-1ĶńĪ»ĶÁ»›ľį0.7 VĶńŅ™¬∑ĶÁ—Ļ°£
1.3 ĶľĶÁĺŘļŌőÔĶÁľęĶÁ»›∆ų [1,2]
ĶľĶÁĺŘļŌőÔĶÁľęĶÁ»›∆ų◊ųő™“Ľ÷÷–¬–ÕĶńĶÁĽĮ—ßĶÁ»›∆ų, ĺŖ”–łŖ–‘ń‹ļÕĪ»ĻůĹū Ű≥¨ľ∂ĶÁ»›∆ųłŁ”Ň‘ĹĶńĶÁ–‘ń‹°£ Ņ…Õ®Ļż…Ťľ∆—°‘ŮŌŗ”¶ĺŘļŌőÔĶńĹŠĻĻ, ĹÝ“Ľ≤Ŕҗ°ŐŠłŖĺŘļŌőÔĶń–‘ń‹, ī”∂ÝŐŠłŖĶÁ»›∆ųĶń–‘ń‹°£
ĶľĶÁĺŘļŌőÔĶÁľęĶÁ»›∆ųŅ…∑÷ő™3÷÷ņŗ–Õ: (1) ∂‘≥∆ĹŠĻĻ°™°™ĶÁ»›∆ų÷–ŃĹĶÁľęő™ŌŗÕ¨ĶńŅ…p–Õ≤Ű‘”ĶńĶľĶÁĺŘļŌőÔ (»ÁĺŘŗÁ∑‘) ; (2) ≤Ľ∂‘≥∆ĹŠĻĻ°™°™ŃĹĶÁľęő™≤ĽÕ¨ĶńŅ…ĹÝ––p–Õ≤Ű‘”ĶńĺŘļŌőÔ≤ńŃŌ (»ÁĺŘŖŃŅ©ļÕĺŘŗÁ∑‘) ; (3) ĶľĶÁĺŘļŌőÔŅ…“‘ĹÝ––p–ÕļÕn–Õ≤Ű‘”, ≥šĶÁ ĪĶÁ»›∆ųĶń“ĽłŲĶÁľę «n–Õ≤Ű‘”◊īŐ¨∂ÝŃŪ“ĽłŲĶÁľę «p–Õ≤Ű‘”◊īŐ¨, ∑ŇĶÁļů∂ľ «»•≤Ű‘”◊īŐ¨, ’‚÷÷ĶľĶÁĺŘļŌőÔĶÁľęĶÁ»›∆ųŅ…ŐŠłŖĶÁ»›ĶÁ—ĻĶĹ3 V, ∂ÝŃĹĶÁľęĶńĺŘļŌőÔ∑÷Īūő™n–Õ≤Ű‘”ļÕp–Õ≤Ű‘” Ī, ĶÁ»›∆ų‘ŕ≥š∑ŇĶÁ Īń‹≥š∑÷ņŻ”√»‹“ļ÷–Ķń“ű—ŰņŽ◊”, ĹŠĻŻňŁĺŖ”–ļ‹ņŗň∆–ÓĶÁ≥ōĶń∑ŇĶÁŐō’ų, “ÚīňĪĽ»Ōő™ «◊Ó”–∑Ę’Ļ«įĺįĶńĶÁĽĮ—ßĶÁ»›∆ų°£
—–ĺŅĻ§◊ų÷ų“™ľĮ÷–‘ŕ—į’“ĺŖ”–”ŇŃľ≤Ű‘”–‘ń‹ĶńĶľĶÁĺŘļŌőÔ, ŐŠłŖĺŘļŌőÔĶÁľęĶń∑ŇĶÁ–‘ń‹, —≠Ľ∑ Ŕ√ŁļÕ»»ő»∂®–‘Ķ»∑Ĺ√ś°£ ĺŘ““»≤°Ę ĺŘŖŃŅ©°Ę ĺŘĪĹį∑°Ę ĺŘŗÁ∑‘Ķ»ĶľĶÁĺŘļŌőÔ «◊Ó‘Á”¶”√”ŕ÷∆ĪłĶÁľęĶńĶľĶÁĺŘļŌőÔ, ĶęňŁ√«≤Ű‘”ļůĶÁ—ĻĻżīůĽÚ’Ŗ—≠Ľ∑–‘ń‹≤Ľļ√∂ÝŌř÷∆ŃňňŁ√«Ķń”¶”√°£ RudgeĶ»Ī®ĶņŃň”√∑ľĽý‘ŕŗÁ∑‘Ķń»żļŇőĽĹÝ––»°īķ∑ī”¶÷∆Ķ√∆š—‹…ķőÔ, ”√ĶÁĽĮ—ßĺŘļŌ∑®‘ŕ÷ōŃŅ«Š∂Ý∂ŗŅ◊ĶńŐľ÷Ĺ…Ō÷∆»°ĶľĶÁĺŘļŌőÔPEPTń§[ĺŘ-3 (4-∑ķ-ĪĹĽý) ŗÁ∑‘], ”…”ŕ‘ŕ≥šĶÁ ĪĶÁ◊”Ņ…ī”ĺŘŗÁ∑‘ĶńĻ«ľ‹…Ō◊™“∆ĶĹ»°īķ∑ľĽý…Ō, ī”∂ÝŐŠłŖ∆šn–Õ≤Ű‘”–‘°£ Õ¨ Ī, ÷∆ĪłŃň“Ľ÷÷–¬–ÕĶÁĹ‚÷ Me4NCF3SO3 (Me: ľ◊Ľý) , “‘““Žś◊ųő™»‹ľŃ, ’‚—ýŅ…‘Ųľ”ĶÁĹ‚“ļĶńĶľĶÁ–‘ļÕĶÁľęĶń∑ī”¶–‘ń‹°£ —–ĺŅĪŪ√ų: ĶĪĶÁľęń§ĶńļŮ∂»≥¨ Ī10 ¶Őm ĪĺŖ”–Ī»∆šňŁĺŘļŌőÔłŁļ√ĶńĶÁ–‘ń‹, ŃĹĶÁľęĽÓ–‘őÔ÷ Ī»Ļ¶¬ ∂ľŅ…īÔ3.5 kW°§kg-1°£
2≥¨ľ∂ĶÁ»›∆ųļÕ–ÓĶÁ≥ō–‘ń‹Ī»ĹŌ [1,2,4]
–ÓĶÁ≥ōĶń–‘ń‹Õ®≥£”…ĽÓ–‘őÔ÷ Ķń»»Ń¶—ß”Ž∂ĮѶ—ß–‘÷ ňýĺŲ∂®°£ “Ľį„«ťŅŲŌ¬, ‘ŕ≥š∑ŇĶÁ Ī, ĶÁľęĶÁőĽĶńĪšĽĮ≤Ľīů, ∆šīĘīśĶńń‹ŃŅEő™: ĶÁ≥ō∑ŇĶÁ ĪĽÓ–‘őÔ÷ ∑Ę…ķ—űĽĮĽĻ‘≠∑ī”¶ňýÕ®ĻżĶńĶÁŃŅQ, ≥ň“‘ĶÁ≥ōŃĹľęĶÁőĽ≤ÓV, ľīE=QV°£
∂‘”ŕ≥¨ľ∂ĶÁ»›∆ų, ĶÁľę…ŌĽÓ–‘őÔ÷ ĶńĽĮ—ßőĽļÕĶÁľęĶÁőĽ «ĶÁľęļ…ĶÁŃŅĶńѨ–ÝļĮ ż, ĺŖŐŚĪŪŌ÷ő™: (1) ĶÁľęĶÁ—ĻļÕĶÁľę÷–≥š»ŽĶÁļ…ĶńŃŅ≥…ŌŖ–‘ĻōŌĶ; (2) »ÁĻŻĶÁľęĶÁőĽňś Īľš◊ųŌŖ–‘ĪšĽĮ, Ņ…“‘Ķ√ĶĹ“ĽłŲīůŐŚļ„∂®Ķń≥šĶÁĶÁŃų°£ ”…”ŕ∆šīĘń‹ ĪĶÁľęĶÁőĽňś≥š»ŽĶńĶÁļ…ŃŅĶń…żłŖ∂Ý…żłŖ, ňý“‘, ňŁňýīĘīśĶńń‹ŃŅő™ŌŗÕ¨ĶÁŃŅļÕĶÁ—ĻŌ¬–ÓĶÁ≥ōń‹ŃŅĶń“ĽįŽ°£ »ÁĻŻ…żłŖĶÁ»›∆ųĶńĶÁ—Ļ, ‘ÚŅ…ŐŠłŖĶÁ»›∆ųĶńĪ»ń‹ŃŅ°£ »ÁĪŪ1, 2ňý ĺ°£
Õľ1ő™≥¨ľ∂ĶÁ»›∆ųļÕ“Ľ–©īęÕ≥ľįŌ»ĹÝĶÁ≥ōĶńĻ¶¬ √‹∂»°Ę ń‹ŃŅ√‹∂»÷ģľšĻōŌĶĶń«ķŌŖĪ»ĹŌ°£ ī”Õľ÷–Ņ…“‘Ņī≥Ų, ≥¨ľ∂ĶÁ»›∆ųĻ¶¬ √‹∂»ļ‹łŖ (400°ę1000 W°§kg-1) , Ķę∆šĪ»ń‹ŃŅ÷Ľ”–ľłłŲWh°§kg-1°£
3 ≥¨ľ∂ĶÁ»›∆ųĶńŌ÷◊īľį”¶”√
≥¨ľ∂ĶÁ»›∆ųĺŖ”–Ļ¶¬ √‹∂»łŖ (īů”ŕ1 kW°§kg-1, …ű÷Ńľł ģ kW°§kg-1) °Ę Ŕ√Ł≥§ (105īő“‘…Ō) °Ę Ļ”√ő¬∂»ŅŪ (-40°ę60 °ś) ľį≥šĶÁ—łňŔ (<3 min) Ķ»”Ň“žŐō–‘, łųĻķ’ĢłģļÕĻęňĺ∂ľĽżľęŅ™’Ļīň∑Ĺ√śĶń—–ĺŅŅ™∑ĘĻ§◊ų, ≤Ę“—”–łų÷÷≤ķ∆∑Ķ√ĶĹŃň…Ő“Ķ”¶”√°£ √ņĻķń‹‘ī≤Ņ“—∂‘—–÷∆»ę√‹∑‚≥¨ľ∂ĶÁ»›∆ų÷∆∂®ŃňńŅĪÍ, ∆šĹŁ∆ŕńŅĪÍ (1998°ę2003ńÍ) ő™: Ļ¶¬ √‹∂»īÔĶĹ500 W°§kg-1, ń‹ŃŅ√‹∂»īÔĶĹ5 Wh°§kg-1; ‘∂∆ŕńŅĪÍ (2003ńÍ“‘ļů) ő™: Ļ¶¬ √‹∂»īÔĶĹ1500 W°§kg-1, ń‹ŃŅ√‹∂»īÔĶĹ15 Wh°§kg-1
ĪŪ1 ≥¨ľ∂ĶÁ»›∆ųļÕ–ÓĶÁ≥ōĶÁ–‘ń‹Ī»ĹŌ
Table 1 Performance comparasion bettween supercapacitor and batteny
| ŐűľĢ | –ÓĶÁ≥ō | ≥¨ľ∂ĶÁ»›∆ų |
ĶÁĽĮ—ßőĽĪšĽĮ |
”…ĽÓ–‘őÔ÷ Ķń»»Ń¶—ß–‘÷ ĺŲ∂® | ňśĽÓ–‘őÔ÷ ĶńĪšĽĮ∂ÝĪšĽĮ |
≥š∑ŇĶÁĶÁľęĶÁőĽĪšĽĮ |
»ÁĻŻ≤Ľ∑Ę…ķ∑«»»Ń¶—ßĻż≥ŐĽÚőÔŌŗĪšĽĮ, ĶÁľęĶÁőĽĪ£≥÷≤ĽĪš | ĶÁľęĶÁőĽňś≥šĶÁ◊īŐ¨∂Ý∑Ę…ķĪšĽĮ |
ĶÁŃŅīĘīś∑Ĺ Ĺ |
∑«ĶÁ»›–‘ | ĶÁ»›–‘ |
ļ„ĶÁőĽĪšĽĮ Ī |
Ķ√≤ĽĶĹļ„Ńų«ķŌŖ | Ņ…Ķ√ļ„Ńų«ķŌŖ |
ļ„Ńų∑ŇĶÁ ĪĶÁőĽĪšĽĮ |
ĽýĪĺ≤ĽĪš | ≥ ŌŖ–‘ĪšĽĮ |
Õľ1 ňęĶÁ≤„≥¨ľ∂ĶÁ»›∆ų°Ę ĶÁĽĮ—ßĶÁ»›∆ų”ŽŅ…≥šĶÁĶÁ≥ōľį»ľŃŌĶÁ≥ōĶńń‹ŃŅ√‹∂»°Ę Ļ¶¬ √‹∂»Ī»ĹŌ
Fig.1Energy density power density of some energy storage device
ĪŪ2 ľł÷÷ĶÁĽĮ—ßīĘń‹∆ųľĢĶń–‘ń‹Ī»ĹŌTable.2 Properties of some energy storage device
ĶÁĽĮ—ßīĘń‹∆ųľĢ |
ń‹ŃŅ√‹∂»/ (Wh°§dm-3) |
Ļ¶¬ √‹∂»/ (W°§dm-3) |
—≠Ľ∑ Ŕ√Ł/ īő |
ĶÁ≥ō |
50°ę250 | 150 | <104 |
ĶÁĽĮ—ßĶÁ»›∆ų |
5 | >105 | >105 |
∆’Õ®őÔņŪĶÁ»›∆ų |
0.05 | >108 | >106 |
ĪŪ3Ń–≥ŲŃňńŅ«įĻķÕ‚≥¨ľ∂ĶÁ»›∆ųĶń—–ĺŅŌ÷◊ī°£ ĪŪ4‘Ú «“Ľ–©≥¨ľ∂ĶÁ»›∆ų…Ő“Ķ≤ķ∆∑Ķń–‘ń‹°£ Ņ…“‘∑ĘŌ÷, —–ĺŅľį…Ő“ĶĽĮĶń≥¨ľ∂ĶÁ»›∆ųīů≤Ņ∑÷≤…”√ŃňŐľ≤ńŃŌ◊ųő™ĶÁľę≤ńŃŌ°£ Ķę «, ő™ĹÝ“Ľ≤ĹŐŠłŖĶÁ»›∆ųĶń–‘ń‹, ŐľĶÁľę≤ńŃŌĽĻīś‘ŕļ‹∂ŗő Ő‚, ”–īżĹÝ“Ľ≤ĹłńĹÝ°£
≥¨ľ∂ĶÁ»›∆ų“Ú∆š”Ň“žŐō–‘∂Ý Ļ∆š‘ŕłųłŲŃž”ÚĶ√ĶĹŃňĻ„∑ļ”¶”√, »Á”√◊ŲīśīĘ∆ų°Ę őĘ–Õľ∆ň„Ľķ°Ę ŌĶÕ≥÷ųįŚļÕ÷”ĪŪĶ»ĶńĪł”√ĶÁ‘ī; ”√◊ŲĶÁ∂ĮÕśĺŖ≥Ķ÷ųĶÁ‘ī°Ę ń໾Ľķ÷–∆Ű∂ĮĶÁѶ°Ę Őę—Űń‹ĶÁ≥ōł®÷ķĶÁ‘ī, ĽĻŅ…”¶”√”ŕļĹŅ’ļĹŐžĶ»Ńž”Ú°£ ĶÁ∂Į∆Ż≥Ķ∂‘∂ĮѶĶÁ‘īĶń“™«ů“ż∆ūŃň»ę ņĹÁ∑∂őß∂‘≥¨ľ∂ĶÁ»›∆ų’‚“Ľ–¬–ÕīĘń‹◊į÷√ĶńĻ„∑ļ÷ō ”°£ īęÕ≥∂ĮѶĶÁ≥ō‘ŕłŖĻ¶¬ š≥Ų°Ę ŅžňŔ≥šĶÁ°Ę ŅŪő¬∂»∑∂őß Ļ”√“‘ľį Ŕ√ŁĶ»∑Ĺ√śīś‘ŕ“Ľ∂®Ķńĺ÷Ōř–‘, ”––©ŅŃŅŐŐűľĢŅ…ń‹ĽŠŌ‘÷ÝĹĶĶÕĶÁ≥ōĶń Ŕ√Ł°£ ∂Ý≥¨ľ∂ĶÁ»›∆ųń‹ĹŌļ√Ķō¬ķ◊„ĶÁ∂Į≥Ķ‘ŕ∆Ű∂Į°Ę ľ”ňŔ°Ę Ňņ∆¬ Ī∂‘Ļ¶¬ Ķń–Ť«ů, »Ű”Ž∂ĮѶĶÁ≥ōŇšļŌ Ļ”√, ‘ÚŅ…ľű…ŔīůĶÁŃų≥š∑ŇĶÁ∂‘ĶÁ≥ōĶń…ňļ¶, —”≥§ĶÁ≥ōĶń Ļ”√ Ŕ√Ł, Õ¨ ĪĽĻń‹Õ®Ļż‘Ŕ…ķ÷∆∂ĮŌĶÕ≥Ĺęň≤ľšń‹ŃŅĽō ’”ŕ≥¨ľ∂ĶÁ»›∆ų÷–, ŐŠłŖń‹ŃŅņŻ”√¬ °£ “Ú∂Ý, ≥¨ľ∂ĶÁ»›∆ų «ĹŁńÍņīĶÁ∂Į≥Ķ∂ĮѶŌĶÕ≥Ņ™∑Ę÷–Ķń÷ō“™Ńž”Ú÷ģ“Ľ°£ √ņĻķMaxellĻęňĺňýŅ™∑ĘĶń≥¨ľ∂ĶÁ»›∆ų“—‘ŕłų÷÷ņŗ–ÕĶÁ∂Į≥Ķ…Ō∂ľĶ√ĶĹŃľļ√”¶”√°£ ĪĺŐÔĻęňĺ‘ŕ∆šŅ™∑Ę≥ŲĶńĶ໿īķļÕĶŕňńīķ»ľŃŌĶÁ≥ōĶÁ∂Į≥ĶFCX-V3ļÕFCX-V4÷–∑÷Īū Ļ”√Ńň◊‘––Ņ™∑Ę—–÷∆Ķń≥¨ľ∂ĶÁ»›∆ųņī»°īķ∂ĢīőĶÁ≥ō, ľű…ŔŃň∆Ż≥ĶĶń÷ōŃŅļÕŐŚĽż, ĻŌĶÕ≥–߬ ‘Ųľ”, Õ¨ ĪŅ…‘ŕ…≤≥Ķ ĪĽō ’ń‹ŃŅ, ≤‚ ‘ĹŠĻŻĪŪ√ų, Ļ”√≥¨ľ∂ĶÁ»›∆ų Ī»ľŃŌ–߬ ļÕľ”ňŔ–‘ń‹ĺýĶ√ĶĹ√ųŌ‘ŐŠłŖ, ∆Ű∂Į Īľš”…‘≠ņīĶń10 minňű∂ŐĶĹ10 s
ĪŪ3 ĻķÕ‚≥¨ľ∂ĶÁ»›∆ųľľ űŌ÷◊īTable 3 State of art for supercapacitor technology Ō¬‘ō‘≠Õľ
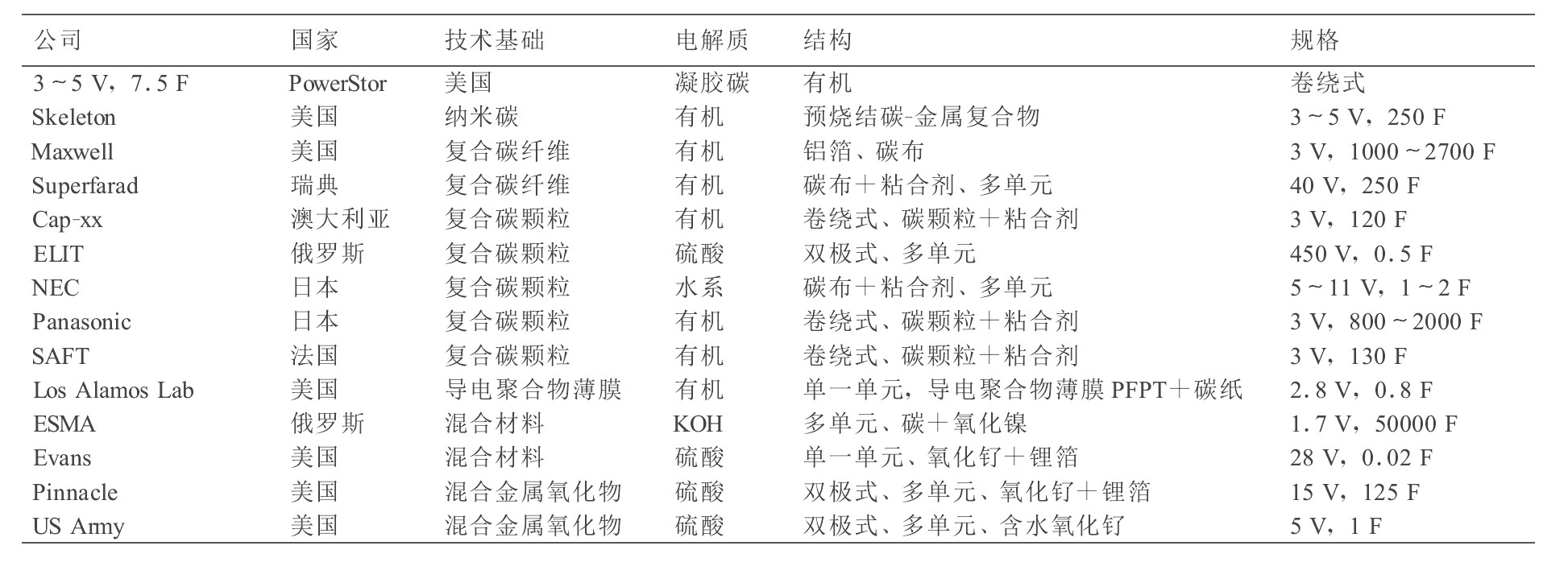
ĪŪ3 ĻķÕ‚≥¨ľ∂ĶÁ»›∆ųľľ űŌ÷◊īTable 3 State of art for supercapacitor technology
‘ŕő“Ļķ, ĪĪĺ©”–…ęĹū Ű—–ĺŅ◊‹‘ļ°Ę Ĺű÷›ĶÁѶĶÁ»›∆ų”–Ōř‘ū»őĻęňĺ°Ę ĪĪĺ©Ņ∆ľľīů—ß°Ę ĪĪĺ©ĽĮĻ§īů—ß°Ę ĪĪĺ©ņŪĻ§īů—ß°Ę ĪĪĺ©Ĺū’ż∆ĹĻęňĺ°Ę Ĺ‚∑ŇĺŁ∑ņĽĮ‘ļ, ĻĢ∂ŻĪűĺř»›Ļęňĺ°Ę …Ōļ£į¬ÕĢĻęňĺĶ»“≤‘ŕŅ™’ĻĶÁ∂Į≥Ķ”√≥¨ľ∂ĶÁ»›∆ųĶńŅ™∑Ę—–ĺŅĻ§◊ų, Ļķľ“ ģőŚľ∆Ľģ°į863°ĪĶÁ∂Į∆Ż≥Ķ÷ōīů◊®ŌÓĻ•Ļō÷–“—ĹęĶÁ∂Į≥Ķ”√≥¨ľ∂ĶÁ»›∆ųĶńŅ™∑ĘŃ–»Ž∑Ę’Ļľ∆Ľģ°£
ĪĪĺ©”–…ęĹū Ű—–ĺŅ◊‹‘ļ≤…”√ĽÓ–‘ŐŅ÷–ŐŪľ”ń…√◊ŐľĻ‹÷∆◊ųŃň≥¨ľ∂ĶÁ»›∆ų”√ľę∆¨, »ÁÕľ2ňý ĺ°£ Ķ—ťĹŠĻŻĪŪ√ų, ŐŪľ”Őľń…√◊Ļ‹Ņ…ĹĶĶÕĶÁ»›∆ųľę∆¨ńŕ◊Ť, ŐŠłŖĶÁ»›∆ų–‘ń‹°£ Ņ…ľŻ, ń…√◊Őľ≤ńŃŌ∂‘ŐŠłŖ≥¨ľ∂ĶÁ»›∆ų–‘ń‹, ŐōĪū «ŐŠłŖ∆šń‹ŃŅ√‹∂», ŐŠłŖŃň»ę–¬Ķń∑Ę’ĻŅ’ľš°£
4 ’Ļ ÕŻ
≥¨ľ∂ĶÁ»›∆ų”…”ŕĺŖĪłłŖĪ»Ļ¶¬ °Ę ≥§—≠Ľ∑ Ŕ√ŁĶ»”Ň ∆, ńŅ«į“—”¶”√”ŕľ∆ň„ĽķĪł”√ĶÁ‘ī°Ę –ŇļŇĶ∆ĶÁ‘īľį”Ž»ľŃŌĶÁ≥ō°Ę ńÝ«‚ĶÁ≥ōĶ»∂ĮѶĶÁ≥ōłīļŌ◊ųő™ĶÁ∂Į∆Ż≥ĶĶń∂ĮѶĶÁ‘ī°£ ňś◊ŇĶÁ∂Į≥Ķ—–ĺŅĶń–ň∆ū, ≥¨ľ∂ĶÁ»›∆ų÷ō“™Ķń—–ĺŅ∑ĹŌÚ÷ģ“Ľ «Ĺę∆š”ŽłŖĪ»ń‹ŃŅĶń–ÓĶÁ≥ōѨ”√, ‘ŕ≥ĶŃĺľ”ňŔ°Ę …≤≥ĶĽÚŇņ∆¬Ķń ĪļÚŐŠĻ©≥ĶŃĺňý–ŤĶńłŖĻ¶¬ , ‘ŕ≥ĶŃĺ’ż≥£–– Ľ Ī‘Ú”…–ÓĶÁ≥ō≥šĶÁĽÚ”…≥ĶŃĺ…≤≥Ķ Īňý≤ķ…ķĶńĶÁń‹≥šĶÁ, ľű…Ŕ∆Ż≥Ķ∂‘–ÓĶÁ≥ōīůĶÁŃų∑ŇĶÁĶń“™«ů, īÔĶĹľű…Ŕ–ÓĶÁ≥ōĶńŐŚĽżļÕ—”≥§–ÓĶÁ≥ō Ŕ√ŁĶńńŅĶń°£
ĪŪ4 “Ľ–©ňęĶÁ≤„≥¨ľ∂ĶÁ»›∆ųĶń–‘ń‹ [1]
Table 4 Properties of some double layer supercapacitor
| Ļęňĺ | ĶÁľę≤ńŃŌ | ĶÁĹ‚“ļ | ń‹ŃŅ√‹∂»/ (Wh°§kg-1) | Ļ¶¬ √‹∂»/ (W°§kg-1) |
FY |
Őľ | H2SO4 | 0.33 | - |
FE |
Őľ | H2SO4 | 0.01 | - |
Panasonic |
Őľ | ”–Ľķ»‹“ļ | 2.2 | 400 |
Evans |
Őľ | H2SO4 | 0.2 | - |
Maxwell-Auburn |
łīļŌŐľ/Ĺū Ű | KOH | 1.2 | 800 |
Maxwell-Auburn |
łīļŌŐľ/Ĺū Ű | ”–Ľķ»‹“ļ | 7 | 2000 |
Livermore National Laboratory |
Őľ (∆ÝńżĹļ) | KOH | 1 | - |
Sandia National Laboratory |
Őľ (ļŌ≥…) | ňģ»‹“ļ | 1.4 | 1000 |
Õľ2 ń…√◊Őľ≤ńŃŌ∂‘ĶÁ»›∆ųĹĽŃų◊ŤŅĻ–‘ń‹Ķń”įŌžFig.2 Influence of nano carbon tube on AC impedence of super capacitor
(a) ĹĽŃų◊ŤŅĻ Ķ°Ę–ťĻōŌĶ; (b) ∆Ķ¬ ”ŽĹĽŃų◊ŤŅĻń£ ż; (c) ∆Ķ¬ ”ŽňūļńĹ«ĻōŌĶ; (1) ļ¨5%ń…√◊ŐľĻ‹; (2) ≤Ľļ¨ń…√◊ŐľĻ‹
ńŅ«į, ≥¨ľ∂ĶÁ»›∆ųĶń—–ĺŅ÷ų“™őß»∆Őľ≤ńŃŌ’ĻŅ™, Ķę «÷∆ĪłĶńĶÁ»›∆ųĪ»ń‹ŃŅļ‹ĶÕ, ∂Ý«“–‘ń‹”–īżĹÝ“Ľ≤ĹŐŠłŖ°£ ń…√◊Őľ≤ńŃŌĶń≥ŲŌ÷ļÕ∑Ę’Ļő™≥¨ľ∂ĶÁ»›∆ųĶÁľę≤ńŃŌ—–ĺŅŐŠĻ©Ńň–¬Ķń∑Ę’Ļ∑ĹŌÚ, ĹęłÝ≥¨ľ∂ĶÁ»›∆ų–‘ń‹ŐŠłŖŐŠĻ©Ļ„ņęĶń∑Ę’Ļňľ¬∑ļÕŅ’ľš°£
≤őŅľőńŌ◊
[2] °°ConwayBE .°°Electrochemicalsupercapacitor.PlenumPublish ing, NewYork, 1999.
[3] °°Ń÷Ņň÷•, –ž—řĽ‘, »ő°°őį, Ķ».°°Őľń…√◊Ļ‹ĶÁĽĮ—ßīĘń‹Ķń—–ĺŅĹÝ’Ļ[J].ĶÁ‘īľľ ű, 2002, 26 (4) :314.
[4] °°’ŇĶ§Ķ§, “¶◊ŕł….°°īů»›ŃŅłŖīĘń‹√‹∂»ĶÁĽĮ—ßĶÁ»›∆ųĶń—–ĺŅĹÝ’Ļ[J].ĶÁ◊”‘™ľĢ”Ž≤ńŃŌ, 1999, 19 (1) :34.
[9] °°Ńű÷ĺŌť, ’Ň√‹Ń÷, …Ń°°–«, Ķ».°°«ß∑®ľ∂≥¨ľ∂ĶÁ»›∆ųĶń÷∆Īł[J].ĶÁ‘īľľ ű, 2001, 25 (5) :354.
[15] °°ľ™ŐÔ’——Ś.°°ĽÓ–‘ŐŅ÷∆ĪłĶńĶÁĽĮ—ßĶÁ»›∆ų.DenkiKagaku, 1998, 66 (9) :884.

