������ʱ��: 2017-05-10 14:49
ϡ�н��� 2018,42(08),814-819 DOI:10.13373/j.cnki.cjrm.xy17030034
���ʽTiNi�Ͻ�Ѫ��֧��֧�����ܵ�����Ԫ����
������ ����� ������ ������ ��Ծ
������ɫ�����о���Ժ����ҽ����е(����)����˾
ժ Ҫ��
ͨ���ı�֧�ܻ��ļ��β���, ������ʽTi Ni�Ͻ�Ѫ��֧�ܵ��������, ���ڸ������������в�Զ���ƿ�ѪҺ������ɵļ�ǻ������ע, �ӿ��ǻѪ˨�����̡�����Solidworks����������ʽ֧�ܻ�ģ��, ����ABAQUS����Ԫ����, �������ʵ�����̽����ͬ���β��������ʽ֧��֧�����ܵ�Ӱ��, �����֧�ܾ���֧����ʵ��Աȷ���, ��֤����Ԫ�����ĺ����ԡ��������:�����֧�ܺ����IJ���ѡ�������֧�������֧�����ܵ���Ҫ;��, ����֧��˿���������֧�ܻ�����, ������������֧�ܵ�֧������, ����������γ������ʹ֧�����ܽ���;˿��������γ��ȡ�����ȡ�֧�ܻ�������֧�����ܵ�Ӱ��̶����μ���;ͨ���Ż����β������֧�ܾ���֧������ʱ, Ӧ��������ƾ���֧�������ܳ����в���Ĥ�ɳ��ܵ���������;��Ʒ����֧������ʵ������ģ�����Ǻ϶ȽϺ�, ��֤������Ԫ�����ĺ����ԡ�
�ؼ��ʣ�
���ʽ֧��;�������в�;֧������;����֧����;����Ԫ����;
��ͼ����ţ� R318.08;TG146.23
����飺������ (1991-) , ��, ������ƽ��, ˶ʿ�о���, �о�����:TiNi�Ͻ�Ѫ��֧��;E-mail:ustb_stuchen@hotmail.com;;*�����, ���ڼ�������ʦ;�绰:13681313309;E-mail:ljt@grimed.com.cn;
�ո����ڣ�2017-03-19
���������п�ί�ƻ���Ŀ (Z161100000116010) ����;
Supporting Behavior of Bulge-Style Ti Ni Alloy Vascular Stents Based on Finite Element Analysis
Chen Zhouyu Li Juntao Ma Liancai Dong Yonghe Cui Yue
GRIMED Medical (Beijing) Co., Ltd., General Research Institute for Nonferrous Metals
Abstract��
By changing geometric parameters, a design of bulge-type stent was established to be used to isolate the continuous perfusion in the false lumen caused by the blood flow from distal tear of the aortic dissection. And the ultimate effect was to promote the process of thrombosis. The orthogonal experiment group, combining Solidworks and ABAQUS software, was designed to study the influence of the geometric parameters on its' supporting performance. The simulation was compared with the experimental results. The comparison results indicated that, the suitable parameter was the key to improve supporting performance of the stents. It would be optimized by increasing the wire diameter, increasing arrangement of stents and reducing the bulge part's length. The wire diameter and the bulge part's length had more remarkable influence on supporting performance than the bulge degree of the stents and arrangement of stents. It should also be noted that radial support force of the stents should be limited under the intimal flap's physiological limit. Experimental result of radial supporting force was consistent with the simulation, demonstrating the rationality of finite element analysis.
Keyword��
bulge-type stent; aortic dissection; supporting performance; radial supporting force; finite element analysis;
Received�� 2017-03-19
Ti Ni�Ͻ�Ѫ��֧���������õij�����������������, �����ٴ��õ�����Ӧ��, �ر����ڴ��������ܶ����Ȳ�λ[1]���ҹ��������������������в㲡��Ϊ��, �����ƿ�λ�ڽ���������Stanford B���������в�, �������������� (Thoracic Endovascular aortic repair, TEVAR) Ϊ��[2]����ȻTE-VAR�ܽ��ͼ�ǻѹ��, �ٽ���ǻѪ˨������, ��������Լв㲡����Ѫ�����ܴ���һ���ľ��ޡ����־����Զ���Զ��δ����ƿڴ��ڳ������еļ�ǻ������ע��ɵ�[3]�����ֳ����Ĺ�ע��ӯ����35%�����Լв㻼��TEVAR����Զ�ڷ�����������ǻ����, �����ڼ�ǻ�ij�����עʹ���������������ѡ���ǻ����, ���յ��¼в���������[4]��
Ϊ�˸���شٽ���ǻѪ˨������, ���о�����ѡ�������ʽϴ��֧��, ��Ϊ���Ƽв���Ĥ����ǻ��, �Դﵽ���Ч��[5]�������������һ�����ʽ֧������ֱͲ����֧�ܻ�����, �ı�֧�ܻ���״�����γɵ�����֧�ܽṹ, ֧���в�ͻ���γ�һ������ȶ������Ƽв���Ĥ (��ͼ1) �����о�ͨ������֧�ܻ������������, ��������Ԫ��������, �о�֧�ܵ�֧������, Ϊ��֧�ܵ��з��Ľ��ṩ����ָ����
1 ʵ��
1.1 �������豸
���о���֧�ܲ���ΪTi Ni�Ͻ�, �Ͻ���ѧ���ܲ���������[6], ��ȡ��ز�����Ϊ����Ԫģ��IJ������ԡ���Ʒ����֧�������Բ���ר�þ���֧������ (��ͼ2) ���в���, �Ի��֧����Ʒʵ�ʵľ���֧������С, ��֤����Ԫģ�����Ч�ԡ�
1.1.1 �����
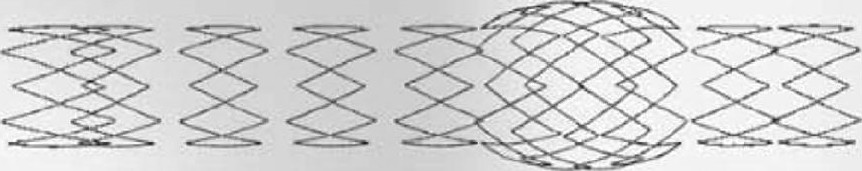
ͼ1 ���ʽ֧��Ч��ͼFig.1 Solidworks model of bulge-style stent's skeleton

ͼ2 ����֧������Fig.2 Radial compression testing machine
���ʽ֧��֧�ܻ�ģ�Ͳ���Solidworks 2014����, ѡ��֧ͬ�ܻ�����̽����֧��֧������Ӱ��, ��Ҫ����:˿���������֧�ܻ�����������γ��ȡ������4������, ����֧�ܳߴ�Ϊ��28 mm, ֧�ܻ��߶Ⱦ�Ϊ15 mm, 5������֧�ܻ�����������ʵ�鷨�������, ����������1��ʾ��
1.1.2 ������Լ������
��ģ�����ABAQUS6.13-4����, �����в���C3D10��Ԫ��������, �ڱ�֤���㾫��ǰ����, �ɽ������䲿�������֧�ܽԪ����Ŵ��� (��ͼ3) ��֧������������Ҫ��Ѫ�ܱ���Ӵ�, Ѫ�ܱڿɽ��Ƽ�Բ��Ͳ״, ͨ������֧�ܻ���Բ��Ͳ״ģ����ģ��Ѫ�ܵľ�����������, ����������λ�ƿ��Ʒ���, ����֧�ܻ���������ΪZ��, ��Բ��Ͳ����ʩ��15%λ���غɡ�֧�ܻ���Ѫ��ģ�;�Ϊ��ת�Գƽṹ, ��˿�ѡȡ֧�ܻ���1/5��ת��Ԫ���н�ģ��֧�ܻ��Գ�����������ת�Գ�����, ����֧�ܻ���ȡһ��̶�����˾���������������ɶ� (U2=U3=0, UR1=UR2=UR3=0) , �Ա�֤֧�������������в��ᷢ������λ����ת����Ϊ��֤����ͬʱ���η����Կ��ء�
��1 ����ʵ������Table 1 Orthogonal experimental design and result of stents ����ԭͼ
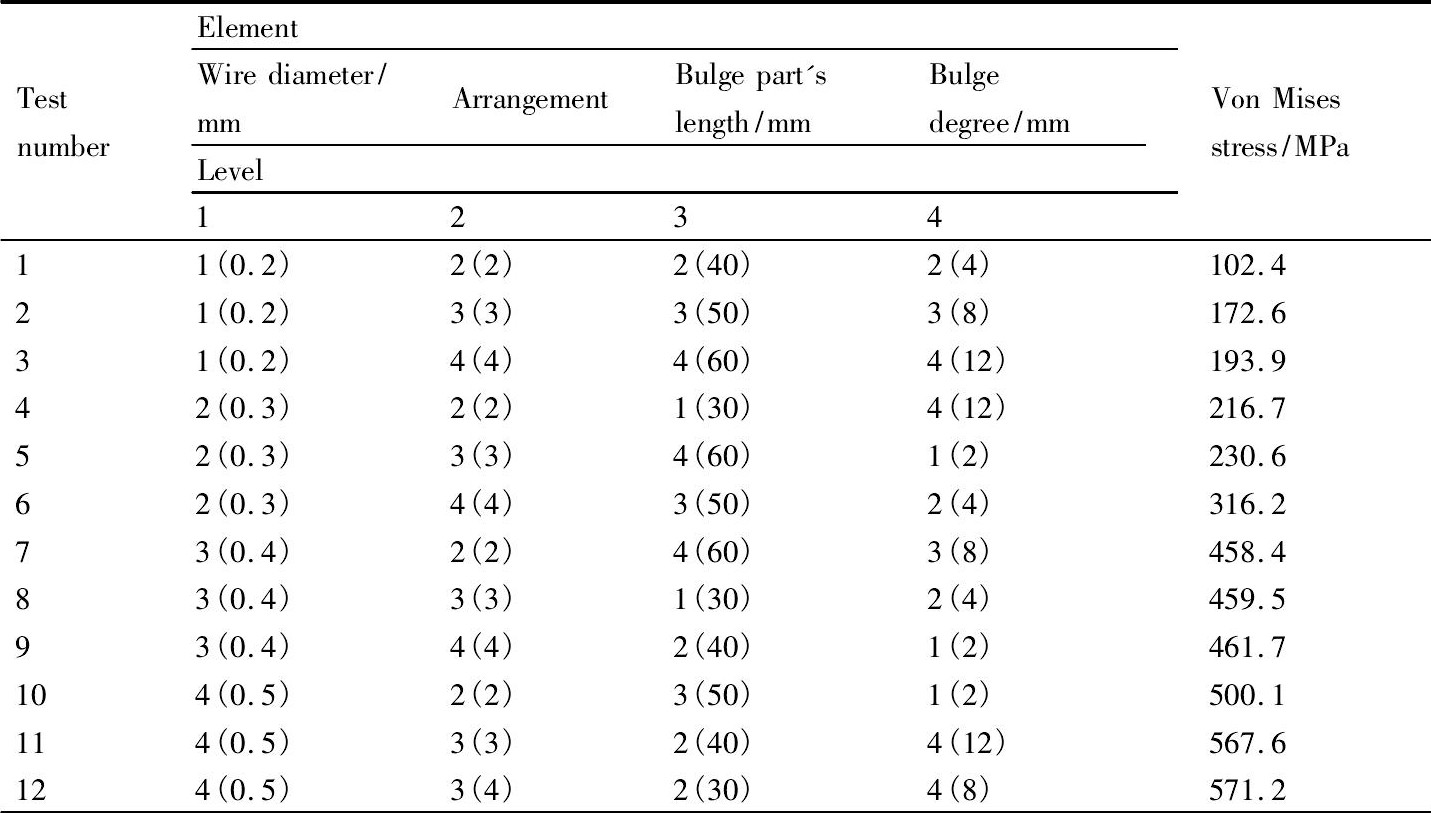
��1 ����ʵ������Table 1 Orthogonal experimental design and result of stents
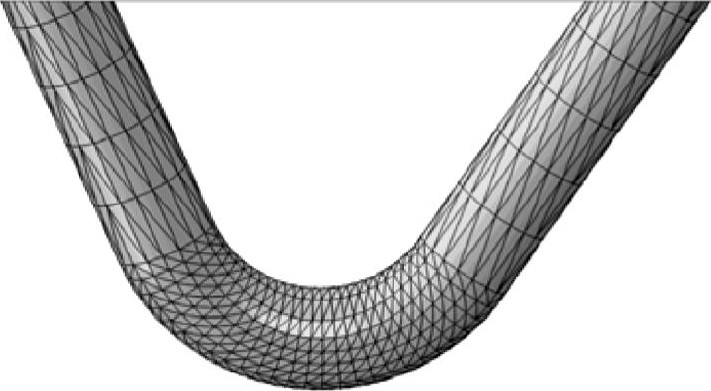
ͼ3 ֧������ͼFig.3 Finite element model of bulge-style stent
2 ���������
2.1 ���MisesӦ���ֲ�
������Ʒ��״�����ı仯, ���Ӧ������λ�þ�������֧�������ڽǴ� (ͼ4) , �����ױ���[7-10]���Ǻ�, ���������֧�ܵķ���������ֱͲ�ͻ���֧�ܽӽ����ڱ��о���Χ��, ��ͬѹ���������, ����ε�֧�ܻ����MisesӦ�������ϳ����Ȳ��仯��
�о�����[11], Ti Ni�Ͻ���ѭ���غ���������״����ЧӦ�ͳ����Իᷢ���˻�, �������ڽ���ѭ��Ӧ����ʼ�մ���ѹӦ����ѹӦ��״̬, �����֧�ܻ����������иô���Ӧ��״̬��Ϊ���ӡ���ѧ������ô���������Ϊ������ѹӦ����ѹӦ�乲ͬ�����²�������[12], ͬʱ���о�����[13], ѭ��Ӧ�����û�ʹTi Ni�Ͻ��Ӧ��Ӧ����Ӧ�����仯, ��������ƣ�Ͷ���, ���о���Ϊ, ��ѭ��Ӧ����, �����ڽ�Ӧ����Ӧ����Խϴ�, ���������Ա���, һ����Բ���α���Ӧ�뽻��Ӧ��Ƶ�ʲ�ƥ��, ����Ӧ��������Ӧ��ƣ��, ��ʱ���ڸô���������Դ����չ, ���տ��ܲ���֧�ܻ�����ʧЧ�IJ��������
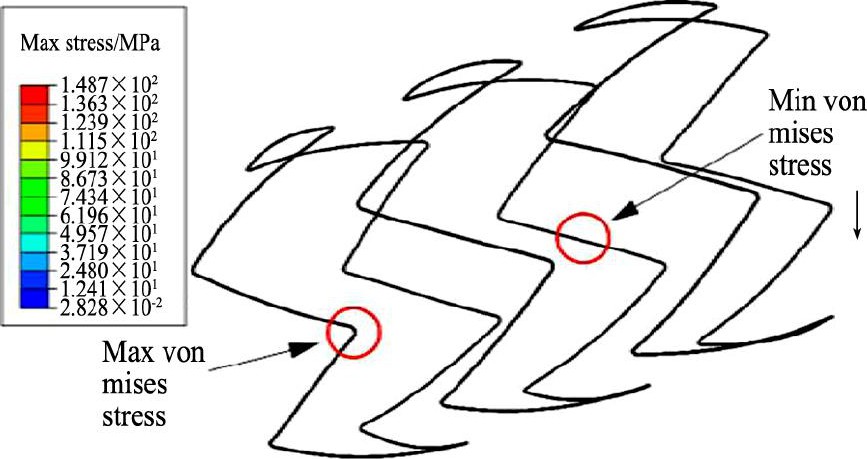
ͼ4 ���֧�ܻ����MisesӦ���ֲ����Fig.4Location of Max Von Mises stress of bulge-style part of stent
2.2 �������
�����ϵ�����ʵ�������з���, �ֱ����֧��˿����֧�ܻ�����������γ��ȡ�����ȵ�ƽ��ʵ��ָ��Kֵ�뼫��Rֵ, ���2��ʾ��
�ɼ����֪, ����ֵ��R (˿��) >R (����γ���) >R (�����) >R (֧�ܻ�����) , ������������ε�֧������, 4�������е�Ӱ���ɴ���С����Ϊ˿��������γ��ȡ�����ȡ�֧�ܻ�������
�����ص�ʵ��ָ��Kֵ��С��ӳ��ʵ�������ʵ��ָ��Ӱ��ij̶ȡ�˿����ƽ��ʵ��ָ��K1<K2<K3<K4, ����˿��Խ��, ֧�ŷ���Խ��, ��Ե�֧�����ܾ�Խ��;ͬ���ɻ��ƽ��ʵ��ָ��ֲ���֧�ܻ����� (K1<K2<K3) ������γ��� (K4<K3<K2<K1) �Լ������ (K2<K4<K1<K3) ���ɸ�ָ��ֲ���֪, ֧�ܻ������������֧�ܵ�֧�����ܳ������, ����γ����������֧�ܵ�֧�����ܳʸ����;����ȵ�ʵ��ָ��ֲ�����, ֧�������Ϊ8 mmʱ��֧������Ϊ�Ϻ�ˮƽ��
2.3 ����֧����������ʵ��Ƚ�
֧�� (��) �ľ���֧�����Ǻ���֧�����ܵ�һ����Ҫָ��, ���ʵľ���֧������������������ͨ·�ؽ��뼲������Զ�ڻָ�, ����ľ���֧�����Ի��������ڱڴ����µ��˺�[14], ��С�ľ���֧����������֧����λ[15]�����о�����ģ��������Ʒʵ��, �����ʽ֧�ܵľ���֧�����ܽ��з�����Ƚϡ�
��2 �����ص�Kֵ��RֵTable 2 Result of K and R ����ԭͼ
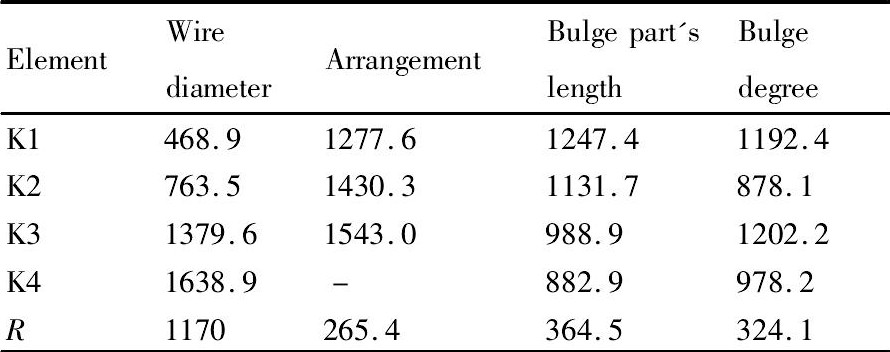
��2 �����ص�Kֵ��RֵTable 2 Result of K and R
Ӧ��״̬������֪������Բ��ΪѹӦ��������, ��Բ��Ϊ��Ӧ����������Ϊ�о�֧�����䴦����Ӧ��״̬, ��֧�ܻ������������������ʿ�, ��¶�������������ĵĽ��� (ͼ5) �����ݾ���ƽ���֪, ����ƽ�����ӦΪѹӦ��������������ƽ���Ӧ���ֲ���ͼ (ͼ6) ��֪, Ӧ������ѹ����ֱ���ϳʶԳƷֲ�����Ӧ�����е�Ч����, �õ���ƽ�������ܺ���ֵ��С, ����֧�ܻ�Ϊ��ת�Գƽṹ, ���ÿһ����������ƽ�����ܺ���ֵӦ���, �����ΪѹӦ����ģ�����õ��ľ���֧�ŷ�����ͼ7��ʾ���о�����[16], �������������в㲡��ʱ, ��Ѫ�ܱڵ���ѧ���ܽ��ᷢ�����Ա仯, �ڼв㻼���е�Ѫ�ܱ������ܵ�����Ӧ��ֵΪ1.719 N��mm-1 (��ͼ�к�ɫ����) , ��ʵ������12��ʵ����ľ���֧�������ڼ���ֵ, ������֧�ܵ���Ʋ�����Լв㲡���������Ӱ��, ����ʵ���龶��֧������С�ڼ���ֵ, ����Զ����Ч��������������ȫ�ġ�
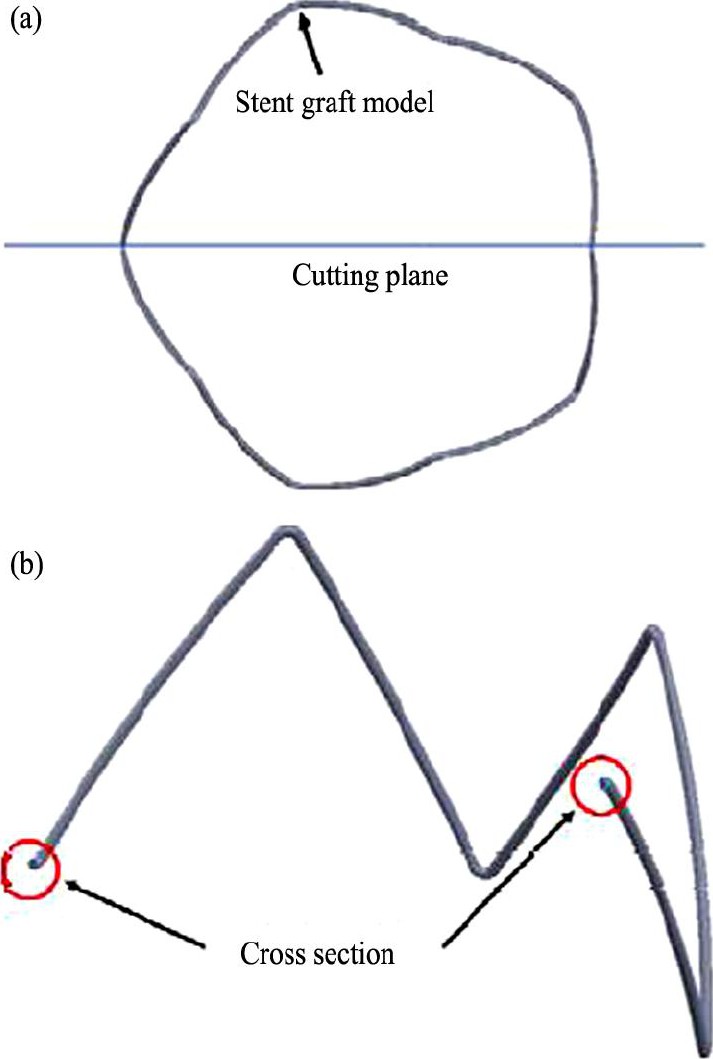
ͼ5 ֧�ܻ�ģ���г��������г���¶���Ľ���ʾ��ͼFig.5 Diagram of stent graft model with section cutting plane (a) and cross section (b)

ͼ6 ��������ƽ��Ӧ���ֲ�ͼFig.6 Stress contour of bending plane
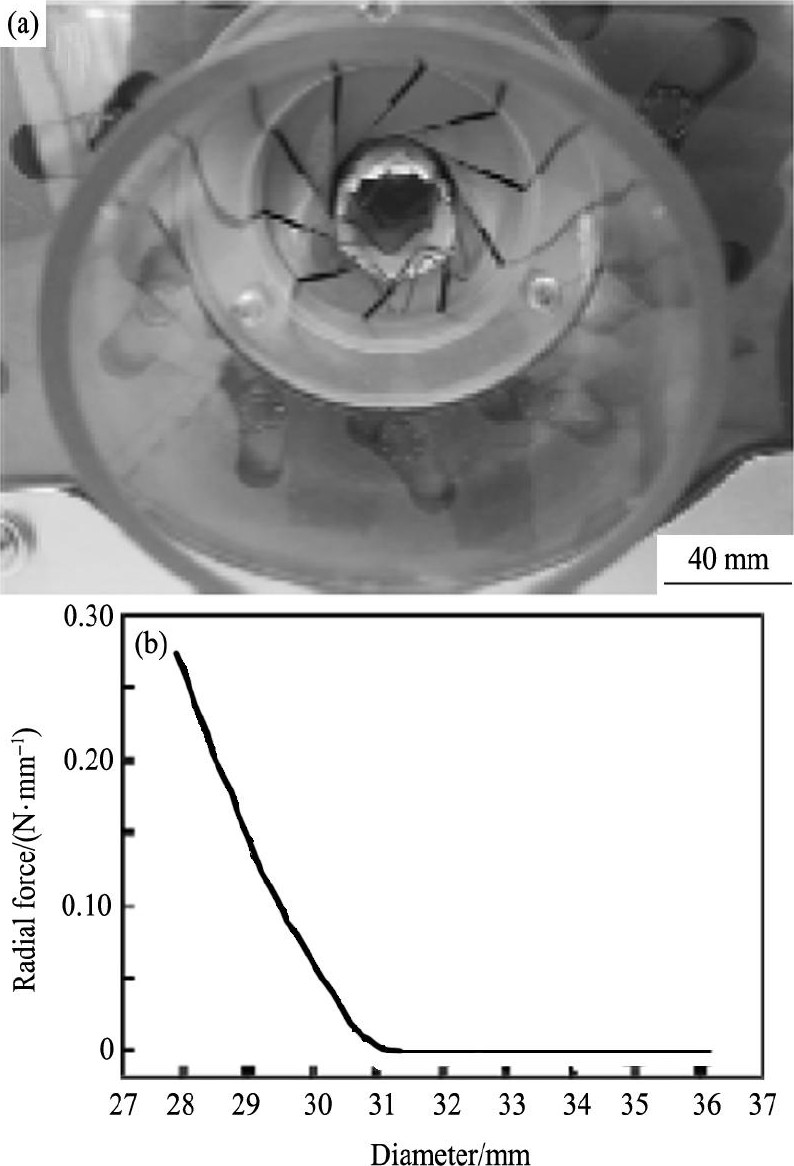
ͼ7 ֧����Ʒ��ֱ��������֧��������Fig.7 Stent sample (a) and diameter-curve (b)
�������ʽ֧����Ʒ, ͨ������֧�����Ƕ������֧�ܽ��о���֧��������, ���ʵ�������֧�ܵľ���֧����ֵ (ͼ7) , ����ģ�������бȽ� (ͼ8) , ��ͼ8�п�֪, ģ����������ֵ�Ǻ϶ȽϺ�;��ͼ8�м���������ģ������·�, ���о���Ϊԭ������Ǽ����Ʒ֧�ܻ��������ӷ�ʽΪ��������, ���Ӳ�������˿�ĵ�Ħ������������, �����������ģ�������Դ���һ���IJ�ͬ, ѹ�������д���һ����ת����
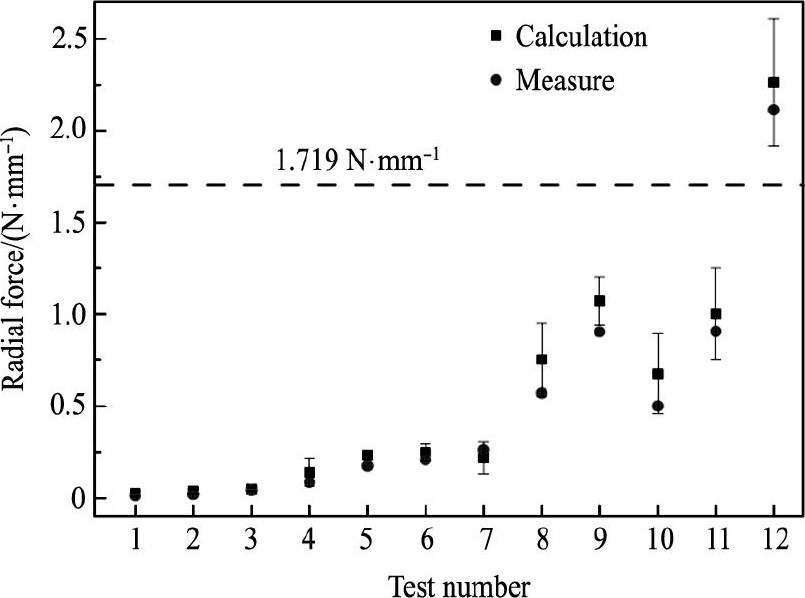
ͼ8 ģ������ε�λ���Ⱦ���֧����Fig.8 Radial force of stent by numerical simulation
3 ����
���ʽ֧�ܵ������Ϊ�˸��õشٽ��в��ǻѪ˨�����̡����ڼв�������������Ҫ��֧�ܵ�֧������������Ӹ��ӵ�Ҫ���ۺ����ϵ�ģ������ʵ�������֪:
1.�����֧������Ӱ��������, Ӱ��̶��ɴ���С����Ϊ˿��������γ��ȡ�����ȡ�֧�ܻ�������
2.����˿������������γ��ȡ�����֧�ܻ���������������ʽ֧�ܵ�֧������;���֧�ܲ���ͬʱ�迼���侶��֧�ŷ������ܳ����в���Ĥ��ǿ�ȼ�����֧�ܿ�ѹ������Ĵ�С��
3.����Ԫģ������֧�ܻ�����֧�������Խ���ǺϽϺ�, ����ģ�����ܹ���Ϊȷ���ж�֧����Ƶĺ�����, ��������Ԫ�����ܹ���Ч��������֧�ܵ��з�������ɱ���
�����
[1] Sun L Z.Aortic Surgery[M].Beijing:People's Medical Publishing House, 2012.380. (������.���������ѧ[M].����:��������������, 2012.380.)
[2] Wang X L, Fu W G.Summary of aortic dissection[J].Chinese Journal of Vascular Surgery, 2016, 8 (1) :1. (������, ��ΰ��.�������в����Ƶ��ֿ�[J].�й�Ѫ�������־���Ӱ�, 2016, 8 (1) :1.)
[3] K9lbel T, Diener H, Larena-Avellaneda A, Debus S.Advanced endovascular techniques for thoracic and abdominal aortic dissections[J].Journal of Cardiovascular Surgery, 2013, 54 (1) :81.
[4] Mani K, Clough R E, Lyons O T A, Bell R E, Carrell T W, Zayed H A, Waltham M, Taylor P R.Predictors of outcome after endovascular repair for chronic type b dissection[J].European Journal of Vascular&Endovascular Surgery the Official Journal of the European Society for Vascular Surgery, 2012, 43 (4) :386.
[5] K9lbel T, Carpenter S W, Lohrenz C, Avelaneda A L.Addressing persistent false lumen flow in chronic aortic dissection:the knickerbocker technique[J].Journal of Endovascular Therapy, 2014, 21 (1) :117.
[6] Gao Y L, Miao W D, Feng Z W, Cui Y, Wang Z G, Li J T.Ti-Ni alloy vascular stents'supporting performance with different design geometric parameters[J].Chinese Journal of Rare Metals, 2017, 41 (1) :8. (������, ������, ����ΰ, ��Ծ, �����, �����.���β�����Ti-Ni�Ͻ�Ѫ��֧��֧�����ܵ�Ӱ��[J].ϡ�н���, 2017, 41 (1) :8.)
[7] Cui S T, Jiang X Q, Yan J.Theoretical analysis of bending deformation of shape memory alloy beam[J].Chinese Journal of Applied Mechanics, 2016, 33 (1) :43. (������, ����Ȩ, �Ͼ�.��״����Ͻ��������������۷���[J].Ӧ����ѧѧ��, 2016, 33 (1) :43.)
[8] Shang Z J, Wang Z M.Nonlinear bending deformation of shape memory alloy beam[J].Journal of Mechanical Engineering, 2011, 47 (18) :28. (�����, ������.��״����Ͻ����ķ�������������[J].��е����ѧ��, 2011, 47 (18) :28.)
[9] Cui S T, Liu S L, Wang B, Zhang K.Research on bending properties for ideal pseudo-elastic shape memory alloy beam[J].Journal of Hefei University of Technology (Natural Science) , 2016, 39 (8) :1043. (������, ������, ����, �ſ�.α������״����Ͻ������������о�[J].�Ϸʹ�ҵ��ѧѧ����Ȼ��ѧ��, 2016, 39 (8) :1043.)
[10] Xing H R, Zhu M, Cui Y, Miao W D, Wang Z G, Ma J L.Finite element analysis and fatigue properties of TiNi vascular stent[J].Chinese Journal of Rare Metals, 2016, 40 (10) :976. (�Ϻ���, ����, ��Ծ, ������, �����, ������.Ti-Ni�Ͻ�Ѫ��֧�ܵ�����Ԫ������ƣ�������о�[J].ϡ�н���, 2016, 40 (10) :976.)
[11] El z.bieta A P, Katarzyna K G, Micha�bM, Maria S, Hisaaki T.Thermomechanical investigation of tini shape memory alloy and PU shape memory polymer subjected to cyclic loading[J].Procedia Engineering, 2014, 74 (9) :287.
[12] Zhang H J, Wang W Q, Qi M.Evaluation of self-expend stents'service performance with different design geometric parameters by finite element[J].Journal of Functional Materials, 2016, 47 (4) :94. (�Ż��, ��ΰǿ, ����.������֧�ܼ��β����Է���Ӱ�������Ԫ����[J].���ܲ���, 2016, 47 (4) :94.)
[13] Rao G B, Wang J Q, Han E H, Ke W.In situ study of evolution of stress induced martensitic transformation in Ti Ni shape memory alloy during cyclic deformation[J].Chinese Journal of Nonferrous Metals, 2005, 15 (1) :12. (�Ĺ��, ������, ������, ��ΰ.ѭ��Ӧ��������Ti Ni��״����Ͻ�Ӧ���շ������Ϊ�ݱ��ԭλ�о�[J].�й���ɫ����ѧ��, 2005, 15 (1) :12.)
[14] Dong Z H, Fu W G, Wang Y Q, Guo D Q, Xu X, Ji Y, Chen B, Jiang J H, Yang J, Shi Z Y, Zhu T, Shi Y.Retrograde type a aortic dissection after endovascular stent graft placement for treatment of type b dissection[J].Circulation, 2009, 119 (5) :735.
[15] Johnston C R, Lee K, Flewitt J, Gail M T.The mechanical properties of endovascular stents:an in vitro assessment[J].Cardiovascular Engineering, 2010, 10 (3) :128.
[16] Li Y S.The Study on Mechanical Properties of Thoracic Aorta and the Optimization of Constitutive Models for Numerical Simulation[D].Shanghai:Fudan University, 2014.37. (������.������ֵ���������������ѧ�����о�������ģ���Ż�[D].�Ϻ�:������ѧ, 2014.37.)