���±�ţ�1004-0609(2011)08-1997-06
Al����������λ�ѧ����Pb����
�����ˣ��¿��Σ��������������壬�� ������ Ԩ���� �£���ҵ��
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083)
ժ Ҫ���������λ�ѧ����Al�������ֱ�Ӷ���Pb����Ͻ𣬲����乤�����������Ż������������������ȶȶԶƲ������������Ӱ��̶Ƚϻ������ʱ��Ĵ����Ź��ȶȵ����ߣ����ǿ����Ѹ��������60 ��֮��仯�����ԡ������ι��ȶ�Ϊ60 �棬�������ʱ��2.5 minʱ���Ʋ��������нϺõĽ��ǿ��(0.76 MPa)���������м��������ĸ���SnCl2���Դٽ�Pb-Al-Sn��Ԫ�Ͻ���γɣ������Ʋ������Ľ��ǿ����ߵ�2.1 MPa���ϡ��ڻ�ѧ��֮�����ӽ���ԡ�������Ʋ��ڻ�ѧ�ƹ������γɵĿ�����Al�����������ס��ɷֿɵ���Pb���Ͻ�Ʋ㡣
�ؼ��ʣ����Σ���ѧ�ƣ�Al���壻Pb�Ʋ㣻���ǿ�ȣ�����ԡ
��ͼ����ţ�TF80���� ���ױ�־�룺A
Electroless Pb plating on Al substrate in molten salt
JIANG Liang-xing, HAO Ke-tao, L? Xiao-jun, LAI Yan-qing, HONG Bo, LI Yuan, LI Jie, LIU Ye-xiang
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Pb and its alloy film were prepared on the Al substrate in molten salt by electroless plating directly, and the procedure was improved. The results show that the superheat of molten salt has greater effect on the combination strength between the film and substrate than dipping time of substrate. With the increase of the superheat, the combination strength increases fast firstly. While the superheat is higher than 60 ��, the superheat has little effect on it. The film and substrate combined well when the superheat of molten salt and the dipping time of substrate are 60 �� and 2.5 min, respectively. The addition of auxiliary salt SnCl2 in molten salt can promote the interdiffusion of Al, Pb and Sn on the interface, and the combination strength can exceed 2.1 MPa. The metal bath procedure after electroless plating can mend the holes of the film, and a compact and composition adjustable Pb alloy film can be obtained on Al substrate.
Key words: molten salt; electroless plating; Al substrate; Pb film; combination strength; metal bath
����Pb����Ͻ���������������ϵ����������ʴ���ܶ��㷺��Ӧ������ɫ���������ȡ��Ǧ���ع�ҵ����Pb����Ͻ�Ҳ�����ܶȴ�ǿ�ȵ͡������Բ��ȱ�㣬�������ʵ��Ӧ���д����ܶ�IJ� ��[1-4]��������ɫ���������ȡ��ҵ�У���ϵ͵�ǿ�Ⱥ���������ܣ�ʹ�缫�������Ρ������������������̽ӡ���Ǧ�����У�Pb��դ������ռ�������������20%~30%���ǵ�������ܶȽϵ�(30~40 W?h/kg)����Ҫԭ��֮һ[5]��
Ϊ���ܹ��ڷ���Pb����Ͻ�������ʴ���ܵ�ͬʱ����ߵ缫�Ļ�еǿ�Ⱥ͵����ʣ�������缫������������ͼ���������ʻ�����㸴��Pb��Pb�Ͻ�����͵缫���ϡ�����Al���ܶȽ�ΪPb��1/4����������Pb��8��(������Ag��Cu)������ǿ����Pb��5�����ϣ��ҷǼ��������£�����Al��������Һ�п��γ����ܵı���Ĥ�����ڴˣ��ڽ���Al���渴��Pb����Ͻ𣬿����Ʊ���Al�����ʸ��ϵ缫�����ǣ�����Al-Pb��ϵ�ǵ��͵��ѻ�����ϵ[6]���ҽ���Al���к�ǿ�������ԣ���������ڽ϶̵�ʱ�����γ�һ��1 ~100 nm�������Ĥ[7]�������谭Pb�Ʋ���Al�������Ч��ϡ�Ϊ�ˣ�����ѡ��һ�ֺ��ʵķ�����Al�������Ԥ�ȶ���һ�����ܡ��ס���������õ�Pb����Ͻ�Ʋ㡣Ŀǰ��Al(��Al�Ͻ�)������Pb(��Pb�Ͻ�)һ����Ҫ���������ǰ��������[8-13]���������ν�п��Ԥ������Ԥ��ͭ�����������ȣ���Ȼ������߶Ʋ���������ǰ�������̲��跱������Ʒ���������ƣ������ɱ��ϸߣ���Ԥ�Ʋ�����������Ե绯ѧϵͳ��ɲ���Ӱ�졣�ź찲�ͳ¸ձ���[14]���� ��-Һ���Ϸ�����˫�������ϲ��ϣ����Ի���������õĸ��Ͻ��档YOLSHINA��[15-16]��TIMMONS��[17]��Al������뺬Pb���Ȼ��������н��л�ѧ��Pb����ý�������õ�Pb�Ʋ㡣�÷�������������Al�����������κ�Ԥ���������ǣ����������к���LiCl��KCl����LiCl�۸�Ϲ�KCl��ˮ���أ��������Ʊ��ɱ����Ѷȡ��ټ��ϸ�������ϵֻ�ܶ��ƴ�Pb�Ʋ㣬�ҶƲ��д��ڿ���������Ӱ�츴�ϵ缫���ϵ�Ӧ�á�
Ϊ�ˣ��������߶�Al�������ֱ�����λ�ѧ��Pb���ս����о����������γɷֺͻ�ѧ��Pb���ս����˸Ľ���ʹ֮�ܹ����������ס��ɷֿɵ���Pb�Ͻ�Ʋ㡣
1 ʵ��
1.1 �����Ʊ�
ʵ��ѡ�õ��Լ���Ϊ�������������Ȼ���(NaCl)���Ȼ���(CaCl2)���Ȼ�Ǧ(PbCl2)���Ȼ�����(SnCl2)������AlƬΪԭ�������ȴ���99.7%��
Al����������λ�ѧ��Pb�Ĺ��̰������²��裺1) ����������Ҫ�����һ�����ĸ�����Ȼ��������ȣ���������¯�м������趨���¶Ⱥ���3 h��2) AlƬԤ������AlƬ����200#��400#ɰֽ��ĥ��ˮϴ����ɴ��ã�3) ��ѧ��Pb���������õ�AlƬԤ����һ���¶ȣ�����������һ��ʱ���ȡ������ȴ��������ˮ�����γ�ϴ�ɾ������Pb�Ʋ㡣
1.2 ���Է���
����ɨ���������(PHILIPS XL30 ESEM)�۲�Ǧ�Ʋ�ı�����ò�ͽ�Ͻ��棬��������������(EDX)�ⶨ�Ʋ�ɷ֡�
�Ʋ������Ľ��ǿ��ͨ�����ܲ��������(CSS-44100)���ԶƲ�İ����������ۡ��������Ʊ�����Ϊ�����������Pb����Ͻ��AlƬ�и�� 10 mm��10 mm��С���û�����֬����Ʒ������ճ�ӣ��Ƴ���ͼ1��ʾ�������������ǿ���������֮��Ĺ�ϵ��ʽ(1)��ʾ��
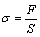 (1)
(1)
ʽ�У���Ϊ������ǿ�ȣ�Pa��SΪ��Ʒ�����m2��FΪ��������жƲ�ӻ������ʱ�������������������N��
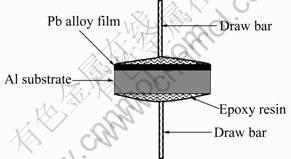
ͼ1 ���ǿ�Ȳ�������
Fig.1 Sample for combination strength tests
2 ���������
2.1 ���γɷݵ�ѡ��
�ѱ��������λ�ѧ��Ǧ������������ΪPbCl2��LiCl��KCl�Ļ������о��Ի�ѧ�Ƶ����γɷֽ��иĽ������ü۸�������õ�NaCl��CaCl2��PbCl2��ϣ�����Al������滯ѧ��Pb��ǰ�ڵ�̽��ʵ�鷢�֣������γɷּ��Ⱥ�ɵó���������Σ�������Al��������Ƶ�ƽ����Pb�Ʋ㡣
��PbCl2-CaCl2-NaCl��Ԫ��ϵ�У�����Ԫ��ϵ��NaCl-CaCl2�⣬��Ϊ������ϵ�����У�PbCl2-NaCl��Ԫ��ϵ�Ĺ�������PbCl2��Ħ������Ϊ70%�����������¶�ԼΪ410 �棬PbCl2-CaCl2��Ԫ��ϵ�Ĺ�������PbCl2��Ħ������Ϊ82%�����������¶�ԼΪ480 �档��NaCl-CaCl2��Ԫ��ϵ��NaClĦ������Ϊ47.9%��79.7%ʱ���ֱ����һ���������һ�������㣬���й����¶�Ϊ504 �档��ˣ������ƶ�PbCl2-CaCl2-NaCl��Ԫ��ϵӦΪ��һ��������Ĺ�����ϵ���ҹ����¶ȵ���410 �档���λ�ѧ�Ƶı��ʾ������ý���Al��Pb���ã�Pb2+�ڽ���Al���淢���û���Ӧ���ɽ���Pb�������������ʵ�Al���档��ˣ�Ϊ��֤��Ӧ���̵��ȶ�����Ҫ�������е�Pb2+�����Ƚϸߣ����ܹ��õ����ϲ��䡣����Ԫ������PbCl2�ĺ���ռ���֣�NaCl��CaCl2�ļ����������������ͽ��ͳ���������á�
�Բ�ͬ��ֵ�PbCl2-CaCl2-NaCl��Ԫ��ϵ�ij�������в��ԣ�����˸���ֵ�ij����¶ȣ��ӽ����ܺIJ���˶Ʋ���ò���ǣ�ѡ��PbCl2 83.2 g+NaCl 10.2 g+CaCl2 6.6 g��ϵ��ΪAl�������ֱ�ӻ�ѧ��Pb�����γɷ֣����Եõ�������¶�ԼΪ400 �档��Al�������õĶƲ����XRD������������ͼ2��ʾ����ͼ2�п��Կ���������Pb��������ʮ�ּ�����δ�����������ʷ壬��˵��ͨ�����λ�ѧ��������Al��������ýᾧ�����õĴ�Pb�Ʋ㡣
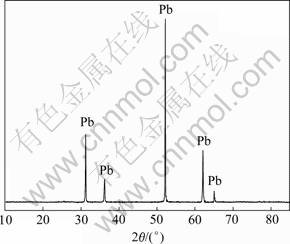
ͼ2 Al�������Pb�Ʋ��XRD��
Fig.2 XRD pattern of Pb film on surface of Al substrate
2.2 ���������Ż�
2.2.1 ���ȶ�
���γ�������ʵ��ʹ���¶�֮��IJ�ֵ����Ϊ���ȶȡ�һ��˵�������ε�ʵ��ʹ���¶ȶ�Ҫ����������¶ȣ�һ������Ա�֤����ʼ�մ�������״̬�����������õ������ԣ���һ�����¶ȶԻ�ѧ��Ӧ��ԭ����ɢ�ٶ�Ӱ��ϴ���Al���������л�ѧ��Pb��������������̬��Pbԭ���ܹ������ʵ���������ɢ�����ţ������������ߵĽ��ǿ�ȡ�
�̶�AlƬ��������ʱ��Ϊ3 min���ڲ�ͬ�Ĺ��ȶ��½���Al����������λ�ѧ��Pb��������Ʒ�Ľ��ǿ�Ƚ��в��ԣ�������ͼ3��ʾ����ͼ3�п��Կ��������Ź��ȶȵ����ӣ�Pb�Ʋ���Al����Ľ��ǿ�����ӣ��ҵ����ȶȵ���60 ��ʱ�����ǿ�������ٶȽϿ죻�����ȶȸ���60 ��ʱ�����ǿ�����ӷ��Ⱥ�С���ڹ��ȶ�Ϊ60 ��ʱ�����ǿ��Ϊ0.68 MPa��
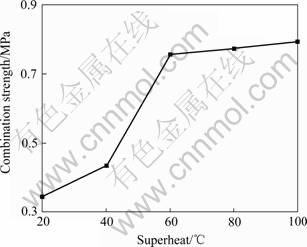
ͼ3 ���ȶȶԽ��ǿ�ȵ�Ӱ��
Fig.3 Effects of superheat on combination strength
�ڻ�ѧ��֮ǰ����Ҫ��AlƬ����Ԥ�ȣ���Ϊ�˷�ֹAlƬ�������ɹ��������Ĥ��Ԥ���¶�һ��С��100 �档��ˣ���AlƬ�������γ����Ƚ��������ʱ��Al������������һ���Ӳ�Ľ�ǣ���ֹ�û���Ӧ�Ľ��С�ֻ����Al������¶ȴﵽ���εij����¶�ʱ����DzŻῪʼ�ڻ������䡣���ȶ�Խ�ͣ����ʱ���Խ����������ʱ��һ��ʱ�������ķ�Ӧʱ���Խ�̡�һ����������л�ԭ������Pb��Խ�٣���һ���棬����Pb��Al������ɢ����Ƕ��ʱ��Խ�̣��Ӷ�Ӱ��Ʋ������Ľ��ǿ�ȡ������ȶȵ���60 ��ʱ�����ʱ����Խϳ����Ի�ѧ�ƹ��̵�Ӱ��ϴ�ʹ�öƲ������Ľ��ǿ������ȶȵ����Ӷ�Ѹ�����ӡ����¶ȼ�������ʱ��Al���ʱ��Ի�ѧ��Ӧ��Ӱ��������Ժ��ԣ��ҵ�Pbԭ�ӽ�Al������渲����ȫ���û���Ӧ�Ѷ�����Ӧ�¶ȵ����߶�������Ӧ��Ӱ���С���Ʋ������Ľ��ǿ����Ҫ��Pb��Al�������ɢ�����Ӱ�졣��Ȼ�¶�������������ɢ��������Al��PbΪ���͵IJ�������ϵ�������������γɶ�Ԫ�Ͻ𣬴Ӷ�����Pb��Al�������ɢ���ޣ����ǿ�Ȳ��ܵõ���Ч����ߡ��ʴӽ��ܽ��ĵĽǶȿ��ǣ�ѡ����ȶ�Ϊ60 �档
2.2.2 ����ʱ��
�̶����εĹ��ȶ�Ϊ60 �棬��AlƬ���������в�ͬʱ���Ʊ�Pb�Ʋ㣬������Ʒ�Ľ��ǿ�Ƚ��в��ԣ�������ͼ4��ʾ��
��ͼ4�п��Կ���������ʱ��Ի�����Ʋ�֮����ǿ�ȵ�Ӱ��Ϲ��ȶ�ҪС�Ķ࣬�ڲ��Ե�ʱ�䷶Χ�ڣ����ǿ����0.7~0.8 MPa�ķ�Χ�ڱ仯��������ʱ��С��2.5 minʱ�����ǿ�Ƚ�С��������ʱ�����2.5 min������ʱ��ļ����ӳ����Ʋ������Ľ��ǿ���������ߡ�������ʱ��Ϊ2.5 minʱ�����ǿ��Ϊ0.76 MPa�����ڹ��ȶȱ��ֲ��䣬AlƬ�ڽ��������еĽ��ʱ��㶨�����Ž���ʱ����ӳ����û���Ӧʱ��䳤����ͬ����Pbԭ����Al�������ɢ�����ޣ�����ѧ��ʱ�����2.5 minʱ����ɢ�ѻ������ͣ�ʱ����ӳ�����ɢӰ�첻�ʽ��ǿ��Ҳ�ͻ������ֲ��䡣��ˣ�ѡ��AlƬ����ʱ��Ϊ2.5 min����ʱ�Ʋ������Ľ��ǿ��Ϊ0.76 MPa��
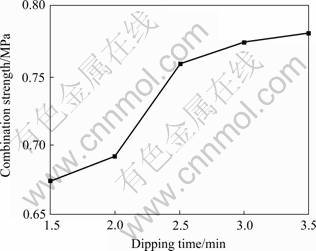
ͼ4 ����ʱ��Խ��ǿ�ȵ�Ӱ��
Fig.4 Effects of dipping time on combination strength
2.2.3 ����SnCl2
��ͼ3��4���Կ�����������Al��PbΪ��������ϵ����Al������ֱ�Ӷ��ƵĴ�Pb�Ʋ������Ľ��ǿ�Ƚϵ͡��ԶƲ������������Pb��AlԪ��EDX��ɨ�����(��ͼ5(a))���ڽ�Ͻ��洦������Pb��Al�Ĺ��ɲ㲻���ԣ����һ��֤��Pb��Al�������ɢ�dz����ޣ��������γ���Ч��ұ���ϡ���ˣ���Ҫ�������м���һ�����ĸ��Σ���Al�����϶���Pb�Ͻ�����߽��ǿ�ȡ�������ĸ�������������������1) ��������ϵӰ���С��2) �������Pb��Al���湲������3) �������Pb��Al�γ���Ԫ�Ͻ�
������[18]��֪��Sn����Pb-Al�Ͻ��п���С����Ļ��ܼ�϶����Pb-Al-Sn��Ԫϵ������������乲����ɷ�Ϊ38.1%Pb��61.7%Sn��0.08%Al���۵�Ϊ183 �档��ˣ��ڴ�Pb�Ʋ��м���Ԫ��Sn�����ڶƲ���Al�����γ�ұ���ϣ����ӽ��ǿ�ȡ��ټ��Ͻ���Sn�Ļ�ѧ������Pb���ƣ�����/��ԭ��λ���[19]��ʵ��������Al�ϵĹ������������Ͼ��п����ԡ�
�ڹ��ȶ�Ϊ60 �棬����ʱ��2.5 minʱ��������������һ������SnCl2���������öƲ��Sn�����������Ľ��ǿ�Ƚ��в��ԣ�������ͼ6��ʾ����ͼ6�п��Կ���������������SnCl2������������1%���ӵ�4%���Ʋ���Sn�������������ӣ��������SnCl2�ļ���������4%ʱ�������е�SnCl2���������û�����Pb�γɺϽ𡣵���������SnCl2�ļ�����ʱ�������ڼ��ȹ����л���������������������α��������һ��δ�����˵��SnCl2�������е��ܽ��Ѿ����ͻ���Ҫ���ߵ��ܽ��¶ȣ��Ӷ����¶Ʋ���Sn�����������ӡ�
��ͼ6�л����Կ����������м���SnCl2�ܹ�������߶Ʋ������Ľ��ǿ�ȣ�ǿ��ֵ�ɲ���SnCl2ʱ�ĵ���0.8 MPa���ӵ���2.1 MPa���ϡ�����������SnCl2�����������ӣ����ǿ��Ҳ������ߡ����ǿ�ȵı仯��Ʋ���Sn�������ֳ��ϺõĶ�Ӧ��ϵ������������SnCl2����������4%ʱ�����ǿ��Ѹ����ߣ�SnCl2����������4%֮���ǿ�ȱ仯�����ԡ���˵���������м�������SnCl2�����Ի��Pb-Sn�Ͻ�Ʋ㣬������������߶Ʋ������Ľ��ǿ�ȡ�
�����úϽ�Ʋ������Ľ�Ͻ������SEM�۲첢��Al��Pb��SnԪ�ؽ���EDX��ɨ�裬������ͼ5��ʾ����ͼ5�п��Կ������Ʋ�������Ͻ��ܣ���Ͻ���δ�����κο��ѡ���Ƥ�����Ҷ���һ���̶��Ϸ�����Ԫ�ص����ɢ���������м���SnCl2������ֵ�Pb��Al��2�ֺϽ�Ԫ�ص�Ũ���ݶȽ�δ��SnCl2ʱ�ĸ�����˵��Ԫ��Sn�ٽ��˽���Ԫ���ڽ�������ɢ���������γ�ұ���ϣ������ǽ��ǿ�ȴ������ߵ�ԭ�ԶƲ�ijɷֽ���EDX�������֣���������SnCl2������Ϊ3%(��������)ʱ���Ʋ��г���Sn�⣬������1.52%(��������)��Al�����һ����֤��������ۡ�ͬʱ���Ʋ��н���Al�Ĵ��ڣ��������ڶƲ���ȫ���ǻ���ʱ�û���Ӧ�ļ��������������ӶƲ�ĺ�ȡ�

ͼ5 �Ʋ�������Ͻ����EDX��ɨ��
Fig.5 EDX linear scanning of interface between substrate and film: (a) Without SnCl2; (b) With SnCl2
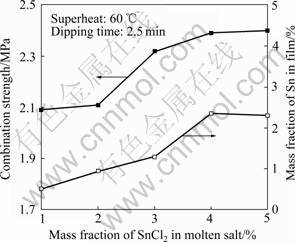
ͼ6 ������SnCl2�������ԶƲ��Ӱ��
Fig.6 Effects of addition of SnCl2 in molten salt on film
2.2.4 ����ԡ����
�������������½��л�ѧ������Pb-Sn�Ʋ�ı�����ò����SEM�۲죬������ͼ7(a)��ʾ����ͼ7(a)�п��Կ��������öƲ㲢����ȫ���ܣ�����ֱ��Լ50 ��m�Ŀ�������YOLSHINA��[9]�ı���һ�¡����ij��֣�һ������Ϊ�û���Ӧ��ͨ����ʹPb2+�ܹ���Al����Ӵ�����֤��Ӧ�ij������У���һ����ʹ�ò�����ʹ�ù��������ױ���ʴ�Խ���������������ĸ�ʴ������Ʒ����5 mol/L H2SO4��Һ�з��֣�����Լ10 h�Ľ��ݣ����ֶƲ���������롣ͬʱ���ɻ�ѧ�Ƶ�ԭ����֪��ͨ����ѧ����Al��������õ�Pb���Ͻ��������ޣ�����ֺ����ֲ������ƣ������ڶƲ����ܵĵ��ء�
�����һ���������߽���ѧ��֮�����Ʒ�������ε��µ�Pb���Ͻ������н��н���ԡ��������������Ʒ�������SEM�۲�(��ͼ7(b))���֣���ʹ�Ŵ�5 000�����Ʋ������Ȼ�dz����ܣ�û�з����κο���ͬʱ���Ʋ�ĺ���������ӣ��ɽ���ԡ֮ǰ��50 ��m�������ӵ�100 ��m���ң�����������߶Ʋ���������ԶƲ�ɷֽ���EDXԪ�ط�����֪���Ʋ�ɷ����������ijɷ���ȫһ�¡�����Pb-1.0%Sn (��������)�����н���ԡ����֮�����Ʒ��5 mol/L H2SO4��Һ�н���3���£�δ�����κ���Ƥ������������˵���ڻ�ѧ��֮����н���������ƣ����ԶԻ�ѧ��֮��Pb�Ʋ�Ŀ�������Ч������óɷֿɿء�������Pb���Ͻ�Ʋ㡣

ͼ7 ����Al����Pb�Ʋ���ò
Fig.7 Morphologies of Pb film on Al substrate: (a) Before dip plating; (b) After dip plating
3 ����
1) ��PbCl2-NaCl-CaCl2������ϵ�н��л�ѧ�ƣ�����Al��������γ�Pb�Ʋ㡣�����εĹ��ȶ�Ϊ 60 �桢AlƬ�Ľ���ʱ��Ϊ2.5 minʱ������������Pb�Ʋ���Al�������ǿ����ߡ�
2) ����SnCl2�ļ��룬�ɴٽ�Ԫ��Pb��Al�ڽ�Ͻ�������ɢ���Ӷ���Al��������������ұ���ϵ�Pb-Al-Sn��Ԫ�Ͻ�Ʋ㣬�Ʋ���ǿ����δ��SnCl2ʱ��0.8 MPa������ߵ�2.1 MPa���ϡ�
3) �ڻ�ѧ��֮�����ӽ���ԡ�������Ч�����Ʋ����Ŀ��������ӶƲ��ȣ�������ܡ���Pb���Ͻ�Ʋ㣬�Ӷ������߸��ϵ缫�������ḯʴ���ܡ�ͬʱ���ɶ�Al��������Pb���Ͻ�Ʋ�ɷֽ��е��أ����������ϵ�Ӧ�÷�Χ��
REFERENCES
[1] YAN Mi-lin, ZHAO Wen-zhen. Influence of temperature on corrosion behavior of PbCaSnCe alloy in 4.5 M H2SO4 solution[J]. Journal of Power Sources, 2010, 195: 631-637.
[2] PEIXOTO L C, OS?RIO W R, GARCIA A. Microstructure and electrochemical corrosion behavior of a Pb-1wt%Sn alloy for lead-acid battery components[J]. Journal of Power Sources, 2009, 192: 724-729.
[3] LAI Yan-qing, JIANG Liang-xing, LI Jie, ZHONG Shui-ping, L? Xiao-jun, PENG Hong-jian, LIU Ye-xiang, ZHONG Shui-ping, L? Xiao-jun. A novel porous Pb-Ag anode for energy-saving in zinc electro-winning (Part ��): Laboratory preparation and properties[J]. Hydrometallurgy, 2010, 102: 73-80.
[4] LAI Yan-qing, JIANG Liang-xing, LI Jie, ZHONG Shui-ping, L? Xiao-jun, PENG Hong-jian, LIU Ye-xiang. A novel porous Pb-Ag anode for energy-saving in zinc electro-winning (Part ��): Preparation and pilot plant test of large size anode[J]. Hydrometallurgy, 2010, 102: 81-86.
[5] ������. Ǧ�����ع���ѧ����[M]. ����: ��е��ҵ������, 2009.
LIU Guang-ling. An introduction to technology of lead-acid battery[M]. Beijing: China Machine Press, 2009.
[6] �� ��, �Ծ���. �ѻ��ܺϽ����Ʊ�����[M]. ������: ��������ҵ��ѧ������, 2002.
JIA Jun, ZHAO Jiu-zhou. Immiscible alloy and its preparation techniques[M]. Harbin: Harbin Institute of Technology Press, 2002.
[7] �� ��, �����, Фҫ��. �������Ͻ���ǰ�������ռ���ԶƲ�������Ӱ��[J]. �����Ϳ��, 2005, 24(10): 20-21.
ZHANG Feng, WANG Xu-hui, XIAO Yao-kun. Pre-plating processes and their influences on deposit adhesion for aluminum and its alloy[J]. Electroplating & Finishing, 2005, 24(10): 20-21.
[8] ������, �� ǿ, ����Զ, �� ��, �� Ƽ, ��Ԫ��. �������Pb-Sn�Ͻ��ռ��Ʋ������о�[J]. ����뾫��, 2006, 28(4): 5-9.
WANG Yuan-yuan, XU Qiang, TANG Zhi-yuan, SU Peng, LIU Ping, LIU Yuan-gang. Study on the technology of Pb-Sn alloy electroplating on aluminium and the performance of the coating[J]. Plating & Finishing, 2006, 28(4): 5-9.
[9] ���鷼, ��־��, �����. ���Ͻ��ƹ����о�[J]. ��ʴ�����, 2003, 24(4): 162-163.
MA Hong-fang, LIU Zhi-bao, YIN Feng-ling. Electroplating of aluminum alloys[J]. Corrosion & Protection, 2003, 24(4): 162-163.
[10] �� ��. �������Ͻ�ĵ�ƹ�������[J]. ���漼��, 2000, 23(4): 3-5.
LI Jun. Review of the electroplating process of aluminum and its alloy[J]. Surface Technology, 2000, 23(4): 3-5.
[11] ��־��, �� ��, ף ��, ���ҳ�. �������Ͻ����ֱ�ӵ��Ǧ����[J]. ���ϱ���, 2009, 42(7): 36-38.
YANG Zhi-hong, HUANG Hui, ZHU Xing, GUO Zhong-cheng. Process for direct lead electroplating of aluminum and its alloy[J]. Materials Protection, 2009, 42(7): 36-38.
[12] ������, �� ǿ, ����Զ. Ǧ������������դ����Ʋ�ĵ绯ѧ�����о�[J]. ��Դ����, 2008, 132(4): 233-235.
YU Zi-yang, XU Qiang, TANG Zhi-yuan. Study on electrochemical performances of deposit of aluminum light grid for lead-acid battery[J]. Chinese Journal of Power Sources, 2008, 132(4): 233-235.
[13] �� ��, ���Ƴ�, ����». ������Ͻ������Լ������о��뷢չ[J]. ���漼��, 2007, 36(5): 75-83.
LIU Dong, WANG Hao-cheng, SUN Rong-lu. Study and development on surface modification technology of aluminum and its alloys[J]. Surface Technology, 2007, 36(5): 75-83.
[14] �ź찲, �� ��. ͭ/�����ϲ��ϵĹ�-Һ���Ϸ��Ʊ���������ϻ���[J]. �й���ɫ����ѧ��, 2008, 18(3): 414-420.
ZHANG Hong-an, CHEN Gang. Fabrication of Cu/Al compound materials by solid-liquid bonding method and interface bonding mechanism[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(3): 414-420.
[15] YOLSHINA L A, KUDYAKOV V Y, ZYRYANOV V G. A lead-film electrode on an aluminium substrate to serve as a lead-acid battery plate[J]. Journal of Power Sources, 1999, 78: 84-87.
[16] YOLSHINA L A, KUDYAKOV V Y, ZYRYANOV V G. Development of an electrode for lead-acid batteries possessing a high electrochemical utilization factor and invariable cycling characteristics[J]. Journal of Power Sources, 1997, 65: 71-76.
[17] TIMMONS J B, ORSINO J A, BHARDWAJ R. High energy, light weight, lead-acid storage battery: USA, 6447954[P]. 2002-09-10.
[18] ������. Ǧ��Ǧ�Ͻ�[M]. ��ɳ: ���ϴ�ѧ������, 1996.
LI Song-rui. Lead and lead alloys[M]. Changsha: Central South University Press, 1996.
[19] ��˹��. Ǧ�����۶�Ԫ�Ͻ���[J]. ��ʴ�����, 2000, 21(2): 76-77.
WENG Si-xiong. Electroplating of lead-tin low melting binary alloy[J]. Corrosion & Protection, 2000, 21(2): 76-77.
(�༭ ����)
������Ŀ������ʡԺʿ����������Ŀ(06FJ4059)
�ո����ڣ�2010-12-20�������ڣ�2011-03-27
ͨ�����ߣ������壬���ڣ���ʿ���绰��0731-88830649��E-mail: csulightmetals03@163.com