采用动态热回流法制备莲花菌多糖
赵永亮1,侯启昌2,李磊1,郭家瑞1,崔羽佳1,李鹏1,王卫国1
(1. 河南工业大学 生物工程学院,河南 郑州,450001;
2. 河南广播电视大学,河南 郑州,450003)
摘 要:以莲花菌子实体为材料,采用动态热回流法制备莲花菌多糖。通过单因素试验和正交试验研究原料颗粒粒径、提取温度、溶液pH、液料比、溶剂回流率、提取时间对莲花菌多糖提取效果的影响,并将动态热回流法与传统热水浸提法进行比较。研究结果表明:动态热回流法制备莲花菌多糖的最佳工艺条件是:原料颗粒粉碎度为3 500 μm,提取温度为95 ℃,溶液pH为6.5,液料比为6.5?1.0,溶剂回流率为15%,提取时间为90 min,在此条件下,粗多糖得率可以达到13.98%,比传统热水浸提法提高16.1%,提取时间比传统法减少了3/4,溶剂用量比传统法减少了7/8。该方法可用于莲花菌多糖的规模化制备生产,亦可为其他真菌多糖及相关产品的大规模工业生产提供借鉴。
关键词:莲花菌(灰树花);多糖;动态热回流法
中图分类号:Q81;Q93;R9;R28 文献标志码:A 文章编号:1672-7207(2011)01-0038-08
Preparation of polysaccharides from Grifola frondosa using dynamic hot reflux extraction
ZHAO Yong-liang1, HOU Qi-chang2, LI Lei1, GUO Jia-rui1, CUI Yu-jia1, LI Peng1, WANG Wei-guo1
(1. School of Bioengineering, Henan University of Technology, Zhengzhou 450001, China;
2. Henan Broadcast University, Zhengzhou 450003, China)
Abstract: A novel method of dynamic hot reflux extraction for the preparation of polysaccharides from the fruitbody of Grifola frondosa was researched. The factors that affect the extraction of maitake polysaccharides including size of raw material particles, extraction temperature, pH, mass ratios of water to material, reflux rate of solvent and extraction time were studied by single factor test and orthogonal test. The extraction effect of dynamic hot reflux method was compared with that of traditional hot water distilling extraction. The results show that the optimal conditions of extraction with dynamic hot reflux technology are as follows: The size of raw material particles is 3 500 μm in diameter, extraction temperature is 95 ℃, mass ratio of water to material is 6.5?1.0, pH=6.5, reflux rate of solvent is 15%, extraction time is 90 min. In the optimal conditions, the maitake polysaccharides extraction rate of dynamic hot reflux method reaches 13.98% and rises by 16.1% compared with traditional hot water distilling extraction. And this novel method can shorten 3/4 time of extraction and save 7/8 of the extraction solvent. The method not only makes large-scale industrial production of maitake polysaccharides, but also can be a reference for large-scale industrial production of other fungal polysaccharides.
Key words:maitake(Grifola frondosa); polysaccharides; dynamic hot reflux
莲花菌(Maitake)又名灰树花(Grifola frondosa),是一种珍贵的食、药两用真菌,营养丰富,含有大量的生物活性物质。莲花菌的提取物莲花菌多糖具有明显的抗HIV(艾滋病病毒),抗肿瘤,改善免疫系统功能,调节血糖、血脂及胆固醇水平,降血压等作用[1-6]。特别是其抗肿瘤活性,Nanba等用灰树花多糖进行抗肿瘤实验,结果表明,灰树花多糖的抑瘤率达86.5%,比国际公认的抗癌生物免疫调节剂香菇多糖抑制率高32%[7]。随着人们对莲花菌多糖的理化性质、生理药理功能等研究的深入,莲花菌多糖广阔的开发应用前景已引起了人们的关注,关于莲花菌多糖提取方法的报道也不断出现。这些方法可以分为传统方法和新型方法2类。传统方法如热水浸提法,酸、碱浸提法等由于存在能源利用率低、溶剂用量大、损失多、生产周期长、生产难以满足生产和研究的需要。研究较多的新型方法有超声波辅助浸提法、酶法、微波辅助浸提法[8-10]等。与传统提取法相比,这些新方法都有提取率较高,节省时间,节约溶剂等特点[11-13]。但超声波法对仪器和容器的要求太高,目前只在实验室小规模研究使用;微波法的研究尚属起步,其工艺上有一些尚未解决的问题,如密闭式萃取时高温高压会破坏物质结构,开放式萃取时萃取不均匀等,因此,目前应用于工业生产的微波提取设备甚少;由于酶的生物特性,酶法提取中对温度及pH等反应条件的要求很严格,因此,对实验设备的要求较高,且酶法提取过程中,有可能改变原料中某些成分,产生新的化学物质[14-17] 。而且这3种新型方法均不能实现浸煮和浓缩的连续化操作,都不利于工业化大规模生产。鉴于此,本文作者以莲花菌子实体干品为材料,探讨了一种提取莲花菌多糖的新方法-溶媒多级循环动态热回流提取法制备莲花菌多糖的效果,并与传统热水提取法进行了比较,旨在为莲花菌多糖的工业化生产提供一定的借鉴。
1 材料及方法
1.1 实验材料及仪器
实验材料为:莲花菌子实体(Grifola frondosa),为市售干品。试验所用苯酚、硫酸、氢氧化钠、葡萄糖、乙醇等,均为分析纯。
实验仪器有:DHG-9140A电热恒温鼓风干燥箱(上海一恒科技有限公司制造);FA1204B电子天平(上海精密科学仪器有限公司制造);SJN Ⅱ-100热回流提取浓缩机组(天津隆业轻工机械有限公司制造);723N可见分光光度计(上海精密科学仪器有限公司制造);HH-4数显恒温水浴锅(河南智诚科技发展有限公司制造);YSW-40B万能粉碎机(北京燕山正德机械设备有限公司制造)。
1.2 试验方法
1.2.1 动态热回流法制备莲花菌多糖方案及工艺流程
制备莲花菌多糖的方案及工艺流程如图1所示。其基本过程及特点如下:把洗净、干燥并粉碎成适当大小的莲花菌子实体放入提取罐内,加入适量的水做溶媒,采用蒸汽加热,使溶媒在药材间循环流动;提取一定的时间后把提取液经过滤器过滤,直接送入双效浓缩器,浓缩罐Ⅰ产生的一次蒸汽可让浓缩罐Ⅱ利用(作为浓缩罐Ⅱ的热源),亦可冷凝后与浓缩罐Ⅱ的二次蒸汽冷凝成的热液体一起回流到常压的提取罐,作为新溶剂和热源,这样边提取边浓缩,直到得到符合工艺要求的浓缩中间体;冷却后将其泵入醇沉罐,用乙醇进行醇沉。最后过滤干燥,得到成品。
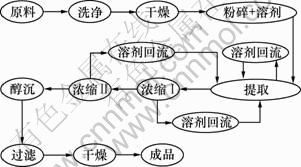
图1 动态热回流法制备莲花菌多糖工艺流程图
Fig.1 Flow chart of preparation of polysaccharides from grifola frondosa using method of dynamic hot reflux
1.2.2 单因素试验
选定6个可能影响多糖提取的因素,包括原料颗粒粉碎度、提取温度、溶液pH、液料比、溶剂回流率和提取时间。针对这6个因素,分别在保持其他因素不变的条件下进行单因素试验,每个水平试验重复3次,取其平均值,考察各因素对灰树花粗多糖得率、粗多糖含糖量及净多糖得率的影响,对结果做显著性分析。
将原料粉碎的颗粒粒径分为0.06,1.00,3.00,5.00和7.00 mm 5个等级,分别进行提取试验,以确定最佳的颗粒粉碎度。
在温度为60,85,90,95和100 ℃时分别进行提取,观察试验结果,以确定最佳提取温度。
分别在溶剂pH为4.0,5.0,6.0,7.0,8.0下进行提取,以确定最佳提取pH。
在液料比分别为4?1,5?1,6?1,7?1,8?1时进行提取,以确定最佳液料比。
在回流率分别为5%,10%,15%,20%,25%时进行提取,以确定最佳回流率。
提取时间分别为30,60,90,120和150 min时进行提取,以确定最佳提取时间。
1.2.3 正交试验
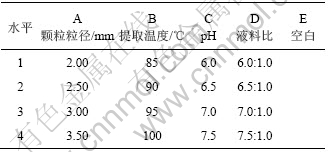
为了进一步优化莲花菌多糖的提取条件,根据单因素试验的结果,选取显著性分析为极显著的4个因素即颗粒粉碎度、提取温度、溶液pH、液料比为考察因素,以灰树花粗多糖得率作为考核指标,每个因素拟定4个水平,采用L16(45)正交表在溶剂回流率为15%,提取时间为90 min条件下进行正交试验,每个试验重复3次,取其平均值。正交试验因素水平如表1所示。
表1 动态热回流法制备莲花菌多糖正交试验因素水平表
Table 1 Factor level of preparation of polysaccharides from grifola frondosa
1.2.4 水分含量测定
采用干燥恒重法测定水分含量[18]。称取莲花菌子实体干品2 g于105 ℃下恒温干燥至恒重,测定其水分。试验重复3次,取其平均值。
1.2.5 莲花菌多糖含量测定
用苯酚-硫酸法测定多糖含量[19]。
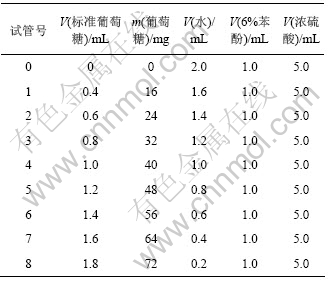
(1) 制作标准曲线:将40 mg/L标准葡萄糖溶液,6%苯酚和浓硫酸按照表2所示比例加入到试管中,静置10 min,摇匀,于室温下反应20 min后于波长490 nm下测吸光度,以2.0 mL水做空白样,以糖含量为横坐标,吸光度为纵坐标做出标准曲线,得到标准曲线回归方程为:y= 0.008 7x-0.005 9,R=0.999 5。
(2) 样品中多糖含量测定:准确称取干燥后的粗多糖150 mg于500 mL容量瓶中定容。吸取1 mL溶液测吸光度,通过标准曲线读出多糖含量。
1.2.6 传统热水浸提法制备莲花菌多糖
称取粉碎后(60 μm)的子实体干品100 g,加3 kg水,调pH至6.5,于98 ℃浸提3 h。在浸提过程中,保持浸提液体积恒定,重复提取2次,过滤后合并滤液,浓缩,用乙醇进行醇沉,干燥,测粗多糖得率[20-21]。
1.2.7 数据处理方法
单因素试验结果取3次重复试验的平均值,考 察粗多糖得率、多糖含量和净多糖得率3个指标。
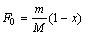
其中:F0为粗多糖得率;m为粗多糖质量;M为原料质量;x为含水量。
表2 苯酚-硫酸法试剂的配制
Table 2 Preparation of phenol-sulfuric acid reagent
净多糖得率为:

其中:d为多糖含量。采用方差分析法对单因素试验及正交试验结果进行统计学分析,用F检验判断组间差异有无显著性。
2 结果与分析
2.1 水分含量
干燥恒重法测得莲花菌子实体的含水量为10.12%。
2.2 动态热回流法制备莲花菌多糖单因素试验结果分析
2.2.1 不同原料粉碎颗粒度对莲花菌多糖提取效果的影响
在提取温度为95 ℃,溶液pH为7.0,液料比为7?1,溶剂回流率为15%,提取时间为90 min的试验条件下,不同的原料颗粒粒径对粗多糖得率、含糖量及净多糖得率的影响如图2所示。由图2可以看出:当颗粒粒径从0.06 mm升高到1.00 mm时,粗多糖得率从10.90%降低到8.77%,但含糖量从12.45%升高到了13.98%。这是因为颗粒粒径的不同,导致原料与溶剂的接触面积不同,对提取速度和多糖得率产生影响,颗粒粒径小,多糖溶出较快,但溶出的多糖所含杂质较多;当颗粒粒径为3.00 mm时,粗多糖得率达到最大的12.24%,含糖量为15.67%,净多糖得率1.91%,均达到最大值;颗粒粒径大于3.00 mm时,粗多糖得率、含糖量及净多糖得率均大幅度下降;当颗粒粒径为7.00 mm时,粗多糖得率仅为9.23%,净多糖得率也只有1.30%。因此,本试验认为颗粒粒径为3.00 mm时的效果最好。F检验结果表明:粗多糖得率F>F0.01,显著性p<0.01,原料颗粒粒径对粗多糖得率的影响是极显著的。
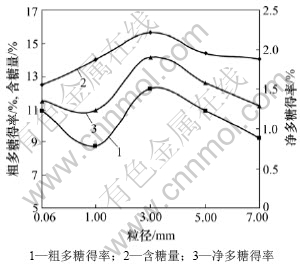
图2 颗粒度对莲花菌多糖提取效果的影响
Fig.2 Effect of raw material particle size on extraction of polysaccharides from grifola frondosa
2.2.2 不同提取温度对莲花菌多糖提取效果的影响
在原料颗粒粒径为3.0 mm,溶液pH为7.0,液料比为7?1,溶剂回流率为15%,提取时间为90 min的试验条件下,不同的提取温度对粗多糖得率、含糖量及净多糖得率的影响如图3所示。由图3可以看出: 60 ℃时,粗多糖得率仅为6.53%,95 ℃时达到了12.73%,净多糖得率也从1.21%升高到2.00%。高温能够提高产量是因为随着提取温度的升高,细胞壁的渗透能力和多糖的溶解度逐渐升高,促进了多糖的溶出。但当温度为100 ℃时,粗多糖的得率和净多糖得率均有所下降,可能的原因是过高的温度会破坏多糖的结构,使多糖含量减少。综合各方面因素考虑,本研究认为提取温度为95 ℃较为合适。F检验结果表明,粗多糖得率F>F0.01,p<0.01,温度对莲花菌多糖制备得率的影响达到了极显著水平。

图3 提取温度对莲花菌多糖提取效果的影响
Fig.3 Effect of temperature on extraction of polysaccharides from grifola frondosa
2.2.3 不同溶液pH对莲花菌多糖提取效果的影响
在原料颗粒粒径为3.00 mm,提取温度为95 ℃,液料比为7?1,溶剂回流率为15%,提取时间为90 min的试验条件下,pH对粗多糖得率、粗多糖的含糖量及净多糖得率均有较大影响。由图4可以看出:当pH小于7.0时,随着pH的升高,粗多糖得率和含糖量都升高;pH为7.0时的粗多糖得率为12.80%,是pH为4.0时粗多糖得率的2倍多;净多糖得率也从0.81%升高到1.95%;当pH从6.0升到7.0时,粗多糖含量、含糖量及净多糖得率只是略有增加;当pH为8.0时粗糖得率急剧下降到8.11%,由此可以推断:莲花菌多糖是一种弱酸或中性物质,其最佳提取pH范围为6.0~7.0。为了使工序更为简单(不用调节溶剂pH),以及从成本方面考虑,本试验选择最适pH为7.0。F检验表明,粗多糖得率F>F0.01,p<0.01,pH对粗多糖得率的影响达到了极显著水平。

图4 pH对莲花菌多糖提取效果的影响
Fig.4 Effect of pH on extraction of polysaccharides from grifola frondosa
2.2.4 不同液料比对莲花菌多糖提取效果的影响
在原料颗粒粒径为3.00 mm,提取温度为95 ℃,溶液pH为7.0,溶剂回流率为15%,提取时间为90 min的试验条件下,液料比对多糖提取效果的影响如图5所示。从图5可见:当液料比小于6?1时,随着液料比的升高,粗多糖得率、含糖量、净多糖得率均增加;当料液比为4?1时,粗多糖得率仅为6.41%,当液料比为6?1时,粗多糖得率达到最大的12.89%;当液料比为7?1时,虽然粗多糖得率为12.69%,比6?1时的略低,但含糖量为15.33%,净多糖得率为1.95%,均比液料比为6?1时的高。当液料比高于7?1后,粗多糖得率、含糖量、净多糖得率均没有明显变化;所以,综合考虑粗多糖得率,含糖量及净多糖得率,本实验认为液料比为7?1时最为适宜。F检验表明:粗多糖得率F>F0.01,p<0.01,液料比对粗多糖得率的影响达到了极显著水平。
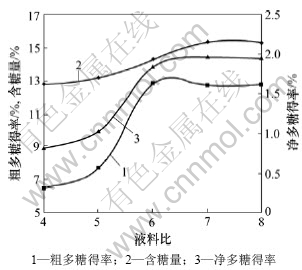
图5 液料比对莲花菌多糖提取效果的影响
Fig.5 Effect of mass ratio of water to material on extraction of polysaccharides from grifola frondosa
2.2.5 不同溶剂回流率对莲花菌多糖提取效果的影响
在原料粉碎颗粒粒径为3.00 mm,提取温度为95 ℃,溶液pH为7.0,液料比为7?1,提取时间为90 min时,不同溶剂回流率对提取效果的影响如图6所示。从图6可见:粗多糖得率及含糖量在回流率从5%到15%呈现增长趋势;当回流率为15%时,粗多糖得率为12.85%,含糖量也达到了15.48%。但F分析可以看出,粗多糖得率F<F0.05,p>0.05,溶剂回流率对粗多糖得率的影响并不显著。这是因为虽然动态热回流法能使药材与溶剂的浓度差(梯度)越来越大,从而使多糖溶出速度加快,但并不能对多糖得率产生明显影响(差异不显著)。当回流率超过20%时,多糖得率反而略有降低。原因是回流率过大,易造成浓缩罐内溶液蒸发过快,使多糖粘附在罐的内壁。因此,本试验选择15%为最适溶剂回流率。
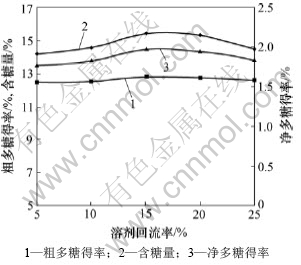
图6 溶剂回流率对莲花菌多糖提取效果的影响
Fig.6 Effect of reflux rate of solvent on extraction of polysaccharides from grifola frondosa
2.2.6 不同提取时间对莲花菌多糖提取效果的影响
在原料粉碎颗粒粒径为3.00 mm,提取温度为95 ℃,溶液pH为7.0,液料比为7?1,溶剂回流率为15%时不同提取时间对莲花菌多糖提取效果的影响如图7所示。从图7可以看出:随着提取时间的延长,粗多糖得率、含糖量和净多糖得率均增加;当提取时间为30 min时,粗多糖得率为9.68%,提取时间为90 min时,粗多糖得率达到12.76%,比30 min时增加了31.82%,可见,适当延长提取时间可以有效提高提取效果。但提取时间超过90 min后,粗多糖得率、含糖量、净多糖得率均无明显的升高,甚至当提取时间为150 min时,含糖量为15.09%,较90 min时的含糖量15.15%有所降低。这是因为可溶物质与溶剂的浓度梯度已经接近最大值,继续增加提取时间已很难使多糖析出,还可能是长时间高温使多糖结构受到破坏。因此,本试验选择90 min为最佳提取时间。F检验结果表明:粗多糖得率F>F0.05,p<0.05,提取时间对莲花菌多糖制备得率的影响达到了显著水平。
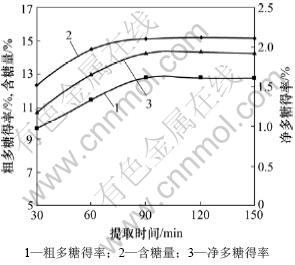
图7 提取时间对莲花菌多糖提取效果的影响
Fig.7 Effect of time on extraction of polysaccharides from grifola frondosa
2.3 正交试验结果分析
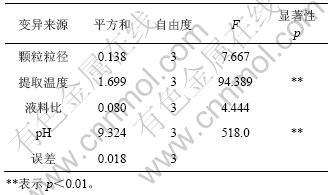
正交试验结果的极差分析结果见表3。从表3可以看出:颗粒粒径、提取温度、液料比、pH对多糖提取效果影响不同,其影响程度从大到小依次为:pH,提取温度,颗粒粒径和液料比。试验的最佳组合应为A4B3C2D2,即颗粒粒径为3.50 mm,提取温度为95 ℃,液料比为6.5?1.0,溶剂pH为6.5。从正交试验方差分析(表4)可以看出,pH和提取温度的影响达到了极显著水平,而颗粒粒径和料液比的影响均不显著。
表3 动态热回流法制备莲花菌多糖正交试验及极差分析结果
Table 3 Orthogonal test and range analysis results of extraction of polysaccharides from grifola frondosa using dynamic hot reflux method
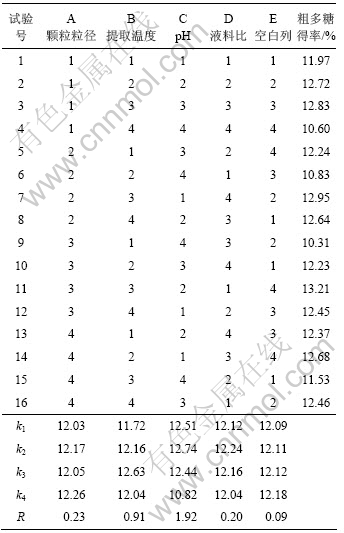
表4 动态热回流法制备莲花菌多糖正交试验方差分析
Table 4 Variance analysis of orthogonal test for extraction of polysaccharides from grifola frondosa using dynamic hot reflux method
综合单因素和正交试验结果,得出动态热回流法制备莲花菌多糖的最佳工艺条件如下:原料颗粒粒径为3.50 mm,提取温度为95 ℃,pH为6.5,液料比为6.5?1.0,溶剂回流率为15%,提取时间为90 min。
按照最佳提取条件做验证试验3次,莲花菌粗多糖得率分别为13.84%,13.98%和14.12%,平均值为13.98%。
2.4 热回流法与传统热水浸提法制备莲花菌多糖的效果比较
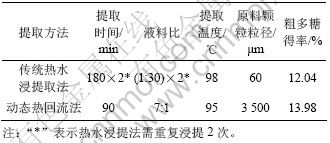
采用传统热水浸提法提取多糖3次,粗多糖得率分别为12.16%,11.65%和12.31%,平均值为12.04%。采用动态热回流法与传统热水浸提法的比较结果如表5所示。从表5可见:动态热回流法得到的多糖得率为13.98%,相对于传统热水提取法的得到的多糖得率12.04%,增幅达到16.1%。并且动态热回流法的提取时间比传统热水浸提法的提取时间减少3/4,提取液用量仅为传统热水浸提法的1/8,颗粒粒径远远比由传统方法所得的颗粒粒径大。
表5 动态热回流法与传统热水浸提法制备莲花菌多糖的效果比较
Table 5 Comparison of extraction of polysaccharides from grifola frondosa using dynamic hot reflux and traditional hot water distilling
3 讨论
动态热回流法的整个提取过程在一个密闭系统内进行,不会产生跑、冒、滴、漏现象,并且还能把提取浓缩过程中所产生的大量的一次/二次蒸汽经冷凝成热液体返回到提取罐内作为提取罐新的溶剂。一级浓缩罐中的蒸汽还可不冷凝直接作为二级浓缩罐新的热源,这样既可节省能源又能使药材与溶剂的浓度差(梯度)越来越大,大大加快有效成分的浸出速度,缩短提取时间。传统提取方法要求药材原料粉碎的颗粒粒径很小(<250 μm),以增大提取溶剂的接触面积,增加药物的浸出,但是,药材粉碎的粒径越小,就越不利于后续的离心、分离等操作。而动态热回流法不需要将药材粉碎的很小,靠不断回流溶剂增加浓度差,就保证了提取率,还有利于后续的离心和分离操作。
对于多糖制备效果多采用粗多糖得率作为考察指标,由于不同条件下制备的粗多糖的杂质含量不一致,仅用粗多糖得率表示提取效果显然不完善。本研究采用粗多糖得率、多糖含量和净多糖量3个指标,这样可以更充分、更科学地表示不同因素水平对莲花菌多糖制备效果的影响。
动态热回流提取法不需要非常贵重的设备,并且高效,节能,经济效益巨大。1个年产600 t莲花菌粗多糖(10%~15%)的工厂,若采用动态热回流工艺代替传统工艺,则每年可节约水24万多t,节约电480多万kW?h,约折合人民币374万元。按莲花菌粗多糖500元/kg计,每年可净赚2 300万元(成本按郑州市工业用电0.671元/(kW?h),工业用水2.28元/m3,灰树花60元/kg计算)。
4 结论
(1) 动态热回流法提取莲花菌多糖的最佳工艺条件如下:原料颗粒粒径3.50 mm,提取温度为95 ℃,pH为6.5,液料比为6.5?1.0,溶剂回流率为15%,提取时间为90 min。与传统热水浸提法相比,动态热回流法的粗多糖得率提高了16.1%,提取时间缩短了3/4,溶剂用量减少了7/8。
(2) 动态热回流法不仅经济效益显著,而且节能环保,具有重要的现实意义。该方法可用于莲花菌多糖的规模化制备生产,亦可为其他真菌多糖及相关产品的大规模工业生产提供借鉴。
参考文献:
[1] Inoue A, Kodama N, Nanba N. Effects of Maitake(Grifola frondosa) D-fraction on the control of the T lymph nodeTh1/Th2proportion[J]. Chem Pharm Bull, 2002, 25(4): 536-540.
[2] Nanma H, Kodama N, Sbchar D, et al. Effects of Maitake (Grifola frondosa) glucan in HIV-infected patients[J]. Mycoscience, 2000, 41(4): 293-295.
[3] Sasisekharan R, Raman R, Prabhakar V. Glycomics approach to structure-function relationships of glycosaminoglycans[J]. Annu Rev Biomed Eng, 2006, 8: 181-231.
[4] Tada R, Adachi Y, Ishibashi K, et al. An unambiguous structural elucidation of a 1,3-beta-D-glucan obtained from liquid-cultured Grifola frondosa by solution NMR experiments[J]. Carbohydr Res, 2009, 344(3): 400-404.
[5] Borchers A T, Krishnamurthy A, Keen C L, et al. The immunobiology of mushrooms[J]. Experimental Biology and Medicine, 2008, 233(3): 259-276.
[6] Chan W K, Law H K W, LIN Zhi-bin, et al. Response of human dendritic cells to different immunomodulatory polysaccharides derived from mushroom and barley[J]. International Immunology, 2007, 19(7): 891-899.
[7] Nanba H. Maitake mushroom-immune therapy to prevent from cancer growth and metastable[J]. Explore, 1995, 45(6): 18-23.
[8] 李磊, 王卫国, 郭家瑞, 等. 几株灰树花菌株液态发酵产多糖性能的比较[J]. 河南工业大学学报: 自然科学版, 2010, 31(2): 87-92.
LI Lei, WANG Wei-guo, GUO Jia-rui, et al. Comparative research on the capability of producing polysaccharides of several strains of Grifola frondosa in liquid fermentation[J]. Journal of Henan University of Technology: Natural Science Edition, 2010, 31(2): 87-92.
[9] 唐小俊, 池建伟, 何焕清, 等. 微波辅助提取灰树花多糖工艺研究[J]. 天然产物研究与开发, 2006, 18(5): 841-845.
TANG Xiao-jun, CHI Jian-wei, HE Huan-qing, et al. Microwave-assisted extraction technology of polysaccharides from Grifola frondosa[J]. Nat Prod Res Dev, 2006, 18(5): 841-845.
[10] Teo C C, Tan S N, Yong J W, et al. Evaluation of the extraction efficiency of thermally labile bioactive compounds in Gastrodia elata Blume by pressurized hot water extraction and microwave-assisted extraction[J]. Chromatogr A, 2008, 1182(1): 34-40.
[11] Teo C C, Tan S N, Yong J W, et al. Validation of green-solvent extraction combined with chromatographic chemical fingerprint to evaluate quality of Stevia rebaudiana Bertoni[J]. Sep Sci, 2009, 32(4): 613-622.
[12] 张士国, 邵伟国. 灰树花子实体多糖提取方法的比较[J]. 中国林副特产, 2005(2): 40-41.
ZHANG Shi-guo, SHAO Wei-guo. Comparison of the extracting methods of polysaccharides from Grifola frondosa hypha[J]. Forest By-Product and Speciality in China, 2005(2): 40-41.
[13] 郑亚凤, 谢宝贵, 徐培雄, 等. 正交法优化三种灰树花多糖提取工艺[J]. 食用菌, 2008, 30(5): 55-57.
ZHENG Ya-feng, XIE Bao-gui, XU Pei-xiong, et al. Optimization of three extracting techniques of polysaccharides of Grifola frondosa by the quadratic design[J]. Edible Fungi, 2008, 30(5): 55-57.
[14] 雷黎明, 胡志祥, 王先教. 微波技术在中药研究领域中的应用[J]. 湖南环境生物职业技术学院学报, 2006, 12(3): 278-282.
LEI Li-ming, HU Zhi-xiang, WANG Xian-jiao. Application of microwave technique in Chinese traditional medicine study field[J]. Journal of Hunan Environment-Biological Polytechnic, 2006, 12(3): 278-282.
[15] 张锦雀, 黄丽莺, 苏聪枚. 中草药多糖提取分离纯化研究进展[J]. 中药材, 2008, 31(11): 1760-1765.
ZHANG Jin-que, HUANG Li-ying, SU Cong-mei. Advances on the extraction, abruption and purification of polysaccharides from Chinese herbal medicine[J]. Journal of Chinese Medicinal Materials, 2008, 31(11): 1760-1765.
[16] 刘富梁, 金卫根, 梁华正, 等. 酶法在中药提取中的研究进展[J]. 时珍国医国药, 2006, 17(7): 1152-1153.
LIU Fu-liang, JIN Wei-gen, LIANG Hua-zheng, et al. Advances on application of enzyme to extraction of Chinese native medicine[J]. Lishizhen Medicine and Materia Medica Research, 2006, 17(7): 1152-1153.
[17] Hartonen K, Parshintsev J, Sandberg K, et al. Isolation of flavonoids from aspen knotwood by pressurized hot water extraction and comparison with other extraction techniques[J]. Talanta, 2007, 74(1): 32-38.
[18] 朱文学. 中药材干燥原理与技术[M]. 北京: 化学工业出版社, 2007: 31-35.
ZHU Wen-xue. Principle and technology on dryness of traditional Chinese medicinal materials[M]. Beijing: Chemical Industry Press, 2007: 31-35.
[19] 张惟杰. 糖复合物生化研究技术[M]. 2版. 杭州: 浙江大学出版社, 1994: 11-12.
ZHANG Wei-jie. The technology of biochemical study of glycoconjugates[M]. 2nd ed. Hangzhou: Zhejiang University Press, 1994: 11-12.
[20] 王卫国, 赵永亮, 包东武. 灰树花多糖的提取及纯化技术初探[J]. 郑州工程学院学报, 2002, 23(4): 60-63.
WANG Wei-guo, ZHAO Yong-liang, BAO Dong-wu. Preliminary study on isolation and purification of medicinal active component grifolan from Grifola frondosa[J]. Journal of Zhengzhou Institute of Technology, 2002, 23(4): 60-63.
[21] 王卫国, 赵永亮, 何泓良, 等. 一种制备真菌多糖的方法. 中国: ZL200810231540.5[P]. 2008-12-29.
WANG Wei-guo, ZHAO Yong Liang, HE Hong-liang, et al. A method on the preparation of fungal polysaccharides. China: ZL200810231540.5[P]. 2008-12-29.
(编辑 赵俊)
收稿日期:2010-04-10;修回日期:2010-07-23
基金项目:河南工业大学引进人才专项(2007BS023);河南省科技厅攻关计划项目(0124060026,0124060011)
通信作者:王卫国(1962-),男,河南汝州人,教授,从事微生物与生化药学研究;电话:0371-67756513;Email: wwgwang@yahoo.com.cn