DOI:10.19476/j.ysxb.1004.0609.2017.10.14
添加Si对Mg-Li合金储氢性能的影响
黄显吞1,覃昌生1,卿培林1,谢政专2,李柳杰2
(1. 百色学院 材料科学与工程学院,百色 533000;
2. 广西大学 物理科学与工程技术学院,南宁 530004)
摘 要:在氩气保护下,采用热处理并结合机械球磨合金化制备Mg90Li10+x%Si(x=0, 2, 5, 8(质量分数))合金储氢材料,研究Si的添加对Mg-Li合金储氢性能的影响。结果表明:Mg90Li10+x%Si(x=2, 5, 8)合金材料经过热处理和机械合金化后,Li容易扩散进入Mg晶格体内形成Mg(Li)固溶体,Si与Mg结合生成Mg2Si,而Mg2Si不仅能改善Mg-Li合金的吸/放氢动力学性能,而且还能提高Mg-Li合金的热力学性能。Mg90Li10+x%Si(x=0, 2, 5, 8)合金的初始脱氢温度从632 K(x=0)分别下降到了610 K(x=2)、598 K(x=5)和598K(x=8);Mg-Li合金的脱氢表观活化能为396.5 kJ/mol,而添加Si后,其分别下降了13.3 kJ/mol(x=2)、21.1 kJ/mol(x=5)和67.4kJ/mol(x=8)。
关键词:Mg-Li合金;淬火处理;催化作用;储氢性能
文章编号:1004-0609(2017)-10-2072-07 中图分类号:TG139 文献标志码:A
氢能因其清洁和高效而被认为是未来的理想能源,目前已经成为全世界研究和开发的热点[1-3]。在众多的固态储氢材料中,Mg和Li分别拥有高达7.6%和11.5%(质量分数)的理论储氢容量,一直是科学家们关注的焦点[4-6],但Mg氢化后热力学稳定性较高、吸/放氢动力学性能较差、Li化学活性很绐、不容易储氢,这些特性极大地限制了Mg-Li合金储氢材料的推广应用[7-9]。为充分利用Mg基储氢材料和金属锂氢化物LiH的各自优点,人们通过改进制备工艺手段和添加过渡族金属作为催化剂的方法都取得了较好的效果[10-13]。LU等[14]通过加氢活化机械球磨工艺制备Mg和Mg-10Ti,经测试发现Ti的添加提高了储氢容量和改善了Mg储氢性能;AMIRKHIZ等[15]研究Fe和Ti的协同作用发现Mg的吸/放氢温度降至523 K,与纯Mg相比,放氢温度降低170 K;HONG等[16]利用快速凝固法制备Mg-33Al合金,在623 K下30 min内就能放出3.17%(质量分数)的H;GOTO等[17]在2~5 GPa高氢压及973 K温度下处理Mg+LiH,成功合成储氢量高达5.65%的Mg2LiH5。
为改善Mg-Li体系的综合储氢性能,研究者们又对MgH2和LiH这两种高容量储氢材料进行复合研究。LENG等[18]制备出吸氢量最高可达8.8%(质量分数)的富锂三元合金Li70Mg10Si20;VAJO等[19]分别对比LiH+Si体系与MgH2+Si体系的储氢性能,结果显示LiH+Si体系在放氢过程中形成Li2.35Si,且可逆性好,但MgH2+Si体系在放氢过程中形成的Mg2Si可逆性差。为此,本文作者中利用Mg-Li体系具有较高的储氢容量以及二元相图中Li和Mg之间具有较高的固溶度等特点,以Mg90Li10体系为研究对象,适当添加Si元素,采用烧结液氮快冷热处理技术并结合机械合金化方法制备Mg-Li以及Mg-Li-Si合金储氢材料,研究Si的添加对Mg-Li固溶体材料综合储氢性能的影响。
1 实验
在氩气保护下,用高纯度的Mg粉(99.5% Alfa Aesar)和LiH粉(99.7% Alfa Aesar)按Mg90Li10的摩尔比均匀混合,然后利用压片机在2.5×106 Pa的压力下把混合粉末冷压成片状样品。随后把片状样品放入充有氩气保护的电阻烧结炉中,在温度为773 K下烧结2 h后立即将烧结过的样品在液氮中作快冷淬火处理。然后将淬火处理后的样品放入充满氩气的Etelux Lab2000手套箱(箱中水和氧的含量均小于0.1×10-6)中进行碾磨破碎,将破碎所得样品分别加入x% (x=0, 2, 5, 8(质量分数))的Si粉(99.9% Alfa Aesar),并将样品分别放入球磨罐中,采用行星式球磨机进行机械球磨,球磨时球料质量比为40:1,转速为300 r/min。其中,为使样品球磨均匀,每间隔5 h打开球磨罐一次进行敲罐处理,总的球磨时间为50 h。这样将制备所得的Mg90Li10+x%Si(x=0, 2, 5, 8)样品利用Rinku Miniflex- 3015型X射线衍射仪对合金的相结构进行测试,测试时采用Cu靶Kα辐射,采用步进式进行扫描,扫描步长为10 (°)/min,扫描范围为20°~80°。利用自制吸放氢测试仪对合金的吸放氢动力学性能进行测试,吸氢时最高氢压为7.0 MPa,放氢时最低氢压为1.1 kPa。使用Linseis STA PT-1000型同步热分析仪对合金进行DSC热分析测试,测试过程用纯度为99.999%的氩气加以保护,氩气流量为30 mL/min。
2 结果与讨论
2.1 合金的相结构分析
图1所示为Mg-Li合金材料烧结后以及Mg90Li10+x%Si(x=0, 2, 5, 8)机械球磨50 h后的XRD谱。从图1可知,Mg90Li10样品经过烧结和液氮快冷淬火热处理后,只出现Mg相,没有发现Li相,这说明通过烧结和液氮快冷淬火的热处理后,Li原子扩散进入了Mg晶格基体中,形成Mg(Li)固溶体。根据Mg-Li二元合金相图可知,在Li的含量小于17%(摩尔分数)时,其主要存在Mg的α相,其中α相是以Mg为基的固溶体,即Mg(Li)固溶体相,因此Mg90Li10中的Li应该是扩散固溶到Mg的基体中,形成Mg(Li)固溶体。同时,实验样品是按Mg90Li10的摩尔比制备所得,所以Mg90Li10为非化学计量比,是Mg-Li合金。而且,经过热处理再结合机械球磨50 h后,合金的相成分并未发生变化,样品主相仍然为Mg相,但添加Si混合球磨后,合金的衍射峰强度变宽,强度减弱,这意味着添加Si混合球磨有利于提高合金的非晶化程度。利用Scherrer公式,即 ,其中,D 为晶粒垂直于晶面方向的平均厚度;B为衍射峰半高宽度;
,其中,D 为晶粒垂直于晶面方向的平均厚度;B为衍射峰半高宽度; 为衍射角;
为衍射角;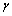 为X射线波长(0.154 nm),常数K=0.89。根据XRD谱中的2θ=37.1°、2θ=35.0°以及2θ=32.7°对应的衍射峰计算出Mg90Li10+x%Si(x=0, 2, 5, 8)合金球磨前后的平均晶粒尺寸,结果列于表1。由表1可知,烧结后Mg90Li10固溶体的晶粒尺寸为30.0 nm。而把烧结所得样品球磨50 h时后,Mg90Li10固溶体的晶粒尺寸下降到21.8 nm;如在Mg90Li10固溶体中添加质量分数为x%(x=2, 5, 8)的Si混合球磨后,合金的晶粒尺寸依次为22.7、18.8和15.7 nm,显然,在Mg90Li10固溶体中添加适当的Si有利于减小合金颗粒尺寸,提高球磨效率,且当添加量为x=8时合金颗粒尺寸最小,球磨效率最高。
为X射线波长(0.154 nm),常数K=0.89。根据XRD谱中的2θ=37.1°、2θ=35.0°以及2θ=32.7°对应的衍射峰计算出Mg90Li10+x%Si(x=0, 2, 5, 8)合金球磨前后的平均晶粒尺寸,结果列于表1。由表1可知,烧结后Mg90Li10固溶体的晶粒尺寸为30.0 nm。而把烧结所得样品球磨50 h时后,Mg90Li10固溶体的晶粒尺寸下降到21.8 nm;如在Mg90Li10固溶体中添加质量分数为x%(x=2, 5, 8)的Si混合球磨后,合金的晶粒尺寸依次为22.7、18.8和15.7 nm,显然,在Mg90Li10固溶体中添加适当的Si有利于减小合金颗粒尺寸,提高球磨效率,且当添加量为x=8时合金颗粒尺寸最小,球磨效率最高。

图1 Mg90Li10+x%Si(x=0, 2, 5, 8)合金的XRD谱
Fig. 1 XRD patterns for Mg90Li10+x%Si(x=0, 2, 5, 8) alloys
表1 Mg90Li10+x%Si(x=0, 2, 5, 8)合金的晶粒尺寸
Table 1 Grain size of Mg90Li10+x%Si(x=0, 2, 5, 8) alloys


图2 Mg90Li10+x%Si(x=0, 2, 5, 8)合金吸/放氢后的XRD谱
Fig. 2 XRD patterns for Mg90Li10+x%Si(x=0, 2, 5, 8) alloys after undergoing hydrogenation(a) and dehydrogenation(b)
为进一步研究Mg90Li10+x%Si(x=0, 2, 5, 8)合金氢化过程的相结构变化情况,图2给出了合金吸/放氢后的XRD谱。如图2(a)所示,合金吸氢后,其主要的吸氢相均为MgH2相;而在图2(b)的放氢XRD谱中,Mg90Li10+x%Si(x=0, 2, 5, 8)合金放氢后又出现了Mg相。综合图1和图2发现,Mg-Li-Si合金中的Mg2Si在脱氢前后并未发生变化,且在Mg-Li合金以及Mg-Li-Si合金氢化前后,并未发现Li或者LiH,这表明Mg(Li)固溶体的吸放氢过程是可逆的,且在脱氢前后Li并未从Mg(Li)固溶体脱溶分解。以上Mg-Li合金以及Mg-Li-Si合金氢化物的氢化反应过程可通过如下未添加Si的方程(1)以及添加Si后的方程(2)分别进行描述:
 (1)
(1)
 (2)
(2)
2.2 储氢性能
为了研究添加Si对Mg-Li合金储氢性能的影响,图3给出了Mg90Li10+x%Si(x=0, 2, 5, 8)合金的变温吸-放氢动力学曲线。如图3(a)所示的经过充分活化后合金的变温吸氢动力学曲线中,添加Si后的Mg90Li10+x%Si(x=2, 5, 8)合金吸氢曲线斜率都比Mg90Li10的吸氢曲线斜率要大,说明Si的添加能提高Mg-Li合金的吸氢速率。图3(b)给出了经过充分氢化后合金的变温放氢动力学曲线,从图中可知,添加Si后合金的初始放氢温度都降低,如Mg90Li10合金的初始放氢温度约为632 K,而Mg90Li10+x%Si(x=2, 5, 8)合金的初始放氢温度分别下降到610、598和598 K,即添加Si后合金的初始放氢温度分别降低22、34和34 K。特别是在加热时间为170 min的时候,Mg90Li10合金才刚开始释放出氢气,而添加Si后Mg90Li10+ x%Si(x=2, 5, 8)的放氢量(质量分数)则已分别高达1.33%、2.63%和2.63%。且当加热时间为180 min时,Mg90Li10+x%Si(x=2, 5, 8)合金样品已经放氢完毕,而Mg90Li10合金的放氢量仅为0.82%。Mg90Li10+x%Si(x=0, 2, 5, 8)合金的放氢量分别为4.35%、3.67%、3.33%和3.92%,这也跟图3(a)的吸氢量基本一致。

图3 Mg90Li10+x%Si(x=0, 2, 5, 8)合金变温吸/放氢动力学曲线
Fig. 3 Kinetic curves obtained during hydrogenation(a) and dehydrogenation(b) of Mg90Li10+x%Si(x=0, 2, 5, 8) alloys
上述实验结果说明Si的添加不仅可以提高合金的热力学性能和动力学性能,而且还能提高Mg-Li合金的可逆吸/放氢性能。这不仅与图1计算得到添加Si后合金颗粒尺寸减小有关,而且可能是在Mg-Li合金中添加Si后,由于Si与Mg结合生成Mg2Si,并在Mg2Si的催化作用下,Mg-Li合金氢化物中的Mg―H键减弱,导致在外部作用条件相同的情况下Mg―H键更容易断裂,从而降低Mg-Li-Si合金的释放氢温度。这也与CHAUDHARY等[20]研究在MgH2中添加Si混合球磨后能降低MgH2的脱氢温度相吻合。
图4所示为Mg90Li10+x%Si(x=0, 2, 5, 8)合金在 623 K温度下的放氢动力学曲线。从图4可知,在相同温度下,Mg90Li10+x%Si(x=0, 2, 5, 8)合金的放氢总量不同,这是因为在实验中所加入的Si为不吸氢元素,那么在样品中加入Si后就会使合金中的有效放氢元素含量降低,所以图4中合金中加入Si后的样品都比没加Si的样品放氢总量减小。同时,随着Si含量的增加,合金的放氢动力学性能逐渐提高,当x=5和x=8时,放氢动力学曲线的斜率基本一致。经过30 min的放氢后,Mg90Li10合金的放氢量仅为0.45%,而Mg90Li10+x%Si(x=2, 5, 8)合金的放氢量(质量分数)已分别达到1.29%、2.03%和2.19%,这进一步说明在Mg2Si的催化作用下,Mg-Li合金的放氢动力学性能得到了明显的提高。这应该得益于如下两方面的因素:1) 在Mg-Li合金中添加Si混合球磨后,由于Si质地较硬,在球磨过程,Si颗粒与Mg-Li颗粒经过反复的碰撞,不仅使合金颗粒尺寸减小,更利于Mg-Li合金颗粒断裂,从而导致Mg-Li合金颗粒的新鲜表面不断出现,这些新鲜表面活性较高,更利于与H原子结合;2) 在Mg-Li合金中添加Si混合球磨后,由于Si易于与Mg结合生成Mg2Si,在Mg2Si的催化作用下,H原子在Mg-Li合金中的扩散势垒降低,因此更有利于提高Mg-Li合金的吸/放氢动力学性能。
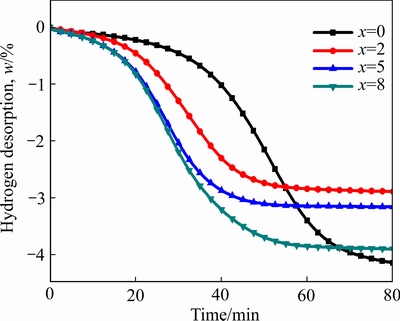
图4 Mg90Li10+x%Si(x=0, 2, 5, 8)合金恒温放氢动力学曲线
Fig. 4 Hydrogen desorption kinetics curves of Mg90Li10+x%Si (x=0, 2, 5, 8) alloys at 623 K
图5所示为Mg90Li10+x%Si(x=0, 2, 5, 8)合金氢化物以10 K/min为升温速率的DSC曲线。从图中可知,Mg90Li10+x%Si(x=0, 2, 5, 8)合金氢化物吸热峰的峰值温度分别为695、689、683和682 K,即添加Si后合金吸热峰的峰值温度分别下降6、12和13 K,即当添加量为x=8时合金吸热峰的峰值温度降幅最大。通常情况下,峰值温度值表示合金反应速率最快的位置,这说明Si的添加降低了Mg-Li合金氢化物的最快反应速率温度和脱氢温度,这也与图3观测到的合金吸/放氢动力学性能结果相吻合。而且,由图5可知,Mg90Li10合金峰值温度所对应的面积较大,添加Si后Mg90Li10+x%Si(x=2, 5, 8)合金峰值温度峰值所对应的面积都减小。这说明Mg90Li10合金氢化物较为稳定,而在Mg2Si的催化作用下,合金氢化物的稳定性降低。这可能是加入Si后,在球磨过程中有利于减小合金的颗粒尺寸,在相同的条件下,H原子在小颗粒体内向外扩散路径缩短,扩散过程所需克服的扩散势垒降低,因此,添加Si后Mg90Li10合金氢化物的稳定性下降。
同时,在通常情况下,金属Li在加热到453.73 K时就开始吸热溶解,但在图5中400~650 K的温度区间范围内,并未发现有任何吸热峰或者放热峰。这说明采用烧结后液氮快冷淬火热处理并结合机械合金化法制备得到的Mg-Li或者Mg-Li-Si固溶体合金,Li已经完全固溶进入Mg晶格体内,形成Mg(Li)二元系固溶体。且Mg(Li)二元系固溶体在吸/放氢过程中,Li原子并未从Mg基体中脱溶分解出来,这也就能说明了在图1和图2的XRD谱分析中并未发现游离Li原子存在的原因。

图5 Mg90Li10+x%Si(x=0, 2, 5, 8)合金氢化物的DSC曲线
Fig. 5 DSC curves of Mg90Li10+x%Si(x=0, 2, 5, 8) alloys hydride
为更进一步研究Si的添加对Mg-Li固溶体合金储氢性能的影响,在氩气保护下,分别以5、10、15和20 K/min的升温速率对合金氢化物进行加热,根据升温曲线中的吸热峰峰值温度并结合Kissinger方程绘制出Kissinger曲线。那么,合金氢化物的脱氢表观活化能就可根据Kissinger方程曲线的斜率进行计算[21]:
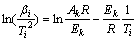 (3)
(3)
式中: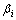 为恒定加热速率;Ti为在恒定加热速率为
为恒定加热速率;Ti为在恒定加热速率为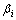 条件下的最大放氢速率,即DTA(差热)或者DSC(差式扫描热量)曲线所对应的峰值温度;R=8.314 J/(mol・K);Ek为表观活化能。Mg90Li10+x%Si(x=0, 2, 5, 8)合金氢化物的Kissinger曲线如图6所示,Mg90Li10合金氢化物的脱氢活化能为396.5kJ/mol,如在Mg90Li10合金中添加Si后,合金的脱氢活化能快速降低,当x=2, 5, 8时对应的活化能分别降低了13.3、21.1和67.4 kJ/mol,即当x=8时合金的脱氢活化能降幅最大。这也更进一步说明由于Mg2Si的催化作用,Mg-Li合金中H原子扩散势垒降低,从而有效提高了合金的储氢动力学性能。
条件下的最大放氢速率,即DTA(差热)或者DSC(差式扫描热量)曲线所对应的峰值温度;R=8.314 J/(mol・K);Ek为表观活化能。Mg90Li10+x%Si(x=0, 2, 5, 8)合金氢化物的Kissinger曲线如图6所示,Mg90Li10合金氢化物的脱氢活化能为396.5kJ/mol,如在Mg90Li10合金中添加Si后,合金的脱氢活化能快速降低,当x=2, 5, 8时对应的活化能分别降低了13.3、21.1和67.4 kJ/mol,即当x=8时合金的脱氢活化能降幅最大。这也更进一步说明由于Mg2Si的催化作用,Mg-Li合金中H原子扩散势垒降低,从而有效提高了合金的储氢动力学性能。

图6 Mg90Li10+x%Si(x=0, 2, 5, 8)复合材料的Kissinger曲线
Fig. 6 Kissinger plots for Mg90Li10+x%Si(x=0, 2, 5, 8) composites
3 结论
1) 经过烧结和液氮快冷淬火的热处理后,Li原子扩散进入了Mg晶格基体中,形成Mg(Li)固溶体。而热处理结合机械球磨合金化后,Mg-Li固溶体以及Mg-Li-Si合金的氢化物均为MgH2,Mg(Li)固溶体的吸放氢过程是可逆的。
2) 在Mg-Li体系中添加Si元素混合烧结容易形成Mg2Si,在Mg2Si的催化作用下能有效降低Mg(Li)固溶体合金的脱氢温度,Mg90Li10+x%Si(x=2, 5, 8)合金对应的脱氢温度分别降低22、34和34 K。
3) 添加Si后形成的Mg2Si能提高Mg(Li)固溶体氢化物的热力学性能,如在Mg-Li合金中添加Si后,降低了Mg-Li合金氢化物的最快反应速率温度和脱氢活化能,Mg90Li10+x%Si(x=2, 5, 8)合金对应的脱氢活化能分别降低13.3、21.1和67.4 kJ/mol。
REFERENCES
[1] KOU Hua-qin, XIAO Xue-zhang, CHEN Li-xin, LI Shou-quan, WANG Qi-dong. Formation mechanism of MgB2 in 2LiBH4+MgH2 system for reversible hydrogen storage[J]. Transactions of Nonferrous Metals Society of China, 2011, 21(5): 1040-1046.
[2] WAN Qi, LI Ping, SHAN Jia-wei, ZHAI Fu-qiang, LI Zi-liang, QU Xuan-hui. Superior catalytic effect of nickel ferrite nanoparticles in improving hydrogen storage properties of MgH2[J]. The Journal of Physical Chemistry C, 2015, 119(6): 2925-2934.
[3] KOU Hua-qin, SANG Ge, CHEN Li-xin, XIAO Xue-zhang, DENG Shuai-shuai, HUANG Zhi-yong. Grain size effect of MgH2 on dehydrogenation kinetics of 2LiBH4+MgH2 system[J]. Chemical Journal of Chinese Universities, 2013, 34(10): 2347-2352.
[4] 张 健, 朱 璞, 毛 聪, 周惦武. 碳材料掺杂对镁基氢化物释氢性能的影响及其微观机理[J]. 中国有色金属学报, 2015, 25(9): 2464-2470.
ZHANG Jian, ZHU Pu, MAO Cong, ZHOU Dian-wu. Influence and micro-mechanism of carbon materials doping on dehydrogenation properties of magnesium based hydride[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(9): 2464-2470.
[5] KATAOKA Riki, GOTO Yasuyuki, KAMEGAWA Atsunon, TAKAMURA Hitoshi, OKADA Masuo. High-pressure synthesis of novel hydride in Mg-Ni(-H) system[J]. Materials Transactions, 2006, 47(8): 1957-1960.
[6] 李志宝, 孙立贤, 张莹洁, 徐 芬, 褚海亮, 邹勇进, 张焕芝, 周怀营, 张 箭. MgH2储氢热力学研究进展[J].中国科学: 化学, 2014, 44(6): 964-972.
LI Zhi-bao, SUN Li-xian, ZHANG Ying-jie, XU Fen, CHU Hai-liang, ZOU Yong-jin, ZHANG Huan-zhi, ZHOU Huai-ying, ZHANG Jian. Progress on hydrogen storage thermodynamic ofMgH2[J]. Scientia Sinica Chimica, 2014, 44(6): 964-972.
[7] GOTO Y, HAYASHI T, KATAOKA R, KAKUTA H, KAMEQAWA A, TAKAMURA H, OKADA M. High-pressure synthesis of novel hydrides in Mg-TM systems (TM=Zr,Nb and Mo)[J]. Materials Transactions, 2005, 46(8):1798-1801.
[8] 丁向前, 朱云峰, 卫灵君, 宦清清, 李李泉. 催化剂对LiAlH4+MgH2体系放氢性能的影响及催化机理[J]. 中国有色金属学报, 2013, 25(5): 1356-1361.
DING Xiang-qian, ZHU Yun-feng, WEI Ling-jun, HUAN Qing-qing, LI Li-quan. Effect of catalysts on dehydrogenation of LiAlH4+MgH2 composite and catalytic mechanism[J]. The Chinese Journal of Nonferrous Metals, 2013, 25(5): 1356-1361.
[9] 张 琦, 李双寿, 董占民, 汤 彬, 李 睿, 林万明. Mg65Ni10RE25(RE=La,Ce,Pr,Nd,Mm)非晶储氢合金电极的性 能[J]. 中国有色金属学报, 2015, 25(6): 1538-1545.
ZHANG Qi, LI Shuang-shou, DONG Zhan-min, TANG Bin, LI Rui, LIN Wan-ming. Properties of amorphous Mg65Ni10RE25 (RE=La,Ce,Pr,Nd,Mm) hydrogen storage alloys electrode[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(6): 1538-1545.
[10] COVA F, ARNEODO L P, GENNARI F. Hydrogen sorption in MgH2-based composites: The role of Ni and LiBH4 additives[J]. International Journal of Hydrogen Energy, 2012, 37(20): 15210-15219.
[11] KOU Hua-qin, XIAO Xue-zhang, LI Jin-xiu, LI Shou-quan, GE Hong-wei, WANG Qi-dong, CHEN Li-xin. Effects of fluoride additives on dehydrogenation behaviors of 2LiBH4+MgH2 system[J]. Hydrogen Energy, 2012, 37(1): 1021-1026.
[12] CUI Jie, WANG Hui, LIU Jiang-wen, OUYANG Liu-zhang, ZHANG Qing-an, SUN Da-lin, YAO Xiang-dong, ZHU Min. Remarkable enhancement in dehydrogenation of MgH2 by a nano-coating of multi-valence Ti-based catalysts[J]. Journal of Materials Chemistry A, 2013, 1(18): 5603-5611.
[13] 丁向前, 朱云峰, 卫灵君, 宦清清, 李李泉. 催化剂对LiAlH4+MgH2体系放氢性能的影响及催化机理[J]. 中国有色金属学报, 2013, 25(5): 1356-1361.
DING Xiang-qian, ZHU Yun-feng, WEI Ling-jun, HUAN Qing-qing, LI Li-quan. Effect of catalysts on dehydrogenation of LiAlH4+MgH2 composite and catalytic mechanism[J]. The Chinese Journal of Nonferrous Metals, 2013, 25(5): 1356-1361.
[14] LU Wen-chun, OU Shih-Fu, LIN Ming-Hong, WONG Man-Fang. Hydriding characteristics of Mg-Ti alloys prepared by reactive mechanical grinding and hydrogen pulverization[J]. Journal of Alloys and Compounds, 2016, 66(4): 193-198.
[15] AMIRKHIZ B S, ZAHIRI B, KALISVAART P, MITLIN D. Synergy of elemental Fe and Ti promoting low temperature hydrogen sorption cycling of magnesium[J]. International Journal of Hydrogen Energy, 2011, 36(11): 6711-6722.
[16] HONG S H, SONG M Y. Preparation of Mg-33Al alloy by rapid solidification process and evaluation of its hydrogen-storage properties[J]. Metals and Materials International, 2013, 19(5): 1145-1149.
[17] GOTO Y, KAKUTA H, KAMEGAWA A, TAKAMURA H, OKADA M. High-pressure synthesis of novel hydride in Mg-M systems (M=Li, Pd)[J]. Journal of Alloys and Compounds, 2005, 404(5): 448-452.
[18] LENG Hai-yan, PAN Yan-biao, LI Qian, CHOU K C. Effect of LiH on hydrogen storage property of MgH2[J]. International Journal of Hydrogen Energy, 2014, 39(25): 13622-13627.
[19] VAJO J J, MERTENS F, AHN C C, BOWMAN R C, FULTZ B. Altering hydrogen storage properties by hydride destabilization through alloy formation-LiH and MgH2 destabilized with Si[J]. Journal of Physical Chemistry B, 2004, 108(37): 13977-13983.
[20] CHAUDHARY A L, PASKEVIUS M, SHEPPARD D A, BUCKLEY C E. Thermodynamic destabilization of MgH2 and NaMgH3 using Group IV elements Si, Ge or Sn[J]. Journal of Alloys and Compounds, 2015, 623: 109-116.
[21] KISSINGE H E. Reaction kinetics in differential thermal analysis[J]. Analytical Chemistry, 1957, 29(11): 1702-1706.
Effect of Si addition on hydrogen storage performance of Mg-Li alloy
HUANG Xian-tun1, QIN Chang-sheng1, QING Pei-lin1, XIE Zheng-zhuan2, LI Liu-jie2
(1. Department of Materials Science and Engineering, Baise College, Baise 533000, China;
2. College of Physical Science and Technology, Guangxi University, Nanning 530004, China)
Abstract: The Mg90Li10+x%Si(x=2, 5, 8 (mass fraction)) alloys hydrogen storage material were synthesized by heat treatment in combination with mechanical milling, and the Si effect on the hydrogen storage properties of Mg-Li alloys were studied. The results show that the Li atom diffuses easily into Mg matrix to Mg(Li) solid solution, and the Si element reacts with Mg element to form Mg2Si. It is clearly that the existence of Mg2Si can improve the hydrogen absorption/desorption kinetic properties and thermodynamic performance for Mg-Li alloys. For example, with the addition of Si, the initial hydrogen desorption temperature for the Mg90Li10+x%Si alloys decreases from 632 K(x=0) to 610 K(x=2), 598 K(x=5) and 598 K(x=8), respectively. The apparent activation energies for the Mg90Li10+x%Si (x=2, 5, 8) alloys are 13.3 kJ/mol(x=2), 21.1 kJ/mol(x=5) and 67.4 kJ/mol(x=8) lower than that of Mg-Li alloy.
Key words: Mg-Li alloy; heat treatment; catalysis; hydrogen storage performance
Foundation item: Project(2014GXNSFAA118346) supported by the Natural Science Foundation of Guangxi, China; Project (KS16ZD06) supported by the Higher Education Disciplines: Material Physics and Chemistry (Baise College) in Guangxi, China; Project(KY2015LX385) supported by the Higher Education Scientific Research Projects in Guangxi, China
Received date: 2016-12-08; Accepted date: 2017-06-01
Corresponding author: HUANG Xian-tun, Tel: +86-13977619898; E-mail: gxbshj008@163.com
(编辑 龙怀中)
基金项目:广西自然科学基金资助项目(2014GXNSFAA118346);广西高校重点学科基金资助项目[KS16ZD06];广西高校科学研究基金资助项目(KY2015LX385)
收稿日期:2016-12-08;修订日期:2017-06-01
通信作者:黄显吞,副教授;电话:13977619898;E-mail: gxbshj008@163.com