DOI��10.19476/j.ysxb.1004.0609.2018.02.22
��绯ѧұ����ȡ�뵼��Ԫ�ء�������Ϊ��
���������ƣ������ˣ������壬�� �£���ҵ��
(���ϴ�ѧ ұ���뻷��ѧԺ����ɳ410083)
ժ Ҫ����Ե绯ѧұ����ȡ�뵼��Ԫ�ش��ڵ����⣬������ù�绯ѧұ��ķ��������а뵼��Ԫ�صĵ绯ѧ������ȡ����ϰ뵼�������Լ���绯ѧ�������ۣ�������绯ѧұ������ƣ���������ȡΪ����֤��绯ѧұ�����Խ�ԡ������������绯ѧ���������У��뵼���������������������������϶���ȵĹ��Ӻ��ܼ���������������-��Ѩ�ԣ��������ӴӰ뵼��������Һ�ٽ��绯ѧ��ԭ��ͬʱ���������ӿɼ�С�����ʺ��ܴ��������������缫����̯�ĵ��Ʋ�볣��ĵ绯ѧ������ȣ���绯ѧ��������ǿ���缫���̡����Ͳ۵�ѹ���Լ���߳������ʡ�����Ч�ʺͲ��ܣ��������õ�Ӧ��ǰ�������ָ����绯ѧұ��δ����չ�������ٵ����⣬�������ں�������չ��
�ؼ��ʣ��뵼��Ԫ�أ����գ��۵�ѹ����绯ѧұ�𣻵绯ѧ����
���±�ţ�1004-0609(2018)-02-0397-09���� ��ͼ����ţ�O782���� ���ױ�־�룺A
1 �绯ѧұ����ȡ�뵼��Ԫ�ص���Ҫ����
�뵼��Ԫ����ָ���а뵼�����ʵ�Ԫ�أ���衢�ࡢ�ڡ�������͵�ȣ��ѳ�Ϊ�ƶ����ú���ᷢչ�ͽ������ɻ�ȱ�����ʡ���ˣ���չ��ͳɱ������ܺġ�����Ⱦ�߲��ܵ���ȡ����ʮ�ֱ�Ҫ���绯ѧ����(��Ƶ���������)���в�Ʒ���ȸߡ�ԭ����Ӧ��ǿ��ѡ�������á�����Ч�ʸߡ������Ѻ��ҳɱ��������ŵ㣬�ڽ�����ȡ�;�������õ��㷺Ӧ��[1-3]�����ǵ�����ڰ뵼��Ԫ��ұ���е�Ӧ�÷dz����ޣ�Ŀǰֻ�ڴ�϶������͡���������õİ뵼��Ԫ���ڵ���ȡ(�;���)�еõ�Ӧ��[4]������Ҫ�����ڳ�����İ뵼�����ԣ����µ������ȡ�뵼��Ԫ�ش�����������ؽ�������
1) ���������������ܵ͡����뵼��Ԫ�ص������������������ڰ뵼��Ԫ�صĵ͵����ԣ��缫�ĵ����Ѹ��������ͬʱ�����İ뵼�������Ӵ��ĵ��Һ����һ���ռ���������Щ����ֱ�ӵ��²۵�ѹ�����ߡ���ֻ�ܲ��ýϵ͵ĵ����ܶȳ�������ȷ�����վ���ƽ�����С�����Ŀǰ��ҵ�ϵ�����������õĵ����ܶ�ͨ��Ϊ50~80 A/m2��Զ����п(350~500 A/m2)��ͭ(180~250 A/m2)����(300~400 A/m2)��[5]�����������ȡʱ���õĵ����ܶȣ�����������ýϴ�ĵ����ܶȣ��������������缫�������ٽ�����Ӧ���У����͵���Ч�ʣ������ڵ�����ĵ����ܶ�����160 A/m2 ʱ������Ч�ʽ��ɳ��õ����ܶ�ʱ��99%����90%[6]�����ڳ������ʵͣ������ڵ�����������賤��150 h���ϣ�Զ����������ɫ�����ĵ��������(һ��Ϊ24 h������Ϊ48 h������е��пʱ)������Ч�ʵ��¡����ڹ�ĵ������Ϊ�˻�ýϸ������Ĺ�Ĥ�������ܶ���Ҫ������100~500 A/m2��Χ��(��������)[7-8]���ù�����������Զ�����������ᴿ�������������ྺ�����ǵ�����蹤��һֱδ�ܵõ�ʵ��Ӧ�õ���Ҫԭ��֮һ��
2) �����ȶ��Բ���ڵ���������У����ų������ȵ����ӣ����������Լ��۵�ѹ���������ߣ����µ�������̲��ȶ�������������ʱ�����������ں��ڣ��۵�ѹ������300 mV����[9]����һ���棬���ڳ���������������ʱ�䳤��Ҳʹ�õ������Ӧ��ϵ�IJ��ȶ������ӡ���������ڵĵ��������������������Һ��Ϊ���Һ�����ų���ʱ����ӳ�����ʹ�õ��Һ���������Ƶ�����������[9]��������ĵ��������Ҫ���ڷ�ˮ��ϵ�н���(ˮ��Һ��ϵ���������λ����[10])��Ŀǰ�����ij������������ѣ�����Ч�ʶ��ܵͣ�����Ӧ����Ӱ������ϵ���ȶ��ԣ����ҳ��ij���ʱ�������ܼ������ʵ���ʧ[11]����ĵ����һ���������н��У����ڹ赼���Բ�������������䣬���¹�Һ���治�ȶ�����ѹ������Ȳ���[12]��
3) ����Ч�ʵͣ��ܺĸߡ��뵼��Ԫ�ص����Բ�ڵ����һ��ʱ���缫�����ס�ʧ������µ����ܶȷֲ������ȣ�����Ӧ��ǿ������Ч�ʽ��͡���Ŀǰ�������������˵�����ڵĵ���Ч�ʽϸ�(�ܳ���95%)�⣬��������ĵ���Ч�ʾ��Ƚϵͣ�ͨ����90%����[13-14]���������ڰ뵼�嵼���Բ�������ڵ缫����������缫��ŷķ�����ӣ��۵�ѹҲ��֮���ߣ����ϳ���ʱ�������ܳ����ܺ�Ҳ��֮�������������������ұ����̽��ܽ����Ƿdz������ġ�
��������һֱ�谭�ŵ�����뵼��Ԫ�ؼ����ķ�չ�������Ϊ�˽����Щ���⣬ ���������������ڵ��ڶ��о���������չ�˴������о���������dz����ֶεĹ����Ż���������������缫���ϡ����Һ��ɡ����Ӽ������۽ṹ�ȣ�������Ч����������⣬ʹ�õ�����ڰ뵼��Ԫ��ұ����Ӧ�÷dz����ޡ�һЩ�뵼��Ԫ�ص�ұ�������࣬��Ըѡ���ܺĺ���Ⱦ�ŷŶ��ߵö࣬�����ܸ��ߡ������ȶ��Ը��õ���������(��������Ȼ�����-ˮ��-�ԭ����[15]������ø��������ӷ�[16]��)��Ҳ�����õ�����ļ�������ʹ�����ڣ������߲��ܺ�����Ч�ʲ������ܺ�Ҳ����ұ����������ٵ�һ�����⡣��ˣ� Ϊ�˴ٽ��뵼��Ԫ�ص������ȡ�����Ľ��������ڵ����������ߺ�
���ܽ��ġ����������ҵ���ȷ���ȡ��ͻ�ƣ�ʵ�ְ뵼��Ԫ�صͳɱ������ܺġ�����Ⱦ�߲��ܵ�ұ����ȡ������Ҫ���µ�˼·��;����ͻ�ƴ�ͳ������IJ��㡣
2 ��绯ѧұ����ȡ�뵼��Ԫ�ص����
����������⣬�����ڰ뵼��Ĺ�絼�Ȼ������ʡ��뵼��缫�Ĺ�绯ѧ����ԭ���Լ��뵼��Ԫ�ص������ȡ���̻�������������˲��ù�绯ѧ�����ķ������а뵼��Ԫ�صĵ绯ѧұ����ȡ�����ڰ뵼��Ԫ�ص������ȡ�����У�����������ʩ�ӹ��գ��Դٽ�������ԭ��Ӧ�Ľ��У���ǿ���������̡��ڵ������ȡ�뵼��Ԫ�ع����У�һ��������ʼ���У��缫�Ͼͻ�����һ��뵼��Ĥ������ԭʼ���ױ��棬�绯ѧ��Ӧ���������ɵ���/���Һ����ת��Ϊ�뵼��/���Һ���档�����������缫����ʱ���뵼�屾���Ͱ뵼��/���Һ��������ʻᷢ�������仯��ʹ�õ���������봫ͳ����״̬��Ȳ������Բ��졣ͼ1��ʾΪ��绯ѧ������ȡ�뵼��Ԫ��(��p�Ͱ뵼��Ϊ��)�����е缫/���Һ���ܼ��ṹʾ��ͼ������MΪ�뵼��Ԫ�ص��ʻ�ԭ̬��M+Ϊ�뵼��Ԫ�ص�����̬��EFΪ�����ܼ�����Ϊ�缫���ƣ� ��
��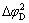 ��
�� �ֱ�Ϊ��̬�µĵ���ŷķ�����ռ��ɲ���Ʋ�͵缫/���Һ������Ʋ
�ֱ�Ϊ��̬�µĵ���ŷķ�����ռ��ɲ���Ʋ�͵缫/���Һ������Ʋ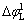 ��
��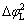 ��
��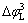 �ֱ�Ϊ�����µĵ���ŷķ�����ռ��ɲ���Ʋ�͵缫/���Һ������Ʋ�����£�����������hv���ڰ뵼���϶����Egʱ���뵼�屻������������-��Ѩ�ԣ���������������֣�1) ������Ũ���������絼�����ӣ�ŷķ��(
�ֱ�Ϊ�����µĵ���ŷķ�����ռ��ɲ���Ʋ�͵缫/���Һ������Ʋ�����£�����������hv���ڰ뵼���϶����Egʱ���뵼�屻������������-��Ѩ�ԣ���������������֣�1) ������Ũ���������絼�����ӣ�ŷķ��(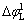 ��
�� )���ͣ�2) �����ܼ��������ܴ�������С���ռ������ĵ��Ʒ�̯(
)���ͣ�2) �����ܼ��������ܴ�������С���ռ������ĵ��Ʒ�̯(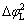 ��
��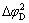 )��С��3) �������ӴӰ뵼��������Һ���뵼��/���Һ������Ʋ�(
)��С��3) �������ӴӰ뵼��������Һ���뵼��/���Һ������Ʋ�(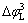 ��
�� )���ӣ��ٽ���ԭ��Ӧ�Ľ��У�4) ���ӱ��͵����������ڲ��ø���ĵ����ܶȳ�����
)���ӣ��ٽ���ԭ��Ӧ�Ľ��У�4) ���ӱ��͵����������ڲ��ø���ĵ����ܶȳ�����
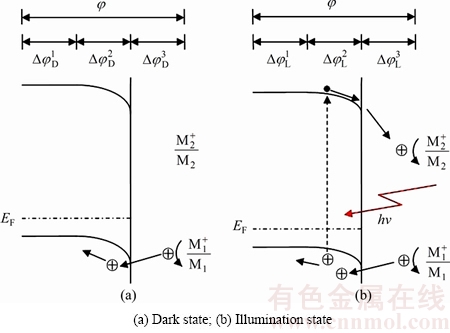
ͼ1 p�Ͱ뵼����������绯ѧ�������̵ĵ缫/���Һ�ܼ��ṹ
Fig. 1 Schematic diagram of band alignment at electrode/electrolyte interface during cathodic photo-electrochemical deposition on p-type semiconductor electrode
��ϰ뵼�������Լ���绯ѧ�������ۣ���绯ѧ������ȡ�뵼��Ԫ�ؿɾ߱�����һϵ�����ơ�
1) ����ŷķ�����뵼����й�絼ЧӦ�������뵼�������������ڴ�϶���ȵĹ����Ժ������������-��Ѩ�ԣ�ʹ������Ũ�ȵ��������絼�����ӣ�����ֱ�ӽ��͵缫��ŷķ�������Ұ뵼��Ԫ�ص����Բ������������ڸ�������������ԭ��֮һ����ˣ����ù�绯ѧ�����������ѳ����뵼��Ĺ�絼ЧӦ��Ϊ����뵼��Ԫ�ص�����а뵼�嵼���Բ������ϵ�������ṩ��Ч;����
2) ǿ���缫���̣����Ƶ���Ч�ʡ��뵼��/���Һ����ʵ������һ�������ᣬ���������������-��Ѩ�Ե�����[17]���������������p �Ͱ뵼��(������Ȼp�Ͱ뵼��[18]������Ҳ��������Ϊp�ͣ�����Ҫ����ԭ��������������С��4����p����)���������ڹ�������������Һ��ʵ��������������/���Һ������Ʋ�ٽ��˻�ԭ��Ӧ�Ľ��У�ǿ�����������̣�������˵���Ч�ʡ�
3) ���Ͳ۵�ѹ������ʱ�����ӵ����·ֲ�(�ռ��ɲ��������Ũ�Ȼ���������)����������ܼ��������Ӷ���С�뵼����ܴ�����[19]�����Ϳռ��ɲ�����̯�ĵ��ƲҲ�����ڽ��Ͳ۵�ѹ��
4) ��߿ɲ��õĵ����ܶȡ��뵼������������ʱ�����ڿռ������Ĵ��ڣ��缫��Ӧ�����ű��͵���(�缫��Ӧ�����ܶȲ�������Ʋ�����Ӷ����ӣ������ܵ��뵼���ڲ������ӹ�Ӧ״��������)��ͨ�����տ�������������Ũ�ȣ��Ӷ�����Ӧ�ı��͵�������������߳������õĵ����ܶȣ��ٽ��������ʵ�����[20]��
5) �ɽ��ͷ�Ӧ�����ơ����⣬���о����ֵ�����ʱ���ڰ뵼��缫�ϵ������������ʱ�����������ӿ��Խ��ͽ����绯ѧ���������Ʋ�������ĵ�� ��[21-22]����һ�������ܻ�뵼��Ԫ�ص����(�������ʼ�Σ�ʵ�������ڰ뵼����ͬ�ʳ���)����ߵ����ܶȺͽ��Ͳ۵�ѹ�Ȳ����������á�
�������Ϸ�������绯ѧұ��ʵ�����Ǽ��⡢�硢��ѧ��һ��İ뵼��Ԫ����ȡ�¼������ɱ��������״���ұ����ȡ�����������ʵ�������ð뵼��Ĺ�绯ѧ���Ժ�絼ЧӦ�Գ������̽���ǿ���ͽ��ܡ�ֵ��ע����ǣ���绯ѧ�����ڻ�����뵼�幦�ܱ�Ĥ�����Ʊ�(��Ҫ��ע��ĤƷ��)��Ӧ�������Ѿ��õ�һ�����о������ڹ���ǿ�����������Ҳ����Щ������뵼�屡Ĥ�����еõ���ֵ����ֺ���֤����Ϊ�÷��ڰ뵼��Ԫ�ص����ұ����ȡ�ṩ�����ۺͼ�����֧�֡�MISHRA��[23]�����˹�絼ЧӦ��绯ѧ��Ӧ�Ե����p ��CdTe ������뵼�屡Ĥ��Ӱ�죬���ֹ����ܴٽ�Cd2+��HTeO2+�ĵ绯ѧ��ԭ��Ӧ��ǿ�������������̡�SUGIMOTO��[24]����CdTe �ij������������ǿ�ȵ�ƽ���������ȡ�MURASE��[25]�Թ�绯ѧ����CdTe������ϸ���о������ֹ����ܼ������ǿ�绯ѧ����CdTe�뵼�屡Ĥ�ĵ����ܶ��Լ��������ʣ������Լ������ߵ���Ч�ʣ�������ڸ�������Ũ����ϵ��ʩ�ӹ��պ������ĵ���Ч���ܴ�30%������97%����ͬ����������ʱ��ɴ�2298 min����47 min����������������߽���50�������Ŷ�[26]Ҳ�״α����˲��ù�绯ѧ�������Ʊ�CuInSe2������뵼�屡Ĥ���о����ֹ��ղ������������CuInSe2��Ĥ�ĵ����ܶȺͳ������ʣ������ܸ��Ʊ�Ĥ����ò��ʹ֮��Ϊ�������ܡ����ڰ뵼��Ԫ�أ�������������ŶӶ�Se[27]��Te[28]��Ĥ�Ĺ�绯ѧ������չ��һЩ�������о����������������紫ͳ�绯ѧ��������绯ѧ����ʱ�绯ѧ��ԭ�ķ������迹�������ͣ����������ܶ��������ӡ���ʹ�ò��û��ڵ绯ѧ�ķ�����ȡSe��Ϊ���ܣ�������Se��ȡұ�����;����ͬʱҲΪ���ù�绯ѧ����Te����ȡ�ṩ���������ݡ��������߽���Щ�����Ļ����ϣ���Te�Ĺ�ҵ���������Һ��ϵΪ�����ù�绯ѧ�����ķ�������Te����ȡ��ͨ����������֤��绯ѧұ�����Խ�ԡ�
3 ��绯ѧұ�����Ƶ���֤����TeΪ��
3.1 ʵ��
���ҺΪ��1 mol/L Na2TeO3 (99.99%) ��2.5 mol/L NaOH�ļ�����Һ(ģ�ҵ����)������Ϊ����ʯӢ���ۡ��绯ѧ�������绯ѧ��Ϊ�о�������PARSTAT 4000�͵绯ѧ����վ��ʵ������������Ϊ˫�缫��ϵ������ó�������缫��ϵ�����вαȵ缫Ϊ���ʹ��缫(SCE�����о����е��Ƴ��۵�ѹ�������ڴ˲αȵ缫)���Ե缫Ϊ�ߴ�ʯīƬ�������缫Ϊ430�����Ƭ��ʵ�����ò����Ƭ����ϴ����Ϊ��ϴ�·�ˮ������ϴ10 min��ȥ����ˮ(18.2 M��/cm)������ϴ10 min����ˮ�Ҵ�������ϴ10 min��ȥ����ˮ(18.2 M��/cm)������ϴ10 min����������ɱ��á���绯ѧ��������Newport 300 W��Դģ��̫����ֱ�����乤���缫��������۴��Ĺ�ǿ��FZ-2A���ռƲⶨΪ100 mW/cm2��
ѭ������/���Է���ɨ�������о��ڵĵ������Ӧ���ƺ��ն��䷴Ӧ���Ƶ�Ӱ�죬�ڷǽ����״̬�½��в��ԣ�ɨ���ٶ�Ϊ10 mV/s������Ƴ������������ƿ�����-0.75 V (vs SCE)������������ĵ����ܶȷֱ������100 A/m2��200 A/m2��ͬʱ��¼�۵�ѹ��ʱ��ı仯�����������ǰ��IJ����Ƭ����ָ�����ȡ�����Լ���������ڵ����������ú���FEI��˾������Quanta-200�ͻ���ɨ��羵�۲�������ڵ���ò��
3.2 ���������
�Ժ���1mol/L Na2TeO3��2.5mol/L NaOH�ĵ��Һ��ϵ����ѭ���������ԣ����Եĵ��Ʒ�ΧΪ0.8 V��-1.0 V�������ͼ2��ʾ���������Ͽ��Թ۲쵽һ�����ԵĻ�ԭ��(���ΪC)������������(���ΪA1��A2)�����֮ǰ���о����[28]���˻�ԭ��C(ԼΪ-0.75 V)��Ӧ��Te�ij�����ͨ��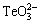 ���ĵ��ӻ�ԭ���У�����Ӧ(1)����ʵ���ڸ����ĵ����»��ᷢ��Te�Ľ�һ����ԭ������Ӧ(2)���仹ԭ����Te2-������Һ�е�Na2TeO3�������з�Ӧ���γ�Te���ʣ�����Ӧ(3)�����ڱ��о������õ�Na2TeO3��Ũ�Ƚϴ�ԭ����Te2-һ���γɾͻ���������Һ�е�Na2TeO3�������з�Ӧ�����µ�Te����ʹ�÷�Ӧ(2)����Ӧ�Ļ�ԭ��û�б��ֳ��������⣬ͨ����ϸ�۲췢�֣��ڸ���ɨ���γɻ�ԭ��C֮ǰ��-0.5 V��-0.7 V��Χ�ڣ�������һ����ԭ����(��ͼ2�в�ͼ)�����û�ԭ������Ӧ�Ļ�ԭ�����dz�������ܿ��ܶ�Ӧ��Te�ڲ���ֻ����Ϸ���Na2TeO3���ĵ���Ԥ��ԭ��������Ϊ�ڵĵ������[29]��
���ĵ��ӻ�ԭ���У�����Ӧ(1)����ʵ���ڸ����ĵ����»��ᷢ��Te�Ľ�һ����ԭ������Ӧ(2)���仹ԭ����Te2-������Һ�е�Na2TeO3�������з�Ӧ���γ�Te���ʣ�����Ӧ(3)�����ڱ��о������õ�Na2TeO3��Ũ�Ƚϴ�ԭ����Te2-һ���γɾͻ���������Һ�е�Na2TeO3�������з�Ӧ�����µ�Te����ʹ�÷�Ӧ(2)����Ӧ�Ļ�ԭ��û�б��ֳ��������⣬ͨ����ϸ�۲췢�֣��ڸ���ɨ���γɻ�ԭ��C֮ǰ��-0.5 V��-0.7 V��Χ�ڣ�������һ����ԭ����(��ͼ2�в�ͼ)�����û�ԭ������Ӧ�Ļ�ԭ�����dz�������ܿ��ܶ�Ӧ��Te�ڲ���ֻ����Ϸ���Na2TeO3���ĵ���Ԥ��ԭ��������Ϊ�ڵĵ������[29]��
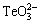 +3H2O+4e��Te+6OH- (1)
+3H2O+4e��Te+6OH- (1)
Te+2e��Te2- (2)
2 Te2-+3H2O+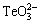 ��3Techem+6OH- (3)
��3Techem+6OH- (3)
ΪŪ����նԵ绯ѧ����ʱTe��ԭ���̵�Ӱ�죬�ֱ��ڹ��պͰ�̬�½������Է���ɨ�����߲��ԣ�ɨ����Ʒ�ΧΪ-0.5 V��-0.95 V��ɨ���ٶ�Ϊ10 mV/S������Խ����ͼ3(a)��ʾ����ͼ3(a)��֪���������ڵij�ʼ��ԭ��λ�Ͱ�̬���ڵij�ʼ��ԭ����һ�£�������Ϊ��ʱ�����ϻ�û��p�Ͱ뵼���ڵ����ɣ��ʹ��ն����ʼ������λû��Ӱ�졣��һ��ɨ����Ƹ����ڵij�ʼ��ԭ���ƣ���ʱ���ױ������ڵij����������µ�������ԭ�����ܶ����Դ��ڰ�̬��������ԭ�����ܶȡ���Ҳ��ζ�ŵ绯ѧ����ʱ���������ͬ�ij��������ܶȣ������µ���ϵ����ij������Ƹ������۵�ѹ���С��ͼ3(b)��ʾΪ�� 1 mol/L Na2TeO3��2.5 mol/L NaOH���Һ��ϵ��ͨ(on)����(off)��״̬�º���Ƴ����ĵ����ܶ�-ʱ������(��������Ϊ-0.75 V)����ͼ3(b)��֪���ڹ��յ�˲�䣬�ڵij��������ܶ�Ѹ������(���ӵĵ�����Ϊ������������)�������Ͽ�����(��̬)ʱ��������ܶ���������С���ý�������Է���ɨ����ԵĽ��һ�¡��������������ԭ���dz������ڻ��������������������������ȵĹ��ӣ��Ӷ������ڼ۴��еĵ���ԾǨ�������ϴӶ�������������-��Ѩ�ԡ�һ���棬��������-��Ѩ��ʹ������Ũ�ȵ��������絼�����ӣ��ܴ�������С�����Խ������缫��ŷķ���Ϳռ������ĵ��Ʋ��̯����һ���棬���������ڰ뵼��/���Һ����ۼ����Ӱ뵼��������Һ����Na2TeO3�Ļ�ԭ�����������Ӱ���������缫/���Һ������Ʋ�ٽ����������ܶȵ����ӣ�ǿ���缫(�绯ѧ����)���̡���1000~1200 s�����̬-����ѭ��Ϊ������1100 s����ϵ���ڹ���״̬�Ժ����ܶ�Ѹ����������3.1 mA/cm2�����4.5 mA/cm2�����45%���������������Ҳ�õ���Ӧ��ߣ�ʹ���ڵ绯ѧ������ȡ���ܵĴ����߳�Ϊ���ܡ���ͼ3(b)���ɿ������ų���ʱ����ӳ���������Խ��Խ��������Ϊ����ʱ��Խ���绯ѧ��������ҲԽ��Խ����ʱ�����ո���Ĺ⣬��������Ĺ�������-��Ѩ�ԣ��ʹ����Ҳ��֮����
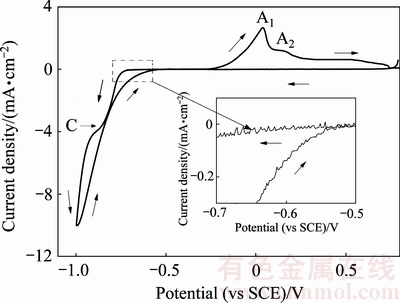
ͼ2 ����ֻ�����Na2TeO3���Һ��ϵ��ѭ����������
Fig. 2 Cyclic voltammogram of Na2TeO3 electrolyte system on stainless steel substrate

ͼ3 1 mol/L Na2TeO3+2.5 mol/L NaOH���Һ��ϵ�ڰ�̬�����µ�����ɨ����������Լ���ͨ���Ϲ�״̬�µ绯ѧ�����ĵ����ܶ�-ʱ������(��������Ϊ-0.75 V (vs SCE))
Fig. 3 Linear sweep voltammograms of 1 mol/L Na2TeO3+2.5 mol/L electrolyte system under dark and light(a), cathodic current-time curve in 1 mol/L Na2TeO3+2.5 mol/L electrolyte system under chopped illumination (��on�� and ��off�� stands for under light and dark, respectively) at deposition potential of -0.75 V (vs SCE)(b)
�����������ұ����ʵ�ʵ绯ѧ������ȡ�������õĹ��ա�Ϊ�˹�绯ѧ����ұ����ȡ����Ч�ԣ��Ժ�1 mol/L Na2TeO3��2.5 mol/L NaOH���Һ��ϵ�ڹ��պͰ�̬�½��к���������������õij��������ܶ�Ϊ100 A/m2��200 A/m2��

ͼ4 ���ò�ͬ���������ܶ��ڹ��պͰ�̬�µ绯ѧ�����ڵ�SEM��
Fig. 4 SEM images of electrodeposited Te with different deposition current densities under illumination and dark
������õIJ����ڵ���ò��ͼ4��ͨ���Աȿ�֪��绯ѧ�����ڵĿ����ߴ�����һ����Կ�����С���������ܶ��»�ò����ڵĿ�����С��֦����ۻ���������أ�������ǰ��ϵ�µij������̲���ȫ����ɢ����(�ܵ绯ѧ��Ӧ���ƣ���绯ѧ��Ӧ/��ɢ��Ͽ���)��֮ǰ�ڵ�Ũ��(10 mmol/L Na2TeO3+2.5 mol/L NaOH)���Һ��ϵ�е��о�[28]���������ղ�����ı��ڵ绯ѧ������ʼ�εijɺ�������ģʽ(��Ϊ��ά�����ɺ˺���ɢ��������)����ʵ�������ڲ��õĸ�Ũ�ȵ��Һ��ϵ�����֮��Ũ��������������ͣ���˴�����ڵ��γ���ζ�Ź��մٽ���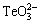 �ĵ绯ѧ��ԭ�Ϳ�������������Ҳ���������ڳ��������ڵ��ռ���
�ĵ绯ѧ��ԭ�Ϳ�������������Ҳ���������ڳ��������ڵ��ռ���
ͼ5(a)��(b)��ʾΪ��������ʱ�IJ۵�ѹ-ʱ�����ߡ���ͼ��֪���������ֳ��������ܶȣ�����ʱ���۲۵�ѹ�����Ե��ڰ�̬ʱ�IJ۵�ѹ�������֪���������ܶ�Ϊ100 A/m2ʱ���ù��պ�۵�ѹ������8%���������������ܶ�Ϊ200 A/m2ʱ�۵�ѹ������13%���۵�ѹU��Ҫ�����¼�������ɣ����۷ֽ��ѹEd����������λ����������λ������Һ��ŷķ��ѹ��IRsol���缫��ŷķ��ѹ��IRm������Ed���ɵ�ⷴӦ�ı��������������ն����Ӱ����Ժ��ԡ����������������ڹ�������-��Ѩ�IJ������������������ӵ�Ũ�ȣ��Ӷ������������缫(����)��ŷķ��IRm��ͬʱ����ʱ�����ӵ����·ֲ�(�ռ��ɲ��������Ũ�Ȼ���������)������p�Ͱ뵼���ڵķ����ܼ��������Ӷ���С�뵼���ڵ��ܴ����������Ϳռ��ɲ�����̯�ĵ��ƲҲ�����ڽ��Ͳ۵�ѹ��

ͼ5 �ڲ�ͬ���������ܶȹ��պͰ�̬�µ绯ѧ�����ڵIJ۵�ѹ��ʱ��ı仯
Fig. 5 Cell voltage-time curves of Te electrodeposition under light and dark at different deposition current densities
��1�г��˲�ͬ�������ڵ绯ѧ�����ĵ���Ч�� �Ǻ͵�������W������Ч�ʦ�Ϊ���������ʵ�ʲ���mE�����۲���mT֮�ȣ���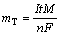 ������IΪ����ǿ�ȣ�tΪͨ��ʱ�䣬MΪ����ķ�������nΪ�缫��Ӧ�ĵ�������FΪ���׳�������������W=U��I��t/mE���ɱ�1��֪�����վ��������ڳ�����ϵ�ĵ���Ч�ʣ�����Ҫ����Ϊ�������������ڻ����������ϸߵĹ��Ӳ�����������-��Ѩ�ԣ����������ڵ糡�������»�Ӱ뵼��������Һ���Ӷ�������Һ�е�
������IΪ����ǿ�ȣ�tΪͨ��ʱ�䣬MΪ����ķ�������nΪ�缫��Ӧ�ĵ�������FΪ���׳�������������W=U��I��t/mE���ɱ�1��֪�����վ��������ڳ�����ϵ�ĵ���Ч�ʣ�����Ҫ����Ϊ�������������ڻ����������ϸߵĹ��Ӳ�����������-��Ѩ�ԣ����������ڵ糡�������»�Ӱ뵼��������Һ���Ӷ�������Һ�е�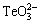 �ĵ绹ԭ���̣����Թ��������µ�����ڵĵ���Ч�ʻ�����������ͬʱ�ɱ�1Ҳ�ɿ������������ܶ�Ϊ100 A/m2ʱ��̬ʱ�ĵ�������Ϊ1.55 kWh/kg�������ù��պ����ܺ�ֵ���͵�1.42 kWh/kg����Լ������8%�������������ܶ�Ϊ200 A/m2ʱ��̬ʱ�ĵ�������Ϊ2.19 kWh/kg�������ù��պ����ܺ�ֵ���͵�1.94 kWh/kg����Լ������11%��������������������������������Ч�ʣ����͵绯ѧ��������ϵ�IJ۵�ѹ���Ӷ����͵������ġ�����Ӧ��˵�����ǣ�������ʵ��Ӧ��ʱ�ɲ�����Ȼ�⣬�˴��������ļ���ʱδ���ǹ�Դ���ܺġ�
�ĵ绹ԭ���̣����Թ��������µ�����ڵĵ���Ч�ʻ�����������ͬʱ�ɱ�1Ҳ�ɿ������������ܶ�Ϊ100 A/m2ʱ��̬ʱ�ĵ�������Ϊ1.55 kWh/kg�������ù��պ����ܺ�ֵ���͵�1.42 kWh/kg����Լ������8%�������������ܶ�Ϊ200 A/m2ʱ��̬ʱ�ĵ�������Ϊ2.19 kWh/kg�������ù��պ����ܺ�ֵ���͵�1.94 kWh/kg����Լ������11%��������������������������������Ч�ʣ����͵绯ѧ��������ϵ�IJ۵�ѹ���Ӷ����͵������ġ�����Ӧ��˵�����ǣ�������ʵ��Ӧ��ʱ�ɲ�����Ȼ�⣬�˴��������ļ���ʱδ���ǹ�Դ���ܺġ�
��1 ���ò�ͬ���������ܶ��ڹ��պͰ�̬�µ绯ѧ�����ڵĵ���Ч�ʡ��۵�ѹ�͵�������
Table 1 Current efficiency, cell voltage and energy comsuption of Te electrodeposition under illumination and dark at different deposition currents
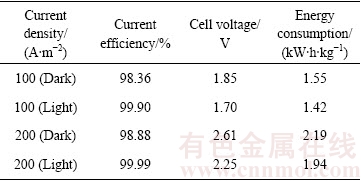
����������ȡʵ��Ľ�������ۿ�֪���볣��ĵ绯ѧ������ȣ����ù�绯ѧ�������п�ǿ���缫���̣���߳������ʡ�����Ч�ʺͲ��ܣ������Ͳ۵�ѹ�����ƣ���һ�������÷�չDZ����ұ����ȡ�¼���������Խ����Ҫ��Դ�ڳ���������������������������϶���ȵĹ��Ӻ��ܼ���������������-��Ѩ�ԡ���һ����ʹ������Ũ�ȵ���������С�˵����ʺ��ܴ�������ֱ�ӽ������缫��ŷķ����Ϳռ���������̯�ĵ��Ʋ��һ����������ӿ��ԴӰ뵼��������Һ�ٽ�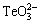 �ĵ绯ѧ��ԭ��
�ĵ绯ѧ��ԭ��
4 ��绯ѧұ�����������⼰�ں���չ
��Ȼ��绯ѧұ������ڴ�ͳ�绯ѧ��������һϵ�е����ƣ�����Ϊһ���¼�������δ����չ�����п�����һЩ������Ҫ�������Ҫ������1) ���ó��õ��˹���Դ����믵ơ�±�ٵƵȣ��������ܺĺͳɱ������������̫��������ܴ��������ȶ������⡣2) ���������ʵ͡���Դ�е��ڳ����뵼���϶���ȵĹ����������ã������ܹ����д��ڴ�϶���ȵIJ�������Ҳ��������(�Ȼ����̣���Thermolization��[29])�����������������Ŀ��з����Dz��þ��и߷���Ч�ʵĵ�ɫ��Դ(������������ڻ��Դ��ڲ���Ĵ�϶���ȼ���)����LED�ȡ�3) ��Ҫ��ֹ�����Ĺ�������¸��ϺͲ��븱��Ӧ����Ҫȷ�������Ĺ���Ӿ����ܶ�����Ŀ�껹ԭ��Ӧ�����������Ѩ���¸��ϻ��߲��븱��Ӧ��������ȡ�����������ͨ���Ż����Һ��ϵ�ͳ��������Խ��ͳ��������ȱ��(���ٷǷ��临�����ģ������ܼ����ʡ������)������������һЩ�������⣬����Һ������Ҫ����ܻ����(��Ҫ���ߵĹ�ѧ����)�����۵IJ�����(��Ҫ���ǹ�·)�������ں���ʵ�ʹ���Ӧ����Ҳ��Ҫ���Կ��ǡ�
���ֵ��ָ�����ǣ���绯ѧұ����һ˼·���ں������Խ�һ�����졣��ǰ�����о���֪����绯ѧұ��ʵ�����������ѳ����뵼��Ĺ��ת�����ԣ������մ��ڴ�϶���ȵĹ��Ӻ��������������ӣ�ʹ�õ缫/���Һ�ĵ�ѧ���ʷ����仯��ͬʱ���������Ӳ���绯ѧ�����ķ�Ӧ���ٽ������Ľ��С���һԭ��ʵ����Ҳ����Ӧ���ڰ뵼��������������ұ����̡����ڹ�绯ѧұ�𣬹�����������������Һ�ٽ����Һ�����ӵĵ绯ѧ��ԭ(�����ں�)����������������Ӳ���������Һ�����Dz���������Ļ�ԭ(��������)������(������Ѩ)����������ڰ뵼�����Ļ�ԭ��������������ˣ����ð뵼��Ԫ�ػ�����ܴ������϶���ȹ��Ӽ��������Ĺ��������Ӳ���ұ����̵�������ԭ��Ӧ����ʵ��ұ����ȡ���̵�ǿ�������������ڹ�绯ѧұ��ķ���(�����ں�)�����ڴ������ɫ�������������������뵼�������ʽ��������Ȼ�磬��˹�绯ѧұ����һԭ����Ϊ��Щ����Ĵ����ṩ�µ�;�����⽫�ں����о������Ա�����
5 ����
1) ����Թ�绯ѧ�������¼������а뵼��Ԫ�صĵ绯ѧ��ȡ����������ȡΪ����֤�����Ŀ����ԡ�
2) ��绯ѧ���������У��뵼�����������������������������϶���ȵĹ����ܼ���������������-��Ѩ�ԡ���һ����ʹ������Ũ�ȵ������������ʺ��ܴ�������С���������缫����̯�ĵ��Ʋ��һ����������ӿ��ԴӰ뵼��������Һ�ٽ��绯ѧ��ԭ��
3) �볣��ĵ绯ѧ������ȣ���绯ѧ�������п�ǿ���缫���̣���߳������ʡ�����Ч�ʺͲ��ܣ������Ͳ۵�ѹ�����ƣ��������õķ�չǰ����
4) ��绯ѧұ���δ����չ��һ������Ҫ�����Դѡ���������ʡ����������Ӹ��ϻ���븱��Ӧ����Һ������·��Ƶ����⣻��һ�������ں������Խ�һ����չ�����������ڰ뵼��Ԫ�صĵ绯ѧ���������ҿ������ڰ뵼����ﴦ����
REFERENCES
[1] O��KEEFE T J. Electrodeposition in extractive metallurgy: Anemerging technology?[J]. JOM, 1992, 44(4): 30-34.
[2] ������, ������, ����ΰ, ������, �� ��, �Ƴ���. �������Ӽ���Zn(��)-NH3-NH4Cl-H2O ��ϵ���п��Ӱ��[J]. �й���ɫ����ѧ��, 2017, 27(8): 1738-1747.
LIN Wen-rong, YANG Sheng-hai, SUN Yan-wei, CHEN Yong-ming, HE Jing, TANG Chao-bo. Effect of polyether additive on zinc electrodeposition in Zn(��)-NH3-NH4Cl-H2O system[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(8): 1738-1747.
[3] �� ï, ������, �� ��, �� Զ, ����Ԩ, �����. 300 kA���������������������ܽ�ģ��[J]. �й���ɫ����ѧ��, 2017, 27(2): 399-405.
LI Mao, GAO Yu-ting, BAI Xiao, LI Yuan, HOU Wen-yuan, WANG Yu-jie. Simulation of alumina particle dissolution in 300 kA aluminum electrolytic cell[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(2): 399-405.
[4] HA Y C, SOHN H J, JEONG G J, LEE C K, RHEE K I. Electrowinning of tellurium from alkaline leach liquor of cemented Te[J]. Journal of applied electrochemistry, 2000, 30(3): 315-322.
[5] ���㾲. �ؽ���ұ��ѧ[M]. ����: ұ��ҵ������, 2011: 74-316.
ZHAI Xiu-jing. Heavy metal metallurgy[M]. Beijing: Metallurgical Industry Press, 2011: 74-316.
[6] HOFFMANN J E,KING M G,CARAPELLA S C, OLDFIELD J E,PUTNAM R D. Tellurium and tellurium compounds[M]. Chichester: John Wiley & Sons, 2001: 6-7.
[7] RAO G M, ELWELL D, FEIGELSON R S. Electrowinning of silicon from K2SiF6-molten fluoride systems[J]. Journal of the Electrochemical Society, 1980, 127(9): 1940-1944.
[8] �� ��, ������, ������, ������, �� ��, ������, ��ҵ��. Na3AlF6-LiF������ϵ�й�ĵ������Ϊ[J]. ������ѧѧ��, 2011, 27(5): 1108-1115.
JIA Ming, LAI Yan-Qing, TIAN Zhong-Liang, LIU Fang-Yang, LI Jie, XIN Peng-Fei, LIU Ye-Xiang. Electrodeposition Behavior of Silicon from Na3AlF6-LiF melts[J]. Acta Physico-Chimica Sinica, 2011, 27(5): 1108-1115.
[9] �ֺ촺. �к������ڵ���ȡ������Ʊ��ߴ����о�[D]. ��ɳ: ���ϴ�ѧ, 2012: 36-39.
LE Hong-chun. Research on extraction of tellurium from neutralization sludge and electrolytic preparation of high purity tellurium[D]. Changsha: Central South University, 2012: 36-39.
[10] LIANG Xue-hai, KIM Y G, GEBERGZIABIHER D K, STICKNEY J L. Aqueous electrodeposition of Ge monolayers[J]. Langmuir, 2009, 26(4): 2877-2884.
[11] FINK C G, DOKRAS V M. Electrodeposition and electrowinning of germanium[J]. Journal of the Electrochemical Society, 1949, 95(2): 80-97.
[12] MATTEI R C D, FEIGELSON R S. Growth rate limitations in electrochemical crystallization[J]. Journal of Crystal Growth, 1978, 44(2): 115-120.
[13] SAITOU M, SAKAE K, OSHIKAWA W. Evaluation of crystalline germanium thin films electrodeposited on copper substrates from propylene glycol electrolyte[J]. Surface and Coatings Technology, 2003, 162(1): 101-105.
[14] BIEBER A L, MASSOT L, GIBILARO M, CASSAYRE L, TAXIL P, CHAMELOT P. Silicon electrodeposition in molten fluorides[J]. Electrochimica Acta, 2012, 62: 282-289.
[15] �� ��. �Ӻ����̳���������ȡ���о�[D]. ����: ����������ѧ, 2009: 10-11.
LIANG Jie. Research on leaching and extraction of germanium from germanium dust[D]. Kunming: Kunming University of Science and Technology, 2009: 10-11.
[16] �� ��, �� ��, ������, �����. ���������ӷ������ྦྷ�辫���յĸĽ�[J]. ��ɫ����: ұ������, 2013, 9: 56-59.
LIU Gang, QIN Rong, LIU Sheng-zhang, WANG Shu-ya. Improvement on rectification process of polycrystalline silicon by improved Siemens process[J]. Non-ferrous Metal (Smelting Section), 2013, 9: 56-59.
[17] MICHEELS R H, DARROW A D, RAUH R D. Photoelectrochemical deposition of microscopic metal film patterns on Si and GaAs[J]. Applied Physics Letters, 1981, 39(5): 418-420.
[18] WEIMER P K. A p-type tellurium thin-film transistor[J]. Proceedings of the IEEE, 1964, 52(5): 608-609.
[19] RAJESHWAR K. Encyclopedia of Electrochemistry[M]. Chichester: John Wiley &Sons Inc, 2007: 1-52.
[20] ����ͩ, ̷����. �绯ѧ�̳�[M]. ���: ����ѧ������, 2000: 219-221.
GUO He-tong, TAN Qi-xian. Course of electrochemistry. Tianjin: Tianjin UniversityPress, 2000: 219-221.
[21] ROSE T L, LONGENDORFER D H, RAUH R D. Photoelectrochemical deposition of metals onto p-silicon using an internal cell[J]. Applied Physics Letters, 1983, 42(2):193-195.
[22] INOUE T, FUJISHIMA A, HONDA K. Photoelectrochemical imaging processes using semiconductor electrodes[J]. Chemistry Letters, 1978(11): 1197-1200.
[23] MISHRA K K, RAJESHWAR K. A re-examination of the mechanisms of electrodeposition of CdX and ZnX (X= Se, Te) semiconductors by the cyclic photovoltammetric technique[J]. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry, 1989, 273(1/2): 169-182.
[24] SUGIMOTO Y, PETER L M. Photoeffects during cathodic electrodeposition of CdTe[J]. Journal of Electroanalytical Chemistry, 1995, 386(1): 183-188.
[25] MURASE K, MATSUI M, MIYAKE M, HIRATO T, AWAKURA Y. Photoassisted electrodeposition of CdTe layer from ammoniacal basic aqueous solutions[J]. Journal of the Electrochemical Society, 2003, 150(1): C44-C51.
[26] YANG Jia, LIU Fang-yang, LAI Yan-qing, LI Jie, LIU Ye-xiang. Photoelectrochemical deposition of CuInSe2 thin films[J]. Electrochemical and Solid-State Letters, 2012, 15(4): 19-21.
[27] FAN Y, YANG J, JIANG L, WANG Y, NG B K, SUN H, LAI Y, LI J, LIU F. Effects of illumination on the electrochemical behavior of selenium electrodeposition on ITO substrates[J]. Journal of the Electrochemical Society, 2017, 164(4): H225-H231.
[28] FAN Y, JIANG L, YANG J, LIU F. The electrochemical behavior of tellurium on stainless steel substrate in alkaline solution and the illumination effects[J]. Journal of Electroanalytical Chemistry, 2016, 771: 17-22.
[29] ������, ������. ̫���ܵ�ػ�����Ӧ��[M]. ����: ��ѧ������, 2009: 109-110.
XIONG Shao-zhen, ZHU Mei-fang. The foundmental and application of solar cell[M]. Beijing: Science Press, 2009: 109-110.
Photo-electrometallurgy for semiconductor elements extraction��taking tellurium as example
LIU Fang-yang, FAN Yan-yun, JIANG Liang-xing, LAI Yan-qing, LI Jie, LIU Ye-xiang
(School of Metallurgy and Environment, Central South University, Changsha 410083, China
Abstract: Photo-electrometallurgy technique was proposed for electrochemical extraction of semiconductor elements in this work aiming to solve the problems in electrometallurgy of semiconductor elements. Based on knowledge of semiconductor characters and photo-electrochemistry, the advantages of the proposed photo-electrometallurgy technique were revealed, and its superiority was experimentally confirmed by an example of tellurium (Te) electrochemical extraction. The results indicate that the semiconductor deposits can absorb the incident photons with energy larger than its band gap and be excited to generate electron-hole pair. The photon-generated electrons can flow from semiconductor electrode into electrolyte, enhancing the electrochemical reduction rate and the photon-generated-carriers can decrease the resistivity and band bending, reducing the potential drop at electrode. Compared with the traditional electrometallurgy, photo-electrometallurgy shows the advantages in intensifying process, reducing cell voltage, improving depositing rate, current efficiency and capacity, therefore exhibiting good development prospect. The issues that should be addressed in the future were also put forward and the connotation was expanded.
Key words: semiconductor element; illumination; cell voltage; photo-electrometallurgy; electrodeposition
Foundation item: Project(51774341) supported by the National Natural Science Foundation of China; Project (2015JJ2175) supported by the Natural Science Foundation of Hunan Province, China
Received date: 2017-11-21; Accepted date: 2018-01-02
Corresponding author: LIU Fang-yang; Tel: +86-731-88830474; E-mail: liufangyang@csu.edu.cn
(�༭ �� ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51774341)������ʡ��Ȼ��ѧ����������Ŀ(2015JJ2175)
�ո����ڣ�2017-11-21�������ڣ�2018-01-02
ͨ�����ߣ����������ڣ���ʿ���绰��0731-88830474��E-mail: liufangyang@csu.edu.cn