DOI��10.19476/j.ysxb.1004.0609.2018.02.25
��ѡ��Ǧ��������ѳ�����
�� ��1����ѧ��1����С��2���Ǻ���2
(1. ��̶��ѧ ��������ԴѧԺ����̶ 411105��
2. ��̶��ѧ ����ѧԺ����̶ 411105)
ժ Ҫ�����һ����(Tl)ƷλΪ48.75 g/t�ĺ�Tl��Ǧ�ֱ����ֱ�������������������-�������ʽ����-����ķ��������о�����Tl�����о��������˿�Ũ�ȡ�������������ʱ�䡢��ʽ����ʱ�䡢�������ʡ����������������¶ȡ�����ʱ������ض�Tlȥ���ʵ�Ӱ�졣�������������ֱ������ʹ�����������-������գ���TlЧ�����ѣ�Tlȥ���ʷֱ�Ϊ17.9%��33.1%�����ü�������-�����Tl���գ���TlЧ�����ã�����������Ϊ����������Ϊ1.25 L/min����Ũ��20%�������¶�Ϊ50 �棬����ʱ��32 h��������ϵH2SO4����12%�������¶�40 �棬����ʱ��3.5 h��Tlȥ���ʿɴﵽ83.4%����TlǦ����PbƷλΪ61.9%��Pb������Ϊ96.9%����Tl���Ǧ������Tl��ƷλΪ8.05 g/t������Ǧұ����ҵ��Ҫ��
�ؼ��ʣ��裻��Ǧ��������������
���±�ţ�1004-0609(2018)-02-0425-09���� ��ͼ����ţ�TF843.1���� ���ױ�־�룺A
Tl�Ƕ��Ժ�ǿ��ϡ��Ԫ�أ�Ǩ���������л���ɼ����Σ��[1-2]��Tl���������ᡢϡ�����У����ɿ����Ե��Σ������ڼ��Һ��[3-4]��Tl�ڽᾧ��ѧ�͵���ѧ�����Ͼ�����ʯ�����������ԣ�������ͬ��ʽ�滻�س�ʯ�����K+������Ԫ����ʽ�����ڷ�Ǧ��������п�����ͭ��ɰ���ۻơ��ƻƵ�������[5]����S֮�⣬Tl��Ҫ��As��Cu��Pb��Fe��Sb��Hg��Ag�γɹ���Ԫ�����[6]��
Tl����Ȼ���в��Ե��ʴ��ڣ�Tl��������ΪTl����������ο���[7-8]�����������о�����[9-10]����Tl��ʯ���Ȼ��Ƶ�������ϵ�У�TlǨ���������죬ͬʱ��������ϵ��pHֵԽ�ͣ��ζ�Խ�ߣ�Խ������Tl�ĻǨ�ơ����������£�Ҳ���൱���ֵ�Tl���ͷš��ر��ǵ������ʯ���汻���������Է�ˮ�IJ��������˶Ժ�Tl��ʯ�������������á���ˣ���Tl��ʯ����ұ�������ķ绯������TlǨ����ˮ�����Ҫ;��[11]��
��Tl����ұ�������У�Tl����̬��ʽ�ڴ�����Ǩ�ƣ����Tl�����ұ���Ǵ�����Tl����Ҫ��Դ[12-13]���о�����[14-18]����Ǧ�����к�Tl 20 g/t~3000 g/ t��������һ��̬��������ڣ���Tl2O��Tl2S��Tl2SO4�ȣ�ұ����Tl��Ҫ�������ս������С���ˣ���Ҫ��ұ�������е��ս��̳����л���Tl��������Ҫ��ֱ���� ��[19]���Ȼ�������[20]����ȡ��[21]���������[22]�ȡ������в���Tl���ɷ�����Tl�����ķ绯���˻��������ý���������ˮ�廷������ɻ�����Ⱦ[23-24]����ǰ��Tl��Ⱦ������ҪΪ��Ⱦ������ı������ƣ�һ��ָ��Tl��ʯ��ұ������TlǨ����ˮ��������������������IJ���Tl��Ⱦ������ʩ��ˮ����Tl��Ⱦ����������Ҫ������������ѧ�����������ﴦ���ȣ�����Tl��Ⱦ����������Ҫ�л�ѧ��������������������������[25-27]��Ŀǰ�����ڷ�Ǧ����п��Ⱥ�Tl��ʯұ��ǰԤ������Tl������о���δ������ر��������о����ǵ��ǴӺ�Tl����ұ��ǰֱ���ѳ�Tl���ں�Tl����Դͷ����Ⱦ�������Ч�ѳ�����һ�ֻ�����������Ⱦ���Ʒ�����
Ŀǰ��һЩǦұ����ҵ��Ǧ����ԭ���е�Tl����˱��������ϸ��Ҫ���磬�㶫�ع�ұ����Ҫ��Ǧ�����е�Tl���ô���10 g/t��Ȼ����Ǧ�����е�Tl�����ߵͲ�������������ɵģ������ɿ�ʯ���ʾ����ġ���ˣ�Ҫ����ұ����ҵ��Ҫ�ͱ���Ժ�TlǦ������ұ��ǰ����Ԥ������Tl������������һ�ֺ�Tl�ĸ�ѡǦ����Ϊ������ֱ�����������-������ս�����Tl�о���ΪǦ������Tl��Tl�Ļ��������ṩ�µ�;����
1 ��������뷽��
1.1 ����
����ȡ�Ժ��ϱ�ɽ��ɫ������ҵ�������ι�˾���Ǹù�˾Ǧпѡ����ѡ�õ��ķ�Ǧ��ĥ��ϸ��Ϊ-0.074 mm70%����Ҫ�ɷ�ΪPbS��ZnS��FeS2���ÿ�����Tl��Ʒλ��48.75��10-6�������Ķ�Ԫ�ط���������1��
��1 ����Ԫ�ط������
Table 1 Element analysis of ore sample (mass fraction)

1.2 Tl�ķֲ�����������(������ȡ)
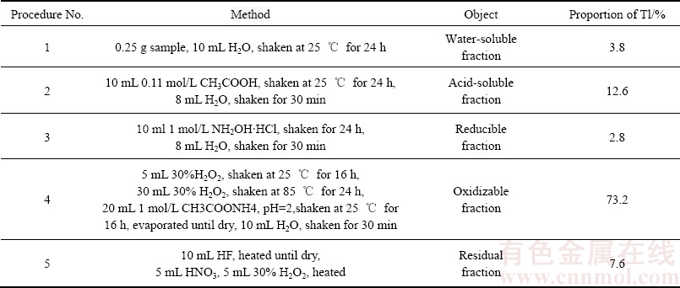
���о�����[28]��Tl�ڷ�Ǧ��������п���е�ˮ��̬����ɽ���̬(̼����)���ɻ�ԭ̬(�������������������̬)��������̬(������̬���л��ʽ��̬)�Լ�����̬(�����Ρ����������)���зֲ������зֲ���Pb��Zn�����п�����̬���ֵ�Tlռ�ܴ��������ͬ�����Pb��Zn�����п�����̬����Tl����Ҳ�нϴ�����𡣱�������øĽ���BCR������ȡ����[29]�����û�ѧҩ��ѡ������ȡ��Ʒ�в�ͬ���̬��TlԪ�أ���Tl�ڿ����еķֲ����������з��������������������2��
�ӱ�2��֪����������е�Tl��Ҫ�����������̬���֣�ռTl������73.2%������Tl��ˮ����(ռ3.8%)�����������(ռ12.6%)����ռ����Ҳ��С����ռ��Tl��16.4%��Tl�ֲ��ڿɻ�ԭ̬���ֺܵͣ���ռ2.8%������̬�е�Tlռ7.6%���ⲿ��Tl����Ǩ�ơ�
����������ȡ�����������������ڿ��������������Tl�ı�����Խϵͣ�����ֱ���������˵ķ��������ܴﲻ��������Tl��Ŀ�ģ���Ҫ�Կ�����������Ԥ������
1.3 ���鷽��
1.3.1 ֱ�������Tl
ȡ����200 g�������ձ��У�����һ����������ˮ��һ����H2SO4��ˮԡ���¼��ȣ���������280 r/min������һ��ʱ�䡣��ʱ�ⶨ��pHֵ��Һλ��������ʧ������ˮ���䡣���������ⶨ��������Tl��Ʒλ��������Tl��ȥ���ʡ�
1.3.2 ������������-�����Tl
�������Tlǰ���ô������ƶԿ�����������������
ȡ����200 g�������ձ��У�����һ������ˮ�����Ӵ������ƣ���������150 r/min����Ӧһ��ʱ���Һ�̷��룬���ù�����������Tl��������Tl��ȥ���ʡ�
1.3.3 ��ʽ����-�����Tl
��ѧ���[30-31]���о��������ڼ��Լ��������£�O2�������и�ǿ��������������ˣ��������Tlǰ���ڼ��������£��ÿ����Կ�����������������
��2 BCR������ȡ����
Table 2 BCR sequential extraction procedures
ȡ����200 g�������ձ��У�����һ������ˮ����10 g NaOH�����������ˮԡ���¼��ȣ���������350 r/min��������ϵH2SO4����15%����Ũ��30%�������¶�60 �棬����ʱ��8 h��������ʧ������ˮ���䡣��Ӧһ��ʱ���Һ�̷��룬���ù�����������Tl������ʽ(1)����Tl��ȥ���ʺ�Pb�Ļ�����R��
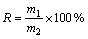 (1)
(1)
ʽ�У�m1Ϊ��TlǦ������Ǧ��������m2Ϊ��Tlǰ������Ǧ��������
1.4 ��������
Tl��Ʒλ��Agilent 7900�����ϵ����������Dzⶨ��pHֵ���״�PHSJ-4A��ȼƲⶨ��������Tl�ķֲ�״̬�������ּ���ȡ������������������ǰ�������ò��JSM-6610LV��ɨ��羵������
2 ���������
2.1 ֱ�������Tl
2.1.1 ������ϵH2SO4�����Ϳ�Ũ�ȶ�Tlȥ���ʵ�Ӱ��
�ڽ����¶�40 �棬����ʱ��8 h�����£����������ϵH2SO4����(���������������Կ��������İٷֱ�)�Ϳ�Ũ�ȶ�Tlȥ���ʵ�Ӱ�죬�����ͼ1��ʾ��
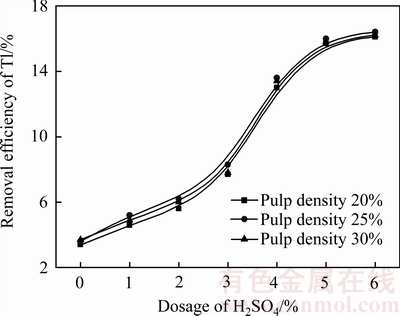
ͼ1 ����������Tlȥ���ʵ�Ӱ��
Fig. 1 Effect of dosage of sulfuric acid on removal efficiency of Tl
��ͼ1��֪��������ˮ��ʱ��Tl��ˮ��Һ����һС�����ܽ⣬Լռ3.4%��Tl���Ž�����ϵH2SO4����Խ����ȥ����Խ�ߣ��ر��ǵ�H2SO4����3%~4%ʱ��Tl��Ǩ�ƻ���������ǿ��ȥ��Ч�����ԣ���H2SO4��������5%��Tlȥ������������ƽ������ʱ��������ϵ����pH��2����ͼ2��
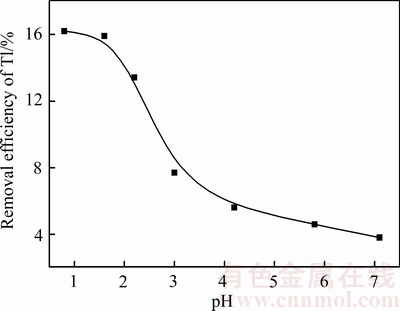
ͼ2 ������ϵ����pH��Tlȥ���ʵĹ�ϵ
Fig. 2 Relationship between pH and removal efficiency of Tl
�ɱ�2��֪���൱һ���ֵ�Tl�����ڿ�������������У����H2SO4������Tlȥ���ʵ�Ӱ�켫������ϵ��H+�Ĵ��ڣ��ܽ��˿����е�̼���Σ�ʹ�ֲ��ڿ�������������е�Tl�õ��ͷţ�����H+��Tl�����������Ŵ����ã������Tl��Ǩ�ƻ��ԡ���Ũ�ȶ�Tlȥ����Ӱ�첻�������ͷ���������Һ��Tl��Ũ�ȼ��ͣ���������������Ӱ���С���£�����Ũ�ȹ������ڳ�ֽ��衣��ˣ���ѡȡTl�����������H2SO4����5%����Ũ��30%��
2.1.2 ����ʱ����¶ȶ�Tlȥ���ʵ�Ӱ��
�ڽ�����ϵH2SO4����5%����Ũ��30%�����£��������ʱ����¶ȶ�Tlȥ���ʵ�Ӱ�죬�����ͼ3��ʾ��
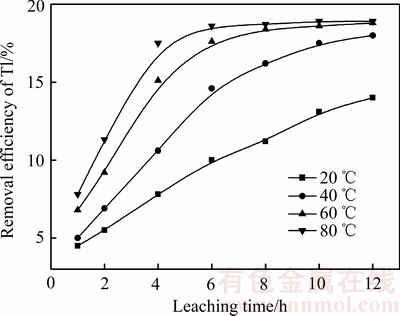
ͼ3 ����ʱ���Tlȥ���ʵ�Ӱ��
Fig. 3 Effect of leaching time on the removal efficiency of Tl
ͼ3�����������£�Tl��Ǩ�ƽ�Ϊ���������Ž�����ϵ�¶����ߣ�Tl�Ļ�����ǿ��Ǩ�����ʼӿ죬�����˵������ƽ���ʱ�䡣���������������������������¼��Ƚ�����ֻ��һС����Tl��Ǩ����������Һ�У�Tlȥ���ʲ�����17.9%��������Ϊ��ֱ��������Դﵽ�Ϻõ���TlЧ����
2.2 ������������-�����Tl
������ϵH2SO4����10%����Ũ��30%�������¶�60 �棬����ʱ��8 h�������������Ũ�Ⱥ�����ʱ���Tlȥ���ʵ�Ӱ�죬�����ͼ4��ʾ��
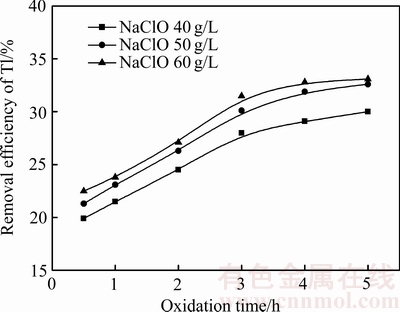
ͼ4 ����ʱ���Tlȥ���ʵ�Ӱ��
Fig. 4 Effect of oxidation time on the removal efficiency of Tl
��ͼ4��֪���������ƶԿ�������������Tl��ȥ������һ��������������Ũ��50 g/Lʱ����������Ũ�ȣ�Tlȥ�������Ӳ����ԡ�����4 h��Tl��ȥ���ʽ�Ϊ33.1%���䷴Ӧʽ���£�
ClO-+PbS��PbSO4+Cl-, E(ClO-/ Cl-)=1.389 V (2)
��Ǧ��(PbS)���汻ClO-����������ˮ��PbSO4Ĥ�������˿�����һ�����������谭�˿��������ڲ���Tl��Ǩ�ơ���ˣ�ѡȡ�������ƶԿ�������Ԥ������ͬ��Ҳ�ﲻ���������TlЧ��.
2.3 ��ʽ����-�����Tl
2.3.1 ����ʱ����¶ȶ�Tlȥ���ʵ�Ӱ��
��ʽ����ʱ���ڳ�������1.5 L/min����Ũ��15%�����������£���������ʱ����¶ȶ�Tlȥ���ʵ�Ӱ�죬�����ͼ5��ʾ��
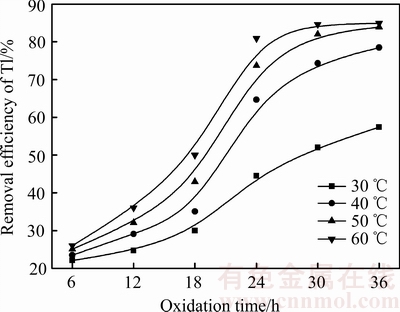
ͼ5 ����ʱ���Tlȥ���ʵ�Ӱ��
Fig. 5 Effect of oxidation time on removal efficiency of Tl
ͼ5��������ʽ������Ҫ�ϳ��ķ�Ӧʱ�䣬�ڷ�Ӧ���ڣ�Tlȥ�������ӻ�����������18~24 hʱ��Σ�ȥ����������ߡ�ͬʱ���ʵ�����߽�����ϵ�¶��ܹ���ǿTl��Ǩ�ƻ��ԣ��������Tlȥ�����ʣ����̽���ʱ�䣬�����¶�Խ�ߣ������ܽ���Ũ�Ƚ��ͣ��������ʼ���������������ʱ����ߵ������¶ȣ��ᵼ�³ɱ������ӣ����ѡȡ�������ʱ��Ϊ32 h����������¶�Ϊ50 �档
ͼ6����������������������NaOH�����ܷ��������·�Ӧ��
PbS+O2+OH-�� PbS2O3+H2O (3)
MxSy+O2+OH-��M(OH)n+ S2O32-+H2O (4)
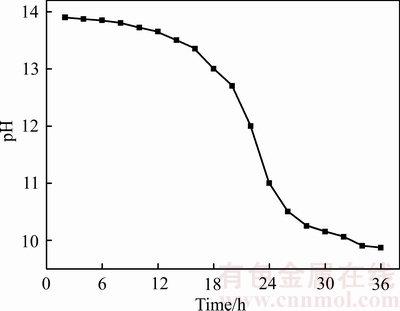
ͼ6 pH�ı仯����
Fig. 6 Changing curve of pH
2.3.2 �������ʺͿ�Ũ�ȶ�Tlȥ���ʵ�Ӱ��
��ʽ����ʱ���������¶�50 �棬����ʱ��24 h�����������£�����������ʺͿ�Ũ�ȶ�Tlȥ���ʵ�Ӱ�죬�����ͼ7��ʾ��
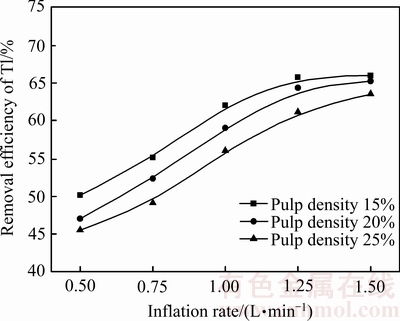
ͼ7 �������ʶ�Tlȥ���ʵ�Ӱ��
Fig. 7 Effect of inflation rate on removal efficiency of Tl
��ͼ7��֪����������Խ�죬��������Խ�죬���������ʴ���1.25 L/minʱ�������������Ӳ����ԣ�������Ϊ�����������ﵽ���ͣ�������Ӧ��ϵ����ƽ�⡣��Ũ��ԽС��ͬ���ij��������£���ϵ�пɽӴ����õ��ܽ���Խ�࣬Խ������������Ӧ�Ľ��У�ͬʱ��������Խ����Լ�����Ũ�ȶ�������Ӧ��Ӱ�졣��˿�ѡȡ��ѳ�������Ϊ1.25 L/min����Ũ��20%��
2.3.3 ������ϵH2SO4�������¶ȶ�Tlȥ���ʵ�Ӱ��
��ʽ����ʱ���ڿ�Ũ��20%�������¶�50 �棬��������1.25 L/min������ʱ��32 h�������£��Լ���ʽ����ʱ���ڽ�����ϵ��Ũ��25%������ʱ��8 h�����������£����������ϵH2SO4�������¶ȶ�Tlȥ���ʵ�Ӱ�죬�����ͼ8��ʾ��
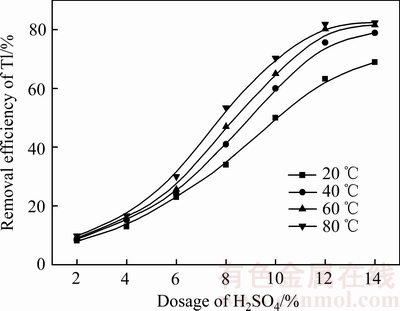
ͼ8 H2SO4������Tlȥ���ʵ�Ӱ��
Fig. 8 Effect of dosage of sulfuric acid on removal efficiency of Tl
ͼ8��������������ϵH2SO4����С��6%ʱ��Tlȥ���ʵͣ���H2SO4����6%~10%ʱ��Tlȥ����������ߣ�����������ʽ�������γɵ������κ���������������¸����ڿ���������棬�谭��Tl��Ǩ�ơ�H2SO4�������������ܽ⣬ʹ�����ڲ�Tl���Ա�¶��ͬʱ��H+����ʹ��Tl��Ǩ�ƻ�����ǿ����Ӧһ��ʱ����ܴﵽ�Ϻõ�ȥ��Ч����
��Ҫ��Ӧʽ�������£�
Fe(OH)3+H+��Fe3++H2O (5)
Zn(OH)2+H+��Zn2++H2O (6)
CaCO3+H+��Ca2++ CO2��+H2O (7)
�ۺϿ��ǣ�ѡȡ��ѽ����¶�Ϊ40 �棬�����������Ϊ12%��
2.3.4 �������ʺͽ���ʱ���Tlȥ���ʵ�Ӱ��
��ʽ����ʱ���ڳ�������1.25 L/min�������¶�50�棬��Ũ��20%�������£��Լ���ʽ����ʱ���ڽ�����ϵH2SO4����12%��������Ũ��25%�������¶�40 ������������£����������ϵ�������ʺͽ���ʱ���Tlȥ���ʵ�Ӱ�죬�����ͼ9��ʾ��
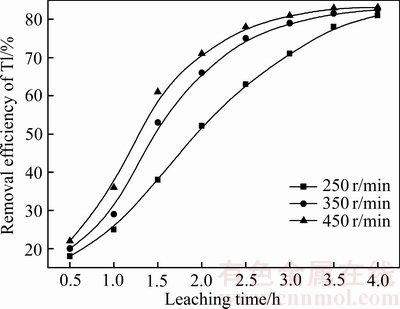
ͼ9 �������ʺͽ���ʱ���Tlȥ���ʵ�Ӱ��
Fig. 9 Effect of stirring speed and leaching time on removal efficiency of Tl
ͼ9�������������ʻ��Tl��ȥ��������һ��Ӱ�죬�����������������̽���ʱ�䣬��������Tl��ȥ����Ӱ���С������������350 r/minʱ������Tl����ƽ���ʱ��Ϊ3.5 h��������ʼ�Σ�Tlȥ���������Ի�������������Ϊ��һ����Ҫ���ܽ����������渲�����ˣ���ѡȡ��ѽ�������Ϊ350r/min������ʱ��Ϊ3.5 h��
2.3.5 ����ʱ���Pb�����ʼ�Ʒλ��Ӱ��
����ѵ�����������(��ʽ����ʱ����������1.25 L/min�������¶�50�棬��Ũ��20%����ʽ����ʱ��������ϵH2SO4����12%��������Ũ��25%�������¶�40 �棬��������350 r/min������ʱ��3.5 h)����������ʱ���Pb�����ʼ�Ʒλ��Ӱ�죬�����ͼ10��ʾ��
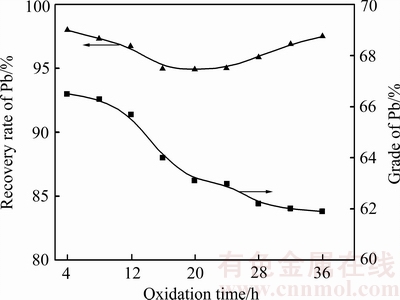
ͼ10 ����ʱ���Pb�����ʼ�Ʒλ��Ӱ��
Fig. 10 Effect of oxidation time on recycling efficiency and grade of Pb
ͼ10������Ǧ������Pb��Ʒλ������ʱ�����н��ͣ�Pb������������ʱ��24 hǰ�ʽ������ƣ�Pb�����ʴ�98.1%������94.8%������ʱ��24 h��Pb�����ʳ��������ơ�������������ԭ�������PbS����������PbS2O3�ĵ�λ�ϵ�(E(PbS|S2O32-)=0.5 V)����Ӧ���У�PbS2O3�ٱ�������PbSO4����PbS2O3���ܽ�ȱ�PbSO4����Pb�����ʳ��Ƚ����������ơ���TlǦ����Ʒλ���ͷ���С��ԭ����Ǧ�����л�����(FeS2)����п��(ZnS)��������ͬ������������̼���������Խ���ʱ�ܽ⣬��֤����TlǦ�����Ʒλ��
��Ҫ��Ӧʽ��
PbS+O2+OH-��PbS2O3+H2O (8)
PbS2O3+O2��PbSO4 (9)
������Ӧʽ���£�
FeS2+ O2+OH-��Fe(OH)3 +S2O32-+H2O (10)
ZnS+ O2+OH-��Zn(OH)2 +S2O32-+H2O (11)
M(OH)n+nH+��Mn+ +n H2O (12)
�����Ŀ���������ְ�����������п�����ʽ���������У���������п��������������ɿ����ܵ���������������Tl��һ���̶��������Pb��Ʒλ��ͬʱʹ���������ϵ�Tl�õ��ͷţ������Tl��ȥ���ʡ�
�ڵ�������������ϣ�ѡȡ������ؽ����ظ������顣���������3���С�
��3 �ظ���������
Table 3 Duplicate tests under optimum condition
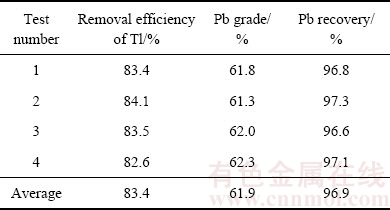
��3���������������������£�Ǧ������Tlȥ����ƽ��Ϊ83.4%����TlǦ����PbƷλƽ��ֵΪ61.9%��Pb������ƽ��ֵΪ96.9%��
2.4 ��ʽ����Ԥ�����Է�Ǧ�������Ӱ��
������ʽ����ǰ���XRD����ͼ11��ʾ��ͨ���Աȿɵã���������ʽ����������PbSO4�࣬�����ڷ�Ǧ��ֻ�Dz�����������ˣ���������Ԥ��������Ҫ��PbS����ڣ������TlǦ���������ұǦ�ӹ�����Ӱ�첻����Ǧ(S2-)������ˮ��Һ�б�����ΪS2O32-�ĵ�λΪ0.5 V���ң���Ӧ�����У�����Ϊ��Ǧ�ȱ�������S2O32-����O2����ʱ��S2O32-���һ��������SO42-(E(S2O32-|SO42-)=0.17 V)�����������ܷ�Ӧʽ���£�
PbS+O2+OH-��PbSO4+H2O (13)
ȡ����������������ǰ�����ֱ���е羵ɨ�裬��ͼ12��ʾ��ͼ12���������������ʽ����ǰ������Ϲ⻬ƽ��������ʽ�����������������ɶ�ס��ۺϷ��������ƶϿ�����ʽ�������䷽Ǧ����ṹ����ƻ���ʹ��������Tl��¶����Կ����ڲ����������ϵ�Tl�Ľ����Ƿdz������ġ�
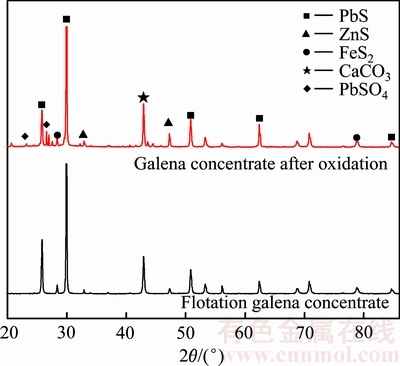
ͼ11 ��Ǧ������ǰ���XRD��
Fig. 11 XRD patterns of galena concentrate before and after oxidation

ͼ12 ��ʽ����ǰ��SEM��
Fig. 12 SEM images of ore surface
3 ����
1) ����ֱ������ʹ�����������-������գ���TlЧ�����ã�Tlȥ���ʷֱ�Ϊ17.9%��33.1%��
2) ���ü�ʽ����-�����Tl���գ��нϺõ���TlЧ����Tl�����ʴﵽ83.4%����ѹ�������Ϊ����ʽ����ʱ����������1.25 L/min�������¶�50 �棬��Ũ��20%��������ϵH2SO4����12%����Ũ��25%�������¶�40 �棬��������350 r/min������ʱ��3.5 h����Tl��õ���Ǧ�����Ʒ��Ǧ��ƷλΪ61.9%��Ǧ�Ļ�����Ϊ96.9%��Tl����������Ϊ8.05 g/t���������й�ұ����ҵ��Ǧ�����е�Tl���ô���10 g/t��Ҫ��
REFERENCES
[1] �� ��, ������, �촫��. ���Ͻ�Ǧп�����衢��Ԫ�طֲ������о�[J]. ������ʯ����ѧͨ��, 2014, 33(5): 753-758.
JIANG Kai, YAN Yong-feng, ZHU Chuan-neng. The distribution research of thalium and cadmium in Jinding lead-zinc deposit, Yunnan province[J]. Bulletin of Mineralogy, Petrology and Geochemistry, 2014, 33(5): 753-758.
[2] ������, ��ΰ��, Ф�Ƹ�. ��ķֲ���������ʽ�뻷��Σ��[J]. ����ѧ��, 2005, 25: 230-236.
HE Li-bin, SUN Wei-qing, XIAO Tang-fu. Distribution and occurring forms of thallium and its potential damage to the environments[J]. Acta Mineralogica Sinica, 2005, 25: 230-236.
[3] PANDEY G P, SINGH A K, PRASAD S, et al. Development of surfactant assisted kinetic method for trace determination of thallium in environmental samples[J]. Microchemical Journal, 2015, 118(2): 150-157.
[4] KAZANTZIS G. Thallium in the Environment and Health Effects[J]. Environmental Geochemistry & Health, 2000, 22(4): 275-280.
[5] PETER A L J, VIRARAGHAVAN T. Thallium: A review of public health and environmental concerns[J]. Environment International, 2005, 31(4): 493-501.
[6] �´���, ������, �δ���. ����ֲ���ǭ������ľ����(��)�ij���Ӧ��[J]. ���ݹ�ҵ��ѧѧ��(��Ȼ��ѧ��), 2000, 29(5): 32-38.
CHEN Dai-yan, ZOU Zhen-xi, Ren,Da-gen. A preliminary application of the geobiotanical method to the Lanmuchang thallium(mercury) ore deposits in southwest Guizhou[J]. Journal of Guizhou University of Technology (Natural Science Edition), 2000, 29(5): 32-38.
[7] ��ӱ��, ������, ��С��. ����������������̬�ֲ�������Դ[J]. ���ݴ�ѧѧ��(��Ȼ��ѧ��), 2003(2): 419-422.
WU Ying-juan, CHEN Yong-heng, CAO Xiao-an. Phase dispersion and origin of thallium in pyritical slag[J]. Journal of Guangzhou University (Natural Science Edition), 2003(2): 419-422.
[8] CHESTER R, SOHAIL M, OGDEN M I, et al. A calixarene- based ion-selective electrode for thallium(��) detection[J]. Analytica Chimica Acta, 2014, 851: 78-86.
[9] �� ƽ, �ϼ, ������. ���ڻ������е���̬�ֲ���̼���������ͷŹ����е�����[J]. ������ѧѧ��, 2007, 27: 166-170.
ZHANG Ping, YANG Chun-xia, CHEN Yong-heng. The phase distribution of thallium in pyrite and the role in the process of carbonate in the release[J]. Acta Scientiae Circumstantiae, 2007, 27: 166-170.
[10] ANTON M A L, SPEARS D A, SOMOANO M D, et al. Thallium in coal: Analysis and environmental implications[J]. Fuel, 2013, 105(7):13�C18.
[11] �� ��, �ű���, ����ƽ. �й�������������軷����Ⱦ�о�[J]. �й���ѧ: �����ѧ, 1997, 27(4): 331-336.
ZHANG Zhong, ZHANG Bao-gui, LONG Jiang-ping. Thallium pollution research in the process of thallium deposit development[J]. Journal of Eaeth Science, 1997, 27(4): 331-336.
[12] �ϼ. ������������ù����ж����ؽ������Ǩ���ͷ���Ϊ�о�[D]. ����: �й���ѧԺ�о���Ժ(���ݵ���ѧ�о���), 2004.
YANG Chun-xia. The migration and release of thallium in the exploitation of pyrite containing thallium[D]. Guangzhou: Guangzhou Institute of Geochemistry, Chinese Academy of Sciences, 2004.
[13] ��ӱ��, �ϼ, ������. �������ղ�������ķֲ��ͻ�������[J]. ���ݴ�ѧѧ��(��Ȼ��ѧ��), 2009, 8(5): 58-63.
WU Ying-juan, YANG Chun-xia, CHEN Yong-heng. Distribution and environmental contribution of thallium in roasting outcome of pyrite[J]. Journal of Guangzhou University (Natural Science Edition), 2009, 8(5): 58-63.
[14] VANEK A, G ROSSLOVA Z, MIHALJEVIC M, et al. Thallium contamination of soils/vegetation as affected by sphalerite weathering: A model rhizospheric experiment[J]. Journal of Hazardous Materials, 2015, 283: 148-156.
[15] CHAEAM V. Thallium contamination of water in Canada[J]. Water Quality Research Journal of Canada, 2001, 36(4): 851-877.
[16] ��־��, ����, ������. ������ɫұ�������е���Ϊ��Σ��������[J]. ɽ������, 2007, 27(6): 47-51.
LIU Zhi-hong, LI Hong-fei, LI Qi-hou. Behavior harm and prevention of thallium in nonferrous attractive metallurgy[J]. Shanxi Chemical Industry, 2007, 27(6): 47-51.
[17] ������. пǦͭұ�����������;��̽��[J]. �й���ɫұ��, 2015, 44 (1): 67-70.
GUO Tian-li. Exploration of thallium treatment in zinc, lead and copper smelting[J]. China Nonferrous Metallurgy, 2015, 44(1): 67-70.
[18] �Է��. ����пԭ��ʪ��ұ��������ʵ��[J]. ��ɫ��ұ, 2008, 24(3): 24-26.
ZHAO Feng-gang. The practices of Tl-Zn materials in the hydrometallurgy[J]. Non-Ferrous Mining and Metallurgy, 2008, 24(3): 24-26.
[19] ���. ��������ֱ�ӽ������о�[J]. �й���ɫұ��, 2001, 30(6): 26-29.
LI Jing-cun. Investigation on derect leaching of material with low thallium[J]. China Nonferrous Metallurgy, 2001, 30(6): 26-29.
[20] �� Ԫ. ���ʪ����ȡ�ߴ�����о�[J]. ���ݻ���, 2000(4): 1-4.
FANG Yuan. Preparation of high pure thallium from thallium ore by wet process[J]. Guizhou Chemical Industry, 2000(4): 1-4.
[21] �۴���, ³����, ������. ��ȡ���Ӻ����̳����ۺϻ���ϡɢ�������о�[J]. ��ɫ����(ұ������), 2014(10): 57-58.
SHAO Chuan-bing, LU Xing-wu, MA Ai-jun. Study of Comprehensive Recovery of Scattered Metals from Thallium- bearing Dust with Extraction Method[J]. Nonferrous Metals (Extractive Metallurgy), 2014(10): 57-58.
[22] ����ƽ. ������Ӻ���������ȡ��Ĺ����о�[D]. ����: ����������ѧ, 2009.
ZHOU Qing-ping. Vacuum distillation extraction thallium from slag containing thallium[D]. Kunming: Kunming University of Science and Technology, 2009.
[23] ������, �� ƽ, ��ӱ��. �㶫��������Ⱦ�IJ���ԭ������Ⱦ���ƶԲ�[J]. ���ݴ�ѧѧ��(��Ȼ��ѧ��), 2013, 12(4): 26-31.
CHEN Yong-heng, ZHANG Ping, WU Ying-juan. The reasons and the control technology for thallium pollution in Beijiang, Guangdong Province[J]. Journal of Guangzhou University ( Natural Science Edition), 2013, 12(4): 26-31.
[24] �赤��. ����������˾�����������˾����Ͻ������β����Һ��������[D]. ����: ���ݴ�ѧ, 2016.
LI Dan-dan. Thiobacillus ferrooxidans and thiobacillus thiooxidans combined leaching thallium ore tailings and the toxicityevaluation of leaching solution[D]. Guiyang: Guizhou university, 2016.
[25] �����, �ź��, ������. pH���¶ȼ���ʼ��Ũ�ȶ������λ�ԭ�������Ӱ��[J]. ��������ѧ��, 2014, 8(10): 4105-4109.
CHEN Wei-ting, ZHANG Hong-guo, CHEN Yong-heng. Effect of pH, temperature and initial concentration on thallium removal by sulfate-reducing bacteria[J]. Chinese Journal of Environmental Engineering, 2014, 8(10): 4105-4109.
[26] ������, ������, Ϳ����. �ؽ�������Ⱦ�����ζԲ��о���չ[J]. ����, 2007, 39(4): 528-535.
LIU Jing-yong, CHANG Xiang-yang, TU Xiang-lin. Thallium Pollution and Its Countermeasures. Soils, 2007, 39(4): 528-535.
[27] ��˳��, ������, ��ʥ��. ˮ���������Ⱦ���������о���չ[J]. ˮ��������, 2014, 40(2): 15-19.
WAN Shun-li, WAN Ming-hai, XU Sheng-you. Removal technologies of thallium from waster: A review[J]. Technology of Water Treatment, 2014, 40(2): 15-19.
[28] �� ��, �� ��, ������. Ǧп��ұ�������������̬�ֲ���ת������[J]. ���ִ�ѧѧ��(�����ѧ��), 2015, 45(1): 1509-1510.
LIU Juan, WANG Jin, SU Long-xiao. Morphological distribution and transformation characteristics of thallium in the process of lead and zinc ore smelting[J]. Journal of Jilin University(Earth Science Edition) , 2015, 45(1): 1509-1510.
[29] KARBOWSKA B, ZEMBRZUSKI W, JAKUBOWSKA M, et al. Translocation and mobility of thallium from zinc-lead ores[J]. Journal of Geochemical Exploration, 2014, 143(3): 127-135.
[30] ��ѧ��, ������, ����ΰ. �Ӻ���������н�����ķ���: CN, CN 103773952 A[P]. 2014.
TIAN Xue-da, WANG Tie-Gang, GUO Shi-Wei. A method of gold leaching from pyrite concentrate containing gold: CN, CN 103773952 A[P]. 2014.
[31] ��ѧ��, ������, ����Ȼ. һ�ֺ�����Ǧ����������ѳ�����: CN, CN 105400954 A[P]. 2016.
TIAN Xue-da, WANG Tie-Gang, YANG Zi-Ran. A method of thallium removal from lead sulfide concentrate containing thallium: CN, CN 105400954 A[P]. 2016.
Removal of thallium from flotation galena concentrate
CHENG Lin1, TIAN Xue-da1, ZHANG Xiao-yun2, RUI Hai-feng2
(1. College of Environment and Resources, Xiangtan University, Xiangtan 411105, China;
2. College of Chemical Engineering, Xiangtan University, Xiangtan 411105, China)
Abstract: To remove Tl from a galena concentrate with a Tl grade of 48.75 g/t, some processes such as direct acid leaching, sodium hypochlorite oxidation-acid leaching and basic oxidation -acid leaching, were investigated, and the effects of inflation rate, pulp density, sodium hypochlorite oxidation time, basic oxidation time, dosage of sulfuric acid, leaching temperature and leaching time on the Tl removal efficiency were studied. The experiment results show that the Tl removal efficiencies are only 17.9% and 33.1% by direct acid leaching process and sodium hypochlorite oxidation-acid leaching process, respectively. However, through basic oxidation-acid leaching process, the Tl removal efficiency can reach up to 83.4% under the condition of inflation rate 1.25 L/min, pulp concentration 20%, oxidation temperature 50 ��, basic oxidation 32 h, dosage of sulfuric acid 12%, leaching temperature 40 �� and leaching time 3.5 h. The thallium grade in thallium removed sulfide concentrates is 8.05 g/t, the grade and recovery of lead are 61.9% and 96.9%, respectively, which meet the requirements of lead smelting enterprises.
Key words: thallium; galena; concentrate; oxidation; leaching
Received date: 2016-11-29; Accepted date: 2017-07-04
Corresponding author: TIAN Xue-da; Tel: +86-15200330996; E-mail: snowy@xtu.edu.cn
(�༭ ��ѧ��)
�ո����ڣ�2016-11-29�������ڣ�2017-07-04
ͨ�����ߣ���ѧ����ڣ���ʿ����ʿ���绰��15200330996��E-mail: snowy@xtu.edu.cn