包埋固定化Rhodopseudomonas palustris对邻氯苯酚的降解
董怡华1, 2,胡筱敏3,张玉革1,高丹1
(1. 沈阳大学 环境学院,辽宁 沈阳,110044;
2. 沈阳大学 区域污染环境生态修复教育部重点实验室,辽宁 沈阳 110044;
3. 东北大学 资源与土木工程学院,辽宁 沈阳 110004)
摘要:以海藻酸钠为包埋载体,活性炭为添加材料,对沼泽红假单胞菌Rhodopseudomonas palustris PSB-1D进行固定化,通过正交试验确定固定化微生物小球的最佳制备条件:活性炭添加量为1%,海藻酸钠质量分数为3%,包埋菌体与包埋材料的质量比为1/20。在最佳条件下,微生物小球培养7 d后对2-氯苯酚(2-CP)的降解率为72.6%。对比研究微生物小球和游离细菌的降酚效果。将微生物小球引入序批式好氧生物反应器(SBR)工艺中,分别研究小球投加量、曝气时间、曝气量对生物反应器降解2-氯苯酚效果的影响。试验结果表明:微生物小球对2-CP的降解率较游离细菌有明显提高。在黑暗好氧条件下,有效容积为5 L的固定化生物反应器对2-CP模拟废水降解处理的最佳稳定工艺条件为:微生物小球投加量为20 g,曝气时间10 h,曝气量为100 L/h。在此条件下,经过连续30个周期的测定,微生物小球对2-CP的平均去除率始终保持在65%左右。
关键词:固定化微生物;沼泽红假单胞菌;2-氯苯酚;序批式好氧生物反应器(SBR);废水处理
中图分类号:X703.1 文献标志码:A 文章编号:1672-7207(2014)04-1369-08
Biodegradation of o-chlorophenol by embedded immobilized Rhodopseudomonas palustris
DONG Yihua1, 2, HU Xiaomin3, ZHANG Yuge1, GAO Dan1
(1. School of Environment, Shenyang University, Shenyang 110044, China;
2. Key Laboratory of Regional Environment and Eco-remediation, Ministry of Education, Shenyang 110044, China;
3. College of Resources and Civil Engineering, Northeastern University, Shenyang 110004, China)
Abstract: In order to enhance degradation efficiency, a strain of o-chlorophenol degrading photosynthetic bacteria, named Rhodopseudomonas palustris PSB-1D, was immobilized with sodium alginate as immobilizing carrier and activated carbon as additive material. The optimal preparation condition of the immobilized cells was determined as follows: 1% of activated carbon, 3% of sodium alginate and 1/20 of the mass ratio of the embedded biomass and investment material. Under the optimal immobilization condition, the removal rate of o-chlorophenol by the immobilized cells is 72.6% after 7 d culture time. The o-chlorophenol degrading efficiency of the immobilized cells and free cells were studied and compared with each other. The immobilized cells were then added to the sequencing batch reactor (SBR) and the effects of reaction parameters(immobilized cells addition, aeration time, aeration rate) on o-chlorophenol degradation efficiency in the reactor were studied. The results indicate that immobilized cells have higher o-chlorophenol degradation ability than free cells. Under the condition of dark aerobic, the optimum technological conditions for the bioreactor with effective volume 5 L are as follows: aeration time 10 h, immobilized cells addition 20 g, and aeration rate 100 L/h. Under the conditions, bioreactor system could treat the o-chlorophenol wastewater effectively and steadily, with the removal rate of 65% or so.
Key words: immobilized cells; Rhodopseudomonas palustris; o-chlorophenol; sequencing batch reactor (SBR); wastewater treatment
氯酚类化合物(CPS)广泛应用于杀虫剂、杀菌剂、防腐剂的生产制造和造纸工业[1-2],具有“三致”(致癌、致畸、致突变)效应和遗传毒性[3-4],被美国、中国等世界诸多国家列入优先污染物名单[5]。生物降解是去除CPS的重要有效途径,而利用光合细菌处理高浓度有机废水是近20多年发展起来的一种新型废水生物处理技术。光合细菌(PSB)法由于工艺设备简单、有机负荷高、菌体能综合利用、不造成二次污染等优良特性,在有机废水处理中正引起人们的高度重视[6-7]。光合细菌的类群较多,用于有机废水治理最多的为沼泽红假单胞菌(Rhodopseudomonas palustris)。该类菌种具有灵活的代谢特性,它们不仅能在厌氧光照条件下以低级脂肪酸、多种二羧酸、醇类、糖类、芳香族化合物等有机物作为光合作用的电子供体进行光能异氧生长,而且能在黑暗有氧条件下以有机物为呼吸基质通过三羧酸循环途径进行有机酸的代谢[8],这种在光照厌氧和黑暗好氧条件下均能降解有机物的特性,决定其良好的应用前景[9]。然而,由于Rhodopseudomonas palustris的细胞相对较小((0.75~1.0) μm×(1.2~2.5) μm),易被原生动物捕食,固液分离困难,在应用中不可避免地产生菌体流失等问题,造成出水水质生物耗氧量(BOD)和化学耗氧量(COD)偏高,无法达到直排标准[10]。采用固定化微生物技术,将菌体细胞同载体结合并固定化,可提高其沉降性能,保持包埋菌占优势,且可增加菌体的抗毒性能和耐受力[11]。固定化微生物技术是通过物理或化学手段将游离微生物细胞定位于限定的空间区域,并使其保持活性反复利用的方法[12]。固定化细胞的制备方法按照固定载体与作用方式的不同,可分为3种类型:吸附法、包埋法与交联法[13]。其中,包埋法是将微生物包埋在富含营养、对外部环境相对封闭的颗粒中。对内部的微生物而言,颗粒形成了一个稳定的微环境,对外部环境起缓冲作用,颗粒的微环境有利于微生物增殖,易于固液分离,且耐毒物冲击较强。国内外学者已对包埋固定化技术处理废水进行了大量研究[14-15]。但利用该技术对Rhodopseudomonas palustris固定化处理氯酚废水的研究目前鲜有报道。
本文采用海藻酸钠作为包埋载体,活性炭为添加材料,对Rhodopseudomonas palustris进行包埋固定化研究。以2-氯苯酚(o-chlorophenol,2-CP)降解率E为考察指标,通过正交试验确定最佳包埋条件;将固定化微生物小球投入SBR生物反应器中对2-CP模拟废水进行降解试验,确定最佳工艺条件。通过本研究,以期为今后固定化微生物技术在氯酚类化合物废水处理中的实际应用提供科学依据。
1 材料与方法
1.1 微生物菌株
试验所用的菌株PSB-1D为某农药厂排污口下游水体浅层底泥中分离、筛选、驯化、诱变得到。该菌对2-CP具有良好的耐受和降解能力[16-17]。经鉴定菌株PSB-1D为沼泽红假单胞菌(Rhodopseudomonas palustris),为紫色非硫菌科红假单胞菌属,16SrDNA序列为GenBank Accession No. HM068966。
1.2 培养基
在厌氧条件下,制造PSB-1D培养基(BM1)的条件:丙酸钠3.0 g,酵母膏2.0 g,MgSO4 0.258 g,CaSO4 0.156 g,KH2PO4 0.6 g,K2HPO4 0.4 g,微量元素液 (Zn,Mn,Co,Mo) 1 mL,蒸馏水1000 mL,pH=7.0。
在好氧条件下,制造PSB-1D培养基(BM2)的条件:葡萄糖3.0 g,(NH4)SO4 0.2 g,酵母膏0.6 g,MgSO4 0.258 g,CaSO4 0.156 g,KH2PO4 0.6 g,K2HPO4 0.4 g,微量元素液 (Zn,Mn,Co,Mo) 1 mL,蒸馏水1000 mL,pH=7.0。
其中,微量元素液组成:H3BO3 1.5 g,ZnSO4・7H2O 0.06 g,MnSO4・H2O 0.8 g,CuSO4・5H2O 0.1 g,CoSO4・7H2O 0.01 g,(NH4)6Mo7O24・4H2O 0.2 g,蒸馏水1 000 mL。
1.3 固定化微生物小球的制备
将培养72 h左右的PSB-1D种子液以10%的接种量接种至装有BM1培养基的锥形瓶中(含质量浓度为50 mg/L的2-CP),加少量无菌水定容至150 mL。用黑色塑料纸包住锥形瓶四周,将锥形瓶置于温度为30 ℃,转速为130 r/min的恒温空气浴振荡箱中黑暗条件下培养4 d。采用Anke TGL-16GB高速离心机将培养液于6 000 r/min高速离心10 min,倾去上清液收集菌体。
将海藻酸钠和活性炭以一定的质量比配制成100 mL混合悬浮液,水浴加热溶解至糊状。待冷却至30 ℃,将糊状物和所收集的湿菌体按一定质量比进行充分混合。用10 mL注射器于20 cm高处把糊状混合物快速地滴入不断搅拌的质量分数为2%的CaCl2溶液中,制成直径为5 mm左右的小球。将小球浸泡在CaCl2溶液中,并置于4 ℃冰箱内固化交联24 h。将固化交联后的小球用蒸馏水清洗2次,即得固定化微生物小球。
1.4 不同供养光照的培养条件
(1) 光照厌氧条件:取30粒微生物小球投加至装有150 mL BM1培养基的具塞细口瓶中(含质量浓度为50 mg/L的2-CP)。盖紧瓶盖,用封口膜封口包扎。将细口瓶静置于30 ℃,光照度为4400 lx的光照培养箱中进行光照培养,定期取样。
(2) 光照好氧条件:取30粒微生物小球投加至装有150 mL BM2培养基的锥形瓶中(含质量浓度为50 mg/L的2-CP)。将锥形瓶放于转速为130 r/min的小型振荡器上,置于光照培养箱中于30 ℃,光照度为4400 lx条件的光照培养箱中进行光照培养,定期取样。
(3) 黑暗厌氧条件:取30粒微生物小球投加至装有150 mL BM1培养基的具塞细口瓶中(含质量浓度为50 mg/L的2-CP)。盖紧瓶盖,用封口膜封口包扎。用黑色塑料纸将细口瓶包严后静置于30 ℃恒温生化培养箱中黑暗培养,定期取样。
(4) 黑暗好氧条件:取30粒微生物小球投加至装有150 mL BM2培养基的锥形瓶中(含质量浓度为50 mg/L的2-CP)。用黑色塑料纸包住锥形瓶四周,将锥形瓶于温度为30 ℃,转速为130 r/min的恒温空气浴振荡箱中黑暗培养,定期取样。
上述每种培养条件试验均设1组平行试验和1组无菌小球对照试验。
1.5 SBR反应器试验装置和运行方式
试验装置为自行设计的生物反应器,装置如图1所示。该生物反应器的主体为圆柱形容器,由有机玻璃制成,其内径为100 mm,高700 mm,有效容积为5 L。沿侧壁设3个排水阀门。反应器内固定化微生物小球所需的氧气由ACO-318型空气压缩机曝气提供,并由LZB-6型转子流量计调节曝气量,DO(溶解氧) 值控制在2~5 mg/L,通过RSS-5100型便携式溶解氧分析仪在线测定溶解氧DO质量浓度。反应器中放置玻璃加热棒,以维持恒温(30±2)℃。
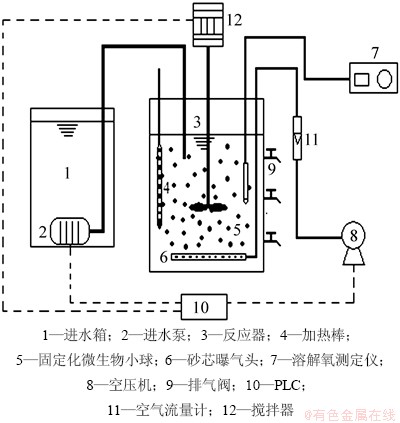
图1 试验装置示意图
Fig. 1 Schematic diagram of experimental setup
试验采用序批式好氧生物反应器(SBR)工艺,设计为每个运行周期12 h,包括进水→曝气→沉淀→排水→静置等5个阶段。进水、排水均为5 min,曝气时间需根据固定化微生物小球对2-CP的降解效果而定。由于试验采用固体化小球处理废水,沉淀时间很短,故设置沉淀时间为30 min,静置时间为1 h。反应器顶部和四周用黑色塑料纸遮光,保证降解反应在黑暗好氧条件下进行。
1.6 SBR反应器试验废水
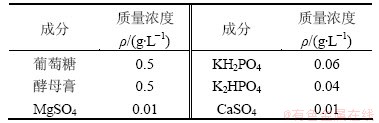
采用人工配水模拟2-CP实际废水。模拟废水成分如表1所示,用自来水进行配制。其中,废水pH为7.0,2-CP的质量浓度根据具体试验而定。
表1 模拟废水成分
Table 1 Composition of synthetic wastewater
1.7 分析项目及测定方法
1.7.1 采样和预处理
试验对锥形瓶培养液进行每天定时取样测定2-CP,对SBR反应器进行静置1 h后出水取样测定2-CP。将水样5 mL于8 000 r/min高速离心10 min,取上清液用正己烷(AR)萃取,将萃取液经0.22 μm微滤膜过滤后收集于5 mL棕色玻璃瓶中待分析测定。
1.7.2 分析方法
采用日立(Hitachi)L-2000高效液相色谱仪(HPLC)测定,分析条件为:C18反相柱(4.6 mm×200 mm),柱温30 ℃;紫外检测器检测波长273 nm;流动相为甲醇45%,高纯水55%;流速1.0 mL/min;进样量25 μL。
2-CP降解率的计算公式如下:
 (1)
(1)
其中:E为降解率;ρ无菌为无菌对照的2-CP质量浓度;ρ处理为固定化微生物小球处理后的2-CP质量浓度。
2 结果与分析
2.1 固定化条件的选择
海藻酸钠是存在于褐藻类中的天然高分子,易与一些二价阳离子结合形成凝胶,而且因其温和的溶胶凝胶过程、良好的生物相容性、稳定的物化性能,使海藻酸钠适于作为包埋微生物细胞的微胶囊[18],故本试验选择海藻酸钠作为包埋材料。为增强固定化微生物小球的机械强度,提高小球的传质性能,选择活性炭作为固定化的添加材料。考察海藻酸钠的浓度、活性炭的添加量、包埋菌体量对固定化微生物小球的制备过程及对2-CP降解效果所产生的综合影响,采用正交试验法,设计3个因素3个水平的正交表L9(3)3。试验所选条件如表2所示。
在表2所示的不同条件下,以2-CP降解率E为考察指标分析固定化操作条件,结果如表3所示。以每种条件下不接菌的固定化小球处理作为对照试验,小球培养时间为7 d。
表2 固定化条件正交实验因素及水平
Table 2 Condition of orthogonal experiments with immobilized cells
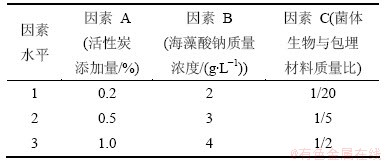
表3 实验结果分析
Table 3 Analysis of experimental results
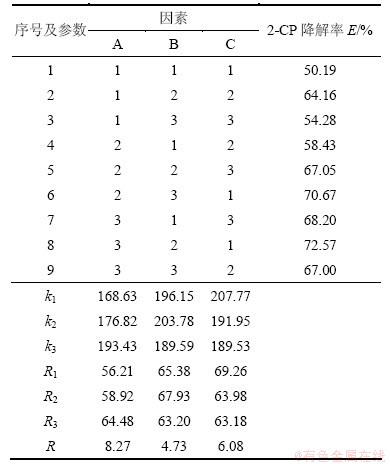
由表3中R的取值可知:各因素对试验结果的影响程度从大至小依次为因素A,因素B和因素C,说明活性炭添加量对2-CP降解效果影响最大,其次是包埋菌体量;海藻酸钠浓度虽然对2-CP降解有一定影响,但是,影响程度较小。此外,2-CP降解率随着活性炭添加量的增加而增加,可能是由于活性炭是多孔性的疏水型吸附剂,具有巨大的比表面积,添加后可以改善固定化微生物小球的传质性能且不影响菌体的生长;海藻酸钠浓度存在最佳值,过高或过低都会影响2-CP降解效果,可能是由于海藻酸钠的质量浓度过高,会增加基质和产物的传质阻力,使小球硬度过强,不利于菌体生长,从而使2-CP去除效果变差;海藻酸钠浓度过低,成球效果相对较差,同样不利于菌体包埋以及对2-CP的去除;包埋菌体量也存在最佳值,其值过高或过低也会影响2-CP的降解效果,可能是由于当包埋菌体量达到限制光合细菌繁殖的浓度时,继续提高包埋菌体量,由于营养缺乏,不但导致2-CP降解率下降,增加制备成本,而且还会影响固定化微生物小球本身的通透性和含水量。
结合因素水平变化趋势和材料成本综合分析,确定用海藻酸钠包埋Rhodopseudomonas palustris制备固定化微生物小球的最佳条件为A3B2C1,即:活性炭添加量为1%,海藻酸钠质量分数为3%,包埋菌体与包埋材料质量比为1/20。在此条件下制得的固定化微生物小球的SEM照片如图2所示。
由图2(a)和(b)可见:固定化微生物小球表面和内部结构的分布状况。微生物小球表面有层极薄的致密球壳,小球内部呈深浅不一的粗糙多孔结构,孔洞直径在1~3 μm之间。当包埋光合细菌后,发现大量不规则微生物细胞聚集群落,细胞任意分布在孔洞内,说明内部的多孔洞微细结构有利于反应底物和营养物质的传递以及微生物细胞在载体内部的附着和增殖生长。而小球致密的外表面球壳又可以有效阻止小球内部菌细胞的外流。这样,光合细菌菌细胞在载体内部获得明显增殖。
2.2 不同供氧光照对固定化微生物小球降解2-CP效果的影响
为考察不同光照和氧气组合对固定化微生物小球降解2-CP的影响,分别将小球置于黑暗好氧、黑暗厌氧、光照好氧及光照厌氧条件下培养7 d,每天定时测定2-CP的质量浓度,结果如图3所示。
试验结果表明:固定化微生物小球在4种条件下都能对2-CP进行降解,并且固定化微生物小球在好氧条件下对2-CP的降解效果整体好于厌氧条件,其中在黑暗好氧条件下培养7 d后对2-CP的降解率为75.6%,降解效果好于光照厌氧条件(此条件下培养7 d对2-CP的降解率为47.1%)。这可能是由于在充氧和搅拌过程中,培养基中2-CP与固定化微生物小球充分接触,有利于2-CP的传质,从而更好地被菌体细胞代谢。而在厌氧条件下,由于小球处于静止沉淀状态,细菌被包埋于小球中,不能够像游离细菌那样均匀悬浮分散于培养液中,与培养基中2-CP接触不充分,故2-CP降解效果相对较差。因此,在后续试验及SBR反应器试验过程中,选择黑暗好氧进行培养固定化微生物小球。

图2 包埋固定化微生物小球及其微生物空间分布SEM照片
Fig. 2 SEM of immobilized microorganism gelatinous pellet and its microbial spatial distributions
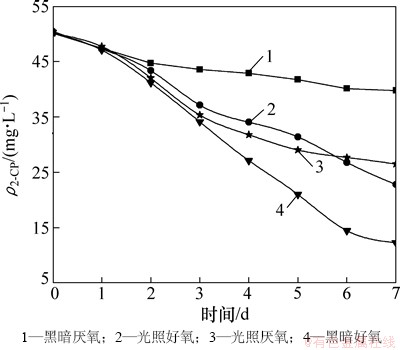
图3 不同供氧光照对PSB-1D降解2-CP效果的影响
Fig. 3 Influence of ways of illumination and oxygen on 2-CP degradation
2.3 固体化细菌与游离细菌对2-CP降解性能的比较
将固定化微生物小球、相同包埋菌体量的游离细菌PSB-1D和等量包埋材料制成的无菌小球分别于黑暗好氧条件下培养7 d,以含酚无菌培养液为空白试验,以添加无菌固定化小球的含酚培养液为对照试验,结果如图4所示。
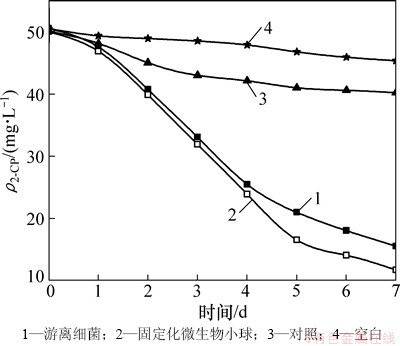
图4 游离细菌和固定化细菌的比较试验
Fig. 4 Comparison test of free bacteria and immobilized bacteria
由图4可见:常压下空白试验过程中出现2-CP挥发现象,但挥发速率较慢(培养7 d后2-CP去除率为10.2%)。其原因可能是2-CP的高水溶性和高溶剂化作用降低2-CP的挥发性。从对照实验2-CP的变化曲线可见:无菌小球对2-CP有一定的去除作用(培养7 d后2-CP去除率为19.7%),这主要是因为包埋材料对2-CP有一定的吸附作用,但吸附量相对较少,并且经过一段时间后,包埋材料对其吸附达到饱和。故培养基中2-CP的损失主要来源于Rhodopseudomonas palustris共代谢作用下对2-CP的降解。由固定化微生物小球和游离细菌降解2-CP的试验可知,培养7 d后固定化微生物小球对2-CP的降解率为76.5%,游离细菌对2-CP的降解率为69.2%,固定化微生物小球对2-CP的降解效果好于游离细菌提高。这是由于固定化载体内部具有较大的孔隙率,有利于底物的扩散与传质,更有利于菌体和底物的接触,这为菌体细胞在固定化微生物小球中的生长提供了良好的条件[19],载体对固定于其中的微生物起到了保护作用,并且使细菌的停滞期缩短。
2.4 各种影响因素对SBR工艺处理2-CP废水的影响
2.4.1 固定化微生物小球投加量对2-CP降解效果的影响
在反应器内加入5 L含2-CP质量浓度为50 mg/L的模拟废水,分别投加不同质量的固定化微生物小球(湿重分别为4 g,10 g,20 g和40 g),研究SBR反应器中固定化小球投加量对2-CP降解效果的影响。其中,曝气时间为10 h,曝气量为100 L/h,沉淀时间为30 min,静置时间为1 h。以等量的固定化无菌小球为对照试验。试验结果如图5所示。
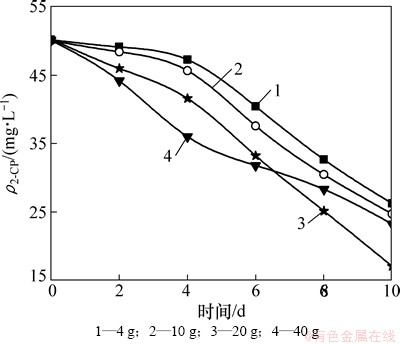
图5 固定化微小球投加量对2-CP降解效果的影响
Fig. 5 Degradation of 2-CP at different addition amount immobilized cells
从图5可知:固定化微生物小球的投加量与2-CP的降解率之间并非呈正比关系,即当固定化微生物小球的投加量小于20 g时,随着小球投加量的增加,2-CP的降解效果相应增加;而当固定化微生物小球的投加量大于20 g时,随着其投加量的增加,2-CP的降解效果反而减小。其原因可能是,在氧气和营养物质充分的情况下,增大固定化微生物小球的投加量,即增大废水中PSB-1D的细胞浓度,从而增强对2-CP的降解作用,而且固定化小球越多,废水与固定化小球接触面积越大,基质和溶解氧等更容易进入到固定化小球内部,更利于内部光合细菌增殖,从而更利于降解2-CP;然而,若持续增大固定化微生物小球的投加量,2-CP降解率开始逐渐下降。其原因可能是废水中的营养物质和供氧是有限的,过多的微生物会引起PSB-1D细胞之间对反应底物、氧气和营养物质的竞争,使得细胞整体处于贫营养和缺氧状态,导致的PSB-1D细胞生长周期延迟、新增细胞减少,最终导致2-CP降解效果变差。综上所述,确定试验中固定化微生物小球的最佳投加量为20 g。在此条件下,曝气10 h时对2-CP的降解率为66.1%。
2.4.2 不同曝气时间对2-CP降解效果的影响
废水进入SBR反应器后,由于微生物对污染物的吸收、分解需要一定的时间和过程,因此,曝气时间在很大程度上影响废水处理效果。
本试验在模拟废水2-CP初始质量浓度分别为高(150 mg/L)、中(100 mg/L)、低(50 mg/L)3种条件下,研究SBR反应器内不同曝气时间对固定化微生物小球降解2-CP效果的影响。其中,微生物小球添加量为20 g,曝气量为100 L/h,沉淀时间为30 min,静置时间为1 h。以等量的固定化无菌小球为对照试验。试验结果见图6。
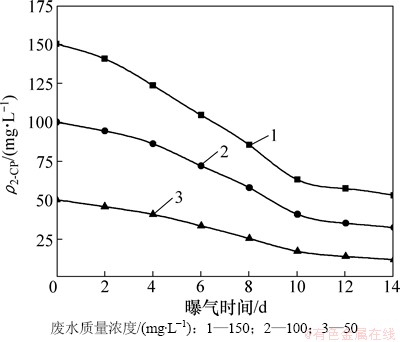
图6 不同曝气时间对2-CP降解效果的影响
Fig. 6 Degradation of 2-CP at different aeration time in SBR
从图6可见:在2-CP不同初始浓度条件下,随着曝气时间的增加,模拟废水中2-CP的质量浓度均呈下降趋势。在反应初始时,3种浓度条件下的2-CP降解速率均较缓慢,其原因可能是PSB-1D菌体细胞包埋于固定化颗粒内,由于包埋材料对固定颗粒外界物质的传质阻力,基质和溶解氧达到包埋材料内部与PSB-1D菌体细胞充分接触需要一段时间;之后,随着曝气时间的增加,2-CP降解速率迅速提高。而当曝气时间大于10 h,2-CP质量浓度下降趋势趋于缓慢。当曝气时间为10 h时,低、中和高3种2-CP初始质量浓度条件下的模拟废水中2-CP降解率分别为65.6%,59.0%和57.9%。因此,从2-CP降解效果和经济节能综合考虑,选定最佳反应时间为10 h。
2.4.3 不同曝气量对2-CP降解效果的影响
在SBR反应器中,改变曝气量,研究不同溶解氧条件对模拟废水中2-CP降解率变化的影响。其中,反应器内模拟废水2-CP的初始质量浓度为50 mg/L,微生物小球添加量为20 g,曝气时间为10 h,沉淀时间为30 min,静置时间为1 h。以等量的固定化无菌小球为对照试验。试验结果如表4所示。
表4 废水中不同溶解氧对2-CP去除的影响
Table 4 Removal of 2-CP at different DO mass concentrations in SBR

从表4可知:当曝气量为30 L/h时,2-CP降解率仅为35.2%;随着曝气量的增加,2-CP的降解率也在逐渐增加,当曝气为120 L/h时,2-CP降解率达最大,其值为69.8%。分析其原因,曝气不仅提供光合细菌生理过程中所需的DO,还可以起到搅拌作用,增大固定化颗粒与废水的接触面积;当曝气量过小时,固定化微生物小球的流化效果不理想,甚至会出现载体堆积现象,且溶解氧过少不利于营养基质扩散到固定化微生物小球内部,从而不利于菌体生长。比较曝气量分别为100 L/h和120 L/h时2-CP的降解情况可知(降解率分别为66.6%和69.8%):当废水中DO控制在5.0 mg/L以上时,继续提高曝气量,对2-CP降解率的影响并不是很明显。并且曝气量过大还会导致流化速度过快,固定化载体碰撞剧烈,影响固定化小球机械强度,降低小球使用寿命,同时也增加了能耗。故在SBR反应器中曝气量控制在100 L/h左右较佳。
2.4.4 SBR生物反应器操作运行的稳定性
为检验固定化光合细菌SBR法处理含氯酚废水的稳定性,在上述确定的优化运行参数条件下,每个周期测定进水和出水中2-CP质量浓度。每个周期结束时,滤出固定化微生物小球,用蒸馏水冲洗后再次加入到新鲜的模拟废水中,进行下一个周期的操作。其中,微生物小球添加量为20 g,曝气时间为10 h,曝气量为100 L/h,沉淀时间为30 min,静置时间为1 h。实验结果如图7所示。
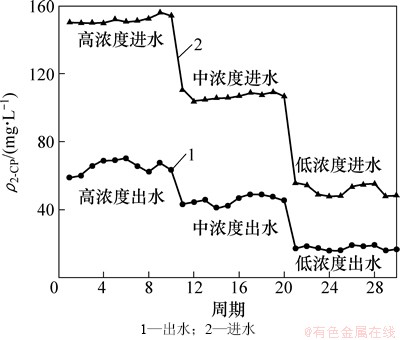
图7 SBR系统稳定性分析
Fig. 7 SBR system stability analysis
从图7可见:进水2-CP质量浓度在50~150 mg/L范围内时,2-CP平均去除率为65%左右,表现出明显的抗冲击负荷能力,且去除率长期保持稳定。因此,固定化光合细菌生物反应器的操作是可行的,具有一定的实际应用价值。
3 结论
(1) 通过以2-CP降解率为指标的正交试验确定了海藻酸钠包埋菌体Rhodopseudomonas palustris PSB-1D制备固定化微生物小球的最优试验方案为:活性炭添加量为1%,海藻酸钠质量分数为3%,包埋菌体与包埋材料质量比为1/20。在此条件下制得的微生物小球对2-CP的降解率为72.57%。
(2) 固定化微生物小球在不同光照供氧组合条件下均可降解2-CP,其中微生物小球在黑暗好氧条件下对2-CP降解效果最好,降解率为75.6%,明显高于光照厌氧条件的47.1%。
(3) 固定化微生物小球对2-CP的降解率为76.5%,游离细菌对2-CP的降解率为69.2%,菌体Rhodopseudomonas palustris PSB-1D被海藻酸钠包埋形成固定化小球后对2-CP的降解效果明显提高。
(4) 将固定化微生物小球投加到有效容积为5 L的固定化生物反应器中,对模拟含酚废水进行试验研究,确定其最佳工艺条件为:反应时间10 h,固定化微生物小球投加量为20 g,曝气量为100 L/h。在此条件下,对2-CP的去除率始终维持在65%左右,系统显示出稳定的2-CP去除性能。
参考文献:
[1] Zhang Y M, Pu X J, Fang M M, et al. 2,4,6-trichlorophenol (TCP) photobiodegradation and its effect on community structure[J]. Biodegradation, 2012, 23(4): 575-583.
[2] Herrera Y, Okoh A I, Alvarez L, et al. Biodegradation of 2,4-dichlorophenol by a Bacillus consortium[J]. World Journal of Microbiology and Biotechnology, 2008, 24(1): 55-60.
[3] Petroutsos D, Katapodis P, Christakopoulos P, et al. Removal of p-cholrophenol by the marine microalga Tetraselmis marina[J]. Journal of Applied Phycology, 2007, 19(5): 485-490.
[4] Bao W H, Peng R H, Zhang Z, et al. Expression, characterization and 2,4,6-trichlorophenol degradation of laccase from Monilinia fructigena[J]. Molecular Biology Reports, 2012, 39(4): 3871-3877.
[5] United States Environmental Protection Agency. Report EPA 822-R-02-047[R]. Washington. D C: National Recommended Water Quality Criteria: 2002.
[6] 戴晓, 张光明. 光合细菌(Z08)啤酒废水资源化研究[J]. 哈尔滨工业大学学报, 2010, 42(6): 937-940.
DAI Xiao, ZHANG Guangmin. Brewery wastewater treatment and resource recovery by photosynthetic bacteria Z08[J]. Journal of Harbin Institute of Technology, 2010, 42(6): 937-940.
[7] 郭冉冉, 向少能, 夏婷, 等. 光合细菌对氯氰菊酯的降解作用[J]. 四川农业大学学报, 2009, 27(4): 471-474.
GUO Ranran, XIANG Shaoneng, XIA Ting, et al. Effects of photosynthesis bacteria on cypermethrin degradation[J]. Journal of Sichuan Agricultural University, 2009, 27(4): 471-474.
[8] Zhao L, Zhao C G, Han D X, et al. Anaerobic utilization of phenanthrene by Rhodopseudomonas palustris[J]. Biotechnology Letters, 2011, 33(11): 2135-2140.
[9] Carlozz P, Pushparaj B, Degl’Innocenti A, et al. Growth characteristics of Rhodopseudomonas palustris cultured outdoors, in an underwater tubular photobioreactor, and investigation on photosynthetic efficiency[J]. Applied Microbiology and Biotechnology, 2006, 73(4): 789-795.
[10] 刘建红, 王雷荣. 海藻酸钠、聚乙烯醇包埋固定化技术对紫色非硫光合细菌脱氢酶活性影响的试验研究[J]. 安全与环境工程, 2009, 16(3): 54-56.
LIU Jianhong, WANG Leirong. Impact of the immobilization technology with sodium alginate and polyvinyl alcohol (PVA) on the dehydrogenase activity of purple non-sulfur photosynthetic bacteria[J]. Safety and Environmental Engineering, 2009, 16(3): 54-56.
[11] 毛雪慧, 徐明芳, 刘辉, 等. 光合细菌固定化及其处理含油废水的研究[J]. 农业环境科学学报, 2009, 28(7): 1494-1499.
MAO Xuehui, XU Mingfang, LIU Hui, et al. Immobilization of photosynthetic bacteria for oily wastewater treatment[J]. Journal of Agro-Environment Science, 2009, 28(7): 1494-1499.
[12] 王娜, 闵小波, 王云燕, 等. 内聚营养源SRB固定化交联剂的选择及对含锌废水的处理[J]. 中南大学学报(自然科学版), 2008, 39(2): 273-278.
WANG Na, MIN Xiaobo, WANG Yunyan, et al. Determination of crocsslinking agent in immobilized beads of SRB sludge with inner cohesive carbon source and treatment of wastewater containing zinc[J]. Journal of Central South University (Science and Technology), 2008, 39(2): 273-278.
[13] 李桂银, 杨栋梁, 蒋玉仁, 等. 交联海藻酸钙固定化酵母醇脱氢酶研究[J]. 中南大学学报(自然科学版), 2009, 40(6): 1510-1516.
LI Guiyin, YANG Dongliang, JIANG Yuren, et al. Immobilization saccharomyces cerevisiae alcohol dehydrogenase on cross-linked calcium alginate beads[J]. Journal of Central South University (Science and Technology), 2009, 40(6): 1510-1516.
[14] 李二平, 闵小波, 舒余德, 等. 内聚营养源SRB污泥固定化处理含锌及硫酸根废水[J]. 中南大学学报(自然科学版), 2011, 42(6): 1522-1527.
LI Erping, MIN Xiaobo, SHU Yude, et al. Treatment of wastewater containing zinc and sulfate ion in immobilized beads of SRB sludge with inner cohesive carbon source[J]. Journal of Central South University (Science and Technology), 2011, 42(6): 1522-1527.
[15] 刘江红, 潘洋, 徐瑞丹. 微生物固定化降解含聚废水的最佳条件[J]. 湖南大学学报(自然科学版), 2012, 39(3): 62-65.
LIU Jianghong, PAN Yang, XU Ruidan. Optimization of degradation conditions of poly-containing wastewater by immobilized microorganism[J]. Journal of Hunan University (Natural Sciences), 2012, 39(3): 62-65.
[16] 董怡华, 胡筱敏, 尚进, 等. 一株微生物絮凝剂产生菌的培养基优化研究[J]. 安全与环境学报, 2009, 9(5): 55-59.
DONG Yihua, HU Xiaomin, SHANG Jin, et al. Study on the ultraviolet mutation of o-chlorophenol degrading photosynthetic[J]. Journal of Safety & Environment, 2009, 9(5): 55-59.
[17] 胡筱敏, 董怡华, 李亮, 等. 光合细菌PSB-1D对2-氯苯酚的降解特性研究[J]. 环境科学, 2010, 31(7): 677-680.
HU Xiaomin, DONG Yihua, LI Liang, et al. Study on biodegradation characterics of o-chlorophenol with photosynthetic bacteria PSB-1D[J]. Environmental Science, 2010, 31(7): 677-680.
[18] 昌宇奇, 赵红卫, 张迅, 等. 流化床固定化沼泽红假单胞菌处理废水的研究[J]. 四川化工, 2009, 12(3): 46-50.
CHANG Yuqi, ZHAO Hongwei, ZHANG Xun, et al. Research of fluidized bed of immobilized Rhodopseudomonas Palustris for wastewater disposal[J]. Sichuan Chemical Industry, 2009, 12(3): 46-50.
[19] 宋昊, 何泽超. 降酚菌株的固定化细胞处理含酚废水的性能研究[J]. 环境污染治理技术与设备, 2005, 6(9): 37-40.
SONG Hao, HE Zechao. Study on immobilized cells of degrading-phenol strain[J]. Techniques & Equipment for Environmental Pollution Control, 2005, 6(9): 37-40.
(编辑 邓履翔)
收稿日期:2013-04-06;修回日期:2013-06-15
基金项目:国家水体污染控制与治理重大专项(2012ZX07202-004);国家科技支撑计划课题(2012BAD14B04)
通信作者:胡筱敏(1958-),男,江西婺源人,教授,从事水污染治理研究;电话:024-83679128;E-mail:harvesttime@163.com