文章编号: 1004-0609(2006)09-1647-06
硫酸盐还原菌与单质铁协同作用处理
酸性含锌废水
常晓雷, 康勇, 冯颖
(天津大学 化工学院, 天津 300072)
摘要: 研究利用硫酸盐还原菌(sulfate reducing bacteria, SRB)与单质铁协同作用处理含Zn2+废水的效果和相应机理。 采用间歇式生物反应器, 在Zn2+名义浓度为0~90mg/L范围内, 分别考察SRB和SRB+Fe0两种体系的处理效果。 实验表明: SRB+Fe0体系的处理效果明显优于SRB体系; 加入单质铁之后, 高Zn2+浓度下(>75mg/L)SRB适应期缩短20%以上; Zn2+对SRB的抑制浓度提高约20%; 硫酸盐还原速率明显加快, 硫酸盐最终还原率以及Zn2+的去除速率都有所提高。 分析了单质铁对废水处理过程的强化机理, 确定Zn2+的去除形式主要为硫化物沉淀。
关键词: 单质铁; 酸性含锌废水; 硫酸盐还原菌 中图分类号: X751
文献标识码: A
Treatment of acid zinc wastewater by
sulfate reducing bacteria cooperated with iron
CHANG Xiao-lei, KANG Yong, FENG Ying
(School of Chemical Engineering and Technology, Tianjin University, Tianjin 300072, China)
Abstract: The treatment of wastewater containing Zn2+ by sulfate reducing bacteria cooperated with Fe0 was studied. Two systems of SRB and SRB+Fe0 were experimented in batch bioreactor, with Zn2+ concentration in the range of 0-90mg/L. The results show that the SRB+Fe0 system performs much better than SRB system. With the presence of iron, the acclimation period of SRB reduces more than 20% under high Zn2+ concentration; the inhibiting concentration of Zn2+ to SRB increases by approximately 20%; the reduction velocity of sulfate is fastened apparently, meanwhile the ultimate sulfate reduction rate and Zn2+ removal rate are improved to a certain extent. The enhancement principle of iron was analyzed and it is concluded that the removal of Zn2+ is mainly in terms of sulfide precipitate.
Key words: iron; acid zinc wastewater; sulfate reducing bacteria
有色金属采矿、 选矿、 冶炼和加工过程中产生大量的酸性重金属废水, 其中含有大量的Zn, Cd, Cr, Cu, Hg, Mo, Ni, Pb, Sb和As等。 这类废水排放到环境中对周围农田和水体造成极大的污染 [1, 2]。 随着我国对环保越来越重视, 这类废水的处理也更加迫切。 常用的石灰中和法容易产生大量的沉淀物, 不易回收有价金属[2, 3]。 利用硫酸盐还原菌(SRB)处理酸性矿山废水(AMD)是一种新型的废水生物处理技术[4, 5], 其主要作用机理是硫酸盐还原菌通过异化的硫酸盐还原作用, 将SO2-4还原成为S2-, 进而与废水中的重金属离子生成溶解度极低的金属硫化物沉淀而去除[6]。 在一些特殊情况下SRB还可通过菌体细胞对金属离子的直接吸附作用去除废水中的重金属[7]。
由于该方法适用性强, 无二次污染, 因此受到环境工作者的广泛关注, 成为酸性矿山废水处理技 术研究的前沿课题[8]。 但目前在实践应用中仍然存在一些难以解决的问题, 如酸性矿山废水的pH值一般小于6.0, 最低可到3.0左右, 在该pH范围内SRB的活性受到抑制[9], 并且水中重金属离子超过一定浓度就会对SRB产生毒性[10], 抑制其活性。 如何使SRB在这种条件下仍然保持较好的活性成为实施该方法的主要困难之一。 同时SRB去除重金属离子的机理相当复杂, 并不是所有重金属离子都是以硫化物沉淀的形式除去, 例如六价铬离子主要靠SRB的生物吸附和絮凝作用除去[11], 铁、 铜则主要是由硫化物沉淀除去, 铝主要是以氢氧化物沉淀除去[12]。 还有多种金属离子混合后出现络合共沉现象等。 本实验室在以前的工作中发现单质铁的厌氧腐蚀与SRB的硫酸盐代谢之间存在相互促进的关系, 可以提高SRB的活性, 加速硫酸盐的还原[13, 14]。 因此, 本实验采用SRB与单质铁协同作用处理酸性重金属废水, 针对比较普遍的Zn2+废水的情况作了研究, 考察其处理效果并探求其作用机理。
1 实验
1.1 实验菌种和材料
厌氧污泥取自华北制药集团环境研究所废水处理车间。 细菌的富集培养、 保存及活化方法见文献[13]。
实验用废水由实验室配制。 废水中硫酸根离子由硫酸钠提供, 有机物由乳酸钠提供, Zn2+离子由Zn(NO3)2提供, 废水的pH值通过盐酸或氢氧化钠溶液调节至5.5。 实验中所用的试剂, 包括培养基和配制废水用药品均为分析纯, 所用的单质铁为铁粉, 粒径为225μm, 纯度为90%。
各个反应器的废水中除Zn(NO3)2含量不同外其余物质含量相同, 各成分的含量见表1。
表1 实验用废水成分
Table 1 Composition of experimental wastewater
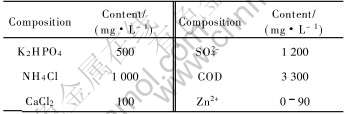
其中K2HPO4、 NH4Cl和CaCl2为细菌培养基, SRB接种量为3%(体积分数), 单质铁用量为每个反应器投加0.3g。 各个反应器中的Zn2+浓度不同, 分别为: 0, 10, 25, 50, 75和90mg/L。
1.2 实验装置
实验装置如图1所示。 反应器有效容积为1.5L, 瓶口密封以保证厌氧, 使用DHT型搅拌恒温电热套加热并通过磁力搅拌使反应器达到完全混合状态, 采用电接点玻璃水银温度计测量和控制反应器内温度为(36±1)℃, 反应产生的气体经上部导气管进入集气装置收集并计量体积。 实验开始前通过氮气管充氮气以赶出反应器中的空气。

图1 间歇实验装置流程图
Fig.1 Schematic diagram of batch bioreactor set-up
每批实验同时启动6个反应器, 实验分为两批, 一批用来考察SRB体系, 另一批考察SRB+Fe0体系。 实验考察因素包括pH值、 SO2-4浓度、 有机物浓度、 Zn2+离子浓度的变化情况。 具体操作步骤同文献[13]。
1.3 测试项目及方法
1) SO2-4、 COD和 pH值的测量参照文献[13]。
2) Zn2+离子的测量 利用意大利哈纳仪器公司生产的“多参数离子测定仪”测量以上各种离子的浓度(测量原理及方法参见产品说明书)。
3) EDS分析 利用英国OXFORD公司生产的INCA型能谱仪对沉淀物的成分进行能谱分析。
2 结果与讨论
2.1 Zn2+浓度对硫酸盐还原的影响
不同Zn2+浓度下SRB和SRB+Fe0两种体系中硫酸盐浓度随时间的变化如图2所示。 在反应初始阶段(0~48h)SO2-4浓度基本保持不变, 原因是细菌接种到新环境后存在适应期, 细菌活性很小, 几乎不发生SO2-4还原反应。 由图2(a)可见, 在SRB实验中, 随着Zn2+浓度的增大硫酸盐还原效果逐渐减弱, 表现为反应适应期延长, 硫酸盐还原速度减小以及硫酸盐最终还原率降低。 当Zn2+浓度小于25mg/L时, 对体系表现出的毒性作用很小, Zn2+浓度为75mg/L时, 体系受到较严重的抑制, 而当Zn2+浓度达到90mg/L时, 几乎没有硫酸盐还原反应发生。 图2(b)所示为SRB+Fe0体系的硫酸盐还原状况, 还原效果同样随着Zn2+浓度的增大而减弱。 但是与SRB实验相比, 在相同的Zn2+浓度下, SRB+Fe0体系中硫酸盐的还原速度及最终还原率都有所提高, 而且Zn2+浓度越大优势越明显。 当Zn2+浓度小于75mg/L时, 大部分硫酸盐都能被还原, 在Zn2+浓度为90mg/L的反应器中, 虽然反应受到一定程度的抑制, 但反应终止时硫酸盐浓度仍然降低了近50%。
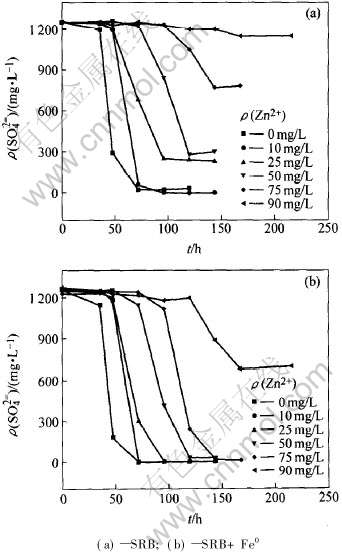
图2 不同Zn2+浓度下硫酸盐浓度随时间的变化
Fig.2 Variations of sulfate concentrations in different systems
2.2 不同体系中Zn2+的去除特点
图3所示为SRB和SRB+Fe0两种体系中Zn2+浓度随时间的变化情况。 加入金属盐后立即测试液中Zn2+的初始浓度, 发现其值比名义浓度降低40%左右。 以SRB+Fe0体系为例说明: 在名义浓度为10和25mg/L的反应器中, 测试的Zn2+初始浓度分别为6.1和14.5mg/L。 利用Visual MINTEQ 2.2离子平衡分析软件对初始反应液进行分析, 结果显示溶液中游离的Zn2+约为73%, 其余部分均与其他离子形成络合物, 此外, 由于接种的菌液中含有微生物代谢产生的S2-, 与Zn2+产生ZnS沉淀, 两者的共同作用导致反应液中Zn2+的初始浓度与名义浓度的差异。 48h后再次测量, 发现Zn2+浓度又一次明显降低, Zn2+浓度小于25mg/L的反应器中其浓度值降为0。 这一阶段为反应适应期, 没有硫酸盐还原反应发生,液中少量FeS与Zn2+发生沉淀转化反应等作用导致。 此后Zn2+浓度呈缓慢下降趋势, 直至硫酸盐还原反应发生时, Zn2+再次迅速下降, 此阶段Zn2+主要与SO2-4还原产生的S2-生成ZnS沉淀。 比较两个体系可以看出, SRB+Fe0体系中Zn2+浓度下降的速度快于SRB体系, 如在SRB体系中, 当Zn2+名义浓度为75mg/L时, 需要145h浓度下降到0, Zn2+名义浓度为90mg/L时, 需要172h浓度下降到0; 而在SRB+Fe0体系中两种浓度的Zn2+分别需要120和145h就可以降低到0, 去除时间分别缩短了17.2%和15.7%。 这也进一步证明了SRB+Fe0体系中硫酸盐还原速率高于SRB体系。

图3 不同体系中Zn2+浓度随时间的变化
Fig.3 Variations of Zn2+ concentrations in different systems
2.3 单质铁对废水处理效果的强化和机理
由图2、 3可以看出含有单质铁的生物反应器的处理效果明显优于不含单质铁的反应器, 说明单质铁的加入对废水处理有一定的强化效果, 具体表现为:
1) 缩短了SRB的适应期, 在高Zn2+浓度下从150h缩短至120h以内, 缩短幅度约为20%。
2) 提高了Zn2+抑制浓度, 从75mg/L提高到约90mg/L, 提高幅度约为20%。
3) 提高了硫酸盐还原速率和最终去除率。
4) 提高了Zn2+的去除速率。
下面着重从硫酸盐还原速率和Zn2+的去除速度两方面分析单质铁的强化效果和机理。
2.3.1 单质铁对硫酸盐还原过程的强化
不同体系中硫酸盐的还原速率如图4所示。 从图中可以看出, 未加入金属离子的反应器硫酸盐还
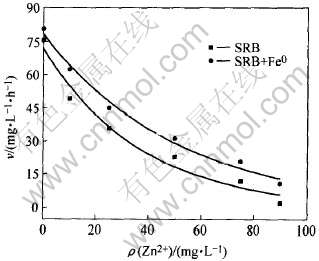
图4 硫酸盐还原速率与Zn2+浓度的关系
Fig.4 Sulfate reduction velocities at different Zn2+ concentrations
原速率最大, 随着Zn2+浓度的增加反应速率逐渐降低。 SRB实验中, 当Zn2+浓度分别为10, 25, 50, 75和90mg/L时, 其还原速率与空白实验相比分别降低了23%, 44%, 62%, 74%和87%。 Zn2+对反应速率的影响是由于金属离子对酶具有毒性抑制作用, 溶液中的Zn2+浓度越高, 上述抑制作用越严重, 导致细菌的代谢活性和反应速率越低。 在SRB+Fe0体系中, Zn2+浓度对反应速率的影响趋势基本与SRB体系相同, 但在相同Zn2+浓度下含单质铁体系的反应速率有所提高, Zn2+浓度从0到90mg/L, 速率分别提高了7%, 27%, 26%, 36%, 75%和415%。 这是由于单质铁是SRB体内很多种酶的重要组成成分, 可以在一定程度上促进酶的合成, 提高SRB的活性[13], 从而相对的降低Zn2+对酶的毒性抑制作用。
2.3.2 单质铁对Zn2+去除过程的强化
由图3和2.2的分析可知SRB+Fe0体系中Zn2+的去除速率高于SRB体系。 可见单质铁的加入加速了Zn2+的去除, 由于单质铁的热力学活性高于Zn0, 所以单质铁本身不会使Zn2+除去, 这一点也在单质铁体系的附加实验中得以确认。 单质铁的强化机理在于: 一方面单质铁在厌氧水环境中发生电化学腐蚀, 可以在一定程度上提高pH值, 促进Zn2+生成氢氧化物沉淀; 另一方面单质铁及其离子对SRB有激活作用[13], 可以减轻Zn2+对细菌的毒性抑止, 强化硫酸盐还原反应, 间接加速Zn2+的去除。
2.4 沉淀物分析
为了进一步确认Zn2+的去除形式, 实验结束后对沉淀物进行能谱分析, 得到其能谱图(见图5)[CM(22]和各元素含量(见表2)。 以SRB+Fe0体系中Zn2+ 浓度为75mg/L的反应沉淀物为例说明。 从图5和表2可以看出, 沉淀物中含有大量的Zn和S, 并且有少量的Fe, 也更加确定了Zn2+的去除形式是硫化物沉淀。 如果S元素的沉淀形式是ZnS和FeS, 从质量百分比来看, S还有10%左右的余量。 原因可能是含有其它硫化物如CaS等, 或者SO2-4在被还原过程中生成了部分硫单质, 也有文献报道存在这种可能性[15]。 称得沉淀物质量为225mg, 按照质量百分比计算, 沉淀物中Zn2+的质量为94.5mg, 与初始Zn2+质量112.5mg相比, 约有18mg的Zn2+损失, 约占总量的16%, 推测这部分为细菌吸附的金属离子量。
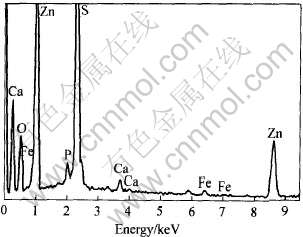
图5 沉淀物能谱图
Fig.5 EDS spectra of precipitates
表2 能谱分析沉淀物元素含量
Table 2 Elements contents of precipitate based on EDS analysis

3 结论
1) SRB体系中加入单质铁之后, 高Zn2+浓度下SRB适应期缩短20%以上; Zn2+对SRB的抑制浓度提高约20%; 硫酸盐还原速率明显加快, 硫酸盐最终还原率以及Zn2+的去除速率都有所提高。
2) 单质铁本身不会直接对硫酸盐还原与Zn2+去除产生作用, 而是通过促进SRB体内酶的合成, 提高细菌活性, 间接强化硫酸盐及Zn2+的去除。
3) Zn2+主要是以金属硫化物的形式去除, 还有约16%通过细菌吸附的方式除去。
REFERENCES
[1]於方一, 过孝民, 张强. 中国有色金属工业废水污染特征分析[J]. 有色金属, 2003, 55 (3): 134 -139.
YU Fang-yi, GUO Xiao-min, ZHANG Qiang. Wastewater pollution characteristics of Chinese nonferrous metals industry[J]. Nonferrous Metals, 2003, 55(3):134 -139.
[2]马晓航, 贾小明, 赵宇华. 用硫酸盐还原菌处理重金属废水的研究[J]. 微生物学杂志, 2003, 23(1): 36 -39.
MA Xiao-hang, JIA Xiao-ming, ZHAO Yu-hua. Research and application of the processes of disposal of wastewater containing heavy metals by sulfate reducing bacteria[J]. Journal of Microbiology, 2003, 23(1): 36 -39.
[3]杨晓松, 吴义千, 宋文涛. 有色金属矿山酸性废水处理技术及其比较优化[J]. 湖南有色金属, 2005, 21(5): 24 -27.
YANG Xiao-song, WU Yi-qian, SONG Wen-tao. The disposing techniques and the comparative optimization of acid wastewater of nonferrous metal mines[J]. Hunan Nonferrous Metals, 2005, 21(5): 24 -27.
[4]Tony J, David L P. Removal of sulfate and heavy metals by sulfate reducing bacteria in short-term bench scale upflow anaerobic packed bed reactor runs[J]. Water Research, 2003, 37: 3379 -3389.
[5]Costa M C, Duarte J C. Bioremediation of acid mine drainage using acidic soil and organic wastes for promoting sulfate-reducing bacteria activity on a column reactor[J]. Water, Air, and Soil Pollution, 2005, 165: 325 -345.
[6]Elliott P, Ragusa S, Catcheside D. Growth of sulfate-reducing bacteria under acidic conditions in an upflow anaerobic bioreactor as a treatment system for acid mine drainage[J]. Water Research, 1998, 32(12): 3724 -3730.
[7]Chen B Y, Utgikar V P, Harmon S M, et al. Studies on biosorption of zinc(Ⅱ) and copper(Ⅱ) on desulfovibrio desulfuricans[J]. International biodeterioration & biodegradation, 2000, 46: 11-18.
[8]李亚新, 苏冰琴. 硫酸盐还原菌和酸性矿山废水的生物处理[J]. 环境污染治理技术与设备, 2000, 1(5): 1 -11.
LI Ya-xin, SU Bing-qin. Sulfate-reducing bacteria and biological treatment of acid mine drainage[J]. Techniques and Equipment for Environmental Pollution Control, 2000, 1(5): 1 -11.
[9]冯颖, 康勇, 张忠国. 硫酸盐生物还原体系的主要影响因素研究[J]. 水处理技术, 2005, 31(3): 20 -24.
FENG Ying, KANG Yong, ZHANG Zhong-guo. Main influential factors of biological sulfate reduction system[J]. Technology of Water Treatment, 2005, 31(3): 20 -24.
[10]Hao O J, Li H G, Chen J M. Effects of metal additions on sulfate reduction activity in wastewaters[J]. Toxicological and Environmental Chemistry, 1994, 46: 197 -212.
[11]张介驰, 田小光, 于德水, 等. 硫酸盐还原菌净化含铬电镀废水的中试研究[J]. 生物技术, 1997, 7(1): 32-34.
ZHANG Jie-chi, TIAN Xiao-guang, YU De-shui, et al. The pilot plant on purification of electroplating waste water of Cr6+ with D.v.d[J]. Biotechnology, 1997, 7(1): 32 -34.
[12]Christensen B, Laake M, Lien T. Treatment of acid mine water by sulfate-reducing bacteria: results from a bench scale experiment[J]. Wat Res, 1996, 30(7): 1617-1624.
[13]冯颖, 康勇, 孔琦, 等. 硫酸盐生物还原的温度效应及Fe0的强化作用[J]. 水处理技术, 2005, 31(7): 27-31.
FENG Ying, KANG Yong, KONG Qi, et al. Effect of temperature on sulfate biological reduction and enhancement of iron[J]. Technology of Water Treatment, 2005, 31(7): 27-31.
[14]冯颖, 康勇, 范福洲, 等. 单质铁强化生物还原法处理硫酸盐废水[J]. 中国给水排水, 2005, 21(7): 32-35.
FENG Ying, KANG Yong, FAN Fu-zhou, et al. Iron enhanced biological reduction process for treatment of sulfate-containing wastewater[J]. China Water & Wastewater, 2005, 21(7): 32-35.
[15]Postgate J R. The Sulphate Reducing Bacteria[M]. London: Cambridge University Press, 1984. 21-23.
基金项目: 国家自然科学基金资助项目(C20106014)
收稿日期: 2006-01-15; 修订日期: 2006-07-15
通讯作者: 康勇, 教授; 电话: 022-27408813; E-mail: ykang@tju.edu.cn
(编辑 龙怀中)