文章编号:1004-0609(2014)02-0468-08
前驱体掺杂-常温球磨还原法制备锂离子电池正极材料LiFe1-3y/2AlyPO4
吕 凡,伍 凌,管 淼,钟胜奎,刘洁群
(苏州大学 沙钢钢铁学院,苏州 215021)
摘 要:采用共沉淀法制备掺Al3+前驱体FePO4・2H2O,并以乙二酸为还原剂,与Li2CO3反应在常温下球磨合成LiFePO4前驱混合物,后经热处理得到橄榄石型LiFe1-3y/2AlyPO4。用XRD、SEM、HRTEM和恒流充放电等对样品进行表征。结果表明:适量Al3+掺杂不会破坏 LiFePO4的晶体结构,当掺杂量较低时(y=0.01),Al3+优先占据Fe位;当掺杂量较高时(y≥0.02),Al3+同时占据Li位和Fe位。电化学测试表明:LiFe0.985Al0.01PO4拥有最优的电化学性能,该样品在0.1C、1C和2C倍率下的首次放电比容量分别为162.4、152.2和142.0 mA・h/g,在1C倍率下循环100次后的放电比容量高达149.7 mA・h/g。
关键词:正极材料;磷酸铁锂;Al3+掺杂;球磨;常温还原
中图分类号:TM912.9 文献标志码:A
Preparation of LiFe1-3y/2AlyPO4 cathode material by precursor-doping combined room temperature reduction via ball-milling
 Fan, WU Ling, GUAN Miao, ZHONG Sheng-kui, LIU Jie-qun
Fan, WU Ling, GUAN Miao, ZHONG Sheng-kui, LIU Jie-qun
(School of Iron and Steel, Soochow University, Suzhou 215021, China)
Abstract: Al3+-doped precursors (FePO4・2H2O) were prepared via a co-precipitation method. LiFePO4 precursor- mixtures were obtained by ball milling at room temperature using FePO4・2H2O, Li2CO3 and oxalic acid as raw materials, and then olivine-type LiFe1-3y/2AlyPO4 were synthesized by the following heat treatment. The samples were characterized by using X-ray diffraction, scanning electron microscope, high resolution transmission electron microscope and galvanostatic charge/discharge test. The results show that a proper amount of Al doping does not obviously change the structure of LiFePO4. When y=0.01, Al3+ ions tend to occupy Fe site, and when y≥0.02, Al3+ ions occupy both Fe and Li sites. LiFe0.985Al0.01PO4 exhibits the most impressive electrochemical performance as follows: its initial discharge capacities are 162.4, 152.2 and 142.0 mA・h/g at 0.1C, 1C and 2C rates, respectively, its discharge capacity is 149.7 mA・h/g even after 100 cycles at 1C rate.
Key words: cathode material; lithium iron phosphate; Al3+ doping; ball milling; room temperature reduction
橄榄石型LiFePO4因具有理论比容量高、安全性能好和循环性能优良等多种优点,成为一种非常有前景的锂离子电池正极材料[1-3]。然而,LiFePO4的电子导电率(10-9~10-10 S/cm)[2]和锂离子扩散速率(1.8× 10-14 cm2/s)[3]较低,使得其高倍率下的电化学性能较差。通过在LiFePO4颗粒表面包覆导电剂(碳或金属粉末)[4-7]和掺杂高导电率金属离子[8-12]的方法,可以大幅度提高LiFePO4的导电率,从而提高材料高倍率放电性能;优化合成工艺,制备精细(如纳米级、亚微米级)LiFePO4粉末[13-16],可以缩短Li+的扩散路径。
研究者们多是以FeC2O4为原料,采用固相法[1-4]制备掺杂型LiFePO4,但是,在掺杂量较低的情况下,机械法难以将锂源、铁源、磷源和掺杂源4种原料混合均匀;而采用溶胶-凝胶法[17-18]虽然能将各原料混合均匀,但成本较高,工业应用价值不大。本文作者采用共沉淀法先将Al3+均匀地沉积在FePO4・2H2O颗粒中,然后将其与锂源混合煅烧制备LiFePO4,相对于4种原料,两种原料更易混合均匀,获得成分均一、电化学性能优异的LiFePO4。最后详细探讨Al3+掺杂对LiFePO4的结构以及电化学性能的影响。
1 实验
1.1 材料的制备
称取一定量FeSO4・7H2O、H3PO4和Al2(SO4)3・18H2O,溶于去离子水中,在强烈搅拌下加入足量的H2O2,使得全部Fe(Ⅱ)氧化成Fe(Ⅲ),用NH3・H2O调节pH值至2.0左右,反应30 min,将得到的乳白色沉淀洗涤-过滤3次,然后于100 ℃干燥12 h即得不同掺Al量的FePO4・2H2O。
按摩尔比n(Li):n(Fe):n(C)=(1+y/2):1:1.8 (其中y为0、0.01、0.02、0.03和0.05) 称取一定量的Li2CO3、前驱体和乙二酸;以乙醇为介质,在常温下球磨4h后得到浅绿色无定形前驱混合物;将混合物于80 ℃烘干后置入程序控温管式炉,在氩气气氛下于600 ℃煅烧12 h,随炉冷却即得橄榄石型Al3+掺杂LiFePO4。
1.2 材料的分析与表征
本研究采用日本Rigaku公司生产的X射线衍射仪对材料的物相进行表征,用Fullprof对XRD数据进行精修。用JEOL公司的JSM6380扫描电镜观察样品的形貌,用HRTEM-EDS分析样品的微区结构及成分。采用电感耦合等离子体发射光谱ICP-AES(Thermo electron corporation)测定前驱体的Al含量;采用重铬酸钾滴定法测定前驱体中的Fe含量。
1.3 电池的组装与测试
将LiFePO4、乙炔黑和粘接剂PVdF按质量比8:1:1混合,以铝箔为基体制备成直径14 mm的圆片作为正极片。将正极片与负极片(直径15 mm的Li片)、隔膜(Celgard2400微孔聚丙烯膜)和电解液(1 mol/L LiPF6/(EC+EMC+DMC),V(EC):V(EMC):V (DMC)= 1:1:1)组装成CR2025型扣式电池。电池静置12 h后,用Newware电池测试系统进行测试。测试在室温下进行,电压范围2.5~4.1 V。
2 结果与讨论
2.1 前驱体
表1所列为不同掺Al3+量前驱体中Fe和Al的含量。结果表明,各样品的Fe含量(质量分数)与FePO4・2H2O的理论Fe含量(29.89%)非常接近,随着掺Al3+量的升高,Fe含量稍有降低。从Al/Fe摩尔比数据可知,各样品的实际掺Al3+量与期望掺Al3+基本接近。
表1 掺Al前驱体中Fe和Al的含量
Table 1 Fe and Al content of precursors
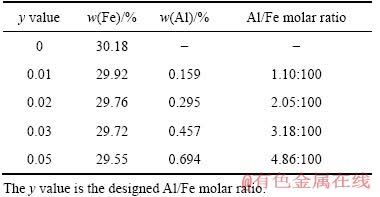

图1 LiFe1-3y/2AlyPO4的SEM像
Fig. 1 SEM images of LiFe1-3y/2AlyPO4
2.2 LiFe1-3y/2AlyPO4
2.2.1 形貌分析
图1所示为LiFe1-3y/2AlyPO4样品的SEM像。由图1可知,各样品都同时存在细小的一次颗粒和由一次颗粒团聚而成的二次颗粒;当掺Al3+量较低时(y≤0.02),掺杂样品的一次颗粒粒径与未掺杂样品相当(约100~500 nm),但是未掺杂样品的颗粒团聚较为严重,掺杂样品较分散;而当掺Al3+量较高时(y≥0.03),样品的一次颗粒粒径增大(200~1000 nm),而且团聚也变得严重。由此可见,少量Al3+掺杂能有效抑制LiFePO4一次颗粒的团聚,但进一步提高掺Al3+量反而促使其团聚,而且也使一次颗粒增大,因此掺Al3+量不宜过高。
2.2.2 结构及掺杂机理
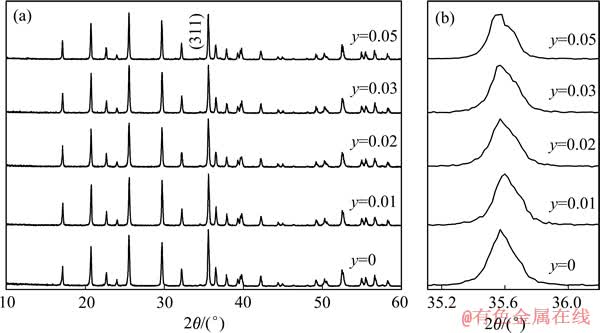
图2 LiFe1-3y/2AlyPO4的XRD谱(a)及(311)面衍射峰的局部放大图(b)
Fig. 2 XRD patterns of LiFe1-3y/2AlyPO4 (a) and partial enlarged figure of (311) peaks (b)
图2(a)和(b)所示分别为LiFe1-3y/2AlyPO4(0≤y≤ 0.05)的XRD谱和最强峰(311)面衍射峰的局部放大图。由图2(a)可知,各样品均为单一的橄榄石结构,无杂质峰;衍射峰的强度随着掺Al3+量的升高稍有变低,说明Al3+已掺入到晶格中,适量的Al3+掺杂不会破坏LiFePO4的晶体结构。从图2(b)可知,随着掺Al3+量的增高,最强峰先向高角度偏移,到y>0.01之后再向低角度偏移。由Scherrer公式(式(1))计算得到的微晶尺寸(D311)列于表2,数据表明,LiFe1-3y/2AlyPO4的微晶尺寸在y=0.01时达到最低,当y>0.01时,随着掺Al3+量的升高而稍有增大。
D=Kλ/(βcosθ) (1)
式中:λ为入射X射线的波长;θ为布拉格衍射角;D为微晶直径;K为Scherrer常数(K=0.89);β为衍射峰的半峰宽。
此外,各图谱中均未发现碳的衍射峰,而碳-硫分析表明各样品中均含有碳,(从y=0到y=0.05,碳含量分别为2.84%、2.68%、2.90%,2.86%和2.77%),这说明样品中残余的碳为无定形结构。
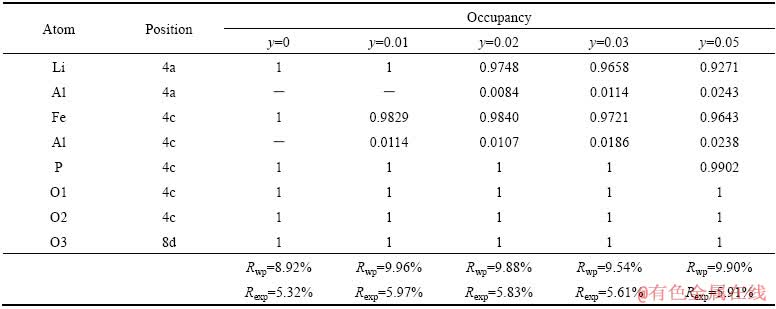
为了进一步研究其结构,用Rietveld方法对XRD进行了精修。在精修过程中,用赝-沃伊格特函数模拟衍射峰,精修了如原子位置、占位率、晶格常数、半峰宽、各向同性温度因子等在内的30多个参数。精修时,分别按照表3中的晶体组成模型和缺陷补偿机制对原子位置和占位进行了假设,当掺Al3+量y=0.01时,按照机制4得到了最佳精修结果,当y≥0.02时,综合机制1和4得到了最佳精修结果,所得晶胞常数和占位率分别列于表2和表4。由表4可知,Rwp和Rexp均小于10%,表明精修结果是合理的。
表2 LiFe1-3y/2AlyPO4的晶胞常数与晶粒尺寸
Table 2 Lattice parameters and crystallite size of LiFe1-3y/2AlyPO4

由表2可知,随着掺Al3+量的升高,晶胞常数a增大,而b、c和晶胞体积V均是先减小后增大,且均在y=0.01时达到最小值。由占位率(见表4)可知,当掺Al3+量y=0.01时,Al3+占据Fe位,并由Fe位产生空穴进行电荷补偿(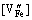 =
=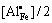 );但是当掺Al3+量y≥0.02时,Al3+同时占据Li位和Fe位,并且在Li位和Fe位都有空穴产生(
);但是当掺Al3+量y≥0.02时,Al3+同时占据Li位和Fe位,并且在Li位和Fe位都有空穴产生(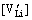 =
=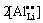 ,
,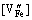 =
=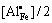 )。因此,当y≥0.02时,Al3+掺杂LiFePO4的实际组成与初始设计的LiFe1-3y/2AlyPO4不同,应记为Li1-3aAlaFe1-3(y+a)/2Aly-aPO4 ,但为了便于表达,下文仍以LiFe1-3y/2AlyPO4表示。
)。因此,当y≥0.02时,Al3+掺杂LiFePO4的实际组成与初始设计的LiFe1-3y/2AlyPO4不同,应记为Li1-3aAlaFe1-3(y+a)/2Aly-aPO4 ,但为了便于表达,下文仍以LiFe1-3y/2AlyPO4表示。
表3 LiFePO4掺杂的理想晶体组成和缺陷补偿机制[8]
Table 3 Ideal composition and defect compensation mechanism of doping for LiFePO4 (where Mn+ represents metal ions)[8]
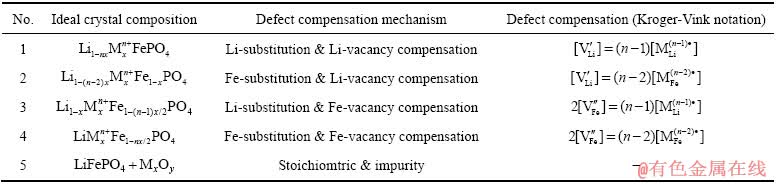
表4 LiFe1-3y/2AlyPO4样品XRD数据的Rietveld精修结果
Table 4 Rietveld-refinement results of XRD data of LiFe1-3y/2AlyPO4 (Occupancy)
根据CHIANG等[2]提出的两相模型,LiFePO4和FePO4两相界面具有极低的电导率,但是,当Al3+掺杂在Fe位产生铁位缺陷时,根据电荷守衡定律,其嵌锂态和脱锂态的表达式如式(2)和(3):
嵌锂态: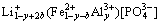 (2)
(2)
脱锂态: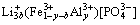 (3)
(3)
式中:y为掺Al3+量,(y+b)为Fe缺陷量。由式(3)可知,当存在Fe空位(即b>0)时LiFePO4中的Li不能完全脱去,阻碍了单相FePO4的形成,从而有利于其电导率的提高,本研究中掺Al3+量y=0.01时即属于这种情况。
但是,当y≥0.02时,Al3+同时占据Li位和Fe位时,并在Li位和Fe位产生空穴,在这种情况下,Al3+掺杂除了会阻碍单相FePO4生成之外,还会导致Fe3+/Fe2+混合电对的产生,二者都能极大地提高LiFePO4的电导率,其嵌锂态和脱锂态的表达式如式(4)和(5):
嵌锂态:
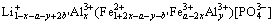 (4)
(4)
脱锂态:
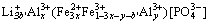 (5)
(5)
式中:x为在Li位的掺Al3+量,y为在Fe位的掺Al3+量, 为Li缺陷量,
为Li缺陷量,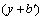 为Fe缺陷量。
为Fe缺陷量。
2.2.3 LiFe0.97Al0.02PO4晶粒的微区研究
图3所示为LiFe0.97Al0.02PO4样品的TEM、HRTEM像和EDS谱。
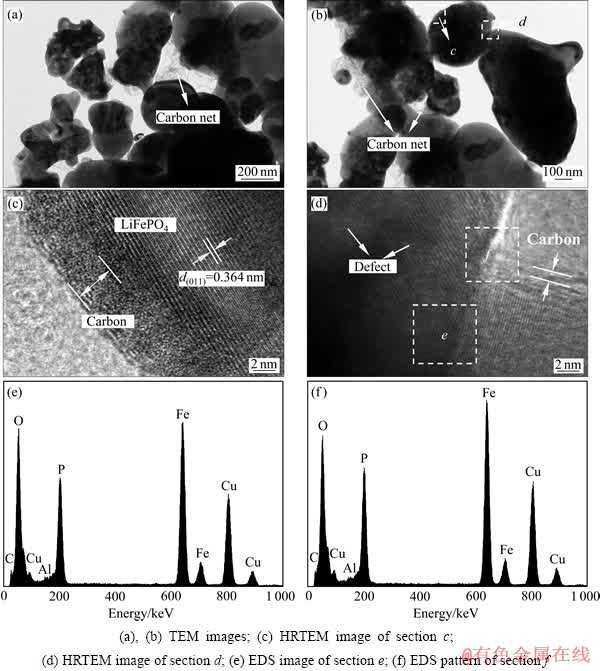
图3 LiFe0.97Al0.02PO4的TEM、HRTEM像和EDS谱
Fig. 3 TEM, HRTEM images and EDS patterns of LiFe0.97Al0.02PO4
由图3(a)和(b)可知,样品晶粒的大小约为0.1~1 μm,晶粒之间有纳米碳网相连。由图3(c)和(d)可知,LiFe0.97Al0.02PO4晶粒的晶格清晰,表明结晶良好,但是晶格中也存在一些缺陷,这些缺陷可能是由于Al3+掺杂引起的;另外,LiFePO4晶粒表面均匀地包覆着一层无定形碳膜(约2~4 nm厚),形成了一种“核-壳”结构。这种无定形碳“壳”不仅能够阻止LiFePO4晶粒“核”进一步长大,而且能大大提高颗粒之间的导电性;而晶格缺陷则能提高材料的本征电导率,还能为锂离子的迁移提供更多的通道。上述因素均能改善LiFePO4的电化学性能。图3(e)和(f)分别为e区和f区的EDS谱,能谱检测到LiFe0.97Al0.02PO4晶粒中和晶界上均有少量Al存在,说明Al3+已成功地掺入到LiFePO4晶格中,且分布非常均匀。此外,其他LiFe1-3y/2AlyPO4样品的微区分析结果也基本相似。
2.2.4 LiFe1-3y/2AlyPO4的电化学性能
图4所示为LiFe1-3y/2AlyPO4样品在不同倍率下的首次充放电曲线。从图4可知,y为0、0.01、0.02、0.03和0.05的样品在0.1C倍率下的首次放电比容量分别为165.0、162.4、157.7、153.0和145.8 mA・h/g。y=0.01的样品与未掺杂样品在低倍率下的容量当相,而当y≥0.01时,随着掺Al3+量的升高,LiFe1-3y/2AlyPO4在低倍率下的放电比容量降低,这是由于掺Al3+量升高使得Li位产生空穴,从而导致可供脱/嵌的Li+减少引起的。但是,在大倍率充放电时,掺杂样品的放电容量明显高于未掺杂样品,y为0、0.01、0.02、0.03和0.05的样品在1C倍率下的首次放电比容量分别为126.4、152.2、147.8、138.4和130.1 mA・h/g;在2C倍率下的首次放电比容量分别为96.2、142.0、140.4、132.1和112.6 mA・h/g;其中LiFe0.985Al0.01PO4在1C和2C下的首次放电比容量最高。此外,所有样品在低倍率下的电压极化相差不大,但在高倍率下,掺杂样品的电压极化明显小于未掺杂样品。
根据前面的分析,Al3+掺杂能显著改善LiFePO4在大倍率下的充放电性能是因为:1) Al3+掺杂在Li位能导致Fe3+/Fe2+混合电对的形成,掺杂在Fe位则能抑制单相FePO4的形成,二者都有利于LiFePO4导电性的提高;2) 适量Al3+掺杂(0.01≤y≤0.02)能有效抑制LiFePO4颗粒的团聚,使材料细化,从而有利于其容量的发挥;3) Al3+掺杂能大幅度提高LiFePO4电极表面以及电极材料中的电荷传递速率,能大大提高LiFePO4电极体系的交换电流密度和Li+扩散系数。
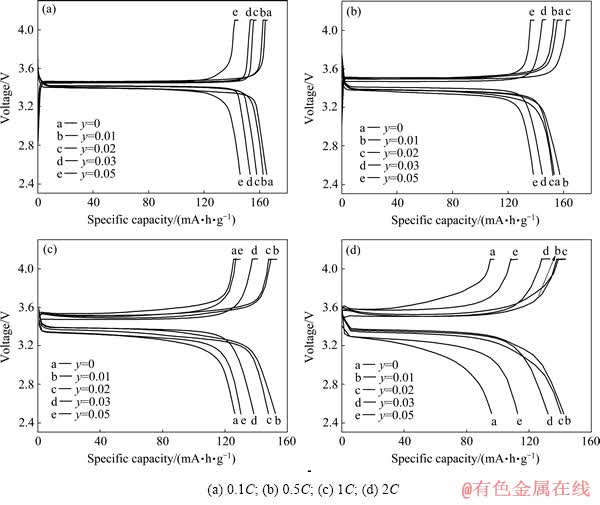
图4 LiFe1-3y/2AlyPO4在不同倍率下的首次充放电曲线
Fig. 4 Initial charge and discharge curves of LiFe1-3y/2AlyPO4 at various C-rates
图5所示为LiFe1-3y/2AlyPO4样品在1C和2C倍率下的循环性能。由图5可知,各样品的放电容量随室温的变化而波动。y为0、0.01、0.02、0.03和0.05的样品在1C倍率下循环100 次后的放电比容量分为105.7、149.7、149.5、132.6和123.5 mA・h/g,相对于首次容量的保持率分别为83.6%、98.4%、101.1%、95.8%和94.9%;在2C倍率下循环100次后的放电比容量分别为76.4、139.6、135.7、126.5和105.0 mA・h/g,相对于首次容量的保持率分别为79.4%、98.3%、96.7%、95.8%和93.3%。可见Al3+掺杂显著地改善了LiFePO4在大电流放电时的循环性能,且当掺Al3+量y=0.01和y=0.02时的循环性能最好。
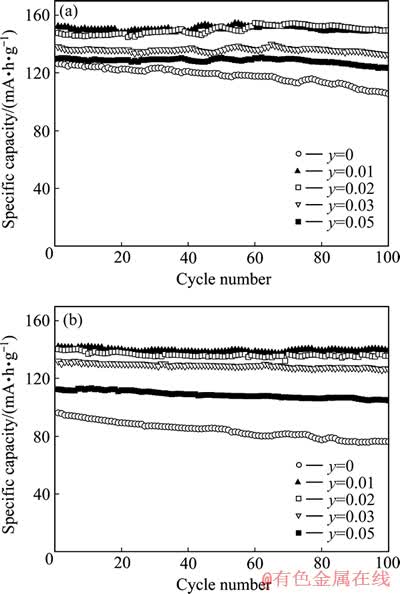
图5 LiFe1-3y/2AlyPO4在1C和2C倍率下的循环性能
Fig. 5 Cycling performances of LiFe1-3y/2AlyPO4 at C-rates of 1C(a) and 2C (b)
综上所述,适量Al3+掺杂极大地改善了LiFePO4在大倍率下的电化学性能,在1C和2C倍率下,y=0.01的样品拥有最高的放电容量,而y=0.01和y=0.02的样品的具有最优异的循环性能,综合来讲,掺Al3+量为y=0.01的LiFePO4综合性能最优。
3 结论
1) 用共沉淀法制备了掺Al3+的FePO4・2H2O。
2) 适量Al3+掺杂不会破坏 LiFePO4的晶体结构,当掺杂量较低时,Al3+优先占据Fe位;当掺Al3+量较高时,Al3+同时占据Li位和Fe位。
3) 随着掺Al3+量的升高,LiFe1-3y/2AlyPO4 (0≤y≤ 0.05)的晶胞常数a逐渐减小,而晶胞常数b、c、晶胞体积V以及微晶尺寸D311先减小后增大。
4) 当y=0.01时,LiFe1-3y/2AlyPO4具有最优的电化学性能。
REFERENCES
[1] PADHI A K, NANJUNDASWAMY K S, GOODENOUGH J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. J Electrochem Soc, 1997, 144: 1188-1194.
[2] CHUNG S Y, BLOKING J T, CHIANG Y M. Electronically conductive phospho-olivines as lithium storage electrodes[J]. Nat Mater, 2002, 1: 123-128.
[3] PROSINI P P, LISI M, ZANE D, PASQUALI M. Determination of the chemical diffusion coefficient of lithium in LiFePO4[J]. Solid State Ionics, 2002, 148: 45-51.
[4] 张 明, 尹周澜, 郭学益, 张 宝. 液氮淬火法制备高性能锂离子电池正极材料LiFePO4/C[J]. 中国有色金属学报, 2012, 22(8): 2283-2288.
ZHANG Ming, YIN Zhou-lan, GUO Xue-yi, ZHANG Bao. Synthesis of high-performance LiFePO4/C by liquid nitrogen quenching method[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(8): 2283-2288.
[5] CROCE F, EPIFANIO A D, HASSOUN J, DEPTULA A, OLCZAC T, SCROSATI B. A Novel concept for the synthesis of an improved LiFePO4 lithium battery cathode[J]. Electrochem Solid-State Lett A, 2002, 5(3): 47-50.
[6] KONAROVA M, TANIGUCHI I. Synthesis of carbon-coated LiFePO4 nanoparticles with high rate performance in lithium secondary batteries[J]. J Power Sources, 2010, 195: 3661-3667.
[7] LIU Y, LI X, GUO H, WANG Z, PENG W, YANG Y, LIANG R. Effect of carbon nanotube on the electrochemical performance of C-LiFePO4/graphite battery[J]. J Power Sources, 2008, 184: 522-526.
[8] MEETHONG N, KAO Y H, SPEAKMAN S A, CHIANG Y M. Aliovalent substitutions in olivine lithium iron phosphate and impact on structure and properties[J]. Adv Funct Mater, 2009, 19(7): 1060-1070.
[9] 张冬云, 张培新, 宋申华, 惠文彬, 黄 磊, 任祥忠. 镍镁掺杂LiFePO4的电子结构[J]. 中国有色金属学报, 2012, 22(8): 2317-2325.
ZHANG Dong-yun, ZHANG Pei-xin, SONG Shen-hua, HUI Wen-bin, HUANG Lei, REN Xiang-zhong. Electronic structure of LiFePO4 doped with Ni and Mg[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(8): 2317-2325.
[10] LI L J, LI X H, WANG Z X, GUO H J, WU L, HAO Y, ZHENG J C. Inexpensive synthesis of metal-doped LiFePO4 from laterite lixivium and its electrochemical characterization[J]. J Alloys Compd, 2010, 497: 176-181.
[11] 李新海, 伍 凌, 王志兴, 郭华军, 彭文杰, 吴飞翔. 综合利用钛铁矿制备二氧化钛、钛酸锂和磷酸铁锂[J]. 中国有色金属学报, 2011, 21(10): 2697-2708.
LI Xin-hai, WU Ling, WANG Zhi-xing, GUO hua-jun, PENG Wen-jie, WU Fei-xiang. Preparation of titanium dioxide, lithium titanium oxide and lithium iron phosphate from ilmenite[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(10): 2697-2708.
[12] SUN C S, ZHOU Z, XU Z G, WANG D G, WEI J P, BIAN X K, YAN J. Improved high-rate charge/discharge performances of LiFePO4/C via V-doping[J]. J Power Sources, 2009, 193: 841-845.
[13] WANG L, HUANG Y, JIANG R, JIA D. Preparation and characterization of nano-sized LiFePO4 by low heating solid-state coordination method and microwave heating[J]. Electrochim Acta, 2007, 52: 6778-6783.
[14] JU S, PENG H, LI G, CHEN K. Synthesis and electrochemical properties of LiFePO4 single-crystalline nanoplates dominated with bc-planes[J]. Mater Lett, 2012, 74: 22-25.
[15] GAO F, TANG Z, XUE J. Preparation and characterization of nano-particle LiFePO4 and LiFePO4/C by spray-drying and post-annealing method[J]. Electrochim Acta, 2007, 53: 1939-1944.
[16] WU X L, JIANG L Y, CAO F F, GUO Y G, WAN L J. LiFePO4 nanoparticles embedded in a nanoporous carbon matrix: Superior cathode material for electrochemical energy-storage devices[J]. Adv Mater, 2009, 21: 2710-2714.
[17] WANG G X, BEWLAY S, NEEDHAM S A, LIU H K, LIU R S, DROZD V A, LEE J F, CHEN J M. Synthesis and characterization of LiFePO4 and LiTi0.01Fe0.99PO4 cathode materials[J]. J Electrochem Soc A, 2006, 153(1): 25-31.
[18] PENG W, JIAO L, GAO H, QI Z, WANG Q, DU H, SI Y, WANG Y, YUAN H. A novel sol-gel method based on FePO4・2H2O to synthesize submicrometer structured LiFePO4/C cathode material[J]. J Power Sources, 2011, 196: 2841-2847.
(编辑 何学锋)
基金项目:国家自然科学基金资助项目(51204114);江苏省自然科学基金资助项目(BK2012216);中国博士后科学基金资助项目(2013M540464)
收稿日期:2013-06-05;修订日期:2013-10-14
通信作者:伍 凌,讲师,博士;电话:0512-67164815;E-mail: lwu_suda@163.com