内氧化Cu/Al2O3界面热力学与杂质效应
来源期刊:中国有色金属学报2013年第11期
论文作者:江 勇 蓝国强 王怡人 周松松
文章页码:3154 - 3165
关键词:Cu/Al2O3界面;内氧化;结合强度;杂质偏聚;第一性原理
Key words:Cu/Al2O3 interface; internal oxidation; adhesion strength; impurity segregation; first principles
摘 要:基于第一性原理方法,研究温度、原子化学配比、Al 活度、O活度和杂质偏聚对内氧化Cu/Al2O3界面的影响作用。计算得到的界面相图及相应能量学结果表明:界面平衡相结构随制备气氛的变化而变化;富O相界面的结合强度最高,富Al相界面的结合强度其次,它们均约3倍于理想化学配比相界面的结合强度;杂质S对界面的危害性明显,对富Al相和理想配比相界面具有强烈的偏聚能力,且严重削弱界面强度(约可达65%),并降低氧化铝颗粒尺寸的稳定性,但S不能向富O 相界面偏聚;相较于S,另一种杂质P向富Al相和理想配比相界面的偏聚能力不强,偏聚后对界面的危害性也较S弱。但P能向富O相界面偏聚,使界面强度严重降低。
Abstract: Based on the first-principles study, the effects of temperature, interfacial stoichiometry, Al activity, O activity and impurity segregation on the internally oxidized Cu/Al2O3 interface were studied. The calculated interfacial phase diagrams and corresponding energetics suggest that, the equilibrium interface structure varies with the ambient; the O-rich type interface, followed by the Al-rich type, has significantly stronger adhesion than its stoichiometric counterpart. Impurity S strongly segregates to Al-rich and stoichiometric type interfaces, degrades the adhesion (up to about 65%) and also reduces the size stability of alumina particles in Cu, while the O-rich interface is immunized from S segregation. P, as another common impurity in Cu, has a limited capability to segregate to the Al-rich and the stoichiometric interfaces, but it can segregate to the O-rich interface and reduce the adhesion seriously.
文章编号:1004-0609(2013)11-3154-11
江 勇1, 2,蓝国强1,王怡人1,周松松1
(1. 中南大学 材料科学与工程学院,长沙 410083;
2. 中南大学 有色金属材料教育部重点实验室,长沙 410083)
摘 要:基于第一性原理方法,研究温度、原子化学配比、Al 活度、O活度和杂质偏聚对内氧化Cu/Al2O3界面的影响作用。计算得到的界面相图及相应能量学结果表明:界面平衡相结构随制备气氛的变化而变化;富O相界面的结合强度最高,富Al相界面的结合强度其次,它们均约3倍于理想化学配比相界面的结合强度;杂质S对界面的危害性明显,对富Al相和理想配比相界面具有强烈的偏聚能力,且严重削弱界面强度(约可达65%),并降低氧化铝颗粒尺寸的稳定性,但S不能向富O 相界面偏聚;相较于S,另一种杂质P向富Al相和理想配比相界面的偏聚能力不强,偏聚后对界面的危害性也较S弱。但P能向富O相界面偏聚,使界面强度严重降低。
关键词:Cu/Al2O3界面;内氧化;结合强度;杂质偏聚;第一性原理
中图分类号:TG146.1 文献标志码:A
JIANG Yong1, 2, LAN Guo-qiang1, WANG Yi-ren1, ZHOU Song-song1
(1. School of Materials Science and Engineering, Central South University, Changsha 410083, China;
2. Key Laboratory of Nonferrous Metal Materials, Ministry of Education, Central South University, Changsha 410083, China)
Abstract: Based on the first-principles study, the effects of temperature, interfacial stoichiometry, Al activity, O activity and impurity segregation on the internally oxidized Cu/Al2O3 interface were studied. The calculated interfacial phase diagrams and corresponding energetics suggest that, the equilibrium interface structure varies with the ambient; the O-rich type interface, followed by the Al-rich type, has significantly stronger adhesion than its stoichiometric counterpart. Impurity S strongly segregates to Al-rich and stoichiometric type interfaces, degrades the adhesion (up to about 65%) and also reduces the size stability of alumina particles in Cu, while the O-rich interface is immunized from S segregation. P, as another common impurity in Cu, has a limited capability to segregate to the Al-rich and the stoichiometric interfaces, but it can segregate to the O-rich interface and reduce the adhesion seriously.
Key words: Cu/Al2O3 interface; internal oxidation; adhesion strength; impurity segregation; first principles
从宏观尺度的结构复合材料到功能薄膜和涂层材料,再到纳米尺度的电子器件,许多材料系统的结构完整性和整体性能都取决于界面的结合质量。S和P作为常见的两种主要工业杂质,具有偏析到各种材料界面(包括晶界和相界等)的强烈趋势,并降低界面的结合强度。例如,有研究发现,S在纯Fe和纯Ni的晶界处偏聚,可严重减弱晶粒间的结合和变形协调性,导致材料易发生脆化[1-3];在镍基和铁基高温合金中,S能够在其热生成氧化物层界面上发生偏聚,减弱界面结合力,引发热障保护层的完全剥落[4-6]。这些现象在材料学界被专门称为“界面硫效应”[7-8]。界面杂质效应直接影响到材料服役过程中的可靠性和使用寿命,因而,成为薄膜与涂层界面领域长期以来的研究热点。为减轻或消除有害的界面杂质效应,一些专门的制备新技术在近20多年来得到发展和成功应用[7-10],其中包括引入多级超纯净脱硫精炼工序,这可大幅度降低S含量到几十个甚至十几个10-6数量级;通过合金化加入一些活性元素(Hf、Y、Zr、Ce),有可能将S钉扎于基体中,从而抑制S的界面偏析能力。
实验证实,杂质S对Cu的自由表面也有很强的偏聚能力。即便在相对低的温度(T≈800 K),S在Cu表面可成1 000~10 000倍地富集[11],偏聚能力与S在Fe、Ni表面相当[12]。据此推断,虽然还没有直接的实验报道,S极有可能具备强烈偏聚到Cu/氧化物界面的潜在能力。
Cu/氧化物界面广泛存在于氧化物弥散强化铜 (ODSC)中。氧化物弥散强化铜(Oxide dispersion- strengthened copper,ODSC)具有许多特殊的优点[13-16],包括抗高温软化性能、兼具优异的高温强度、高温导电性和抗蠕变性能以及应用于电阻点焊电极材料的抗粘接性能。Al2O3因其高强、高韧、在铜基体中的热稳定性高以及低成本等优点,成为这类材料中最常用的氧化物强化相。由此形成的氧化铝弥散强化铜(Alumina dispersion-strengthened copper,ADSC)广泛应用于电子元器件用塑封三极管、高速电气化铁路架空线、高速列车牵引电机、工业点焊电极、大推力火箭发动机内衬、导电弹簧、电气接插件、半导体引线框架、微波元器件以及热核堆体结构材料等用途。ADSC这一类金属基复合材料,其整体力学性能主要取决于铜基体与氧化铝弥散相的界面微观结构和性能,而界面结构与性能在很大程度上受制备过程热力学条件以及服役过程中杂质行为的重要影响,人们对决定其中相互作用和关系的基本原理尚缺乏深刻认识。
随着界面科学的不断发展,已经诞生了许多新的专门用于界面分析的实验研究和测试方法,包括聚焦离子束切割与高分辨电镜分析技术的结合、离子束轰击与俄歇电子能谱和X射线光电子能谱的结合等。但单纯依赖这些实验方法和检测技术仍然不足以系统而全面地认识界面微观结构及其宏观性能的内在联系和发展变化。第一性原理计算研究方法,近年来已成为研究材料界面不可或缺的工具,相关能量学计算研究与实验测试研究方法的结合,能够对界面的精细原子结构进行非常深入细致的研究[17-18]。本文作者选择内氧化型铜合金中广泛存在的Cu/Al2O3界面为例,基于高分辨电镜分析测定所获得的初步界面位向关系,通过构建界面原子结构模型,结合第一性原理热力学计算研究,从理论上深入探究界面微观结构及其宏观性能的内在联系,以及杂质元素的影响作用。
计算研究内容具体包括纯净内氧化界面的精细原子结构与理论结合强度,基体合金成分和制备条件对界面微观结构乃至性能的热力学影响:杂质元素在界面的偏析行为以及杂质偏聚对界面强度的影响等。
1 理论方法
第一性原理计算研究方法的最大特点是从最基本的热力学原理出发,以计算量子力学为手段,对体系能量(焓、熵、自由能)、晶体结构和电子结构等进行无参数的精确计算,结合合理的物理和热力学模型,可对材料的宏观物理性能、化学性能和力学性能等展开直接的理论预测。其计算过程由于不需要引入任何经验性参数或实验数据,计算结果依靠能量准则(或原子间力准则)自我收敛,故可排除一切人为因数的影响,研究结论可以做到自我支持。近20年来,随着并行计算科学和技术的飞速发展,基于第一性原理的计算研究方法,已成为当今材料交叉、前沿学科日渐受到重视的一个主要的、可靠的理论研究手段。
针对拟研究的目标,所展开的计算项目主要包括:1) 计算Cu/Al2O3纯净的界面相结构;2) 通过第一性原理热力学计算,确定不同氧分压条件下热力学稳定的界面相结构;3) 计算S和P的界面偏析能,并确定可能的偏析路径;4) 计算和比较理想纯净界面和S偏析界面的界面脱粘功(Work of separation,Wsep),评估界面偏析对结合强度的影响。
本文作者所有计算采用半商业化的VASP(Vienna ab-initio simulation package)软件包[19-20]进行。计算采用赝势和平面波基组,交换关联能采用广义梯度近似(GGA)[21],电子与离子核之间的相互作用采用投影扩充波(PAW)方法描述[22],平面波展开采用较高的能量截断(550 eV)。其中Al化学活度的有关计算,采用包含单个Al原子的2×2×2面心Cu超点阵,布里渊内的能量积分在3×3×3 Monkhorst-Pack(M-P)K点网格中进行, 温度对能量的贡献通过直接超胞法的声子计算和准简谐近似估算[23];界面的有关计算,采用三明治型的共格Cu/Al2O3/Cu界面模型,整个超胞包含8层Ni原子、8层Al原子、4层O原子和至少12  的真空层,布里渊内的积分采用3×3×1 M-P K点网格。所有的结构驰豫计算采用Hellmann-Feymann原子净力收敛判据20 meV/
的真空层,布里渊内的积分采用3×3×1 M-P K点网格。所有的结构驰豫计算采用Hellmann-Feymann原子净力收敛判据20 meV/  (1 eV/
(1 eV/ =1.6 nN)。相关的收敛计算结果表明,对于本文作者所研究的体系,上述参数设置足以确保计算效率和计算精度。
=1.6 nN)。相关的收敛计算结果表明,对于本文作者所研究的体系,上述参数设置足以确保计算效率和计算精度。
2 结果与讨论
2.1 界面结构
Cu/α-Al2O3界面的基本取向关系已被相关实验报导[24-28]。根据实验测定结果,在此,采用的基本界面取向关系为(111)Cu<110>Cu//(0001)Al2O3<1010>Al2O3。然而,这样的基本取向关系不足以反映界面的精细结构信息,比如共格应变量(Commensuration strain)、原子化学配比(Stoichiometry)以及界面原子的相对配位(Coordination)。这些细节信息将在本计算模型中充分考虑到,因为它们决定着界面的精细原子结构及其自由能。
一个实际界面在形成过程中,由于两侧晶格常数存在差异,会导致在界面附近不可避免出现有失配位错[29]。考虑到在界面模拟中,构建一个足够大的异型界面超胞将这类失配位错“自然”包含在内,会导致极大的计算量,在此采用的折衷方案是,依据实验确定的基本取向关系,在Cu/α-Al2O3界面附近晶格中引入相应合理的尽可能小的变形量,即通过将Cu(111)和Al2O3(0001)面的晶格以相同应变量3.8%分别拉伸和压缩后,形成理想共格界面原子结构模型。考虑到由此引入的应变能可能会影响界面强度 (即分离功Wsep)的计算评价,但通过界面和两个脱粘表面之间的体能量相消,可以最大程度地消除应变对界面强度的干扰[17, 30]。文献[30]中图7显示的结果充分说明相对于界面附近的原子化学配比(即参与界面化学反应的各元素原子的相对含量),共格应变的方式对界面强度的最终计算值影响并不大。
原子化学配比由实际制备过程的条件(如温度和化学反应气氛)决定。参考表面终端(Termination)的概念,针对该界面可构建出3种原子化学配比(或界面终端)类型,即理想化学配比(Stoichiometric),富铝型(Al-rich),富氧型(O-rich)。针对每种界面终端类型,Cu(111)和Al2O3(0001)的原子配位关系又分为3种(见图1),分别为Cu原子位于Al原子上方(Al-top)、O原子上方(O-top)和3个O原子构成的空隙位上方(hollow-top)。为了方便观察,图中只显示了最靠近界面的一层铜原子和两层Al2O3原子。其中Cu、O和Al原子分别以蓝球、红球和绿球表示。对上述一共9种结构模型进行充分的结构弛豫计算,同时设定总能和原子受力的迭代收敛判据,可以分别确定热力学最稳定的界面原子结构。

图1 Cu(111)<110>//Al2O3(0001)<1010>界面基本位向关系所对应的3种配位关系
Fig. 1 Top views of stoichiometric interface Cu(111)<110>// Al2O3(0001)<1010> with three coordination types (Al-top, O-top and hollow)
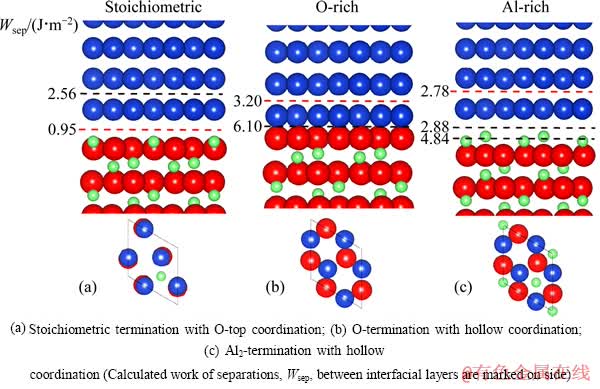
图2 弛豫后获得的Cu(111)<110>//α-Al2O3(0001)<1010>稳定界面侧视图和顶视图
Fig. 2 Side views and top views of stable interface structures of Cu(111)<110>//α-Al2O3(0001)<1010> after full relaxations
图2所示为计算确定的3种原子化学配比类型所对应的热力学稳定结构。各原子层间所对应的分离功(Wsep)也相应标注在图侧。计算结果显示,对于Al终端(Stoichiometric,NAl=(2/3)NO)界面,O-top型比Al-top和hollow-top型的总量低很多,表明尽管在Al2O3(0001)面上的O原子可以获得单层Al原子的部分饱和,但仍会倾向于与界面上的Cu原子结合。文献[31]中的态密度分析也表明,此界面的键合主要源于界面Cu原子在O-top位置的d轨道极化。由此形成的O-top型Al终端界面,其界面强度是3种终端类型中最低的(Wsep=0.95 J/m2)。
对于O终端(O-rich,NAl<(2/3)NO)界面,hollow-top型总能最低,但与Al-top型的总能差值不大。在界面附近的几层原子中,最弱的层间结合并不是发生在界面处,而是在Cu侧的第一层和第二层之间,且对应的分离功很高,Wsep=3.20 J/m2。
对于Al2终端(Al-rich,NAl>(2/3)NO)界面,O-top型和hollow-top型的总能相差非常小。界面键合具有明显的金属键特性。类似O终端界面,其最弱的层间结合并不是发生在界面处,而是在Cu侧的第一层和第二层之间,分离功为2.78 J/m2,与界面处的分离功(Wsep=2.88 J/m2)相差不大。
2.2 内氧化热力学计算
2.2.1 界面能的计算
根据界面能的定义,可以推导出热力学平衡条件下Cu/Al2O3界面能( )的表达式[14]:
)的表达式[14]:

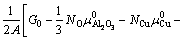
 (1)
(1)
式中:A是界面模型的横截面积;G0是整个界面超胞的Helmholtz自由总能;Ni和μi分别是各组元元素i的原子个数和化学势(或单位自由能);aAl为Al活度;k为玻尔兹曼常数。上标“0”表示各组元的纯净态。由于前4项中,温度对自由能的影响在较大程度上相互抵消,故总体来说,温度对界面能的影响主要体现在最后一项,即kTlnaAl[30]。因此,在后续计算中,G0和各项化学势将采用0 K时的计算值近似。
图3所示为计算得到的界面能随Al活度的变化关系。从图3可以看出,随着Al活度的减少,界面能先线性增大到一个最高值,而后保持常值,再逐渐变小。热力学平衡条件下,氧分压和Al活度存在以下换算关系: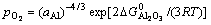 。换算的氧分压也标示在图3中。从图3可以推断,为了避免生成结合强度最弱的理想化学配比(Stoichimetric)界面,氧分压应控制在
。换算的氧分压也标示在图3中。从图3可以推断,为了避免生成结合强度最弱的理想化学配比(Stoichimetric)界面,氧分压应控制在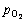 <1×10-22.0 Pa或
<1×10-22.0 Pa或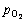 <1×10-6.7 Pa,即aAl>1×10-7.2 或 aAl<1×10-18.7,以期得到强度较高的富铝型(Al-rich)或富氧型(O-rich)界面。
<1×10-6.7 Pa,即aAl>1×10-7.2 或 aAl<1×10-18.7,以期得到强度较高的富铝型(Al-rich)或富氧型(O-rich)界面。
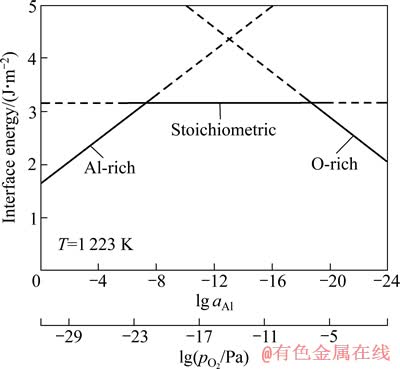
图3 1 223 K时计算得到的下界面能与Al活度aAl和氧分压pO2的关系
Fig. 3 Relationships among calculated interface energies and Al activity (aAl) and oxygen partial pressure (pO2) at 1 223 K
2.2.2 Al2O3形成的活度范围
在不同的氧分压、Al活度和温度条件下,Cu-Al-O体系中不仅仅会形成Al2O3,还有可能形成CuAlO2和CuO2 等其他氧化物相。
Cu-Al合金内氧化时,可能发生的化学反应式和对应的标准形成吉布斯自由能为[32-34]

 (2a)
(2a)
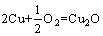
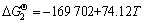 (2b)
(2b)
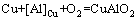
 (2c)
(2c)
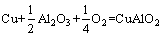
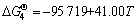 (2d)
(2d)
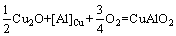
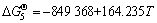 (2e)
(2e)
当上述反应都达到各自的热力学平衡时,依次对应有
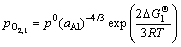 (3a)
(3a)
 (3b)
(3b)
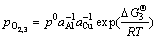 (3c)
(3c)
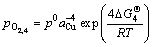 (3d)
(3d)
 (3e)
(3e)
式中:Al2O3、Cu2O和CuAlO2作为纯净物,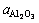 =
=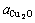 =
=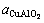 =1,p0 代表一个标准大气压,即101 325 Pa。
=1,p0 代表一个标准大气压,即101 325 Pa。
同时,Al浓度很低时,aCu≈1。Al在Cu(Al)合金中的活度(aAl)由温度和Al浓度直接决定:
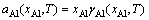 (4)
(4)
式中:γAl为对应的Al活度因子。可以推导Al活度因子随温度的变化关系如下[20]:
 (5)
(5)
式中:DH和DSn-c分别为Al 固溶到Cu中形成Cu(Al)合金所对应的焓变和非型熵变(主要包含电子熵和振动熵)。在较低的浓度范围内(xAl<10%),一般可以近似γAl(xAl,T)≈γAl(T)。
图4所示为计算得到的gAl 随温度的变化规律。T=1 223 K 时,γAl≈3.25×10-4。由式(4)可进一步推算xAl为0.1%~10%所对应的Al活度范围。同时,由式(3(a))也可计算各温度下生成氧化铝的下限氧分压。T=1 223 K时, 生成氧化铝的下限氧分压也只有1×10-23 Pa。根据图3,如果按照该下限氧分压进行内氧化,只要时间充分,所获得的氧化铝颗粒应为结合强度较高的富Al相。
由富Al相向理想化学配比相界面,或理想化学配比相界面向富O相界面发生转变,对应的临界Al活度分别为
 (6a)
(6a)
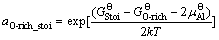 (6b)
(6b)
式中:GΘAl-rich、GΘStoi和GΘO-rich分别是富Al相,理想化学配比相和富O相界面模型的总Helmholtz自由能,μ0Al指纯铝原子的化学势。
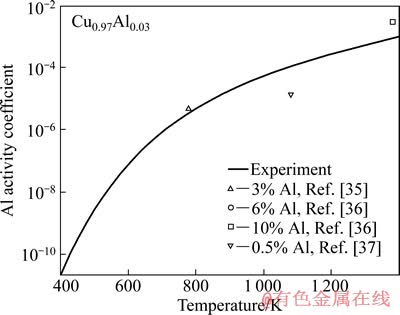
图4 计算得到的Al在Cu(Al)合金中的活度系数随温度的变化规律
Fig. 4 Calculated activity coefficient compared with experiments of dilute Al in Cu(Al) as function of temperature
由式(3)和式(6)确定的热力学关系,可计算得到内氧化Cu-Al-O体系的优势区位图(见图5)。该体系中还可能形成CuO和CuAl2O4相,但所需氧分压过高,故在优势区图中暂时不予考虑。图5中的灰色柱表示给定温度下初始Al浓度0.1%~10%所对应的Al活度范围。其中,灰色柱标示Al浓度xAl为0.1%→10% 所对应的Al活度大致范围。由图5可以确定形成Al2O3的下限氧分压(e点区域),并可同时预测生成CuAlO2所需的氧分压,也就是形成Al2O3的上限氧分压(b点),从而有助于在给定温度条件下,确定内氧化的热力学条件。高于a点对应的氧分压, 内氧化会优先获得Cu2O颗粒。只有将氧分压降低到b点以下,才有可能获得Al2O3颗粒,且随氧分压的逐渐降低,将依次优先获得富O相、理想化学配比相和富Al相的Al2O3颗粒。其中c和d点对应的氧分压分别表示所获得的Al2O3颗粒界面结构,由富Al相向理想化学配比相,或理想化学配比相向富O相发生转变的临界氧分压。低于形成Al2O3的下限氧分压,即e对应的氧分压(具体位置由合金中的初始Al浓度决定), 任何氧化反应都无法进行。
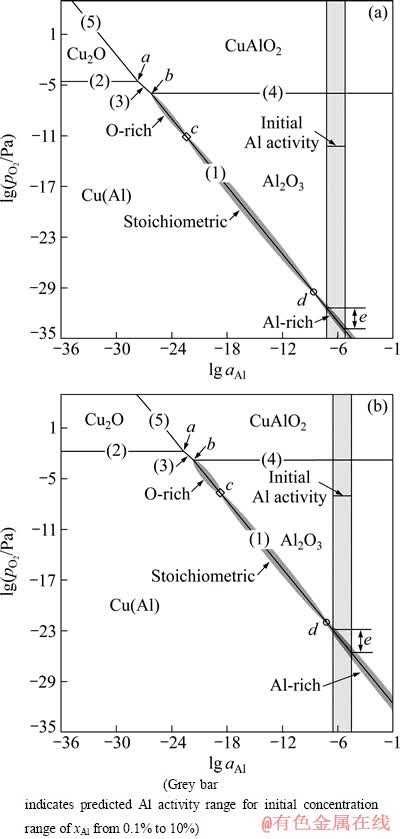
图5 计算预测的1 023和1 223 K下Cu(Al) 内氧化合金相组成的热力学优势区位图
Fig. 5 Calculated stability diagrams of precipitates in internally-oxidized Cu(Al) alloy as function of oxygen pressure (pO2) and Al activity at 1 023 (a) and 1 223 K (b)
进一步地,将温度作为一个变量,考察各化学反应的平衡氧分压(即图5中的各标志氧分压,点a~e)随温度的变化关系,可以得到对应的内氧化加工工艺曲线,结果如图6所示。图6可用来预测不同内氧化工艺条件(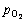 和T)下获得的不同界面相结构。为保证材料获得较优的整体力学性能和电导率,应尽量避免生成界面强度最弱的化学计量比相。从图6可以看出,为有利于生成界面强度较高的富氧相Al2O3颗粒(Ⅳ区),可采用的两种工艺选择路线:降低温度(A→B)或提高氧分压(A→C)。实际应用中,应该尽可能选择提高内氧化时的环境氧分压,并保持相对较高的温度。较高的温度和环境氧分压(A→C)有助于提高O原子在合金基体中的扩散速率,Al2O3颗粒也容易弥散分布。如果温度较低(A→B),O原子扩散速率低,不利于内氧化的制备效率,同时对应的内氧化上限氧分压偏低(b曲线),给实际制备过程中氧分压的准确控制带来困难。
和T)下获得的不同界面相结构。为保证材料获得较优的整体力学性能和电导率,应尽量避免生成界面强度最弱的化学计量比相。从图6可以看出,为有利于生成界面强度较高的富氧相Al2O3颗粒(Ⅳ区),可采用的两种工艺选择路线:降低温度(A→B)或提高氧分压(A→C)。实际应用中,应该尽可能选择提高内氧化时的环境氧分压,并保持相对较高的温度。较高的温度和环境氧分压(A→C)有助于提高O原子在合金基体中的扩散速率,Al2O3颗粒也容易弥散分布。如果温度较低(A→B),O原子扩散速率低,不利于内氧化的制备效率,同时对应的内氧化上限氧分压偏低(b曲线),给实际制备过程中氧分压的准确控制带来困难。
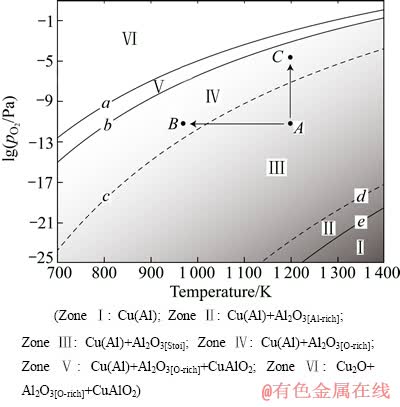
图6 计算预测的Cu(3%Al)内氧化合金相组成的加工工艺图
Fig. 6 Calculated processing diagram for internal oxidized Cu-3%Al
类似地,如果保持温度不变,选择降低环境氧分压(Ⅱ区),或许有助于形成富Al相Al2O3颗粒,其界面结合强度也比较高,但由于过于靠近内氧化的下限氧分压(e曲线),实际制备过程难以保证氧化反应的充分进行。
2.3 杂质效应
2.3.1 杂质偏析能和偏析路径的关系
如前所述,对于同样的基体,在不同生长条件下(温度和气氛),得到的界面平衡相可能不同,因此,活性元素和杂质的界面偏析能力也会相应不同,从而直接影响到它们对界面的影响和作用。界面偏析能力可以用界面偏析能(ΔGsep)来计量。首先计算3种纯净界面对应的总能量,然后从基体中引入杂质到纯净界面的不同位置,计算前后总能的变化,即可得该元素针对某类界面某个特定位置的界面偏析能。在此,定义正值的界面偏析能代表从基体向界面的偏析趋势(反之亦然)。比较同一元素在界面不同位置上的界面偏析能,可以确定该元素的偏析路径。比较界面上同一位置不同元素的界面偏析能,可以确定元素之间的偏析优先权。
图7所示为计算得到的界面偏析趋势。此处的界面偏析度以Cu(111)层上每个Cu原子为单位。括号中的数字代表各偏析进程对应的界面偏析能(eV/atom)。元素符号S、P的下标表示偏析的位置,下标“I”表示界面填隙位,下标”Cu”表示界面上的Cu原子被取代。
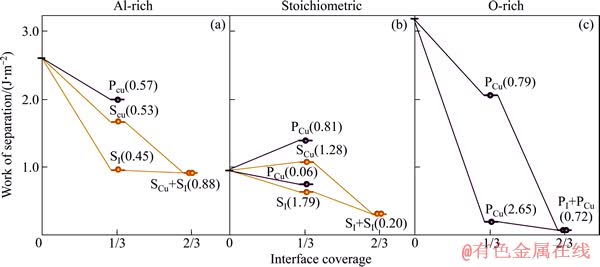
图7 计算得到的富Al相、理想化学配比相和富O相界面的界面脱粘功(Wsep)随界面偏析度的变化
Fig. 7 Calculated work of separation (Wsep) as function of interfacial coverage for Al-rich (a), stoichiometric (b) and O-rich interfaces (c)
对于富Al相界面,S可以偏析到间隙位(SI)或Cu取代位(SCu),对应的界面偏析能(ΔGsep)分别为0.45或0.53 eV/atom;P只能偏析到Cu取代位(PCu),界面偏析能为0.57 eV/atom。对于理想化学配比相界面,S偏析到间隙位(SI)或Cu取代位(SCu)的能力很强,界面偏析能高达1.79或1.28 eV/atom;P也可以偏析到界面的Cu取代位(PCu),对应的界面偏析能为0.81 eV/atom,但基本不能偏析到间隙位(PI ),界面偏析能只有0.06 eV/atom。对于富O相界面,S的偏析能为负,即S不能偏析到该界面。相反地,P偏析到界面间隙位(PI )的能力很强(ΔGsep=2.65 eV/atom)。
对于富O相界面,在首个P偏析后,后续的P能继续偏析到Cu取代位(PCu),ΔGsep=0.72 eV/atom。对于富Al相界面,若首个S偏析到Cu取代位(PCu),后续的S偏析到间隙位(SI)能继续降低体系能量,ΔGsep=0.88eV/atom。对于理想化学配比相界面,当间隙位(SI)被占据后,后续的S还能偏析到另一个间隙位(SI),ΔGsep=0.20 eV/atom。而P在上述两种界面中均不能继续偏析。
2.3.2 杂质偏析对界面强度的影响
针对每一种可能的偏析路径,可以通过一系列总能的计算,在对应的界面结构中寻找结合强度最弱的原子层,计算从该处分离界面所需的能量,即界面脱粘功(Wsep),并以此作为该界面结合强度的度量。显然,比较偏析前后界面结构的变化,计算相应所需的界面脱粘功,可以定量预测该元素偏析对界面结合强度的影响。
有关界面脱粘功的计算结果如图7和8所示。其中图8中每个分图的下方为相应的界面俯视图,以显示界面共格关系以及偏析元素在界面上的原子位置。对于感兴趣的界面,可进一步绘制出相应的基态价电子的密度分布云图(见图9),结合计算得到的界面脱粘功,从而能够定性地分析界面附近电子成键的特点,以及杂质偏析对界面化学成键的不同影响。
富O相和富Al相的纯净界面都具有较高的界面结合强度,分别为3.20和2.78 J/m2,约3倍于理想化学配比相界面的界面结合强度。对比图9(a)、(b)和(c)可知,这是因为富氧相界面上形成很强的Cu―O共价键(见图9(a)),富Al相界面上也形成较强的Cu―Al金属键(见图9(b)),远强于理想化学配比相界面上的Cu―O键(O同时和Cu和Al成键,使Cu―O键减弱,见图9(c))。
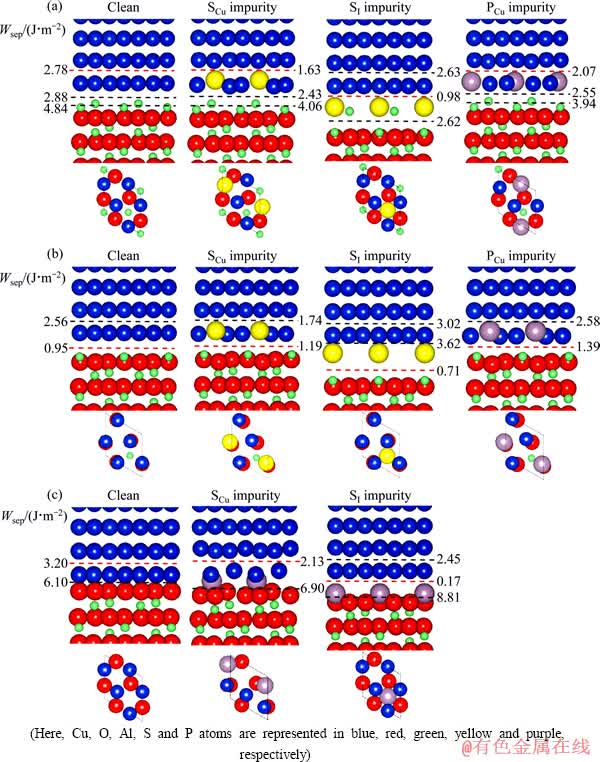
图8 计算预测的界面覆盖率为1/3ML的杂质偏析对富Al 相、理想化学配比相和富O相界面结构及其结合强度的影响
Fig. 8 Predicted atomic structures and Wsep for Al-rich (a), stoichiometric (b) and O-rich interfaces (c) under 1/3 monolayer (ML) coverage of segregated impurities
对于理想化学配比相界面,S具有很强的偏析作用:S会优先偏析到间隙位,把界面脱粘功从0.95降低到0.71 J/m2,这是由于Cu―O键被更弱的S―Al离子键和S―O共价键取代(见图9(d))。除此之外,S也可能偏析到Cu取代位,但界面脱粘功变化不大,从0.95增加到1.19 J/m2。此时S和O之间的价电子密度(见图9(e))和图9(c)中Cu和O 间的价电子密度基本相同。当S偏析的覆盖率达到2/3ML(Monolayer)时,S倾向于占据两个间隙位(SI+SI),可降低总能1.99 eV, 并使脱粘功降到0.38 J/m2(界面强度下降65%左右)。另外,P也可偏析到Cu取代位,使界面脱粘功从0.95 增加到1.39 J/m2。从图9(f)可看出,P―O间的价电子密度比图9(c)的价电子密度略大。但P无法达到2/3ML的覆盖率。
对于富Al相界面,若S偏析到Cu取代位时,界面脱粘功从2.78 J/m2降低到1.63 J/m2;若S偏析到间隙位,界面脱粘功从2.78 J/m2降低到0.98 J/m2。当S的界面覆盖率为2/3ML时,S倾向于占据一个取代位和一个间隙位(SCu+SI),最终降低总能1.41 eV,界面脱粘功下降到0.89 J/m2(同样也是65%左右的降低)。而P只可偏析到Cu取代位,使界面脱粘功从2.78 J/m2下降到1.39 J/m2。此情况下,P也无法达到2/3的偏析覆盖率。
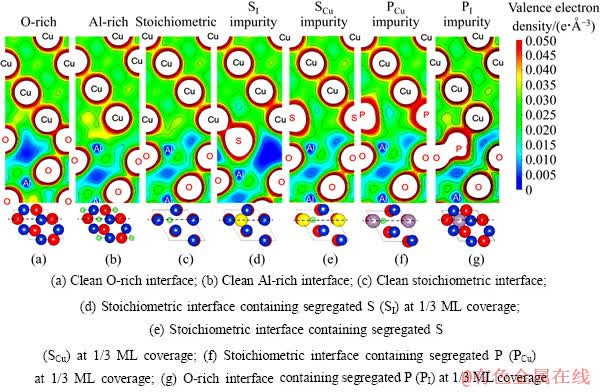
图9 界面基态电子密度云图
Fig. 9 Valence electron density contours
对于富O相面,S无法偏析到界面。但P却有较强的偏析趋势,并且严重降低界面强度。P偏析到Cu取代位或间隙位时,界面脱粘功从3.20 J/m2分别降低到2.13和0.17 J/m2。当P的界面覆盖率达到2/3ML时,界面脱粘功几乎下降为0。从价电子密度(见图9(g))可看出,P和Al2O3表面的O原子结合相当紧密,形成很强的P―O键,使Cu原子和O原子的结合完全隔断,而P和Cu间的键却比较弱,导致界面强度降低。
2.3.3 杂质偏析对氧化铝颗粒尺寸稳定性的影响
除了与基体之间的界面结合强度,影响第二相强化性能的关键因素还包括第二相颗粒的尺寸稳定性。对于一个成分确定的Cu-Al二元合金,当内氧化反应充分完成以后,Al2O3颗粒在基体内所占的体积比随之确定,颗粒尺寸将决定颗粒间距的大小,从而对合金中位错与颗粒间的相互作用,以及再结晶行为发挥重要影响。理想的氧化铝弥散强化铜合金,要求Al2O3颗粒细小且弥散分布,并在较高使用温度下,具有尽可能小的团聚趋势,以保持适当尺寸。
第二相颗粒的尺寸稳定性和界面能具有密切关系。假设基体中的颗粒均为球型,且平均半径为r,则颗粒团聚的吉普斯自由能变可表示为
 (12)
(12)
式中:γMP 表示基体/颗粒的界面能,ragg表示团聚后颗粒尺寸,n表示参与团聚的颗粒数。当团聚前颗粒总体积和团聚后颗粒的体积相等时,即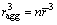 ,可得
,可得
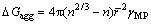 <0 (13)
<0 (13)
从式(13)可知,ΔGagg始终是负值,提供第二相颗粒团聚的热力学驱动力。且该驱动力的绝对值大小随着界面能和颗粒平均粒径增大而进一步增大。显然,除了确保颗粒细小弥散,设法降低界面能,同样,有利于减少团聚趋势,保证第二相颗粒的尺寸稳定性和分布均匀性。
综上所述,Cu/Al2O3的界面能并非恒定不变,取决于给定温度下的界面平衡相结构,同时受杂质偏析的强烈影响。界面能越低,对应的界面结合越强。对于氧化铝弥散强化铜合金,富O或富Al相界面比理化学配比相界面的界面能更低,因此,富O或富Al相界面的氧化铝颗粒的团聚趋势较小。若杂质S或P偏析到界面,并降低界面的结合强度,将使铜基体内的氧化铝颗粒的尺寸稳定性降低,颗粒易于合并长大,不利于最终合金制品保持组织和性能的均匀性。
3 结论
1) Cu/Al2O3界面相和对应界面能随制备气氛变化而变化。在保证形成氧化铝的热力学条件下,随着氧活度增加或Al活度减小,热力学平衡界面相经历自富Al相,依次向理想化学配比相和富氧相的转变。
2) 富氧终端界面的结合强度最高(3.20 J/m2),富Al终端界面强度次之(2.78 J/m2),约为理想化学计量比的Al终端界面强度(0.95 J/m2)的3倍。
3) 从计算得到的加工工艺图可知,内氧化制备Al2O3弥散强化铜合金时,温度和氧分压的调节必须同步。为了使反应迅速,并获得结合强度最高的富O相界面,应尽量在较高温度和较高氧分压的条件下进行制备。
4) 杂质S偏析到理想化学配比相的能力最强,富Al相界面次之,但无法向富O相界面偏析;杂质P偏析到富O相界面的能力最强,理想化学配比相和富Al相界面的能力次之。
5) 偏析到理想化学配比相和富Al相界面后,杂质S严重降低界面结合强度(最高可达65%);杂质P效应对界面相更加敏感,可极大地弱化富O相界面,导致其完全脱粘,或降低富Al相界面结合强度达25%,但杂质P对理想化学配比相界面表现出一定的强化作用,结合强度可提升约30%。
6) 相比于富Al或富O相界面,具有理想化学配比相界面的氧化铝颗粒更容易团聚长大。对界面有弱化效应的杂质偏析,会进一步降低颗粒尺寸稳定性。
REFERENCES
[1] LEA C, SAWLE R, SELLARS C M. Hot ductility and sulphur segregation in 1%C-1%Cr steels[J]. Philosophical Transactions of the Royal Society of London, 1980, 295(1413): 121.
[2] WHITE C L, SCHNEIBEL J H, PADGETT R A. High temperature embrittlement of Ni and Ni-Cr alloys by trace elements[J]. Metallurgical and Materials Transactions A, 1983, 14: 595-610.
[3] YAMAGUCHI M, SHIGA M, KABURAKI H. Grain boundary decohesion by impurity segregation in a nickel-sulfur system[J]. Science, 2005, 307: 393-397.
[4] SMIALEK J L. Effect of sulfur removal on Al2O3 scale adhesion[J]. Metallurgical and Materials Transactions A, 1991, 22(3): 739-752.
[5] STOTT F H. The oxidation of alumina-forming alloys[J]. Materials Science Forum, 1997, 251/254: 19-32.
[6] EVANS A G, HUTCHINSON J W, WEI Y. Interface adhesion: Effects of plasticity and segregation[J]. Acta Materialia, 1999, 47: 4093-4113.
[7] FUNKENBUSCH A W, SMEGGIL J G, BORNSTEIN N S. Reactive element sulfur interaction and oxide scale adherence[J]. Metallurgical Transactions A, 1985, 16(6): 1164-1166.
[8] LEES D G. On the reasons for the effects of dispersions of stable oxides and additions of reactive elements on the adhesion and growth-mechanisms of chromia and alumina scales―the “sulfur effect”[J]. Oxidation of Metals, 1987, 27: 75-81.
[9] HOU P Y. Segregation phenomena at thermally grown Al2O3/alloy interfaces[J]. Annual Review of Materials Research, 2008, 38: 275-298.
[10] JIANG Y, LIU R. Gettering of S in Ni from first principles[J]. Scripta Materialia, 2010, 62: 782-785.
[11] VILJOEN E C, PLESSIS J D. Auger/LEED linear heating study of Sn and S bulk to surface diffusion in a Cu(111)(Sn, S) single crystal[J]. Surface and Interface Analysis, 1995, 23(2): 110-114.
[12] BENARD J, BERTHIER Y. Adsorption on metal surfaces: An integrated approach: Studies in surface science and catalysis, (volume 13)[M]. Amsterdam, Oxford, New York: Elsevier Science Ltd, 1983.
[13] STOBRAWA J P, RDZAWSKI Z M. Dispersion-strengthened nanocrystalline copper[J]. Journal of Achievements in Materials and Manufacturing Engineering, 2007, 24: 35-42.
[14] 帅歌旺, 张 萌. 高强度、高导电铜合金及铜基复合材料研究进展[J]. 特种铸造及有色合金, 2005, 25(9): 534-537.
SHUAI Ge-wang, ZHANG Meng. Progress in high-strength and high-conductivity copper alloys and copper Base composites[J]. Special Casting & Nonferrous Alloys, 2005, 25(9): 534-537.
[15] 李美霞, 郭志猛, 赵奇特. 氧化铝弥散强化铜的研究进展及其应用[J]. 粉末冶金工业, 2008, 18(1): 36-40.
LI Mei-xia, GUO Zhi-meng, ZHAO Qi-te. Progress in and applications of copper-base alloys[J]. Powder Metallurgy Industry, 2008, 18(1): 36-40.
[16] 郭铁明, 季根顺, 马 勤, 周 琦, 贾建刚, 陈辉. 弥散强化型导电铜基复合材料的研究进展[J]. 材料导报, 2007, 21(7): 27-31, 35.
GUO Tie-ming, JI Gen-shun, MA Qin, ZHOU Qi, JIA Jian-gang, CHEN Hui. New progress in researches on dispersion hardening copper matrix composite materials[J]. Materials Review, 2007, 21(7): 27-31, 35.
[17] ZHANG W, SMITH J R, WANG X G, EVANS A G. Influence of sulfur on the adhesion of the Ni/Al2O3 interface[J]. Physical Review B, 2003, 67: 245414.
[18] JIANG Y, SMITH J R, EVANS A G. First principles assessment of metal/oxide interface adhesion[J]. Applied Physics Letters, 2008, 92: 141918.
[19] KRESSE G, HAFNER J. Ab initio molecular dynamics for liquid metals[J]. Physical Review B, 1993, 47: 558-561.
[20] KRESSE G,  J. Efficient iterative schemes for ab initio total energy calculations using a plane-wave basis set[J]. Physical Review B, 1996, 54: 11169-11186.
J. Efficient iterative schemes for ab initio total energy calculations using a plane-wave basis set[J]. Physical Review B, 1996, 54: 11169-11186.
[21] PERDEW J P, WANG Y. Accurate and simple analytic representation of the electron-gas correlation energy[J]. Physical Review B, 1992, 45: 13244-13249.
[22] KRESSE G, JOUBERT J. From ultrasoft pseudopotentials to the projector augmented-wave method[J]. Physical Review B, 1999, 59: 1758-1775.
[23] JIANG Y, SMITH J R, EVANS A G. Temperature dependence of the activity of al in dilute Ni(Al) solid solutions[J]. Physical Review B, 2006, 74: 224110.
[24] DEHM G, SCHEU C, RUHLE M, RAJ R. Growth and structure of internal Al2O3(0001) and Cu/T i/Al2O3 interfaces[J]. Acta Materialia, 1998, 46: 759-772.
[25] OH S H, SCHEU C, WAGNER T, TCHERNYCHOVA E,  M. Epitaxy and bonding of Cu films on oxygen-terminated α-Al2O3(0001) surfaces[J]. Acta Materialia, 2006, 54: 2685-2696.
M. Epitaxy and bonding of Cu films on oxygen-terminated α-Al2O3(0001) surfaces[J]. Acta Materialia, 2006, 54: 2685-2696.
[26] SASAKI T, MIZOGUCHI T, MATSUNAGA K, TANAKA S. HRTEM and EELS characterization of atomic and electronic structures in Cu/α-Al2O3 interfaces[J]. Applied Surface Science, 2005, 241: 87-90.
[27] DEHM G,  M, DING G, RAJ R. Growth and structure of copper thin films deposited on (0001) sapphire by molecular beam epitaxy[J]. Philosophical Magazine Part B, 1995, 71: 1111-1124.
M, DING G, RAJ R. Growth and structure of copper thin films deposited on (0001) sapphire by molecular beam epitaxy[J]. Philosophical Magazine Part B, 1995, 71: 1111-1124.
[28] DEHM G, SCHEU C, MOBUS G, BRYDSON R,  M. Synthesis of analytical and high resolution transmission electron microscopy to determine the interface structure of Cu/Al2O3[J]. Ultramicroscopy, 1997, 67(1/4): 207-217.
M. Synthesis of analytical and high resolution transmission electron microscopy to determine the interface structure of Cu/Al2O3[J]. Ultramicroscopy, 1997, 67(1/4): 207-217.
[29] GUTEKUNST G, MAYER J,  M. The niobium/sapphire interface: Structural studies by HREM[J]. Scripta Metallurgica et Materialia, 1994, 31(8): 1097-1102.
M. The niobium/sapphire interface: Structural studies by HREM[J]. Scripta Metallurgica et Materialia, 1994, 31(8): 1097-1102.
[30] SMITH J R, JIANG Y, EVANS A G. Adhesion of the γ-Ni(Al)/α-Al2O3 interface: A first-principles assessment[J]. Philosophical Magazine Part B, 2007, 98: 1214-1221.
[31] ZHANG W, SMITH J R, EVANS A G. The connection between ab initio calculations and interface adhesion measurements on metal/oxide systems: Ni/α-Al2O3 and Cu/α-Al2O3[J]. Acta Materialia, 2002, 50: 3803-3816.
[32] CHASE M W. NIST-JANAF Themochemical Tables: Monograph 9[J]. Journal of Physical and Chemical Reference Data, 1998.
[33] JACOB K T, ALCOCK C B. Thermodynamics of CuAlO2 and CuAl2O4 and Phase Equilibria in the System Cu2O-CuO-Al2O3[J]. Journal of the American Ceramic Society, 1975, 58(5/6): 192-195.
[34] 申玉田, 崔春翔, 徐艳姬, 武建军, 刘 华. Cu-Al合金内氧化的热力学分析―Ⅱ热力学函数的应用[J]. 稀有金属材料与工程, 2004, 33(7): 692-695.
SHEN Yu-tian, CUI Chun-xiang, XU Yan-ji, WU Jian-jun, LIU Hua. Thermodynamic analysis of internal oxidation of Cu-Al alloy[J]. Rare Metal Materials and Engineering, 2004, 33(7): 692-695.
[35] MIETTINEN J. Thermodynamic description of the Cu-Al-Sn system in the copper-rich corner[J]. Metallurgical and Materials Transactions A, 2002, 33: 1639-1648.
[36] WILDER T C. Extractive metallurgy division-the thermodynamic properties of the liquid aluminum-copper system[J]. Trans TMS-AIME, 1965, 233: 1202-1208.
[37] GUO F, LI L, ZONG Y, CANG D, PAN W, ZHANG J. Effect of electric field on the activity and quenching structure of liquid Cu-Al alloys[J]. Journal of University of Science and Technology Beijing, 2005, 12(2): 155-159.
(编辑 龙怀中)
基金项目:国家自然科学基金面上项目(51171211);广东省教育部产学研结合重点项目(2011B090400 552);国家教育部新世纪优秀人才支持计划项目(NCET-10-0837)
收稿日期:2012-07-20;修订日期:2013-08-20
通信作者:江 勇,教授,博士;电话:0731-88830263;E-mail:yjiang@csu.edu.cn

