DOI: 10.11817/j.issn.1672-7207.2018.06.008
典型氧化铁皮结构电化学腐蚀行为
曹光明,汤军舰,林飞,李志峰,杨名,刘振宇
(东北大学 轧制技术及连轧自动化国家重点实验室,辽宁 沈阳,110819)
摘要:利用电化学腐蚀实验系统研究4种典型氧化铁皮结构及基体钢在Cl-环境下的腐蚀行为,通过极化曲线和交流阻抗谱(EIS)对比分析不同氧化铁皮结构的低频容抗弧的半径和电化学阻抗(Ra+Rt),同时借助Tafel外推法拟合得出试样自腐蚀电位和自腐蚀电流变化规律。研究结果表明:不同结构氧化铁皮的耐蚀性从强到弱依次为Ⅳ型氧化铁皮,Ⅲ型氧化铁皮,Ⅱ型氧化铁皮,Ⅰ型氧化铁皮,钢板基体,这是由于Ⅳ型的氧化铁皮(外层为非常薄Fe2O3层,中间为Fe3O4层,靠近基体的为较厚FeO层)表面的孔隙率最低为16.61%,并且Ⅳ型氧化铁皮中的共析组织最少,因此通过控制氧化铁皮结构可以达到提高热轧带钢的常温耐蚀性的目的。
关键词:氧化铁皮;共析组织;电化学腐蚀;极化曲线;耐蚀性
中图分类号:TG335.1 文献标志码:A 文章编号:1672-7207(2018)06-1366-07
Electrochemical corrosion behavior of typical structure of oxide scale
CAO Guangming, TANG Junjian, LIN Fei, LI Zhifeng, YANG Ming, LIU Zhenyu
(State Key Laboratory of Rolling & Automation, Northeastern University, Shenyang 110819, China)
Abstract: The corrosion behavior of four types of oxide scale and substrate were investigated in the condition with Cl- by electrochemical corrosion tests. The low frequency capacitance arc radius and Ra+Rt of the different structures of oxide scale were comparatively analyzed by polarization curves and electrochemical impedance spectroscopy (EIS). The results show that the corrosion resistance of the different structures of oxide scale from strong to weak is followed by type IV, type III, type II, type I, substrate, which is because the structure of type IV consists of outer thin layer of Fe2O3, the intermediate layer of Fe3O4 and inner thick layer of FeO, which has the lowest porosity as 16.61% and the least eutectoid structure. Therefore, the corrosion resistance of hot-rolled plates can be improved by controlling the structure of oxide scales.
Key words: oxide scales; eutectoid structure; electrochemical corrosion; polarization curves; corrosion resistance
热轧带钢(卷、板)容易出现因雨淋和凝露等原因而导致的表面锈蚀现象,每年我国由于腐蚀而报废的钢材的量为年产量的10%~20%。在大气环境中,钢的腐蚀主要是在其表面形成的水膜下不断形成锈蚀产物的电化学反应[1-3],在湿润的大气中,由于钢表层具有一定的吸附作用,致使其表层易覆盖一层非常薄的水膜,同时其表层成分或者受力变形等不均匀,使相邻部分产生了电极电位的差异,形成了很多微电池[4]。在阳极区,铁基体发生化学反应被氧化成Fe2+进入水膜;在阴极区,水中溶解的氧被还原成OH-,继而与水膜里的Fe2+结合生成白色物质Fe(OH)2,紧接着在O2和H2O参与下其被氧化成松脆易脱落铁锈Fe(OH)3[5-6]。在热轧钢材生产过程中,钢材表面会形成一层氧化铁皮,这层氧化铁皮会对钢基体的电化学腐蚀行为造成显著影响。HIROKI[7]研究了锈层在钢铁腐蚀与防腐蚀保护中所起的作用。根据腐蚀过程中有关化学反应的定量分析,建立了关于钢铁大气腐蚀的过程以及腐蚀产物(锈层)性质的模型,并依次阐明具有防腐蚀性的锈层形成所需的条件。MA等[8]通过失重法研究了低碳钢在热带海洋和工业场所环境中的大气腐蚀动力学,结果表明:在相对湿度高的环境下的腐蚀机制和腐蚀动力学存在过渡行为,在过渡阶段前后瞬时腐蚀速度遵循不同的指数函数。DONG等[9]通过电化学测量和表面表征的方法,研究了热轧带钢在质量分数为1%的NaCl溶液中的电化学腐蚀行为,其结果证明了在致密氧化铁皮层的覆盖下,钢基体的腐蚀将受到阻碍。COLLAZO等[10]通过对表面带有氧化铁皮钢板的电化学腐蚀行为的实验研究,得出致密性氧化铁皮的存在能够明显提升钢板基体的耐蚀性能。THEE等[11]通过电化学阻抗谱和薄膜厚度的测量,研究了耐候钢在干、湿交替大气环境中腐蚀情况,研究表明:氧化锈层的出现使钢腐蚀速度大大降低。张华民等[12]通过运用静态挂片法,研究了表面有、无氧化铁皮层的试样在质量分数3%的NaCl溶液中的腐蚀行为,结果表明,钢板表面氧化铁皮层的稳定电位比基体稳定电位正和氧化铁皮层自身的不完整性是钢铁表面在含氯离子的中性介质中发生明显局部腐蚀的主要原因。何爱花等[13]利用极化曲线和电偶法研究了含Cl-中性介质中氧化皮对碳钢腐蚀的影响,研究表明在含Cl-中性介质中,氧化皮/碳钢电偶的存在将急速加剧碳钢的腐蚀。孙彬等[14]研究发现:含有不同氧化铁皮的热轧钢在干湿交替的腐蚀试验中表现出不同的耐腐蚀性能。研究含有不同氧化铁皮的热轧钢板的电化学行为对于利用表面氧化铁皮来提高热轧钢板的耐腐蚀性十分必要。一般热轧钢材氧化铁皮主要有3种存在形式[15-16]:赤铁矿Hematite(α-Fe2O3)、磁铁矿Magnetite(Fe3O4)、方铁矿Wustite(FeO);而3种氧化物相在其晶体结构和物理特性方面各不相同,不同性质的氧化铁皮与热轧钢板的电化学腐蚀有紧密的相关性。本文作者通过工艺控制得到了4种不同的氧化铁皮结构,同时采用电化学实验,利用极化曲线以及电化学阻抗谱(EIS)[17-20]对带不同氧化铁皮结构试样和基体试样的电化学腐蚀行为进行系统研究,以获取最优的耐蚀性铁皮结构。
1 实验
本实验材料取自国内某钢厂的热轧带钢Q235B,其化学成分见表1。结合生产现场实际条件,通过采用不同的热轧和冷却工艺制度得到了4种不同的氧化铁皮结构类型试样,将试样依次进行热镶嵌、砂纸打磨、抛光、1%(体积分数)盐酸酒精[21]腐蚀,然后使用JXA-8530F型场发射电子探针(EPMA)来观察实验试样的氧化铁皮组织形貌。本实验所用4种工艺参数如表2所示,其中,实验冷取样温度为室温(约25 ℃),热取样温度为卷曲温度(600 ℃);实验中采用的密集冷却是将层流冷却区的集管阀门打开使带钢试样快速冷却,稀疏冷却是将层流冷却区的集管不连续打开使试样均匀冷却。
表1 实验用钢化学成分(质量分数)
Table 1 Chemical composition of tested steel %

表2 实验热轧带钢工艺
Table 2 Hot rolling processes of strips with different oxide scales

采用CS350型腐蚀电化学工作站对典型氧化铁皮结构的钢板样品进行动电位极化曲线与交流阻抗谱的测定。电化学实验采用的三电极体系,辅助电极为Pt电极,参照电极为饱和甘汞电极,研究电极为实验所用钢板试样,电化学测试液为质量分数3.5% 的NaCl溶液,电极面积为1 cm2,测试温度为25 ℃。同时,在动电位极化曲线测定时,设定扫描的电位在-0.8~-0.2 mV之间,扫描的速度为0.33 mV/s;在阻抗测定时使用频率响应分析程序(FRA),测定的频率范围为105~107 Hz,交流信号电压的振幅为10 mV,测量电位是试样在实验液体里的开路电位。根据对所测得的极化曲线用ZView电化学分析软件拟合计算得到不同钢板试样的自腐蚀电流与自腐蚀电位,同时根据阻抗数据的Nyquist图,对其等效电路进行拟合与分析,计算得到不同实验用钢的阻抗,由此可以判断不同铁皮结构类型的耐蚀性差异。
2 结果与讨论
2.1 氧化铁皮断面形貌分析
4种不同工艺条件下实验试样氧化铁皮的断面形貌如图1所示。由图1可见:Ⅰ型氧化铁皮主要由靠近基体的共析组织(Fe3O4+Fe)和外侧的Fe3O4组成,其中原始FeO的共析转变量超过70%。Ⅱ型氧化铁皮由Fe3O4,共析组织(Fe3O4+Fe)及少量残留的FeO组成,其中FeO的共析转变量小于30%。Ⅲ型氧化铁皮由原始 Fe3O4、残留FeO及先共析Fe3O4组成。Ⅳ型氧化铁皮由靠近基体的较厚FeO层、中间Fe3O4层及表面极薄的Fe2O3层组成。
2.2 电化学实验结果
2.2.1 极化曲线
整个电化学实验过程中,电化学腐蚀的阳极过程为试样在电解液里的溶解,阴极过程为O2的去极化。如图2所示为含不同类型氧化铁皮的钢板试样以及钢板基体试样在质量分数3.5% 的NaCl溶液中测定的极化曲线。从图2可以看出:氧化铁皮试样的极化曲线的形状基本相同,说明氧化铁皮的存在只是影响的是阴、阳极反应的电流,并未改变钢板基体在电解溶液中阴、阳极反应机理。同钢板基体的极化曲线形式相比较,含不同氧化铁皮结构的实验试样的极化曲线均向左移动,同时其自腐蚀电位向正方向偏移,只是偏移幅度有所不同。
用ZView电化学分析软件通过Tafel外推法拟合计算出各个实验用钢的自腐蚀电位与自腐蚀电流,见表3。从表3可见:自腐蚀电位从大到小依次为Ⅳ型氧化铁皮、Ⅲ型氧化铁皮、Ⅱ型氧化铁皮、Ⅰ型氧化铁皮、基体,而自腐蚀电流大小规律与之相反。自腐蚀电位越正,表明试样发生腐蚀倾向越小;而自腐蚀电流密度越小,表明试样发生腐蚀的速度越慢。由此可知,带氧化铁皮的试样腐蚀倾向和腐蚀速率均比基体的小,氧化铁皮一定程度上起到了耐蚀保护作用,减缓了钢板基体的腐蚀速率。而含不同氧化铁皮的实验用钢的耐蚀性由强到弱依次为Ⅳ型氧化铁皮、Ⅲ型氧化铁皮、Ⅱ型氧化铁皮、Ⅰ型氧化铁皮,即保留原始三层结构的氧化铁皮对基体的保护性最好,以先共析Fe3O4为主的氧化铁皮耐蚀性优于以共析组织为主的氧化铁皮,且在氧化铁皮层中共析组织越多其耐腐蚀性越差。
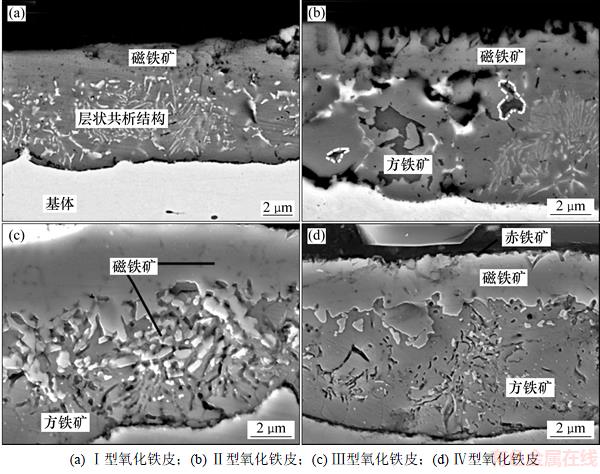
图1 实验用钢氧化铁皮的断面形貌
Fig. 1 Cross-sectional microstructure of oxide scales on steel samples

图2 试样在3.5% NaCl溶液中的极化曲线
Fig. 2 Polarization curves of samples in 3.5% NaCl solution
表3 试样的自腐蚀电位和自腐蚀电流
Table 3 Corrosion potential and corrosion current of samples

2.2.2 氧化铁皮孔隙率的测定
钢铁表面氧化铁皮的致密性是决定其耐腐蚀性能的关键[22],钢铁在氧化腐蚀中产生的氧化铁皮耐蚀性能取决于氧化铁皮的完整性。完整性的必要条件是P-B比,以γ表示:
 (1)
(1)
式中:M为铁皮的相对分子质量;A为铁的相对原子质量;n为氧化铁皮中铁的化合价;m=nA为形成氧化铁皮所消耗的铁的质量;ρM和ρOX分别为钢铁和氧化铁皮的密度。
当表面氧化铁皮完整、致密时,在腐蚀过程中,氧化铁皮首先充当电极发生电化学反应;在热轧生产过程中,由于轧制变形和温度变化引起的应力会造成钢板表面氧化铁皮不可避免地存在孔隙和裂纹,而这些缺陷成为腐蚀液体离子侵入到基体的快速通道,致使其与基体直接接触并发生反应,加速了腐蚀的进行[23]。本文引入孔隙率作为判定氧化铁皮致密度的参数[9]:
 (2)
(2)
式中:Jcorr,f与Jcorr,o分别为表面带与不带氧化铁皮碳钢的电化学腐蚀电流密度。利用式(2)得出不同形式氧化铁皮的孔隙率如表4所示。由表4可知:在4种典型氧化铁皮结构中,Ⅰ型的孔隙率最高,为41.32%,而Ⅳ型的孔隙率最低,仅为16.61%;此外,Ⅰ型和Ⅱ型的氧化铁皮结构的孔隙率较为接近。
表4 不同结构的氧化铁皮的孔隙率
Table 4 Porosity of four types oxide scale

2.2.3 交流阻抗谱(EIS)结果
图3所示为不同结构氧化铁皮实验用钢及无氧化铁皮实验用钢在质量分数3.5% 的NaCl液体里浸泡30 min的Nyquist图。从图3可知:无氧化铁皮试样的Nyquist曲线只存在单个容抗弧;而带有氧化铁皮试样的交流阻抗谱出现2个容抗弧,分布在低频与高频阶段,这说明其具有2个电容,一个为电极表面与溶液的双电层电容,另一个为溶液离子通过氧化铁皮空隙等缺陷渗入到基体形成的膜电容。同时,低频容抗弧的半径由大到小依次为Ⅳ型氧化铁皮、Ⅲ型氧化铁皮、Ⅱ型氧化铁皮、Ⅰ型氧化铁皮,钢板基体。用ZView电化学分析软件对其电化学阻抗谱进行拟合,拟合时采用的等效电路见图4(其中,Rs为溶液电阻;C1为电极表面与溶液形成的双电层电容;Q为氧化铁皮的膜电容;Rt为电化学反应电阻;Ra为氧化铁皮的膜电阻,其值反映氧化铁皮对基体腐蚀阻碍作用[24])。以Ra+Rt作为评价指标评价试样的耐蚀性能,其值越大,表示氧化铁皮的耐腐蚀作用越强[25]。

图3 不同试样在3.5% NaCl溶液中浸泡30 min的Nyquist图
Fig. 3 Nyquist diagram of samples in 3.5% NaCl for 30 min

图4 电化学阻抗谱拟合的等效电路
Fig. 4 Equivalent circuits of EIS fitting
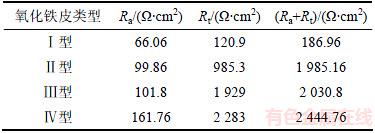
对氧化铁皮试样拟合出的电化学反应电阻见表5。从表5可见:4种不同结构氧化铁皮试样的Ra+Rt从大到小依次为Ⅳ型氧化铁皮、Ⅲ型氧化铁皮、Ⅱ型氧化铁皮、Ⅰ型氧化铁皮,无先共析或共析转变的三次氧化铁皮电化学反应电阻最大,达2 444.76 Ω/cm2,电极反应比较缓慢,离子在氧化铁皮层中不容易扩散,其耐腐蚀性能最强。而以共析组织为主的氧化铁皮电化学阻抗仅为186.96 Ω/cm2,远小于其他3种结构氧化铁皮的阻抗,其对基体的保护作用最弱。电化学阻抗Ra+Rt的变化规律与Nyquist 曲线中的低频容抗弧变化规律一致。由于氧化铁皮与钢基体二者在电化学性质方面的不同,当腐蚀溶液通过缺陷浸入到基体时,会形成氧化层/碳钢电偶并促进钢基体的腐蚀。此时形成的电极受活化影响,在阻抗谱图中会有附加的容抗弧出现。由图3可知:含有不同氧化铁皮的试样都出现了附加容抗弧,而无氧化铁皮试样则没有附加容抗弧出现。附加容抗弧的出现说明氧化铁皮存在缺陷并且其活性点较多,腐蚀液能够透过缺陷与基体直接接触构成腐蚀。
表5 不同氧化铁皮试样在3.5% NaCl溶液浸泡30 min的交流阻抗谱参数
Table 5 EIS data of samples with different microstructure oxide scales in 3.5% NaCl for 30 min
2.3 实验结果分析
针对热轧钢材生产过程,钢材表面形成一层氧化铁皮会在钢材后续使用过程中能起到保护作用,这层膜组织结构的连续性和合理性对于提高热轧钢耐腐蚀性非常关键。Ⅳ型为原始的三层结构氧化铁皮,表层为非常薄的Fe2O3层,中间为Fe3O4层,靠近基体的为最厚的FeO层。由于Ⅳ型为热取样,其表面氧化铁皮形貌如图5(a)所示;而其他氧化铁皮结构为冷取样,经过了后续冷却、开卷和平整工序,因此表面氧化层出现微裂纹,如图5(b)所示。根据Fe-O相图可知,氧化铁皮会因所处温度的改变而在其内部发生相变。由于不同氧化产物的密度不同,在发生相变过程中会出现体积膨胀形成内应力,同时会在氧化铁皮内部形成微裂纹。因此,从取样方式和氧化铁皮相变来说,Ⅳ型氧化铁皮保存最为完整,这也是其孔隙率最低,而其他结构氧化铁皮孔隙率高的根本原因。
氧化铁皮组成形式也是决定氧化铁皮耐蚀性的关键因素,钢材在高温腐蚀时,生成的氧化膜由FeO,Fe3O4与Fe2O3层构成[26]。其中这3种氧化物的PBR参数分别为1.68~1.76,2.10和2.14。由氧化铁皮致密性可知,Fe2O3耐腐蚀性最强,FeO的耐蚀性能最弱,考虑到Fe2O3过多容易造成红锈缺陷,因此,Fe3O4的控制是提高耐蚀性的关键。针对热轧生产流程,在卷取阶段,富氧的FeO在冷却过程中率先形成先共析Fe3O4[27],当冷却速率较低时,共析反应能够完全进行,氧化铁皮中会出现明显的共析组织,而当冷却速率较高时,则共析反应难以完全进行,甚至会将FeO组织保留至室温条件。Ⅰ型和Ⅱ型氧化铁皮层中均存在含量不等的共析组织,这种组织的结构特点是Fe3O4和单质Fe成片层状交替存在,由于Fe和Fe3O4本身存在着电位差,这样,相互交叉的Fe3O4和Fe自动形成腐蚀原电池,同时,由于单质Fe的腐蚀电位低于Fe3O4的腐蚀电位,所以,单质Fe作为腐蚀电池的阳极,在电化学腐蚀液中优先溶解掉,快速地形成局部腐蚀,这也是这2类氧化铁皮的试样易快速腐蚀的原因。因此,提高氧化铁皮致密性,减少氧化铁皮孔隙率,合理控制氧化铁皮结构类型,抑制共析组织的产生是提高氧化铁皮耐蚀性的关键。在实际生产中,钢带在热轧过程中形成的三层氧化铁皮主要以FeO为主,在后续卷曲过程中FeO发生先共析或共析转变。结合氧化层变温转变曲线[23],可以通过控制卷取温度和冷却速率,来抑制FeO共析转变的进行,从而实现对于氧化铁皮结构的精确控制。

图5 氧化铁皮表面形貌
Fig. 5 Surface morphology of oxide scales
3 结论
1) 含4种典型的氧化铁皮试样及基体试样的自腐蚀电位从大到小依次为Ⅳ型氧化铁皮、Ⅲ型氧化铁皮、Ⅱ型氧化铁皮、Ⅰ型氧化铁皮、基体试样,自腐蚀电流则与之相反。
2) Ⅰ型~Ⅳ型氧化铁皮的孔隙率分别为16.61%,27.72%,39.52%和41.32%。利用热取样工艺获得的氧化铁皮结构比较完整,孔隙率较低,同时氧化铁皮经过相变会造成孔隙率增高。
3) 与基体试样相比较,含氧化铁皮试样的交流阻抗谱会出现高、低频容抗弧,由电化学阻抗(Ra+Rt)可知耐蚀能力从大到小依次为Ⅳ型氧化铁皮、Ⅲ型氧化铁皮、Ⅱ型氧化铁皮、Ⅰ型氧化铁皮。
4) 氧化铁皮中共析组织形成腐蚀电池会加速基体腐蚀,抑制共析反应获得足够多的Fe3O4,同时提高氧化铁皮致密性和合理性可以有效地提升钢材的耐蚀性能。
参考文献:
[1] SUZUKI I, MASUKO N, HISAMATSU Y. Electrochemical properties of iron rust[J]. Corrosion Science, 1979, 19(8): 521-533.
[2] de LA FUENTE D, D AZ I, SIMANCAS J, et al. Long-term atmospheric corrosion of mild steel[J]. Corrosion Science, 2011, 53(2): 604-617.
AZ I, SIMANCAS J, et al. Long-term atmospheric corrosion of mild steel[J]. Corrosion Science, 2011, 53(2): 604-617.
[3] HAN Wei, PAN Chen, WANG Zhenyao, et al. A study on the initial corrosion behavior of carbon steel exposed to outdoor wet-dry cyclic condition[J]. Corrosion Science, 2014, 88(16): 89-100.
[4] MENG G Z, ZHANG C, CHENG Y F. Effects of corrosion product deposit on the subsequent cathodic and anodic reactions of X-70 steel in near-neutral pH solution[J]. Corrosion Science, 2008, 50(11): 3116-3122.
[5] HOERLE S, MAZAUDIER F, DILLMANN P, et al. Advances in understanding atmospheric corrosion of iron. II: Mechanistic modeling of wet-dry cycles[J]. Corrosion Science, 2004, 46(6): 1431-1445.
[6] CHEN Y Y, TZENG H J, WEI L I, et al. Corrosion resistance and mechanical properties of low-alloy steels under atmospheric conditions[J]. Corrosion Science, 2005, 47(4): 1001-1021.
[7] HIROKI T. The role of rusts in corrosion and corrosion protection of iron and steel[J]. Corrosion Science, 2008, 50(7): 1872-1883.
[8] MA Yuantai, LI Ying. The atmospheric corrosion kinetics of low carbon steel in a tropical marine environment[J]. Corrosion Science, 2010, 52(5): 1796-1800.
[9] DONG C F, XUE H B, LI X G, et al. Electrochemical corrosion behavior of hot-rolled steel under oxide scale in chloride solution[J]. Electrochemica Acta, 2009, 54(17): 4223-4228.
[10] COLLAZO A, N VOA X R, P
VOA X R, P REZ C, et al. EIS study of the rust converter effectiveness under different conditions[J]. Electrochemica Acta, 2008, 53(25): 7565-7574.
REZ C, et al. EIS study of the rust converter effectiveness under different conditions[J]. Electrochemica Acta, 2008, 53(25): 7565-7574.
[11] THEE C, HAO L, DONG J H, et al. Atmospheric corrosion monitoring of a weathering steel under an electrolyte film in cyclic wet-dry condition[J]. Corrosion Science, 2014, 78(1): 130-137.
[12] 张华民, 齐公台, 戴金彪, 等. 钢铁表面高温氧化铁皮对基体钢腐蚀的影响[J]. 材料保护, 1995, 28(6): 24-25.
ZHANG Huamin, QI Gongtai, DAI Jinbiao, et al. Effect of oxide scale on the corrosion of substrate steel[J]. Materials Protection, 1995, 28(6): 24-25.
[13] 何爱花, 孟洁, 王佳, 等. 表面氧化膜对B510L热轧钢板腐蚀行为的影响[J]. 中国腐蚀与防护学报, 2008, 28(4): 197-200.
HE Aihua, MENG Jie, WANG Jia, et al. Effect of surface oxide scale on corrosion behavior of B510L hot rolled steel[J]. Journal of Chinese Society for Corrosion and Protection, 2008, 28(4): 197-200.
[14] 孙彬, 何永权, 刘振宇. 氧化铁皮微观组织对热轧带钢耐候性能的影响[J]. 功能材料, 2016, 47(2): 2072-2077.
SUN Bin, HE Yongquan, LIU Zhenyu. Effect of microstructure of oxide scale on weathering-resistance of hot rolled steel[J]. Journal of Functional Materials, 2016, 47(2): 2072-2077.
[15] CHEN R, YUEN W Y D. Oxide-scale structures formed on commercial hot-rolled steel strip and their formation mechanisms[J]. Oxidation of Metals, 2001, 56(1/2): 89-118.
[16] CHEN R Y, YUEN W Y D. Review of the high-temperture oxidation of iron and carbon steels in air of oxygen[J]. Oxidation of Metals, 2003, 59(5/6): 433-468.
[17] FU X X, DONG J H, HAN E H, et al. A new experimental method for in situ corrosion monitoring under alternate wet-dry conditions[J]. Sensors, 2009, 9(12): 10400-10410.
[18] 王芸, 汤滢, 谢长生, 等. 电化学阻抗谱在材料研究中的应用[J]. 材料导报, 2011, 25(7): 5-9.
WANG Yun, TANG Ying, XIE Changsheng, et al. Application of electrochemical impedance spectroscopy in the study of materials[J]. Materials Review, 2011, 25(7): 5-9.
[19] BOSCH R W. Electrochemical impedance spectroscopy for the detection of stress corrosion cracks in aqueous corrosion systems at ambient and high temperature[J]. Corrosion Science, 2005, 47(1): 125.
[20] KELES H, EMIR D M, KELES M. A comparative study of the corrosion inhibition of low carbon steel in HCl solution by an imine compound and its cobalt complex[J]. Corrosion Science, 2015, 101: 19-31.
[21] VOURLIAS G, PISTOfiDIS N, CHRISSAfiS K. High-temperature oxidation of precipitation hardening steel[J]. Thermochimica Acta, 2008, 478(1/2): 28-33.
[22] 朱日彰. 金属腐蚀学[M]. 北京: 冶金工业出版社, 1989: 14.
ZHU Rizhang. Corrosion of metals[M]. Beijing: Metallurgical Industry Press, 1989: 14.
[23] ALQODAH Z, LAFI W K, ALANBER Z, et al. Adsorption of methylene blue by acid and heat treated diatomaceous silica[J]. Desalination, 2007, 217(1/2/3): 212-214.
[24] MARTINI E M A, MULLER I L. Characterization of the film formed on iron in borate solution by electrochemical impedance spectroscopy[J]. Corrosion Science, 2000, 42(3): 443-454.
[25] HAMADOU L, KADRI A, BENBRAHIM N. Characterization of passive films formed on low carbon steel in borate buffer solution (pH 9.2) by electrochemical impedance spectroscopy[J]. Applied Surface Science, 2005, 252(5): 1510-1519.
[26] CAO G M, LIU X J, SUN B, et al. Morphology of oxide scale and oxidation kinetics of low carbon steel[J]. Journal of Iron and Steel Research(International), 2014, 21(3): 335-341.
[27] CHEN R, YUEN W Y D. A study of the scale structure of hot-rolled steel strip by simulated coiling and cooling[J]. Oxidation of Metals, 2000, 53(5/6): 539-560.
(编辑 赵俊)
收稿日期:2017-01-29;修回日期:2017-03-22
基金项目(Foundation item):国家自然科学基金资助项目(51204047,U1660117);国家科技支撑计划项目(2011BAE13B04);中央高校基本科研业务费资助项目(N130407004)(Projects(51204047, U1660117) supported by the National Natural Science Foundation of China; Project (2011BAE13B04) supported by the National Science and Technology Pillar Program; Project(N130407004) supported by the Fundamental Research Funds for the Central Universities)
通信作者:曹光明,副教授,从事氧化铁皮控制技术研究;E-mail:caogm@ral.neu.edu.cn