DOI:10.19476/j.ysxb.1004.0609.2018.11.24
黄铁矿对硫砷铜矿化学浸出的促进作用
伍赠玲1, 2, 3
(1. 福州大学 紫金矿业学院,福州 350108;
2. 低品位难处理黄金资源综合利用国家重点实验室,厦门 361101;
3. 厦门紫金矿冶技术有限公司,厦门 361101)
摘 要:为了考查黄铁矿对硫砷铜矿浸出的影响,在添加黄铁矿、常压化学浸出条件下研究硫砷铜矿的浸出动力学和电化学。采用自制浸出装置在H2SO4 - Fe2(SO4)3 体系中开展混合矿物化学浸出实验。结果表明:添加黄铁矿后硫砷铜矿的表观活化能降低至48.15 kJ/mol;随着黄铁矿加入比例的升高,硫砷铜矿的浸出率逐渐提高,当硫砷铜矿与黄铁矿质量比为1:6时,12天硫砷铜矿的浸出率可达23.6%。通过XPS分析了混合矿物表面化学浸出前后硫和砷形态的变化,加入黄铁矿后促进砷转化为五价砷,降低毒性。电化学工作站测定硫砷铜矿的静止电位为0.48 V,无菌条件下的电化学行为解释了黄铁矿和硫砷铜矿混合化学浸出时形成原电池,促进了硫砷铜矿的溶解。
关键词:硫砷铜矿;黄铁矿;化学浸出;静电位;原电池效应
文章编号:1004-0609(2018)-11-2376-07 中图分类号:TF11;TF811 文献标志码:A
硫砷铜矿是一种典型的难处理硫化铜矿,其化学性质稳定,表观活化能较高[1-3]。硫砷铜矿既具有有价金属铜,又含有害元素砷,是影响生产的重要矿石[4]。众多科研工作者致力于提高硫砷铜矿的浸出,主要采取焙烧[5-7]、压力浸出[8]、生物浸出[9-11]措施以及利用原电池效应等[7-9, 11-13]。硫化矿的原电池效应在湿法冶金、矿山酸性废水污染治理等方面起着重要作用,受到广泛科研工作者的关注[14-19]。尤其是加入黄铁矿后,与静电位不同的硫化矿接触组成原电池,发生电化学腐蚀,静电位低的硫化矿充当阳极加剧氧化,促进硫化矿的溶解[17-19]。黄铁矿的静电位和表观活化能高[20],黄铁矿与砷黄铁矿质量比为10:2 时,可以促进砷黄铁矿的生物浸出,砷的浸出率比不加黄铁矿时提高了43.18%[17]。在黄铜矿中加入黄铁矿时,黄铁矿颗粒与黄铜矿颗粒间形成原电池,加速了作为阳极的黄铜矿的细菌氧化分解,黄铜矿的浸出率大大提高[19]。
在硫砷铜矿的电化学以及浸出原电池效应方面,始终存在着争议。硫砷铜矿与黄铁矿混合浸出体系中,一些观点认为混合浸出加速了硫砷铜矿的浸出[7-8, 13],而另一种观点则认为加速了黄铁矿的溶解[9, 11]。在硫砷铜矿和黄铁矿混合高温硫化焙烧后浸出的实验中发现铜的溶解比纯硫砷铜矿浸出要快[7]。在硫砷铜矿压力浸出条件下,添加黄铁矿促进硫砷铜矿的溶解,生成的三价铁是促进硫砷铜矿溶解的重要原因[8]。但是,一些报道称,在黄铁矿和硫砷铜矿混合矿生物浸出过程中黄铁矿先于硫砷铜矿浸出。CANALES等[9]研究生物连续氧化处理含黄铁矿和硫砷铜矿的金精矿时发现,浸出的主要对象是黄铁矿,硫砷铜矿变化不大。LEE等[11]研究辉铜矿、硫砷铜矿和黄铁矿3种不同类型的混合矿物浸出时发现,在硫砷铜矿的浸出渣表面出现了一些空洞,经检测是辉铜矿和黄铁矿浸出后产生的,认为在混合矿样中,辉铜矿和黄铁矿先于硫砷铜矿被分解浸出。目前有关硫砷铜矿原电池效应的研究中,大多数研究是在热压浸出、焙烧浸出或者生物浸出条件下进行的,且未测定硫砷铜矿的静止电位,未能为相关理论提供电化学依据。硫砷铜矿的电化学特性、硫砷铜矿和黄铁矿混合化学浸出中的原电池效应有待进一步研究。
本文作者针对现有研究的不足,采用自制动力学浸出装置在H2SO4-Fe2(SO4)3 体系中开展混合矿物常压化学浸出实验,考查了添加黄铁矿后对硫砷铜矿浸出的影响,并运用XPS等分析手段研究了混合矿物表面化学浸出前后性质的变化。通过硫砷铜矿的静止电位测定以及无菌条件下的电化学行为解释了黄铁矿促进硫砷铜矿浸出的原因。
1 实验
1.1 矿样制备
实验所用硫砷铜矿纯矿物标本采自福建某矿山,矿物经过破碎、镜下挑选、细磨、筛分、表面处理、真空干燥后得到纯矿物粉体并密封保存待用。矿物主要元素分析结果见表1,XRD分析结果见图1。
表1 硫砷铜矿样品元素分析
Table 1 Chemical composition of minerals (mass fraction, %)


图1 硫砷铜矿样品的XRD谱
Fig. 1 XRD pattern of enargite sample
1.2 化学浸出实验
化学浸出实验在自制实验装置中进行,装置如图2所示,将配置好的硫酸铁/硫酸亚铁等反应体系溶液置于反应釜内,开启电动搅拌机和高温恒温循环水浴锅,待温度达到设定值并稳定后按固液比(g/mL)1:100的比例加入实验样品,反应开始计时。实验过程中用双氧水和硫酸亚铁溶液调节氧化还原电位,微电脑控制器将视电位情况启动蠕动泵自动泵入调节液至反应体系中,直至体系电位达到实验设定值。到达指定取样时间,停止搅拌,静置2 min后快速移取上清液进行固液分离,分析检测浸出液Cu、Fe、As浓度。待反应结束时过滤矿浆,用蒸馏水反复清洗浸出渣,浸出渣置于45 ℃真空干燥箱内12 h,密封保存在抽气式厌氧罐中。
对硫砷铜矿纯矿物、硫砷铜矿与黄铁矿配比(质量比)为1:4时的化学浸出渣分别采用XPS(X射线扫描微探针电子能谱仪,Quantum 2000,Physical electronics 公司,美国)进行测试分析。

图2 化学浸出实验装置
Fig. 2 Experimental device of chemical leaching
1.3 电化学实验
循环伏安曲线的测定采用典型的三电极体系,工作电极为碳糊电极(Carbon Paste Electrode, CPE),参比电极为Ag/AgCl电极,辅助电极为碳对电极,参比电极和工作电极之间由盐桥连接。在1 L的普林斯顿腐蚀电解池中,运用Metrohm公司PGSTAT 302N 型电化学工作站进行测试,电解质为Fe3+浓度30.5 g/L、Fe2+浓度0.02 g/L、初始pH 1.0酸性溶液9K无铁培养基。
2 结果与分析
2.1 化学浸出动力学实验
在初始Fe3+浓度30.5 g/L、Fe2+浓度0.02 g/L、初始pH 1.0、搅拌速度200 r/min、不同温度(30、45、60 和75 ℃)实验条件下,对混合矿物(硫砷铜矿与黄铁矿配比为1:6)进行浸出动力学实验,浸出过程中溶液电位维持在(850±5) mV。不同温度下硫砷铜矿溶解动力学曲线如图3(a)所示。根据不同温度下得到的矿物浸出分数R,作1-(1-R)1/3(R为矿物浸出分数)与时间t的关系曲线,如图3(b)所示。计算不同温度下直线的斜率即k,再作lnk对1000/T(T为热力学温度)曲线,如图3(c)所示。
前期我们进行了硫砷铜矿浸出动力学实验,结果表明电位恒定在800 mV时,硫砷铜矿硫酸铁酸性化学浸出的表观活化能Ea=57.87 kJ/mol[1]。从图3可以看出,在恒定电位850 mV、加入黄铁矿浸出时,硫砷铜矿的浸出率随着温度的升高而提高;浸出12天时,75 ℃的硫砷铜矿浸出率升高至17.10%,比60 ℃的提高10.52%。由图3(b)可知,1-(1-R)1/3~t曲线呈现良好的线性关系,证明加入黄铁矿后高铁酸性浸出硫砷铜矿的过程仍然符合典型的缩核模型,速率受表面化学反应控制。从图3(c)可以看出,lnk与1000/T成线性比例关系。电位恒定在850 mV,添加黄铁矿后硫砷铜矿的表观活化能从57.87 kJ/mol[1]降低至48.15 kJ/mol,有利于硫砷铜矿的浸出。

图3 不同温度对混合矿中硫砷铜矿浸出的影响
Fig. 3 Effect of temperature on enargite dissolution
2.2 不同黄铁矿配比常压化学浸出实验
在初始Fe3+浓度30.5 g/L、Fe2+浓度0.02 g/L、初始pH 1.0、浸出温度60 ℃、搅拌速度200 r/min实验条件,浸出过程中溶液电位维持(850±5) mV。考查不同黄铁矿的添加量对硫砷铜矿浸出率的影响,实验结果如图4所示。从图4可以看出,硫砷铜矿纯矿物浸出12天时,浸出率为11.45%。随着配入黄铁矿比例的升高,硫砷铜矿的浸出率逐渐提高,当黄铁矿加入量为硫砷铜矿的6倍(质量比)时,硫砷铜矿浸出率快速升高,浸出12天时浸出率可达23.6%。

图4 不同黄铁矿配比对硫砷铜矿浸出率的影响
Fig. 4 Effect of different pyrite proportion on enargite dissolution
对硫砷铜矿纯矿物、混合矿(硫砷铜矿与黄铁矿配比为1:4)化学浸出渣分别进行XPS分析,浸出前后硫砷铜矿表面的XPS分析结果如图5和表2所示。分析结果表明,由于自旋轨道分裂,S 2p峰出现双峰 (S 2p3/2和S 2p1/2),S 2p3/2峰的强度为S 2p1/2的两倍(见图5(a)和5(b)),结合能高出1.19 eV(见表2)。此外,在164.0 eV时元素S与多硫化物重叠(见图5(a)和5(b))。浸出前后表面S物相存在差异:浸出前矿物表面未检测到亚硫酸盐,浸出后表面生成少量亚硫酸盐,硫酸盐增加。
从图5(c)和(d)可以看出,在As 3d峰中,As 3d5/2峰强度为As 3d3/2峰强度的1.5倍,其结合能比As 3d3/2的高出0.68 eV[10]。浸出前后表面As物相存在差异:浸出前矿物表面未检测到五价砷,浸出后五价砷比例升至10.02%,降低砷的毒性。
2.3 电化学实验
在无铁9 K培养基、42 ℃、无菌条件下,测定硫砷铜矿和黄铁矿纯矿物的静止电位,结果如表3所示。
从表3可知,在无铁9 K培养基,42 ℃无菌条件下测定黄铁矿和硫砷铜矿的静止电位分别为0.52 V、0.48 V,黄铁矿的静止电位高于硫砷铜矿。

图5 浸出前后矿物表面XPS分析图谱
Fig. 5 XPS analysis of mineral surface
表2 化学浸出渣表面结合能
Table 2 Binding energy of chemical leaching residue on surface

在电解质为灭菌的无铁9k培养液、pH = 1.5、温度42 ℃、扫描范围-0.6~1.2 V、扫描速度0.02 v/s实验条件下,对硫砷铜矿纯矿物、混合矿(硫砷铜矿与黄铁矿配比为1:6)制备的碳糊电极进行循环伏安曲线扫描,碳糊电极循环伏安曲线如图6所示。
表3 静止电位测定表
Table 3 Rest potential of enargite and pyrite

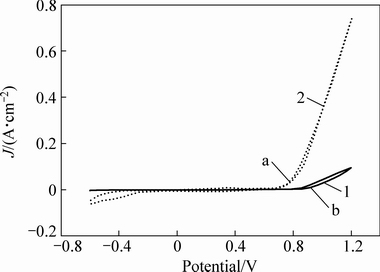
图6 循环安扫描曲线
Fig. 6 Circle voltammetry curves: 1―Enargite; 2―Enargite+ pyrite
图6结果可知,在硫砷铜矿中加入黄铁矿,循环福安曲线(曲线2)未出现明显的黄铁矿的氧化峰,证明在硫砷铜矿中加入黄铁矿进行扫描时,极化的仍为硫砷铜矿,而黄铁矿受到保护未被极化。对照图中两条曲线可知,加入黄铁矿后硫砷铜矿阳极氧化峰a明显高于不加黄铁矿矿物的氧化峰b,表明加入黄铁矿使硫砷铜矿的阳极氧化反应变得剧烈。硫砷铜矿与黄铁矿混合后,硫砷铜矿电流升高、氧化峰电位负移,表明在此酸性体系下黄铁矿的存在导致了硫砷铜矿氧化反应的加强,从而加速了硫砷铜矿的溶解。
在硫砷铜矿与黄铁矿混合浸出体系中,硫砷铜矿与黄铁矿颗粒混合接触时,形成一个原电池,硫砷铜矿充当阳极,促进了溶解,在其表面发生阳极反应(1),黄铁矿充当阴极,受到保护,在其表面发生阴极反应(2)。电化学实验结果验证了常压化学浸出体系加入黄铁矿后促进硫砷铜矿溶解的结果,并且解释了其发生的原因。
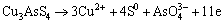 (1)
(1)
 (2)
(2)
3 结论
1) 电位恒定在850 mV时,添加黄铁矿后硫砷铜矿的表观活化能降低至48.15 kJ/mol,有利于硫砷铜矿的浸出。
2) 硫砷铜矿与黄铁矿混合常压化学浸出实验结果表明,随着黄铁矿加入比例的升高,硫砷铜矿的浸出率逐渐提高,当硫砷铜矿与黄铁矿质量比为1:6时,12天浸出率可达23.6%,远高于纯矿物的浸出率(11.45%)。浸出前后矿物表面XPS分析结果表明,浸出后表面生成少量亚硫酸盐,硫酸盐增加,五价砷比例升高,进一步验证了加入一定比例黄铁矿后促进硫砷铜矿的溶解。
3) 在无铁9 K培养基,42 ℃无菌条件下测定黄铁矿和硫砷铜矿的静止电位分别为0.52 V、0.48 V,黄铁矿的静止电位高于硫砷铜矿。
4) 硫砷铜矿与黄铁矿混合矿碳糊电极循环伏安曲线分析结果表明,添加黄铁矿后,与硫砷铜矿形成原电池,硫砷铜矿充当阳极,促进了溶解,而作为阴极的黄铁矿受到保护。
REFERENCES
[1] 伍赠玲, 吴 智, 朱永官. 硫砷铜矿化学浸出动力学研究[J]. 稀有金属, 2015, 39(8): 734-739.
WU Zeng-ling, WU Zhi, ZHU Yong-guan. Kinetics of enargite chemical leaching[J]. Chinese Journal of Rare Metals, 2015, 39(8): 734-739.
[2] LATTANZI P, DA PELO S, MUSU E, ATZE, D, ELSENER B, FANTAUZZI M, ROSSI A. Enargite oxidation: A review[J]. Earth Science Reviews, 2008, 86: 62-88.
[3] 范道焱, 庄荣传, 陈水波. 硫砷铜矿热压浸出研究现状及进展[J]. 黄金, 2016, 37(6): 64-67.
FAN Dao-yan, ZHUANG Rong-chuan, CHEN Shui-bo. Current situation and progress of the pressure oxidation of enargites[J]. Gold, 2016, 37(6): 64-67.
[4] 孔维长, 伍赠玲, 刘金艳. 硫砷铜矿浸出技术进展[J]. 有色金属(冶炼部分), 2014, 8: 14-17.
KONG Wei-zhang, WU Zeng-ling, LIU Jin-yan. Technical progress of enargite leaching technology[J]. Nonferrous Metals (Extractive Metallurgy), 2014, 8: 14-17.
[5] SAFARZADEH M S, MOATS M S, MILLER J D. Recent trends in the processing of enargite concentrates[J]. Mineral Processing and Extractive Metallurgy Review, 2014, 35(5): 283-367.
[6] SAFARZADEH M S, MOATS M S, MILLER J D. An update to “Recent trends in the processing of enargite concentrates”[J]. Mineral Processing and Extractive Metallurgy Review, 2014b, 35(5): 390-422.
[7] PADILLA R, ARACENA A, RUIZ M C. Reaction mechanism and kinetics of enargite oxidation at roasting temperatures[J]. Metallurgical and Materials Transactions B, 2012, 43B (5): 1119-1126.
[8] RUIZ M C, VERA M V, PADILLA R. Mechanism of enargite pressure leaching in the presence of pyrite[J]. Hydrometallurgy, 2011, 105: 290-295.
[9] CANALES C F, ACEVEDO J C. GENTINA. Laboratory-scale continuous bio-oxidation of a gold concentrate of high pyrite and enargite content[J]. Process Biochemistry, 2002, 37: 1051-1055.
[10] CORKHILL C L, WINCOTT P L, LLOYD J R, VAUGHAN D J. The oxidative Dissolution of arsenopyrite and enargite by Leptospirillum ferooxidans[J]. Geochimica et Cosmochimica Acta, 2008, 72: 5616-5633.
[11] LEE J, ACAR S, DOERR D L, BRIERLEY J A. Comparative bioleaching and mineralogy of composited sulfide ores containing enatgite, covellite and chalcocite by mesophilic and thermophilic microorganisms[J]. Hydrometallurgy, 2011, 105: 213-221.
[12] PLACKOWSKI C, HAMPTON M A, BRUCKARD W J, NGUYEN A V. An XPS investigation of surface species formed by electrochemically induced surface oxidation of enargite in the oxidative potential range[J]. Mineral Engineering, 2014, 55: 60-74.
[13] RIVERA-VASQUEZ B F, DIXON D. Rapid atmospheric leaching of enargite in ferric sulfate media[J]. Proceedings of the V International Copper Hydrometallurgy Workshop, Antofagasta, Chile, 2009: 194-204.
[14] GU Guo-hua, SUN Xiao-jun, HU Ke-ting, LI Jian-hua, QIU Guan-zhou. Electrochemical oxidation behavior of pyrite bioleaching by Acidthiobacillus ferrooxidans[J]. Transaction of Nonferrous Metals Society of China, 2012, 22(5): 1250-1254.
[15] LIU Hong-chang, XIA Jin-lan, NIE Zhen-yuan, MA Ya-long, MA Chen-yan, ZHENG Lei, HONG Cai-hao, ZHAO Yi-dong. Iron L-edge and sulfur K-edge XANES spectroscopy analysis of pyrite leached by Acidianus manzaensis[J]. Transaction of Nonferrous Metals Society of China, 2015, 25(7): 2407-2414.
[16] 马 骏, 汪菊香, 武 彪, 温建康, 尚 鹤, 武名麟. 晶体结构对黄铜矿、黄铁矿生物浸出差异性影响[J]. 中国有色金属学报, 2015, 25(10): 2898-2904.
MA Jun, WANG Ju-xiang, WU Biao, WEN Jian-kang, SHANG He, WU Ming-lin. Effects of crystal structure on differences of chalcopyrite and pyrite bioleaching[J]. The Chinese Journal of Nonferrous Metals, 2015,25(10): 2898-2904.
[17] 方 芳, 钟 宏, 江放明, 罗忠银, 孙晓伟, 许凯扬. 黄铁矿对砷黄铁矿生物浸出的影响[J]. 中国有色金属学报, 2013, 23(10): 2970-2976.
FANG Fang, ZHONG Hong, JIANG Fang-ming, LUO Zhong-yin, SUN Xiao-wei, XU Kai-yang. Effect of pyrite on bioleaching of arsenopyrite[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(10): 2970-2976.
[18] 刘 伟, 杨洪英, 佟琳琳, 刘媛媛. 活性炭对含钴矿物生物浸出的催化作用[J]. 中国有色金属学报, 2014, 14(4): 1050-1055.
LIU Wei, YANG Hong-ying, TONG Lin-lin, LIU Yuan-yuan. Catalytic effect of activated carbon on bioleaching of cobalt mineral[J]. The Chinese Journal of Nonferrous Metals, 2014, 14(4): 1050-1055.
[19] 李宏煦, 邱冠周, 胡岳华, 王淀佐. 原电池效应对混合硫化矿细菌浸出的影响[J]. 中国有色金属学报, 2003, 13(5): 1283-1287.
LI Hong-xu, QIU Guan-zhou, HU Yue-hua, WANG Dian-zuo. Galvanic effect on mixed sulfide bioleaching[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(5): 1283-1287.
[20] ZHONG Shui-ping. Leaching kinetics of gold bearing pyrite in H2SO4-Fe2(SO4)3 system[J]. Transactions of Nonferrous Metals Society of China, 2015, 25: 3461-3466.
Effect of pyrite on chemical leaching of enargite
WU Zeng-ling1, 2, 3
(1. College of Zijin Mining, Fuzhou University, Fuzhou 350108, China;
2. State Key Laboratory of Comprehensive Utilization of Low-Grade Refractory Gold Ores, Zijin Mining Group Co., Ltd., Xiamen 361101, China;
3. Xiamen Zijin Mining & Metallurgy Technology Co., Ltd., Xiamen 361101, China)
Abstract: In order to investigate the effect of pyrite on enargite leaching, the leaching kinetic and electrochemistry of enargite and pyrite mixture by chemical leaching under the condition of atmospheric pressure were studied. Leaching experiments of enargite and pyrite mixture in H2SO4-Fe2(SO4)3 system were investigated by leaching experimental device. The results show that the activation energy of enargite is decreased to 48.15 kJ/mol, while enargite leaching is increased by the addition of pyrite. Enargite leaching is increased dramatically up to 25% after 12 days with the proportion of enargite to pyrite equaled to 1:6. The morphological changes of sulfur and arsenic of mixture before and after leaching were demonstrated by XPS. Arsenic is promoted to transfer to pentavalent arsenic, which means less toxic. The rest potential of enargite is detected to 0.48 V by the electrochemical workstation. Electrochemical behavior explains the galvanic effect of chemical leaching of enargite and pyrite mixture, which promotes the dissolution of enargite.
Key words: enargite; galvanic effect; pyrite; rest potential; chemical leaching
Foundation item: Projects(51504071, 51474075) supported by the National Natural Science Foundation of China
Received date: 2017-08-24; Accepted date: 2018-01-12
Corresponding author: WU Zeng-ling; Tel: +86-592-7765281; E-mail: wu_zengling@zijinmining.com
(编辑 何学锋)
基金项目:国家自然科学基金资助项目(51504071,51474075)
收稿日期:2017-08-24;修订日期:2018-01-12
通信作者:伍赠玲,高级工程师,博士;电话:0592-7765281;E-mail:wu_zengling@zijinmining.com