��Ȼ�Ż������е�ǿ�����鼼��
��Դ�ڿ������ϴ�ѧѧ��(��Ȼ��ѧ��)2019���11��
�������ߣ������� ����� ������ ��ѧ�� ��ΰ ����� ����
����ҳ�룺2623 - 2633
�ؼ��ʣ��Ż�����As��III����ˮ��������е�
Key words��pyrrhotite; As(III); water treatment; mechanically activated
ժ Ҫ������Ȼ�Ż�����Ϊ���������о�As��III���ڴŻ���������������ת����Ϊ�����ڻ�е�ԭ��������������Ũ�Ⱥ����ˮ�������鼼�����о����������As��III�������ڴŻ�������棬�������S2-������������As2S3���������ͬʱ����������Ӧ��������As2S5��As2O3��As2O5�����溬����ּ���������һ���̶����谭�Ż���������Һ����Ľ�һ����Ӧ��ͨ���ԴŻ�������л�е�������һ���棬�ɼ�С�Ż��������ȡ�����ȱ��������һ���棬��¶���нϸ��Ե����ʱ��棬�������ߴŻ�����ij���Ч�ʣ���pHΪ3.0~3.5���¶�Ϊ80 �桢��Ӧʱ��Ϊ24 h���Ż������ʼ����Ũ��Ϊ12 g/Lʱ�����ȥ���ʴ���97%��
Abstract: Natural pyrrhotite was used as a purifying agent to study the adsorption and transformation behavior of As(III) on the surface of pyrrhotite. Based on the mechanical activation, the arsenic removal technology of acid wastewater with high mass concentration of arsenic was developed. The results show that As(III) adsorbs on the surface of pyrrhotite and reacts with surface S2- to form As2S3. The surface of the mineral is simultaneously oxidized to form a small amount of As2S5, As2O3 and As2O5. The presence of arsenic-containing components and elemental sulfur on the surface hinder the further reaction of pyrrhotite with arsenic in the solution to some extent. On the one hand, activated treatment of pyrrhotite by mechanical activation reduces the size of pyrrhotite and increases the specific surface area. On the other hand, it exposes the fresh surface with higher activity, and greatly improves the arsenic removal efficiency of pyrrhotite. The removal rate of arsenic is over 98% when pH is 3.0-3.5 and temperature is 80 ��, with reaction time being 24 h, and an initial dosage of pyrrhotite being 12 g/L.
DOI�� 10.11817/j.issn.1672-7207.2019.11.001
�����1, 2,������1, 2,��ѧ��1, 2,������1, 2,��ΰ1, 2,�����1, 2,����1, 2
��1. ���ϴ�ѧ ��Դ�ӹ������﹤��ѧԺ������ ��ɳ��410083��
2. ���ϴ�ѧ ս�Ժ��ƿ�����Դ����Ч���ú���ʡ�ص�ʵ���ң����� ��ɳ��410083��
ժҪ:����Ȼ�Ż�����Ϊ���������о�As��III���ڴŻ���������������ת����Ϊ�����ڻ�е�ԭ��������������Ũ�Ⱥ����ˮ�������鼼�����о����������As��III�������ڴŻ�������棬�������S2-������������As2S3���������ͬʱ����������Ӧ��������As2S5��As2O3��As2O5�����溬����ּ���������һ���̶����谭�Ż���������Һ����Ľ�һ����Ӧ��ͨ���ԴŻ�������л�е�������һ���棬�ɼ�С�Ż��������ȡ�����ȱ��������һ���棬��¶���нϸ��Ե����ʱ��棬�������ߴŻ�����ij���Ч�ʣ���pHΪ3.0~3.5���¶�Ϊ80 �桢��Ӧʱ��Ϊ24 h���Ż������ʼ����Ũ��Ϊ12 g/Lʱ�����ȥ���ʴ���97%��
�ؼ���:�Ż�����As��III����ˮ��������е�
��ͼ�����:TD923 ���ױ�־��:A ���±��:1672-7207��2019��11-2623-10
ZHANG��Xingfei1, 2, LIU��Shenmiao1, 2, CAO��Xuefeng1, 2, HAN��Haisheng1, 2,SUN��Wei1, 2, CHENG��Pengfei1, 2, WANG��Li1, 2
(1. School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China��
2. Key Laboratory of Hunan Province for Clean and Efficient Utilization of Strategic Calcium-containing Mineral Resources, Central South University, Changsha 410083, China)
Abstract: Natural pyrrhotite was used as a purifying agent to study the adsorption and transformation behavior of As(III) on the surface of pyrrhotite. Based on the mechanical activation, the arsenic removal technology of acid wastewater with high mass concentration of arsenic was developed. The results show that As(III) adsorbs on the surface of pyrrhotite and reacts with surface S2- to form As2S3. The surface of the mineral is simultaneously oxidized to form a small amount of As2S5, As2O3 and As2O5. The presence of arsenic-containing components and elemental sulfur on the surface hinder the further reaction of pyrrhotite with arsenic in the solution to some extent. On the one hand, activated treatment of pyrrhotite by mechanical activation reduces the size of pyrrhotite and increases the specific surface area. On the other hand, it exposes the fresh surface with higher activity, and greatly improves the arsenic removal efficiency of pyrrhotite. The removal rate of arsenic is over 98% when pH is 3.0-3.5 and temperature is 80 ��, with reaction time being 24 h, and an initial dosage of pyrrhotite being 12 g/L.
Key words: pyrrhotite; As(III); water treatment; mechanically activated
��(As)��һ���ж��ǽ���Ԫ�أ�����Ȼ������Ҫ���������ʽ���ڣ��ڻ�ԭ�����£��������ת�����ˮ�У�����Ǩ�ƺ�����ʹ����ˮ�е��麬�����ӣ��������ý�������Ӱ���˵����Ľ���[1]������ɫұ����ҵ�������У����������������Ũ�ȵ�ǿ���Ժ����ˮ�������������Ŀɳ�����չ��������Σ�����������о��߶Ժ����ˮ�Ĵ��������˴����о������ڵ�����Ũ�Ⱥ����ˮ���������Ǵ��������ˮ��õķ���֮һ[2]�����������ױ����˲�ͬ��������(��Ҫ������(��)������[3]�������[4]������[5-6])������������ü��������������Ȼ����ͺϳ���������������Ϊ�о����ȵ�֮һ[7-9]������20����70���������������������Һ�е��ؽ��������н�ǿ������������������ˮ��Һ�е��ؽ�������[10]�ͺ����ˮ[11]��KATSOYIANNIS��[9, 12]�ֱ��о��˻��������������Լ���Ȼ�������FeS(����ŵ��)��������������õ��˸������As(III)��As(V)����������ϵ�������ַ���ϵ���IJ�����ɻ��������������ͬ��ɵġ�ʷ�ǵ�[14]�����������������Ȼ������ʹ��ת��Ϊ�Ż����������������պ�Ļ������As(III)��As(V)��ȥ������������ǰ��ȥ��Ч��������б�Ż������As(III)��As(V)����������ܡ�����[15]�о�����Ȼ�Ż������ˮ�е�����Ũ��As(V)��ȥ�������ִŻ������As(V)��ȥ���ʴﵽ��99%����������������֮��ϳ�ʱ����δ������ͷţ������Ż�������Ϊ�������������й�����Ӧ��ǰ����Ȼ������ɫѡұ��ˮ��ͬ�ڴ�ͳ�ĵ�����Ũ���ؽ�����ˮ����������Ũ�������ߴ�1 g/L���������Խ�ǿ����ͳ�����������Խ��������Ũ����ľ������������еĴ��������������ȱ�㣬�����������Ϊ���صĻ������⡣�Ż��������Һ����ѧ�Ͷ���ѧ�о���������ǿ���������¿ɻ����ֽ⣬���ͷ�S2-����ΪAs(III)��������������������ˣ��Ż���������ǿ���Ը�����Ũ�Ⱥ����ˮ�ľ�������һ�������ԡ����������ڴŻ�������ܽ���Ϊ�����As(III)�������������ܣ��о���Ȼ�Ż�����������Ũ�Ⱥ�As(III)��ˮ������ѧ��Ϊ�Ͷ���ѧ��Ϊ����������ۻ���Ϊ��ͨ����е���ǿ�Ż����������ԣ�����龻��Ч�ʣ��Ա�Ϊ������Ũ�Ⱥ����ˮ�ĸ�Ч�����ṩ�ο���
1 ʵ������뷽��
1.1��ʵ�����
ʵ�����ôŻ���������ͭ�����ؿ��Ʒ��������˾�������ѡ���������������С��0.5 mm���پ�����ѡ���õ��ϸߴ��ȵĴŻ�����ֿ�������С��ֿ����Ż�����С���ʽ���������������С��0.2 mm��������ĥĥ������С��0.074 mm��ʵ�����ôŻ�����������С��0.074 mm��
ʵ��������������(NaAsO2)���Ժ���ʡ��ɳ�з�ԣ����������������˾����������Co2+��Cu2+���������ӡ�ʵ�����ú�����Һ��Ϊ����ȥ����ˮ���Ƶ�2 g/L����������Һ��
1.2��ʵ�鷽��
1.2.1����Ȼ�Ż��������ľ���ʵ�顡
�ԴŻ�����Ϊ�о����ԴŻ�����ȥ����Һ��As(III)���е�����ʵ�飬̽���¶ȡ�pH����Ӧʱ��ȶԴŻ�����As(III)�Ķ���ѧ������ѧ���̵�Ӱ�졣
����һ������Ũ�ȵ�As(III)��Һ������ʵ��������������Ũ�ȣ���ȡ200 mL As(III)��Һ�����뵽500 mL���ձ��У���1 mol/L��H2SO4��NaOH��Һ����pH���趨ֵ�������ں��´���������У�����һ�����ĴŻ������ý�������һ�����ٶȽ��跴Ӧ�����һ��ʱ��ȡ�����˼�⡣
1.2.2����е��ĴŻ�������������ʵ�顡
Ϊ��һ����ߴŻ����������Ч�ʣ����û�е��ԴŻ��������Ԥ���������ó�ɳ�촴��ĩ��������˾������ʵ�����ĥ�ԴŻ�������и�����ĥ��ȡ��ĥ����Ʒ���뵽���ڲ�����ƿ�У�ˮԡ������80 ����з�Ӧ���ý�������500~600 r/min���ٶȽ��裬����Һ��ȴ����й��˼�⡣
1.3�����������
�����ձ����ӹ�˾��JSM-649CLVɨ���������(SEM)������EDAX��˾��EDS-WDS���ײ����ǶԷ�Ӧ��ĴŻ��������������ò���б����������仯ѧ��ɡ���������ThermoFisher Scientific��˾��ESCALAB250Xi X�߹����������(XPS)�Է�Ӧ��ĴŻ���������Ԫ�سɷֽ��з�����ʹ�õ¹���³�˹�˾S4 Pioneer X��ӫ������Ǻ͵¹�˹�ɿ˷���������˾SPECTRO BLUE SOP�����ӹ����Ƿֱ��������Һ�е�����������������Ӣ�������Ĺ�˾��Mastersizer 2000�������ȷ����Ǻ�����������˾��Quadresorb SI�ȱ���������Ƿ�����е���ĴŻ�������������Ⱥͱȱ������
2 ���������
2.1���Ż�������������ѧ�о�
ͼ1��ʾΪ�¶�Ϊ25 ��ʱAs-O2-H2O��ϵEh-pHͼ[16]��������ԭ��λEh��pH��Ӱ����Һ����������͵���Ҫ�����������������͵�pH�£�H2AsO4-ռ��������λ������pH������HAsO42-��AsO43-����Һ�е����������ࡣ�ڻ�ԭ�����£���pHС��9.2ʱ����Һ�е�As��Ҫ��H3AsO3����ʽ���ڡ���Һ�е�As(III)�����pH�ı仯��ͼ1(����pE=-lg



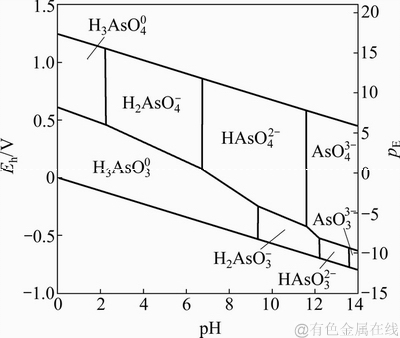
ͼ1��25 ��ʱAs-O2-H2O��ϵEh-pHͼ[16]
Fig. 1��Eh-pH diagram for aqueous As in system of As-O2-H2O at 25 ��[16]
ͼ2��ʾΪ�Ż�������ˮ��ϵ�е�Eh-pHͼ[18]����ͼ2���Կ����������������£��Ż������е�S2-���ױ�����Ϊ���ʺ���������ӣ���������������������ʽ���ڣ�����pH���������������Һ�е�OH-�γ�Fe(OH)3���������Ի�ԭ�������£��Ż�������ɷֽ����������S2-��������Һ�У������As(III)��ȥ��������ġ�
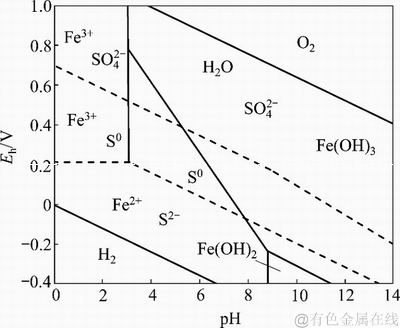
ͼ2���Ż�������ˮ��ϵ�е�Eh-pHͼ[18]
Fig. 2��Eh-pH diagram for aqueous pyrrhotite in system of Fe1-xS-H2O at 25 ��[18]
��1��ʾΪ��As(III)ʱ�Ļ�ѧ��Ӧ�������¶�Ϊ25 ��ʱ��ƽ�ⳣ�����ӱ�1���Կ�������������������Ҫ������As2S3�����Դﵽȥ���������Ŀ�ģ�����pH���ߣ���Һ�е�������̬�����ı䣬��ʱ��Ҫͨ���Ż����������ǻ���������������ȥ�����ӡ�
��1����As(III)ʱ�Ļ�ѧ��Ӧ�������¶�Ϊ25 ��ʱ��ƽ�ⳣ��
Table 1��Equilibrium constants and chemical reactions in process of As(III) removal (25 ��)

��Ԫ���[23]����Eh-pHͼ��������As(III)ʱ�ķ�Ӧ���̴��·�Ϊ3�ࣺ
H3AsO3+2FeS+4H+ = HAsS2+2Fe2++3H2O��
pH<3.8 (1)
3FeS +H3AsO3+8H+ = As2S3��+3Fe2++6H2O��
3.8

H2AsO3-+2FeS+H2O = AsS2-+2Fe(OH)2��
pH>6.6 (3)
�Ż�����ijɷ���FeS���ƣ���ˣ��ڳ�������е���Ҫ����ΪAs2S3���䷴Ӧ���̴��·��������ķ�Ӧ���̣�����ǿ������Һ�У��Ż��������ͷų��IJ���S2-����Һ�е�H+��Ӧ������������H2S����ֱ�Ӳ�����Һ�еķ�Ӧ������As2S3��������Ӧ����ʽ���£�
S2-+2H+=H2S�� (4)
2H3AsO3+3H2S = As2S3��+6H2O (5)
ͨ�����Ϸ������Կ������ڻ�ԭ�������������������ôŻ���������Һ�е�As(III)������ѧ�Ͽ��еġ�
2.2���Ż��������鶯��ѧ�о�
2.2.1��pH�ԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ�졡
��ͬpH�ԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ����ͼ3��ʾ(��ʼAs(III)����Ũ��Ϊ2 g/L���Ż���������Ũ��Ϊ10 g/L���¶�Ϊ25 �棬��Ӧʱ��Ϊ4 h)����ͼ3��֪��pH�ԴŻ�����ȥ����Һ��As(III)���нϴ�Ӱ�죬����pH������Һ��As(III)��ȥ������������С����pHΪ3.0~3.5ʱ��As(III)��ȥ���ʴﵽ���ֵ24.8%�����������������ﵽ4.98%���Ż������������pHԼΪ3.2������ʽ(1)��(3)��֪������ҺpH����ʱ����Һ�е�As(III)��Ҫ��H3AsO3����ʽ���ڣ�����ζ����ȥ����Ҫ�ԴŻ���������������ʽΪ��������pH���Ż�������淢����Ӧ����As2S3��������ȥ������������pH��������ʱ����Һ��OH-�������࣬����������ľ�����ҪԴ����Fe(OH)2��Fe(OH)3�����������������ˣ���pH�ϵͻ�ϸ�ʱ��As(III)��ȥ���ʶ��ϵ͡�
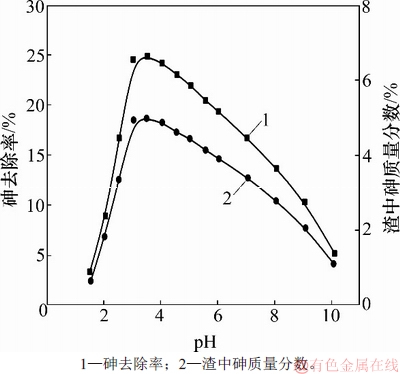
ͼ3��pH�ԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ��
Fig. 3��Effect of pH on removal efficiency of As(III) from pyrrhotite
2.2.2���¶ȶԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ�졡
ͼ4��ʾΪ�¶ȶԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ��(��ʼAs(III)����Ũ��Ϊ2 g/L���Ż���������Ũ��Ϊ10 g/L��pH=3.0����Ӧʱ��Ϊ4 h)����ͼ4���Կ���������¶ȶԴŻ�����ȥ����Һ��As(III)ȥ�����������Ĵٽ����ã������¶ȵ����ߣ�As(III)ȥ���ʴ�25%��ߵ�53%���ң�������Ϊ�Ż�����ķֽ������ȷ�Ӧ�������¶������ڷֽ�ʹ���������鷴Ӧ�������¶ȵIJ������ߣ���Һ��As(III)ȥ���������ߣ����¶�������������ߴŻ�����ľ���Ч�ʣ�����ѡ��Ӧ�¶�Ϊ80~85 �档
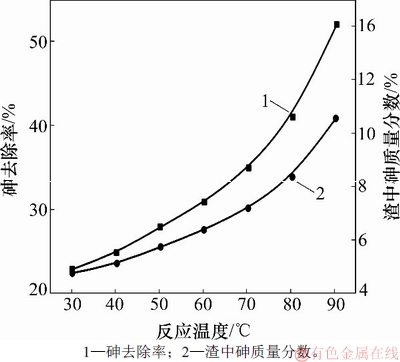
ͼ4���¶ȶԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ��
Fig. 4��Effect of temperature on removal efficiency of As(III) from pyrrhotite
2.2.3����Ӧʱ��ԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ�졡
ͼ5��ʾΪ��Ӧʱ��ԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ��(��ʼAs(III)����Ũ��Ϊ2 g/L���Ż���������Ũ��Ϊ10 g/L��pH=3.0���¶�Ϊ80 ��)����ͼ5���Կ��������ŷ�Ӧʱ����ӳ�����Һ��As(III)ȥ���������ߣ������ߵ�������С���ڷ�Ӧ24 h��As(III)ȥ�������ӻ��������ȶ����������ӷ�Ӧʱ�����As(III)ȥ����Ӱ�첻����ˣ�ʵ��������ݶ���Ӧʱ��Ϊ24 h���Ż����������ʱ��Ҳ��Ӱ��Ż�����ȥ����Һ��As(III)ȥ���ʵ���ҪӰ�����أ�����ﵽһ��ʱ�䣬�����ôŻ������ַֽ⣬�ͷų�S2-�� As(III)��ַ�Ӧ����ߴŻ�����������ʺ�As(III)��ȥ���ʡ�
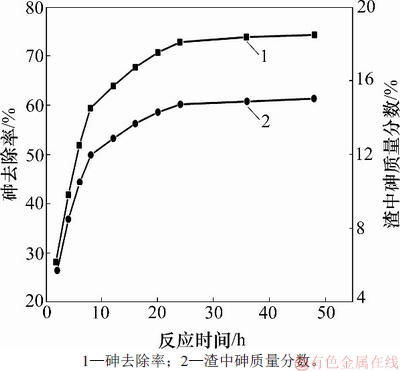
ͼ5����Ӧʱ��ԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ��
Fig. 5��Effect of reacting time on removal efficiency of As(III) from pyrrhotite
2.2.4���Ż���������Ũ�ȶ�ȥ����Һ��As(III)ȥ���ʵ�Ӱ�졡
ͼ6��ʾΪ�Ż���������Ũ�ȶ�ȥ����Һ��As(III)ȥ���ʵ�Ӱ��(��ʼAs(III)����Ũ��Ϊ2 g/L����Ӧʱ��Ϊ24 h��pH=3.0���¶�Ϊ80 ��)����ͼ6���Կ��������ŴŻ���������Ũ�ȵ����ӣ���Һ��As(III)ȥ��Ч��������ǿ�����Ż���������Ũ��Ϊ6 g/Lʱ��As(III)ȥ���ʽ�Ϊ29.2%�����������������ﵽ8.65%�����Ż���������Ũ��Ϊ12 g/Lʱ��As(III)ȥ���ʴﵽ71.1%�������ӴŻ���������Ũ�ȣ�As(III)ȥ�������������������������������������ͣ�˵���Ż����������Ч�����Կ�ʼ���ͣ��ۺϿ���ѡ��12 g/L��Ϊ�Ż������������Ũ�ȡ�
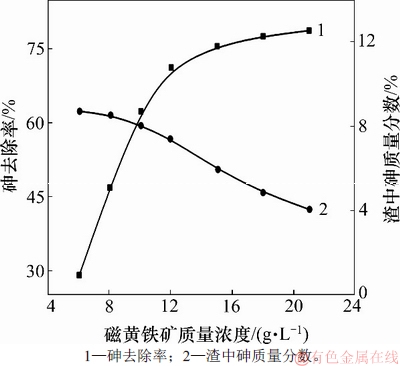
ͼ6���Ż���������Ũ�ȶ�ȥ����Һ��As(III)ȥ���ʵ�Ӱ��
Fig. 6��Effect of pyrrhotite mass concentration on removal efficiency of As(III) in solution
�����о�����������Ż���������������ѧ���ǿ��еģ�pH���¶ȡ���Ӧʱ�����Ӱ���䶯��ѧ���̵���Ҫ���ء����ۼ�������Ż��������ʵ�������Ⱦ�����Ȼ��ʵ�����������룬�����Ż������ڳ�������б��淢�����ع���������ۻ����Ӷ�Ӱ���˺�����Ӧ��Ϊ�˷����Ż������뺬As(III)��Һ���¶Ⱥ�ʱ��Ӱ�췴Ӧǰ���������ò�ı仯�����뺬As(III)��Һ��Ӧǰ��ĴŻ��������ɨ��羵��EDS�������۲�Ż�����������ò�仯�������ͼ7��ʾ(As(III)����Ũ��Ϊ2 g/L��pH=3.5����Ӧʱ��Ϊ20 h���Ż���������Ũ��Ϊ12 g/L)��
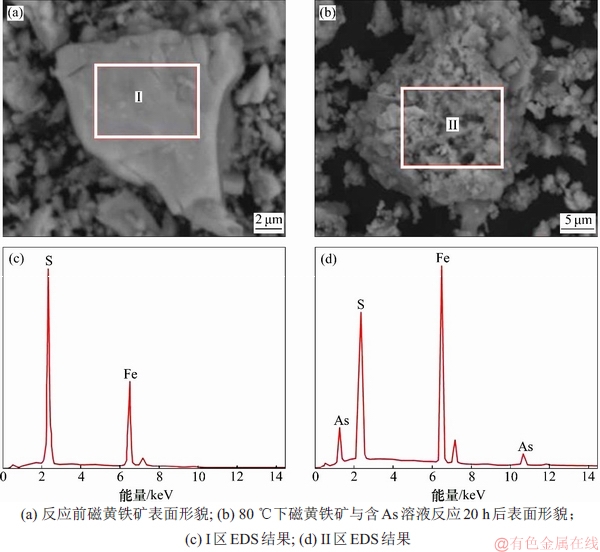
ͼ7���Ż������뺬As��Һ��Ӧǰ�����SEM��EDS����ͼ
Fig. 7��SEM and EDS spectra of pyrrhotite before and after reaction with As solution
��ͼ7(a)��֪����Ӧǰ�Ż�����������������ʣ��ȽϹ⻬����������û�����ʸ��š���ͼ7(b)���Կ������Ż�������80 ���������뺬As(III)��Һ��Ӧ��ԭ���⻬�ı�����80 ���������д���������ҳ���״����״�������ڴŻ�����ı��档��ͼ7(c)��(d)��֪���Ż������뺬As(III)��Һ��Ӧǰ��FeԪ�غ�SԪ�ص������������������û�����Եı仯������Ӧ����������AsԪ�ص������壬��80 ��������³�����2��AsԪ�ص������壬AsԪ����������Ϊ13.31%���ɼ���80 �������£��Ż�������渽�ŵĺ������ʽ϶࣬�Ż���������Һ�е�As(III)��Ӧ�̶Ƚϴ�ͨ��SEM��EDS������������ȷ��As(III)���Ժ���������ʽ�����ڴŻ�������棬���ǿ��Գ��˵��As(III)��Ż�������淢�������ã�������һ��ϸ�������ʸ����ڴŻ�������档
2.3��XPS����
Ϊ�˷����Ż������뺬����Һ��Ӧ�������Է�Ӧǰ�Ż�����ͷ�Ӧ�������������X�߹������������ͼ8��ʾΪ�Ż������뺬����Һ��Ӧ��As 3d�ַ����ͼ��ͼ8�г����˽���ֱܷ�Ϊ43.56��44.30��44.91��45.64 eV��4����ͬ�ķ�ֵ���ֱ��������������[24]�����������[25]��������������[26]�Լ������������[27]���γɡ��ɴ˿ɼ����ڴŻ������뺬��������Һ��Ӧ�Ĺ�����������As2S3��������һ���������鱻�����γ�������飬���ԣ���Ӧ���γ���As2S5��As2S3��As2O3��As2O5�����ɱ�������������������������Ҳ����Ϊ����������As2S3��As2S5�������γɡ�
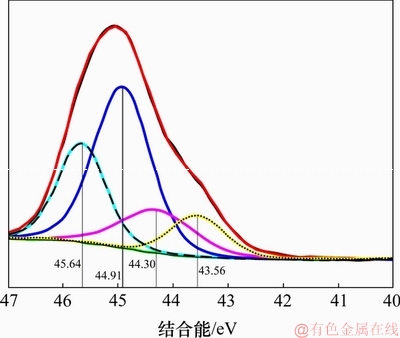
ͼ8���Ż������뺬����Һ��Ӧ��As 3d�ַ����ͼ
Fig. 8��XPS-peak-differentiation-imitating analysis of As 3d after reaction of pyrrhotite with arsenic-containing solution
Ϊ�˷�����Һ��As(III)��Ż�����Ӧ���SԪ�ص�������̬���ԴŻ������뺬����Һ��Ӧ�� S 2p�ַ���ϣ���ͼ9��ʾ��ͼ9�г�����7����ͬ�ķ�ֵ����Ӧ�Ľ���ֱܷ�Ϊ161.05��161.49��162.07��162.61��163.33��163.71��164.91 eV�������Ϊ161.05��161.49��162.07��162.61 eV�ķ�ֵ�ֱ��Ӧ������Ȼ�Ż�������������еĴŻ�����������[28]����п��[29]�ͻ�����[28]��������ܷ�ֵ163.33��164.91 eV�ij��֣������Ż������뺬����Һ���̵ķ�Ӧ�в����������������As2S3������������As2S5[30]������ܷ�ֵ163.71 eV�ij��֣������ڷ�Ӧ�����г����˵�����[31]����������S2-��һ���������
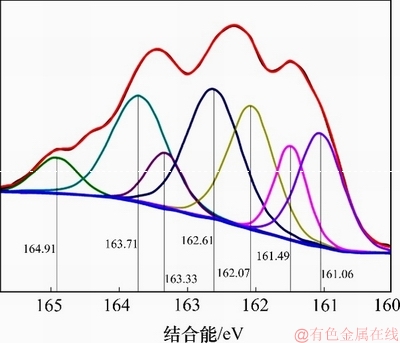
ͼ9���Ż������뺬����Һ��Ӧ��S 2p�ַ����ͼ
Fig. 9��XPS-peak-differentiation-imitating analysis of S 2p after reaction of pyrrhotite with arsenic-containing solution
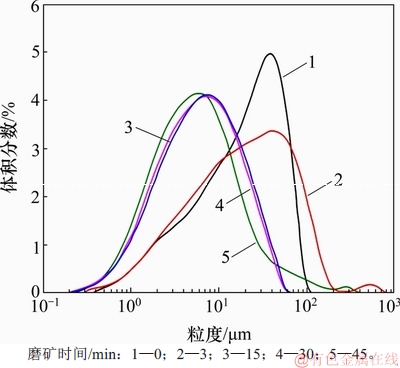
ͼ10����ͬĥ��ʱ���´Ż��������ȷֲ�ͼ
Fig. 10��Particle size distribution of pyrrhotite in different grinding time
XPS�ķ�������������Ż��������뺬����Һ��Ӧ�Ĺ����У��Ż��������Ҫ�ɷ�FeS�����˽��룬������S2-����ΪAs2S3���ܶȻ���FeS���ܶȻ��ͼ��������������ԣ�һ����S2-���������ϣ��γ�As2S3������һ����S2-����������γ���As2S5���������γɵ���Դһ����������һ����S2-����Һ�������γɣ���һ��������ԭ�Ż��������������������е������������ɣ����ָ��ڴŻ�����ı��棬��һ���̶����谭�˴Ż���������Һ����Ľ�һ����Ӧ��
2.4�����ڻ�е��ĴŻ�����ǿ�����鼼���о�
�����о��������Ż�����������Ũ�Ⱥ������Է�ˮ����һ�������ԣ�������Ч���ܴŻ�������������Լ���Ӧ�����е��ָǶۻ�Ӱ��ϴ���ˣ������ߴŻ�����Ӧ���ԣ�ͬʱ������Ӧ�����е��ָ���Ϊ����Ϊ�Ż���������Ĺؼ�����ʪ��ұ����һ����û�е�ǿ����������е���ͨ������е��������ʹ���������ϸ������ȱ�����ӣ���Ӧ������ǿ�Ӷ�ʹ�������нϴ������[32]��Ϊ�˽�һ�����ӴŻ�����������ʣ���ߴŻ�����ķ�Ӧ���ԣ�������С��0.074 mm�ĴŻ���������ý���ĥ��һ��ʪĥ����С���ȣ�����������ԣ������ø�ǿ�Ƚ�������Ӧ�����е��ָ����⣬Ϊ������Ũ����ľ����������õ�������
2.4.1���Ż������������ȱ������ĥ��ʱ��Ĺ�ϵ
ͼ10��ʾΪ��ͬĥ��ʱ���´Ż�����������ȷֲ�ͼ����ͼ10��֪��������ĥĥ��3 minʱ��15~80 ��m�����ĴŻ�������������������٣�2~10 ��m�����Ż����������������������ĥĥ��15 min�Ż��������ȷֲ����ӽ���̬�ֲ�N(�̣���2)������̬�ֲ��ľ�ֵ�̱�ĥ��3 minʱ�Ħ̴���ȼ�С��ĥ��30 min��45 min���Ż��������ȷֲ���δ���������仯�����Կ���ĥ��15 min������ĥ���ʱ�䣬�Ż���������������ᷢ�����Ա仯������������ڴŻ��������������С��һ���̶Ⱥ�㿪ʼ�����žۡ�
����ĥ��ԴŻ�����������Ȳ����ϴ�Ӱ�죬��ȻҲ�ԴŻ���������ȱ���������ϴ��Ӱ�졣ͼ11��ʾΪ�Ż���������ȱ������ĥ��ʱ��Ĺ�ϵ����ͼ11���Կ�������ĥ��3 minʱ���Ż���������ȱ������0.867 m2/g���ӵ�0.919 m2/g��ֻ��С�������ӣ���ĥ��15 min�ȱ�������ӵ�1.780 m2/g���Ż�����ȱ���������˽�1������ĥ��30 min��45 min�Ż�����ȱ�������ĥ��15 minʱֻ��С�������ӣ��ɴ˿ɼ�ĥ��15 min�Ժ�ʹĥ��ʱ���������ӣ��Ż�����ȱ����Ҳ�����������ӡ�
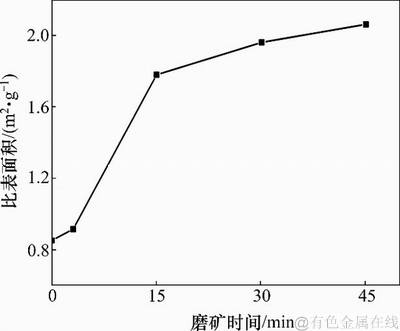
ͼ11��ĥ��ʱ��ԴŻ���������ȱ������Ӱ��
Fig. 11��Effect of grinding time on specific surface area of pyrrhotite particles
2.4.2����е��Ż������ȥ����Һ��As(III)ȥ���ʵ�Ӱ�졡
ͼ12��ʾΪ��ͬĥ��ʱ��ԴŻ�����ȥ����Һ��As(III)ȥ���ʵ�Ӱ��(As(III)����Ũ��Ϊ2 g/L��pH=3.0����Ӧʱ��Ϊ24 h���Ż���������Ũ��Ϊ12 g/L����Ӧ�¶�Ϊ80 ��)����ͼ12�ɼ������ŴŻ�����ĥ��ʱ�����ӣ���Һ��As(III)��ȥ���������ӣ���ĥ��3 minʱ������ĥ��ʱ������ӣ�As(III)��ȥ���ʴ�δĥ��ʱ��69%������75%����ĥ��15 minʱ������ĥ��ʱ������ӣ�As(III)��ȥ���ʼ���������As(III)��ȥ���ʴ�75%���ӵ�97%����ĥ��30 min��45 minʱ��As(III)��ȥ�������ĥ��15 minʱ�ֱ�����1.4%��2.2%���ɴ˿ɼ���ĥ��15 min���ڣ�����ĥ��ʱ�����ӣ�As(III)��ȥ�����������ӣ�ĥ��15 min�Ժ����ӴŻ�����ĥ��ʱ���As(III)��ȥ����Ӱ�첻��
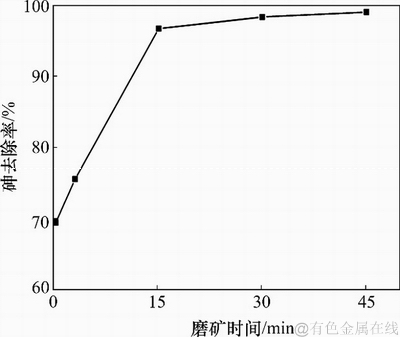
ͼ12��ĥ��ʱ��Ի�е��ĴŻ�����ȥ����Һ��As(III)��Ч�ʵ�Ӱ��
Fig. 12��Effect of grinding time on As(III) removal efficiency in mechanically activated pyrrhotite solution
��ʵ������֪����δ������ĥĥ��֮ǰ���Ż��������������е������ã�����������Ӧ��������S����������ָ��ڴŻ�����������棬�谭�˴Ż���������Һ��As(III)�ķ�Ӧ����е�ʹ�ôŻ����������������ƻ�����¶�˿����ڲ����ʱ��棬��ǿ�˴Ż���������Һ��As(III)��������������ȥ���ʵõ��ϴ���ߡ�
3 ����
1) �Ż������������������£�pHΪ3.0~3.5���¶�Ϊ85 �棬��Ӧʱ��Ϊ24 h��
2) As(III)�����ڴŻ�������棬�������S2-������������As2S3�����溬����ּ�������Ĵ�����һ���̶����谭�˴Ż���������Һ����Ľ�һ����Ӧ��
3) ���ڻ�е�ԭ������ʹ�ý���ĥĥ�����������˴Ż�����ȱ��������¶�����ʱ��棬�Ӷ��Ż��˴Ż�����ij���Ч�ʡ���ĥ��ʱ��Ϊ15 minʱ�����ȥ���ʴ���97%��
�ο����ף�
[1] ����, �彨��, ������, ��. �й���ˮ�����ж�����ˮ��ѧ���������ж���ϵ[J]. ��̬����ѧ��, 2013, 8(2): 222-229.
TANG Jie, BIAN Jianming, LI Zhaoyang, et al. Relationship between hydrochemical environment and arsenism in areas with arsenic poisoning drinking water in China[J]. Asian Journal of Ecotoxicology, 2013, 8(2): 222-229.
[2] VAISHYA R C, GUPTA S K. Modelling arsenic(III) adsorption from water by sulfate-modified iron oxide-coated sand (SMIOCS)[J]. Journal of Chemical Technology and Biotechnology, 2003, 78(1): 73-80.
[3] KIM E J, BATCHELOR B. Macroscopic and X-ray photoelectron spectroscopic investigation of interactions of arsenic with synthesized pyrite[J]. Environmental Science & Technology, 2009, 43(8): 2899-2904.
[4] MAMINDY-PAJANY Y, HUREL C, MARMIER N, et al. Arsenic(V) adsorption from aqueous solution onto goethite, hematite, magnetite and zero-valent iron: Effects of pH, concentration and reversibility[J]. Desalination, 2011, 281: 93-99.
[5] LI Yiran, WANG Jun, ZHAO Ying, et al. Research on magnetic seeding flocculation for arsenic removal by superconducting magnetic separation[J]. Separation and Purification Technology, 2010, 73(2): 264-270.
[6] TAVARES D S, LOPES C B, COELHO J P, et al. Removal of arsenic from aqueous solutions by sorption onto sewage sludge-based sorbent[J]. Water, Air, & Soil Pollution, 2012, 223(5): 2311-2321.
[7] KATSOYIANNIS I A, ZOUBOULIS A I. Removal of arsenic from contaminated water sources by sorption onto iron-oxide-coated polymeric materials[J]. Water Research, 2002, 36(20): 5141-5155.
[8] HAN Jingtai, FYFE W S. Arsenic removal from water by iron-sulphide minerals[J]. Chinese Science Bulletin, 2000, 45(15): 1430-1434.
[9] FARQUHAR M L, CHARNOCK J M, LIVENS F R, et al. Mechanisms of arsenic uptake from aqueous solution by interaction with goethite, lepidocrocite, mackinawite, and pyrite: an X-ray absorption spectroscopy study[J]. Environmental Science & Technology, 2002, 36(8): 1757-1762.
[10] BOSTICK B C, FENDORF S. Arsenite sorption on troilite (FeS) and pyrite (FeS2)[J]. Geochimica et Cosmochimica Acta, 2003, 67(5): 909-921.
[11] BLANCHARD M, ALFREDSSON M, BRODHOLT J, et al. Arsenic incorporation into FeS2 pyrite and its influence on dissolution: a DFT study[J]. Geochimica et Cosmochimica Acta, 2007, 71(3): 624-630.
[12] KATSOYIANNIS I A, ZOUBOULIS A I. Removal of arsenic from contaminated water sources by sorption onto iron-oxide-coated polymeric materials[J]. Water Research, 2002, 36(20): 5141-5155.
[13] ʷ�ǵ�. ���ջ�����ṹ�ݻ����侻��ˮ��������úͻ���[D]. �Ϸ�: �Ϸʹ�ҵ��ѧ��Դ�뻷������ѧԺ, 2015: 65-71.
SHI Yadan. The structure evolution of heat-treated pyrite and its performance and mechanism for arsenic removal from groundwater[D]. Hefei: Hefei University of Technology. School of Resources and Environment Engineering, 2015: 65-71.
[14] ��, ��С÷, Ф����, ��. ������Ȼ�Ż�����ȥ��ˮ��As(V)���о�[J]. ������ѧѧ��, 2016, 36(10): 3701-3708.
LIU Zhuo, ZHANG Xiaomei, XIAO Cailin, et al. As(V) Removal from water with natural pyrrhotite[J]. Acta Scientiae Circumstantiae, 2016, 36(10): 3701-3708.
[15] SMEDLEY P L, KINNIBURGH D G. A review of the source, behaviour and distribution of arsenic in natural waters[J]. Applied Geochemistry, 2002, 17(5): 517-568.
[16] CULLEN W R, REIMER K J. Arsenic speciation in the environment[J]. Chemical Reviews, 1989, 89(4): 713-764.
[17] ������. �Ż������廯ѧ�Ϳɸ����о�[D]. ��ɳ: ���ϴ�ѧ��Դ�ӹ������﹤��ѧԺ, 2011: 47-52.
HONG Qiuyang. Study on the crystal chemistry and floatability of pyrrhotite[D].Changsha: Central South University. School of Minerals Processing and Bioengineering, 2011: 47-52.
[18] HELZ G R, TOSSELL J A. Thermodynamic model for arsenic speciation in sulfidic waters: a novel use of ab initio computations[J]. Geochimica et Cosmochimica Acta, 2008, 72(18): 4457-4468.
[19] VLASSOPOULOS D, BESSINGER B, O'DAY P A. Aqueous solubility of As2S3 and thermodynamic stability of thioarsenites[C]//Proceedings of the 13th International Conference on Water-Rock Interaction. London, UK: Taylor & Francis Group, 2010: 823-826.
[20] CORNELIS G, POPPE S, VAN GERVEN T, et al. Geochemical modelling of arsenic and selenium leaching in alkaline water treatment sludge from the production of non-ferrous metals[J]. Journal of Hazardous Materials, 2008, 159(2/3): 271-279.
[21] ����, ֣�Ž�, ������, ��. �������ļ��Խ�������������ѧ[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2008, 39(2): 268-272.
BAI Meng, ZHENG Yajie, LIU Wanyu, et al. Alkaline leaching and leaching kinetics of arsenic sulfide residue[J]. Journal of Central South University(Science and Technology), 2008, 39(2): 268-272.
[22] ��Ԫ��, ������. ���������������ˮ�������̬�仯[J]. ������ѧ, 1996, 15(2): 118-126.
JIANG Yuanru, HUANG Qiongyu. The change of arsenic forms in the treatment for arsenic wastewater by ferrous sulfide[J]. Environmental Chemistry, 1996, 15(2): 118-126.
[23] BAHL M K, WOODALL R O, WATSON R L, et al. Relaxation during photoemission and LMM Auger decay in arsenic and some of its compounds[J]. The Journal of Chemical Physics, 1976, 64(3): 1210-1218.
[24] STEC W J, MORGAN W E, ALBRIDGE R G, et al. Measured binding energy shifts of ��3p�� and ��3d�� electrons in arsenic compounds[J]. Inorganic Chemistry, 1972, 11(2): 219-225.
[25] TAYLOR J A. An XPS study of the oxidation of AlAs thin films grown by MBE[J]. Journal of Vacuum Science and Technology, 1982, 20(3): 751-755.
[26] EPP J M, DILLARD J G. Effect of ion bombardment on the chemical reactivity of gallium arsenide(100)[J]. Chemistry of Materials, 1989, 1(3): 325-330.
[27] LEGRAND D L. Oxidation/alteration of pentlandite and pyrrhotite surfaces at pH 9.3: Part 1. Assignment of XPS spectra and chemical trends[J]. American Mineralogist, 2005, 90(7): 1042-1054.
[28] AGOSTINELLI E, BATTISTONI C, FIORANI D, et al. An XPS study of the electronic structure of the ZnxCd1�CxCr2(x = S, Se) spinel system[J]. Journal of Physics and Chemistry of Solids, 1989, 50(3): 269-272.
[29] PETKOV K, KRASTEV V, MARINOVA T. XPS study of amorphous As2S3 films deposited onto chromium layers[J]. Surface and Interface Analysis, 1994, 22: 202-205.
[30] PEISERT H, CHASS T, STREUBEL P, et al. Relaxation energies in XPS and XAES of solid sulfur compounds[J]. Journal of Electron Spectroscopy and Related Phenomena, 1994, 68: 321-328.
T, STREUBEL P, et al. Relaxation energies in XPS and XAES of solid sulfur compounds[J]. Journal of Electron Spectroscopy and Related Phenomena, 1994, 68: 321-328.
[31] ������, ������, �����. ��е��ԴŻ������������ѧ��Ӱ��[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2010, 41(6): 2085-2090.
ZHANG Youxin, HE Lihua, LIU Xuheng. Effect of mechanical activation on leaching kinetics of pyrrhotite[J]. Journal of Central South University(Science and Technology), 2010, 41(6): 2085-2090.
���༭ �������
�ո����ڣ� 2019 -01 -26; �����ڣ� 2019 -03 -26
������Ŀ(Foundation item)�����ϴ�ѧ�����У��������ҵ���ר���ʽ�������Ŀ(2019zzts702)��������Ȼ��ѧ����������Ŀ(51634009, 51804340)(Project(2019zzts702) supported by the Fundamental Research Funds for the Central Universities of Central South University; Projects(51634009, 51804340) supported by the National Natural Science Foundation of China)
ͨ�����ߣ�����������ʿ�������ڣ�����ʪ��ұ������Դ���������о��� E-mail: hanhaishengjingji@126.com

