���ᱵ���Ƿ��ĸ�������������ұ�������ϵ�����Ũ�Ȳⶨ�е�Ӧ��
������1, 2�������1, 2��������1, 2���Ľ���1, 2��������1
(1. ���ϴ�ѧ ��Դ�ӹ������﹤��ѧԺ������ ��ɳ��410083��
2. ���ϴ�ѧ ����������ұ���ص�ʵ���ң����� ��ɳ��410083)
ժҪ��Ϊ�����������ᱵ���Ƿ�������Ӧ����ұ������Ʒ������ϵ�����������Ũ�ȵIJⶨ��̽�ֲ�ͬ�ȶ�������ˮ�Ҵ�������Tween-80��������ȵȶ����ᱵ��ɢ��ϵ�ȶ��Ե�Ӱ�죬�õ����Ƿ��ⶨ���������Ũ����ϵ�е���������ǣ���ˮ�Ҵ�3.0 mL��0.1 g/L Tween 1.0 mL��pH=1.0���ڲ�������420 nm ���������Ũ����0.1~0.8 mmol/L��Χ�ڷ��ϱȶ����ɡ��÷����ļ����Ϊ0.55 mg/L��������Ϊ1.82 mg/L���÷��������٣�������Ϊ98.9%~101.9%����Ա�ƫ��Ϊ0.68%~1.90%����GB/T 5750.5��2006���귨�Ƚϣ��÷���������㡢��ݣ�����ɿ������������Һ���������Ũ�ȵIJⶨ�еõ��Ϻý����
�ؼ��ʣ����Ƿ����ȶ��Ը���������ұ�����������Ũ�Ȳⶨ
��ͼ����ţ�TF18��O657.3 ���ױ�־�룺A ���±�ţ�1672-7207(2013)06-2186-06
Improvement of barium sulfate turbidimetry for determination of sulfate concentration in complex bioleaching samples
PENG Anan1, 2, LIU Hongchang1, 2, NIE Zhenyuan1, 2, XIA Jinlan1, 2, ZHAO Zhengdong1
(1. School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China;
2. Key Laboratory of Biometallurgy of Ministry of Education, Central South University, Changsha 410083, China)
Abstract: In order to improve the BaSO4 turbidimetry in determining sulfate concentration in the complex bioleaching samples, the effects on the stability of barium sulfate dispersion system from different stabilizing agents, the amounts of Tween-80 and ethanol, and pH values were evaluated. The results show the optimal conditions are: ethanol 3.0 mL; 0.1 g/L Tween-80 1.0 mL; pH=1.0 and the absorbance at 420 nm observes Beer-Lambert law for 0.1-0.8 mmol/L of sulfate concentration. The detection limit is 0.55 mg/L, and the quantitative limit is 1.82 mg/L. The recovery ratio of the method is 98.9%-101.9% with the relative standard deviation of 0.68%-1.90%. Compared with the national standard method GB/T 5750.5��2006, the method in this work gives satisfying results in determining the sulfate ion concentration in the bioleaching samples, and it is faster and easier to operate, indicating its wide applicability to the determination of sulfate concentration of complex samples.
Key words: turbidimetry; stability improvement; bioleaching; sulfate concentration determination
�������������ѧ�Ϳ�ұ����ѧ���ϵĿ�����Դ�ӹ�����ȡұ���¼����������ý�����������л����ӵ�Ʒλ����(��ҪΪ��)��ѡ������ȡ�м۽����Ĺ���[1-2]�������������ϵ�У������ܾ����������̺������������ԣ�Ӱ���Ž������ӵĽ������ʺͽ����ʣ���ʵ���о�������������Ҫ���Ϳ����ָ�꣬һ��ͨ������ֱ�Ӽ������ⶨ����Һ��ϸ��Ũ�ȣ��ⶨ��ϵ���������������ʡ�pH�仯������ӳ�����ڽ�����ϵ��һ�����ӡ�ǿ���Ի�����pH����ϸ����л���̿����½���1.2�������ͣ�ϸ�������������һ�����������Ķ�̬���̣���ˣ���Ͻ���Һ�����������Ũ�ȵIJⶨ��ͨ������ϸ����������л�����ܸ�ȷ�ط�ӳϸ���Խ�����ϵ�Ĺ���[3]����ȷ���˽���������������̡�Ŀǰ��ʵ���Ҳⶨ������ϵ�����Ũ�ȱ仯�ķ���ͨ���б��Ƿ�������ɫ������ɫ��������������������[4-6]��ʵ��֤������ɫ���ɱ��ϸߣ���ɫ������������������������Ϊ���������Ƿ��ڿ��ٲⶨ���������Ũ��ʱ�кܴ��Ӧ������[7]��Ϊ�������ô˷������Ķ��ȶ�����ѡ�����̽�֣��о���ͬ�ȶ�������ˮ�Ҵ�������Tween-80��������ȵȶ����ᱵ��ɢ��ϵ�ȶ��Ե�Ӱ�죬ȷ����ѵ����������Ũ�Ȳⶨ��ϵ�����ø÷������ⶨ����ұ����������ϵ�����������Ũ�ȡ�
1 ʵ��
1.1 �������Լ�
����-�ɼ���ֹ��ȼ�(UV-3000���ձ�����˾)��������ȼ�(PHS-25���Ϻ��ǵ��ѧ�����ɷ�����˾)������������ϩ��(�ۺ϶�1750��50����ҩ����ҩҵ�ɷ�����˾)��Tween-80(�Ϸʲ�������Ƽ��������ι�˾)�������Լ���Ϊ������������
����Һ��0. 14 mol/L BaCl2����Һ��5 mmol/L Na2SO4����Һ��
�ȶ�����Һ��50 mg/g ����ϩ����Һ[8]��0.1 g/L Tween-80��Һ��
���������������ҺpH��1.0��
1.2 ���ᱵ���Ƿ���ɢ��ϵ�ȶ����о�
��25 mL��ɫ���зֱ����3.0 mL BaCl2����Һ��3.0 mL��ˮ�Ҵ���1.0 mL 0.1 g/L Tween-80��2.5 mL Na2SO4����Һ������pHΪ1.0��������Һ���ݣ�����5 min���ڲ���Ϊ400~800 nm�ɼ��ⷶΧ��ɨ�����շ�ȷ��������ղ�����
��������ϵ�У��ֱ�ı��ȶ������ࡢ�ȶ����������Ⱥ���ˮ�Ҵ��������������ղ�����������ˮΪ�αȲⶨ45 min�ڷ�ɢ��ϵ������ֵ�仯��
1.3 ���������ϵ�����������Ũ�Ȳⶨ
���÷������ڵ��ͽ����ܾ���������������˾�(Acidithiobacillus ferrooxidans)ҡƿ������ͭ����������н�����ϵ���������Ũ�ȵIJⶨ��������귨[9]�ⶨ�����Ƚϡ������������£�
������������[10](MgSO4��7H2O��0.5 g/L��K2HPO4��0.5 g/L��(NH4)2SO4��3.0 g/L��KCl��0.1 g/L��Ca(NO3)2��0.01 g/L)�м���10 g/L�Ļ�ͭ��������(����С��75 ��m)��������ʼpH��2.0����ʼ������10%�����ij�ʼŨ��Ϊ5��107��/mL���¶�Ϊ30 �棬170 r/min����ԡ����������A. ferrooxidansϸ�����������У�ÿ��ȡ1.5 mL��Һ����ת��12 000 r/min����2 min��ȡ����Һ����������ˮ�ʵ�ϡ�͡���25 mL��ɫ���зֱ����3.0 mL BaCl2����Һ��3.0 mL��ˮ�Ҵ���1.0 mL 0.1 g/L Tween-80��Һ��1.0 mL������Ʒϡ��Һ������pHΪ1.0������Һ���ݣ�����5 min֮���ڷֹ��ȼ�����1 cm��ɫ������Ʒ�հ�Ϊ�α�����Ѳ������ⶨ����ֵ��
2 ���������
2.1 ��Ѳ�����ȷ��
���ᱵ��Tween-80��ɢ��ϵΪ���ɫ������Һ����1.2�ڷ����ڲ���Ϊ400~800 nm��Χ��ɨ����ϵ����ֵ�������ʾ��һ���IJ�����Χ�ڣ����Ų����ļ�С����ɢ��ϵ������ֵ�����ӣ���������[11]������������Ƿ�����ԭ��һ�¡����ݷֹ��ȼƲ���ɨ��ȷ����ɢ��ϵ�ⶨ����Ϊ420 nm��
2.2 �ȶ��������ᱵ��ɢ��ϵ��Ӱ��
�����Ӻ��������������Һ�н���γɳ���֮�����ڳ������ȶ������������۳�����ʱ����ѡ�����һ�������ȶ���ά����ϵ�ȶ��ԡ�ʵ���ҳ��ú����б������ȶ����и���[12]������[13-14]�;���ϩ ��[8]�ȡ������Ҵ���������Ϊ���ӣ�����������������ϩ���ȸ߷����л���Ϊ�ȶ��������ƹ��̽��鷳�������ƺõ���Һ���ױ��棬������»���ù����Ⱦ�����ʣ�����Ӱ��ʵ����������������ʵ������з���Tween-80��ά����Һ�ȶ��Է���Ҳ����Ҫ���á�Tween-80�������³�Һ̬����һ�������Եķ����ӱ�����Լ�[15]����ѡ��ҵ�г�������ѡҩ����һ��Ũ�ȵ�Tween-80�����������������[16]��
ͼ1��ʾΪ��420 nm����50 mg/g����ϩ����0.1 g/L Tween-80�Է�ɢ��ϵ�ȶ��Ե�Ӱ�졣��ͼ1�ɼ���ʹ��Tween-80��Ϊ�ȶ�����5 min֮�����ʾ�Ϻ��ȶ��ԣ�������ϩ����Ҫ��15 min֮�����ʾ�Ϻõ��ȶ��ԡ����ȶ������·���3 d��Tween-80��Ϊ�ȶ�����ϵ������ֵ�������������仯��������ϩ���ȶ���ϵ�����ϴ�仯��
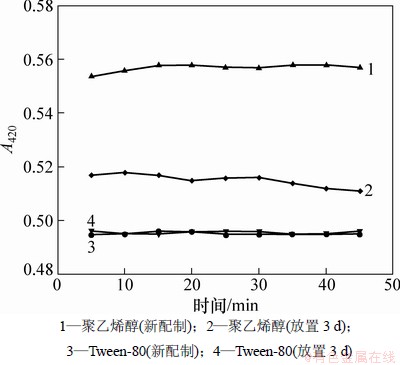
ͼ1 �ȶ��������ᱵ��ɢ��ϵ�ȶ��Ե�Ӱ��
Fig. 1 Effects of different stabilizing agents on stability of barium sulfate dispersion system
2.3 Tween-80���������ᱵ��ϵ��Ӱ��
ͼ2��ʾΪTween-80���������ᱵ��ɢ��ϵ��Ӱ�졣ʵ����1.2���������������²ⶨ0.1 g/L Tween-80��Һ����ֱ�Ϊ0.5��1.0��2.0��4.0 mL ʱ��ϵ��420 nm��������ֵA420��������֪����Tween-80��Һ����С��0.5 mLʱ��ɢ��ϵ������ֵ��С����ϵ���ȶ��Խϵͣ���Tween-80��Һ��������2.0 mL ʱ����ɢ��ϵ������ֵ�ϴ��ȶ��Եͣ���Tween-80��Һ����Ϊ1.0 mLʱ����ɢ��ϵ���ȶ�����á�Ϊ��֤ʵ������ȷ�ԣ�ѡȡ1.0 mL 0.1 g/L Tween-80��Һ��Ϊ�ȶ������������

ͼ2 Tween-80���������ᱵ��ɢ��ϵ�ȶ��Ե�Ӱ��
Fig. 2 Effect of amounts of Tween-80 on stability of barium sulfate dispersion system
2.4 �Ҵ����������ᱵ��ϵ��Ӱ��
��ˮ�Ҵ��ܹ��������ͳ������ܽ��[17]��ʹ���ᱵ�����Ͼ��ȵط�ɢ����Һ�У�ʹ��ɢ��ϵ���ȶ�����ǿ����ˮ�Ҵ����������ᱵ��ɢ��ϵ�ȶ��Ե�Ӱ����ͼ3��ʾ��ʵ����1.2�����������£��ⶨ��ˮ�Ҵ�����ֱ�Ϊ1.0��2.0��3.0��4.0��5.0 mLʱ����ɢ��ϵ��420 nm��������ֵA420����ͼ3�ɼ������Ҵ�����С��3.0 mLʱ�������Ҵ����������ӣ���ɢ��ϵ������ֵ�����ߣ��ȶ�������ǿ�����Ҵ�����Ϊ3.0 mLʱ����ֵ�Դ��ȶ�����ߣ����Ҵ���������3.0 mLʱ����ɢ��ϵҲ���ȶ���������ֵ���½�����ˣ�ѡȡ��ˮ�Ҵ�Ũ��Ϊ3.0 mLʱ��Ϊ��ɢ��ϵ���������
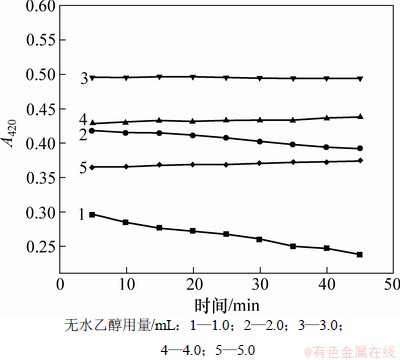
ͼ3 ��ˮ�Ҵ����������ᱵ��ɢ��ϵ�ȶ��Ե�Ӱ��
Fig. 3 Effect of amounts of ethanol on stability of barium sulfate dispersion system
2.5 ��ȶ����ᱵ��ϵ��Ӱ��
����淵�[11]̽����ȶ����ᱵ��ɢ��ϵ�ȶ���Ӱ��Ļ����������ᱵ����Һ�У���BaSO4����Ϊ���ˣ����˱�������SO42-�������硣���ڵ糡����ǿ�ҵ�������Һ��Ba2+��ʹBa2+�����ڳ���������棬�γɵ�һ������(���ܲ�)��ʹ����������������ɣ�Ȼ����������Һ�и����ӣ����ɵ����Ե�˫��㡣����Һ����Ƚϵͻ�ϸ�ʱ����Ӱ��˫���Ĺ��ɣ�Ӱ������ȵ��ȶ��ԡ�
ͼ4��ʾΪ��ȶ����ᱵ��ɢ��ϵ�ȶ��Ե�Ӱ�졣��ʵ��ֱ���Ʒ�ɢ��ϵ��pHΪ0.5��1.0��1.5��2.0���ⶨ��ͬ��ȶԷ�ɢ��ϵ�ȶ��Ե�Ӱ�졣��ͼ4��֪����pHΪ1.0ʱ����ɢ��ϵ5 min֮�����ʾ�ϸ��ȶ��ԣ���pH���ڻ����1.0ʱ��ɢ��ϵ���ȶ��Զ��ϲ˵������pHΪ1.0ʱ��ʹ�����ᱵ������������ȶ�״̬����ˣ�ȷ��pHΪ1.0��Ϊ��ɢ��ϵ�������ȡ�
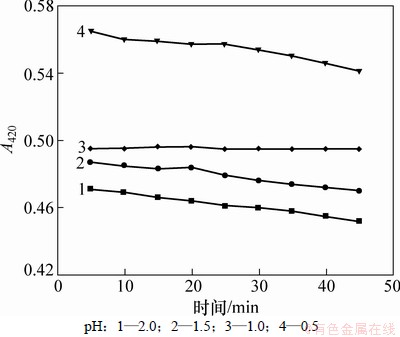
ͼ4 ��ȶ����ᱵ��ɢ��ϵ�ȶ��Ե�Ӱ��
Fig. 4 Effect of pH on stability of barium sulfate dispersion system
2.6 ���ᱵ���Ƿ��������ߵĽ���
�����������ۣ���25 mL��ɫ�������μ���3.0 mL���Ȼ�����Һ��3.0 mL��ˮ�Ҵ���1.0 mL 0.1 g/L Tween-80��Һ���ֱ����0��0.5��1.0��1.5��2.0��2.5��3.0��3.5��4.0 mL���������Һ������pHΪ1.0������Һ���ݣ�5 min���ڲ���420 nm������ֵA420�����ݲ����������Ũ��0.1~0.8 mmol/L��Χ������ֵA��Ũ��c֮������������Թ�ϵ��A=0.989 7C+0.005 5��R2=0.999 7��n=9����Ʒ���������Ũ�Ȳⶨ��������ͼ5��ʾ��
2.7 �����������ȷ��
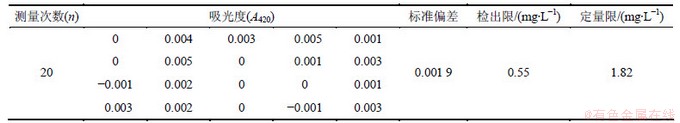
��1.3�ڵķ����������ᱵ��ɢ��ϵ�հ���Һ20�ݣ���������ʵ�������ֱ�ⶨ������ֵ������Ͷ�����ȷ���ֱ����3����ƫ���10����ƫ����м���[18]��������1��ʾ����֪���������Ϊ0.55 mg/L������������Ϊ1.82 mg/L��
2.8 �ظ���ʵ��
��2.6�������£�ȡϡ�ͺ�Ľ���Һ1 mL��ƽ���Ʊ�6����Ʒ���ⶨ���������Ũ�ȡ��ɸ��ݲ����������õ���ƫ��(DS)����Ա�ƫ��(DRS)��������2��ʾ����������÷������ڽ���Һ�����������Ũ�Ȳⶨ���ظ��ԽϺá�
2.9 ������ʵ��
Ϊ���鱾�������������Ӵ���ʱ�������Ũ�ȵIJⶨ��Ӱ�켰������ȷ�ԣ����н���Һ��Ʒ�м���������εĻ�����ʵ�顣��ʵ���У���ȷ��ȡ1.0 mLϡ�ͺ��2�ֲ�ͬ����Һ��Ʒ���ⶨ���������Ũ�ȣ��ټ��벻ͬ���������������Һ���ⶨ�京����ʵ�������3��ʾ��������֣�������Ϊ98.9%~101.9%����Ա�ƫ��Ϊ0.68~1.9���ɼ��÷�����ȷ��

ͼ5 ��Ʒ���������Ũ�Ȳⶨ������
Fig. 5 Standard curve for determining sulfate concentration
��1 �����������ȷ��
Table 1 Determination of detection limit and quantitative limit
��2 ���ᱵ���Ƿ����ظ���(n=6)
Table 2 Stability of barium sulfate turbidimetry (n=6)
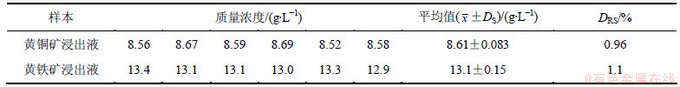
��3 ����Һ��Ʒ�������εĻ�����(n=3)
Table 3 Recovery of sulfate in bioleaching solution (n=3)
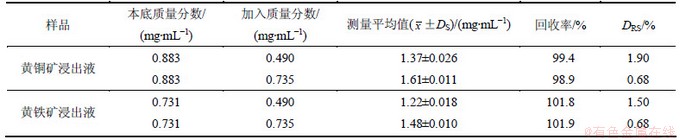
��4 ���������ϵ�����������Ũ�ȵIJⶨ(n=3)
Table 4 Determination of sulfate concentrations of bioleaching samples (n=3)

2.10 ���Ƿ�������ұ�������ϵ�����������Ũ�Ȳⶨ�е�Ӧ��
�����������ۣ���2.3����ʾ�������Ի�ͭ��ͻ��������������ϵΪ�����ⶨ����Һ�����������Ũ�ȣ�������귨[9]�Ƚϣ��������4����������÷��������ڲⶨ������ϵ���������Ũ����Ӧ�õĿ�������ȷ�ԡ�
3 ����
(1) Tween-80���ᱵ���Ƿ��ⶨ���������Ũ����ϵ�У������������ˮ���Ҵ����Ϊ3.0 mL��0.1 g/L Tween-80 1.0 mL��pH=1.0����������Ϊ420 nm��
(2) �÷����ڲⶨ���ӽ���Һ��Ʒʱ���нϸߵĿɿ��ԣ����Ҿ��м��ȷ���ص㡣
(3) ͨ��ʵ����Ʒ�IJⶨ����GB/T 5750.5��2006�����Ƚϣ���������÷����ڲⶨ������ϵ���������Ũ���о��п����ԡ�
�ο����ף�
[1] �����. ��ͭ�������ұ��[M]. ����: ұ��ҵ������, 2007: 1-8.
LI Hongxu. Bioleaching of copper sulfides[M]. Beijing: Metallurgical Industry Press, 2007: 1-8.
[2] Rohwerder T, Gehrke T, Kinzler K, et al. Bioleaching review part A: Progress in bioleaching: fundamentals and mechanisms of bacterial metal sulfide oxidation[J]. Applied Microbiology and Biotechnology, 2003, 63: 239-248.
[3] �λ�, �Ľ���, ������, ��. ����������ϸ��������Ԫ����ѧ��̬���о���չ[J]. �й���ɫ����ѧ��, 2008, 18(6): 1143-1151.
HE Huan, XIA Jinlan, PENG Anan, et al. Research progress of sulfur chemical speciation impacted by acidophilic sulfur- oxidizing bacteria[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(6): 1143-1151.
[4] ����, ������, �ܷ�, ��. ����ɫ�����ٷ�������ˮ�е�����������[J]. ��������: ��ѧ�ֲ�, 2006, 42(10): 21-23.
LI Yi, LIU Xiaosong, ZHOU Fan, et al. Rapid determination of four anions in drinking water by ion-chromatography[J]. Physical Testing and Chemical Analysis Part B: Chemical Analysis, 2006, 42(10): 21-23.
[5] Bertolacini R J, Barney J E. Colorimetric determination of sulfate with barium chloranilate[J]. Analytical Chemistry, 1957, 29(2): 281-283.
[6] �º�, ��ѧ��. dz̸����������������������ⶨ[J]. �й�������, 2005. 36(4): 41-42.
CHEN Hong, WANG Xuehua. Brief discussion on the determination of sulfate radicals with gravimetric method and volumetric method[J]. China Well and Rock Salt, 2005 36(4): 41-42.
[7] Kolmert  ,
,  P, Hallber K B. A fast and simple turbidimetric method for the determination of sulfate in sulfate-reducing bacterial cultures[J]. Journal of Microbiological Methods, 2000, 41(3): 179-184.
P, Hallber K B. A fast and simple turbidimetric method for the determination of sulfate in sulfate-reducing bacterial cultures[J]. Journal of Microbiological Methods, 2000, 41(3): 179-184.
[8] ϯ����, ������. ���ᱵ���Ƿ���ɢ��ϵ���ȶ����о�[J]. �ӱ�ʦ����ѧѧ��: ��Ȼ��ѧ��, 2007, 31(4): 503-505.
XI Gaiqing, PANG Xiuyan. Study on the stability of BaSO4 dispersing system in the turbidimetric detection[J]. Journal of Hebei Normal University: Natural Science Edition, 2007, 31(4): 503-505.
[9] GB/T 5750.5��2006, ��������ˮ�����鷽�����ǽ���ָ��[S].
GB/T 5750.5��2006, Standard examination methods for drinking water�Cnonmetal parameters[S].
[10] CHEN Ming-lian, ZHANG Lin, GU Guo-hua, et al. Effects of microorganisms on surface properties of chalcopyrite and bioleaching[J]. Transaction of Nonferrous Metals Society of China, 2008, 18(6): 1421-1426.
[11] �����, ���, ��־��. ���ᱵ������Ƿ��ⶨ������̽��[J]. ��������: ��ѧ�ֲ�, 2001, 37(3): 111-112.
DING Gendi, WU Jie, XU Zhisui. On the mechanism of the turbidimetric determination of SO42- by the BaSO4 method[J]. Physical Testing and Chemical Analysis Part B: Chemical Analysis, 2001, 37(3): 111-112.
[12] ������, ����, ����O, ��. ���ᱵ�ֹ��ȱ��Ƿ��ⶨ������Ʒ[J]. ���Ŵ�ѧѧ��: ��Ȼ��ѧ��, 2007, 46(6): 880-883.
FU Jiaoyan, DING Zhenhua, WU Yanmin, et al. Determination of high-sulfur content environmental samples by spectroscopic barium turbidity method[J]. Journal of Xiamen University: Natural Science, 2007, 46(6): 880-883.
[13] ������. �Ը������ᱵ���Ƿ��ⶨˮ������������ĸĽ�[J]. �����������뼼��, 1997, 9(2): 44-45.
QIU Wanjun. Improvement of sulfate ion detection in water for the modified nephelometry with barium sulfate[J]. The Administration and Technique of Environmental Monitoring, 1997, 9(2): 44-45.
[14] ������, ��ѧ��, ��־��, ��. ���ᱵ���Ƿ��ⶨ�������ºϽ��ȸ�ʴ�����������[J]. ұ�����, 2006, 26(1): 77-78.
LIU Changfeng, LIU Xuegui, NING Zhigao, et al. Determination of sulfate radical in molten salt corrosion product of Ni-base superalloy by turbidimetry[J]. Metallurgical Analysis, 2006, 26(1): 77-78.
[15] Noudeh G D, Khazaeli P, Rahmani P. Study of the effects of polyethylene glycol sortitan esters surfactants group on biological membranes[J]. International Journal of Pharmacology, 2008, 4(1): 27-33.
[16] ZHANG Chenggui, XIA Jinlan, ZHANG Ruiyong. Comparative study on effects of Tween-80 and sodium isobutyl-xanthate on growth and sulfur-oxidizing activities of Acidithiobacillus albertensis BY-05[J]. Transaction of Nonferrous Metals Society of China, 2008, 18(4): 1003-1007.
[17] ����, ��˼Զ, �ƺ���, ��. �̲���Ʒ�������ⶨ���о�[J]. ����ʵ����, 2000, 17(5): 534-535.
LI Zhong, LI Siyuan, HUANG Haitao, et al. Study on determination of sulphur in tobacco[J]. Chinese Journal of Spectroscopy Laboratory, 2000, 17(5): 534-535.
[18] Thomsen V, Schatzlein D, Mercuro D. Limits of detection in spectroscopy[J]. Spectroscopy, 2003, 18(12): 112-114.
(�༭ ������)
�ո����ڣ�2012-03-20�������ڣ�2012-05-03
������Ŀ��������Ȼ��ѧ����������Ŀ(50974140)����������ʿ�����������Ŀ(20090162110054)
ͨ�����ߣ��Ľ���(1964-)���У����������ˣ����ڣ����½�����/����������������ұ���о����绰��0731-88836944��E-mail��jlxia@csu.edu.cn