������ʱ��: 2013-12-27 16:44
ϡ�н��� 2014,38(03),509-515 DOI:10.13373/j.cnki.cjrm.2014.03.024
�������������LiBH4�о���չ
������ ������
�����żҽ纽�չ�ҵְҵ����ѧԺ����ά����ϵ
���ϴ�ѧ���������Ƚ������������ص�ʵ����
ժ Ҫ��
���ܾ�����ࡢ��Ч�����������õ��ص�, ��δ���з�չǰ����������Դ֮һ�����������á���Ч����ȫ�Ĵ��漼�������ܴ��ģӦ�õĹؼ�, ����ڸ�ѹ��̬�����Һ������, ͨ��������ϼ��������γɹ��������λ�⻯��Ĺ�̬���⼼�������������Ұ�ȫ�Ժ�, ����Ϊ�����з�չǰ���Ĵ��淽ʽ����λ�⻯���е�LiBH4�����۴��������ߴ�18.5% (��������) , Զ��������Դϵͳ����������������5%��Ҫ��, �ǵ�ǰ������������ϵĵ��ʹ������о��ȵ�, �����������ص�����������ѧ������ѧ���⡣�Ӹ���LiBH4�����������ܳ���, �����˴��⼼����������ϵ��о���չ, �����˽�������ȡ����Ҫ��ʩ, �ر��������ʵ���Ӧ�����γɸ��ϴ�����ϵ, �������������Ըı�縺��, ���Ӵ���, ��С�����ߴ缰����������䷨�ȼ���������о��ɹ����о���չ, �ص��ע����������ơ��������������������¶ȼ������������ⷴӦ����ѧ������ѧ�����⡣�������������LiBH4�dz�����Դϵͳʵ�û��Ĺؼ�, �����л������з���������Ѹ�١�������������������桢���²����ķ�������ϵ, ��δ���о����ص㡣
�ؼ��ʣ�
����;�������;������;LiBH4;
��ͼ����ţ� TB34
����飺������ (1970-) , ��, ����������, ˶ʿ, ������, �о�����:����Դ����;�绰:13974468282;E-mail:hyxialuosheng@si-na.com;
�ո����ڣ�2013-07-26
��������ʡ�Ƽ�����Ȼ��ѧ���� (09JJ6079);�żҽ纽�չ�ҵְҵ����ѧԺ������Ŀ (ZHKT2013-008) ����;
Progress in High Capacity Hydrogen Storage Material of LiBH4
Xia Luosheng Zhu Shuhong
Aviation Maintenance Department, Zhangjiajie Institute of Aeronautical Engineering
State Key Laboratory of Advanced Design and Manufacturing for Vehicle Body, Hunan University
Abstract��
Hydrogen, which has the characteristics of clean, efficient and renewable utilization, was one of the promising new energies in the future. The safe, efficient and economical hydrogen storage was the key technique for the large scale application of hydrogen energy, relative to the high pressure gaseous hydrogen storage and liquid hydrogen storage, the solid state hydrogen storage technology could store hydrogen in materials by forming solid solution or hydrides, which was regarded as the most promising technique because of its good safety and high energy density. LiBH4 was the typical representative of high capacity of hydrogen storage material and research hot spot because of its theory capacity of 18. 5% ( mass fraction) , far from overtaking hydrogen source system load weight greater than 5% of hydrogen storage capacity requirements, but it was faced with serious thermodynamics and kinetics problems. Starting from improving performance of the absorption and releasing LiBH4 hydrogen, the research progress of hydrogen storage technology and hydrogen storage material was analyzed, and the major measures taken in recent years were reviewed, such as adding reactants to form a composite hydrogen storage system, the appropriate doping anion and cation to change the electronegativity, adding catalyst, reducing the grainsize and nanometer filling method. The emphases were focused on the mechanisms, hydrogen storage capacity, temperature and condition thermodynamics and kinetics. High capacity LiBH4 hydrogen storage materials were the key to practical onboard hydrogen source system, the focus of future research was to develop method and system of quick hydrogen absorption, a large amount and reversibility of hydrogen absorption and desorption, and room temperature operation.
Keyword��
hydrogen energy; hydrogen storage material; high capacity; LiBH4;
Received�� 2013-07-26
���ܾ�����ࡢ��Ч�����������õ��ص�, ���������ǵĹ㷺��ע, ��δ���з�չǰ����������Դ֮һ[1]��������Ϊһ����Դʹ��ʱ, ���������漰���䷽������⡣������, ������ȼ�ϵ�ؼ����������Ŀ��ٷ�չ, �����ƶ������ܼ����Ŀ�ѧ�о�������Ľ���, ����Ч�����á���ȫ���ⴢ�漼�������ֽ�����Ӧ�õ�ƿ��[2]������0���1��105Pa��ѹ������������ʽ����, ���ܶ�Ϊ0.0899 kg��m-3;��-259����, ���Թ�����ʽ����;���������ٽ��֮��һ����С��������, ����-253��-259�����Һ����ʽ����, �ܶ�Ϊ70.8kg��m-3�������������, ��ǰ���õĴ��ⷽʽ��3��:��ѹ��̬���⡢Һ̬���⡢���ϻ���̬���⡣��ѹ��̬������Ҫ���ص���ѹ����, ѹ��������Ľϴ�, ���Ҵ�����������й©����ѹ�������ƵȲ���ȫ����[3]��Һ̬�������������ܶȸ�, ������Һ��������������Լ�Ǵ���������ֵ��50%, ���������Ա�����Իӷ����⡣���ϻ���̬������ϴ�����ͨ����ѧ��Ӧ���������������������ڹ�̬������, �������ܶȸ��Ұ�ȫ�Ժ�, ����Ϊ�����з�չǰ����һ���������淽ʽ�����ĴӸ���Li BH4�����������ܳ���, �����˴��⼼����������ϵ��о���չ, �����˽�������ȡ����Ҫ��ʩ��
1 �������
�ۺϵ�ǰ�о���չ, ���ϻ���̬���������Ҫ����������:���ѻ���ϡ������ﯻ���þ������Ͻ���λ�⻯��ȴ�����ϡ�ͼ1Ϊ��ǰ��Ҫ��������뼼���Ĵ�����������������ܶ�[4], �������۴����������ﵽ5%�Ե��ϸ������������, �����⻯����⻯������⻯��ͽ����л���ܲ��ϵ�, �ǹ�̬��������뼼�����о��ص㡣
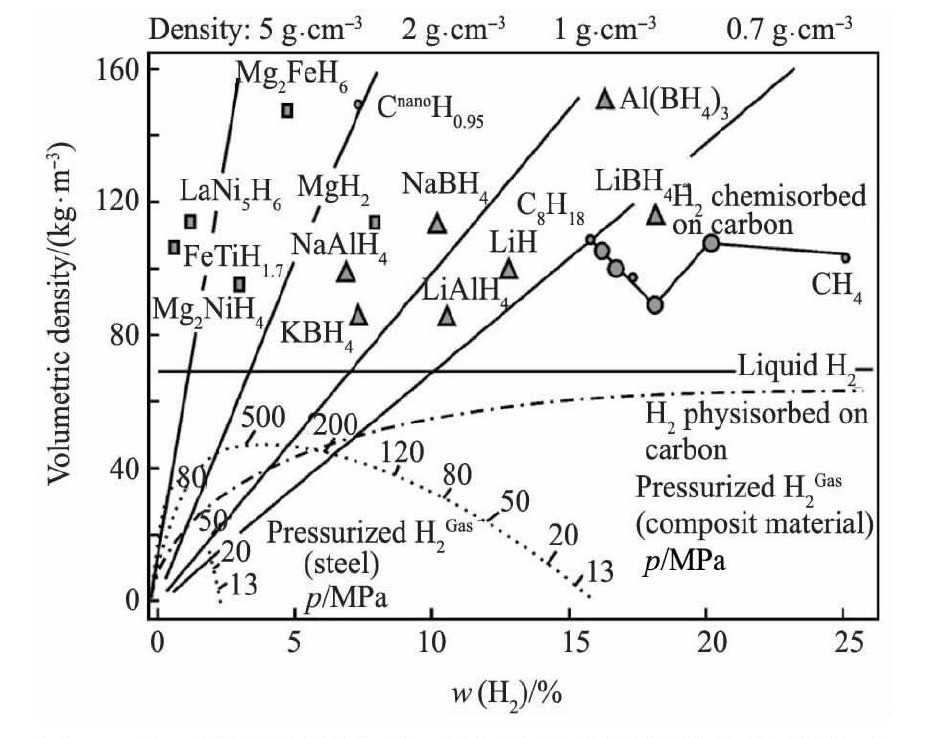
ͼ1 ��Ҫ��������뼼���Ĵ�����������������ܶ�Fig.1 Mass fraction and volumetric density of some hydrogen storage materials and technologies
1.1 �ѻ�����Ͻ�
һ����ָ��������˹ (Laves) ��ṹ��AB2�ͽ����仯����, �����������̴���Ͻ��о���Ϊ�㷺, ���ʹ�����Ti Fe[5], ��۸����, �ڳ������ܿ�������պ��ͷ���, �䴢�������Ը���La Ni5 (1.85% (��������) ) , �������ٶȽϿ�, �����Ƚ�����, ����������������н����ص��ͺ�ЧӦ��
1.2 ϡ��������Ͻ�
ϡ��������Ͻ����������������[6,7], �������¼���ʵ��������, ����ʹ�����La Ni5[8], ��ϡ��������Ͻ�������, �䴢���������ϵ� (1.37%) , ���������ڳ�����Դϵͳ��
1.3 ﯻ��Ͻ�
ﯻ��Ͻ�[9]��������ȱ��о�, ����20����80������������ڵ缫���ϡ������ڼ۸��⻯��������ʴ�, ������ƽ̨ѹ��̫��, �����������ʵ��Ӧ�á�
1.4 þ������Ͻ�
MgԪ�ش����ḻ���۵�����, þ������Ͻ���������, ���зdz������ķ�չǰ��, ��Mg H2���۴�������������7.7%[10], �����ڷ����¶ȸ�, �����ѧ�ٶ�����ȱ��, �о��ص��ǽ��ͷ����¶Ⱥ������⡢���ⷴӦ��
1.5 ��λ�⻯�ﴢ�����
��λ�⻯����д��漰�����ⰲȫ������ŵ�, ��Ŀǰ�о��ȽϹ㷺�ĸ�����������ϡ������������ü����IJ��Ϸ�չ, �Դ���ϵͳ������ش�����ϵ�����ָ��Ҳ����˸��ߵ�Ҫ��:������Դ�� (IEA) ������о�Ŀ����150���¶��´���ϵͳ�����������ܶȺ���������ܶȷֱ����5%��50 kg��m-3;������Դ�� (DOE) �Գ��������洢ϵͳ������о�Ŀ����100���µ����������ܶȺ���������ܶȴﵽ5%~6%��62 kg��m-3��Ԫ�����ڱ���Na, Li, Mg, B, Al��Ԫ�ض����γɸ��ֽ�����λ�⻯��, ������λ�⻯��Li BH4�Ĵ����ܶȸ�, �����۴��������ߴ�18.5%, �������õĿ����Ժ�ѭ���ȶ���, ����Ϊ��Ŀǰ��߷�չǰ���Ĵ������, �ѳ�Ϊ������������о������ȵ�[11]��
2 �������������Li BH4
Li BH4�Ǿ��д����Եĸ�������λ�������⻯��, Ϊ��ɫ���׳���ľ���, ��Pnma (No.62) �ռ�Ⱥ, ������ϵ, �侧����Ϊa=0.7179 nm, b=0.4437 nm, c=0.6803 nm, ��=��=��=90��[12]��Friedrichs��[13]���ݵ�һ��ԭ������, Bԭ�����ٽ���4��Hԭ����Ҫ�Թ��ۼ�����γ�[BH4]-������, ����Li+�����Ӽ�����γ�Li BH4, ����ÿ��[BH4]-����4��Li+����Χ, ÿ��Li+Ҳ��4��[BH4]-����Χ, ��ռ乹�;�Ϊ������ṹ, ��ͼ2��ʾ, �������Ԫ�ؼ��ǿ��ѧ��������, Li BH4����/���ⷴӦͨ�����������ص�����ѧ������ѧ���⡣
���ռ�������, Li BH4�ڲ�ͬ���¶ȷ�Χ����ֲ�ͬ�����ⲽ��, ���ɲ�ͬ�Ļ�����, ͼ3�ܽ���Li BH4���ⷴӦ���ʱ���̡����ȶ���״̬�ǵ����µ������ṹ (Pnma) , ��118���ת��Ϊ������ϵ (P63mc) , ��280��ʱ���ۻ�, ���ֽ����, �����м䲽��, ����LH����B��
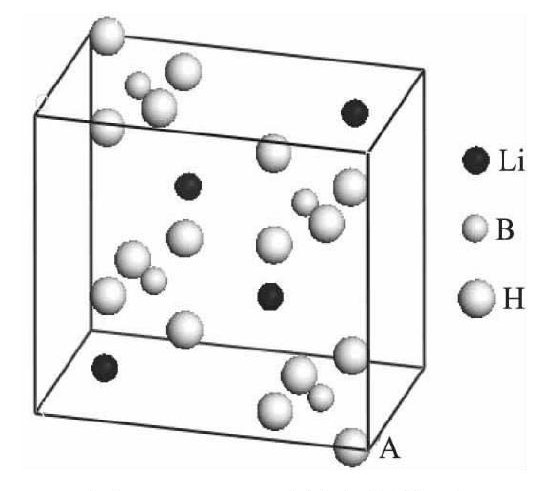
ͼ2 Li BH4��ԭ��ģ��Fig.2 Original cell model of Li BH4
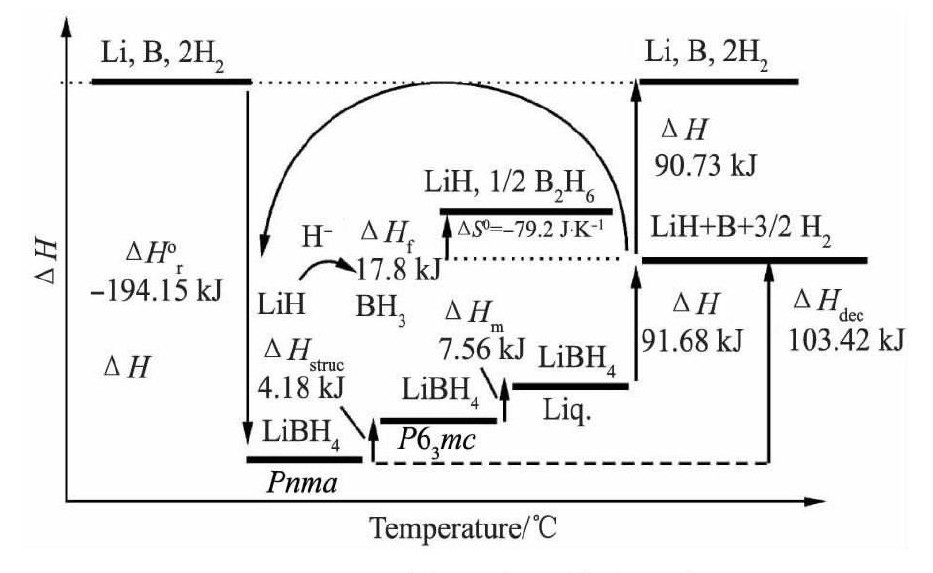
ͼ3 Li BH4���ⷴӦ���ʱ�ʾ��ͼFig.3Schematic diagram of enthalpy change of dehydrogena-tion process of Li BH4
�������о���Ϊ��Щ��λ�������⻯�ﲻ�ܿ���������, �����ڷ���, ͨ�����Ӵ����ȷ���, ���������⻯��Ҳ�ܿ��洢�⡣Vajo��[14]����Li BH4/Mg H2��ϵ����ʵ�ֿ���������, �÷���Ϊ̽������Li BH4�Ŀ����������ṩ�˽����������, ������ѧ��Ŭ��, �ѷ�����������Ч;��������Li BH4������������ѧ�붯��ѧ���ܡ�
3 ���Ƹ������������Li BH4���������ܵ���Ҫ����
��Li BH4�����������ܲ�, ��ǰ����Li BH4���������ܵ���Ҫ˼·����Li BH4�����ӽ����������⻯�����������ǽ��������̼���ʼ�����±����ȴӶ��γɸ�����ϵ, ���������ɷ�ΪΪ����: (1) �����ʵ���Ӧ��, �γɸ��ϴ�����ϵ:ͨ�������ʵ��ķ�Ӧ��, ��Ӧ����Li BH4�γ�����ѧ���ܽϲ��ȶ�����ϵ, ʹ���ⷴӦ���ͷ����¶Ƚ��͡� (2) ������������, �ı�縺��:ͨ�����������ӻ����������ı�ԭ���������ӵĵ縺��, ����Li BH4�е����Ӽ�ǿ��, ��������B-H���ۼ�ǿ��, �������ڽϵ��¶��·ֽ���������� (3) ���Ӵ���:ͨ��������������, ��ʹLi BH4�����ⷴӦ�ٶȼӿ졣 (4) ��С�����ߴ�, ����������䷨:ͨ����С�����ߴ����������ӵ���ɢ��, ��߷����ٶ�, ��������ײ�����Ϊ��ɢ����, �������ϵ��������, �������ȶ��ԡ�
3.1 �����ʵ���Ӧ��, �γɸ��ϴ�����ϵ
Vajo��[14]����ͨ�������ʵ���Ӧ��, �γ��µĸ��ϴ�����ϵ�ܸ���Li BH4����������, ����Ч����Li BH4������ѧ�ȶ��ԡ����������Mg H2, ���ƻ����ȶ���[15], ��Ӧ����ʽ��ʽ (1) ��ʾ��

�����Ӧ�����˷�Ӧ��, ��HΪ46 k J��mol-1H2, TΪ170��, 170�濪ʼ����, Mg B2���γ���Ч�Ľ�����Li BH4�����ȶ���Wan��[16]ͨ����ʵ�����о�Li BH4/Mg H2��Ӧ��ϵ, ���ָ���ϵ�����Ժ�, ����5��������ѭ��, ��Ŀ��洢������Ϊ10%, ��315~450�������, ����ϵ�����洢�������Դﵽ8%~10%����400��ʱ������Ϊ4%, ��ƽ������ѹ��ԼΪ1.2 MPa, ����ͬ�����´�Li BH4��10����, ������Ϊ���ڷ�����������ɵ�Mg B2ʹ��Li BH4��Mg H2�����ȶ�, �ƻ��������Ӽ����ۼ�, �Ӷ������˷�Ӧ�ӡ�Vajo��[17]����Mg S, Mg F2��Mg Se�Ⱥ�þ������Ҳ�ܽ���Li BH4���ȶ���, ���1��ʾ, ������ĥʵ��, ��Щ������ܹ���0.1 MPa��ѹ������, ��300~350������, �������ܳ���������������75%��
3.2 ������������, �ı�縺��
Nakamori��[18]�������⻯��M (BH4) n���ȶ��������Ľ���ԭ��M�ĵ縺������һ�������ڹ�ϵ, ���Ľ���ԭ��M�ĵ縺��Խ��, ���⻯����ȶ���Խ�͡�Orimo��[19]��������Ӿ��е縺�Խϸߵ������Ӳ������Liԭ��������Li+��[BH4]-������Ӽ�ǿ��, �Ӷ�����Li BH4���ȶ��ԡ�Xia��[20]���õ�һ��ԭ���������Li BH4����������Al���������Ӻ�, Al�Ͻ���ϵ��ṹ�ȶ��Ա��, ��ϵ��������������յ���������, Hԭ�ӽ����ܼ�С, ��ϵ����������ǿ��������ΪAl-Li BH4��ϵFermi�ܼ�������϶ֵ�����仯�Լ�Li-BH, B-H��ɼ����ü�����Al������ǿLi BH4��ϵ�������ܵ���Ҫԭ��Hagemann��[21]�ȷ��ֲ���˫�����ӿ����ı����Ľ���ԭ�ӵĵ縺��, �����������������ֲ����ȱ��, �ɽ��ͷ����¶ȡ�Yin��[22]����ͨ������������Ҳ�ɸ���Li BH4������ѧ����, ��F-���ӵ�Li BH4��, F-����ȡ��Li BH4�������Li H���⻯��ľ������, �ı�������ѧ���ܡ�����Li BH3.75F0.25������������Ϊ9.6%��������, ���ڵ�һ��ԭ������������ʱ�ΪԼ36.5 k J��mol-1H2, ����ζ����0.1MPa��ѹ����, �����¶�ԼΪ100�档
��1 Li BH4/Mg-��������������ϵTable 1 Rehydrogenation and dehydrogenation of Li BH4/Mg-compounds system ����ԭͼ

��1 Li BH4/Mg-��������������ϵTable 1 Rehydrogenation and dehydrogenation of Li BH4/Mg-compounds system
3.3 ���Ӵ���
���Ӵ�������Ч�ĸ���Li BH4���������ѧ������ѧ����, Zuttel��[12]��Si O2��ĩ (25%��75%) ���ӵ�Li BH4��, ����Li BH4�ķֽ�ӿ첢��3���ֽ����¶ȶ�������, 200����ֵ�һ������߷�, 453����ֵڶ�������߷�, ����400���ʱ�����ͷų�9%���⡣Kostka��[23]��Si O2���� (50%��50%) ���ӵ�Li BH4��, ��ĥ��Ϻ�, 170�濪ʼ����, 260������ٶ���졣Yu��[24]�о���Si O2, V2O3, Sn O2, Ti O2, Zr O2��Li BH4���������ܵ�Ӱ��, ����Ti O2����Ч���ͷ����¶�, ��Ti O2 (25%��75%) ���ӵ�Li BH4��, ��ĥ��Ϻ�, ��175��ʱ���ɿ�ʼ�������ⷴӦ, ��������600��ʱ, ������Ϊ8%~9%��
Guo[25]ͨ������SWNTs��Li BH4, ��������30%SWNTsʱ, ��ĥʱ��Ϊ1 h, ����Ч���ȽϺ�, Li BH4�ֱ���30 min, 1 h, 2 h���ͷ�4.3%, 9.1%, 10.8%����, ��280�����ҿ�ʼ����, 3��������¶ȷֱ�Ϊ382, 402��424�档Au��[26]�ֱ�Ti Cl3, Mg Cl2, Ti F3, Zn F2, Ca Cl2, Sr Cl2, Mg F2, Fe Cl3���ӵ�Li BH4��, ����Ti Cl3, Ti F3, Zn F2����Ч����Li BH4�����¶ȡ���Li BH4/0.1Ti Cl3����ĥ������������Ti (BH4) 3��Li Cl, �ܷ������ﵽ6%, ����7 MPa, 500������������, ������Ϊ3.4%;Li BH4/0.1Ti F3������ĥ��, 100�濪ʼ����, ������B2H6����, ��500��ʱ, �ܷ������ﵽ12%, ���ڷ���9%��, ����7 MPa, 500������������, �������ɴﵽ6%����Fang��[27]��Ti F3 (75%��25%) ���ӵ�Li BH4����ĥ��Ϻ�, ��70~90���¿�ʼ����, ������Ϊ5%, ��Zn F2 (10%��90%) ���ӵ�Li BH4, ����������7%��, ����7 MPa, 500������������, �������ﵽ4%��
3.4 ��С�����ߴ�, ����������䷨
��С�����ߴ��Ǹ��Ʋ��ϴ������ܵ���Ҫ�����ֶ�, ��������ڽ����������¶�Ϊ��̬����, ����С�侧���ߴ絽��������, �Ϳ���������ӵ���ɢ�ʼ�������Ľ�����, �Ӷ���߷����ٶȡ���ĥ���ǹ㷺ʹ�õ�һ�ַ���, һ��ֻ�ܽ���Ʒĥ����Լ1~10��m, �ڸ�����ĥ������ĥ��100nm, ��ЩС�����ܹ������ɢ�ʼ�������Ľ�����, �Ӷ����Ʒ������
������䷨�ǽ�����������һ�·���, ����������������Ʒ��ʹ���ײ����е�������С������, �����Ľ�����, Ŀǰ���õ�������������̼����������������衢̼��ĭ������̼��̼���ܵȡ�Opalka��[28]�ֱ����ṹ��Si O2, Zr O2, Al2O3 (50%��50%) ���ӵ�Li BH4��, ���ṹ��Si O2, Al2O3, Zr O2���нϴ�ı�����ͽ�С��ƽ����, ��ĥ15 min��, ��ϵ�ķ�����450��ֱ���310, 350, 410�档Gross��[29]��Li BH4��䵽������� (13 nm) ��̼��������, ������ܴ�146 k J��mol-1�½���103k J��mol-1, 70�����ҿ�ʼ����, ��ͬ�¶��µķ�����������˽�50����Fang��[30]���û�ѧ���ռ�����Li BH4��䵽���û���̿AC (2 nm, 30%) ��, ���������Ĵ���������, ��ͼ4, ������¶�����ڴ�ͳLi BH4������Լ150��, �������������Լһ��������, ����������Ҳ�õ���ʵ���Ը��ơ�Zhang��[31]��Li BH4��䵽���̼CMK-3 (5 nm, 50%��50%) , ��ĥ�����ϵ���ȵ�600��ʱ, ����������7%, ������̰�����Li2C2����, ˵�����̼CMK-3����������ԭ����ɢ��·��, ͬʱ������Li BH4����Li H������Ӧ, ����Li2C2, ʹ���ⷴӦ���ӳ��ס�Yu��[32]��Li BH4��䵽���̼����MWNT, ��MWNT��Li BH4�ֱ���������1��2, 1��1, 2��1��ĥ��Ϻ�, Li BH4����ʼ�����¶ȴ�380�潵����250��, ��������ֱ�Ϊ16.5%, 17.1%, 18.2%��
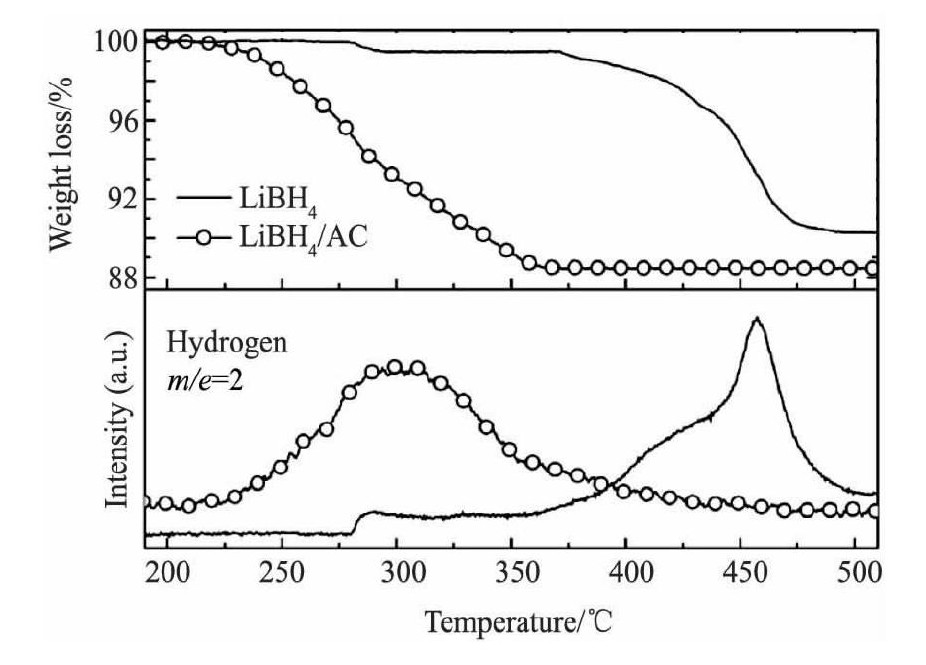
ͼ4 Li BH4/AC�����ϲ��ϼ�Li BH4������/���� (H2) ����Fig.4 TG/MS (H2) profiles of Li BH4/AC nanocomposite and bulk Li BH4
4 ����
Li BH4�����۴�������Ϊ18.5% (��������) , �Ǹ�����������ϵ��о��ȵ�, Ϊ����������������, ��������ַ�����ȡ����һЩ�ɹ�����Ȼ��ʵ��Ӧ�û���һЩ���, ��Ϊ������Դϵͳʵ��Ӧ��ָ���˷��������л������з���������Ѹ�١�������������������桢���²����ķ�������ϵ, ��δ���о����ص㡣
�����
[1] Johnston B, Mayo M C, Khare A.Hydrogen:the energy source for the 21st century[J].Technovation, 2005, 25 (6) :569.
[2] Schlabach L, Zuttel A.Hydrogen-storage materials for mobile applications[J].Nature, 2001, 414:353.
[3] Zuttel A, Borgschulte A, Orimo S.Tetra hydroborates as new hydrogen storage materials[J].Scr.Mater., 2007, 56 (10) :823.
[4] Zuttel A.Materials for hydrogen storage[J].Materials Today, 2003, (6) :24.
[5] Jankowska E, Jurczyk M.Electrochemical behaviour of high-energy ball-milled TiFe alloy[J].J.Alloys Compd., 2002, 346 (1-2) :L1.
[6] Deng G X, Zhao X S, Wang S M, Li Z N, Liu X P, Jiang L J.Research of Ti-Zr hydrogen absorbing alloys[J].Chinese Journal of Rare Metals, 2013, 37 (2) :237. (�˹�ϼ, ����ɽ, ����ï, ��־��, ������, ������.Ti-Zrϵ������ϵ��о�[J].ϡ�н���, 2013, 37 (2) :237.
[7] Zhang S C, Luo Y C, Zeng S P, Wang K, Kang L.Influence of magnesium content on self-discharge property of A2B7-type RE-Mg-Ni hydrogen storage alloys[J].Chinese Journal of Rare Metals, 2013, 37 (4) :511. (�����, ������, ����ƽ, ����, ����.þ������ϡ��-þ-��ϵA2B7�ʹ���Ͻ�缫�Էŵ����ܵ�Ӱ��[J].ϡ�н���, 2013, 37 (4) :511.)
[8] Liang G, Huot J, Schul Z R.Hydrogen storage properties of the mechanically alloyed LaNi5-based materials[J].J.Alloys Compd., 2001, 320 (1) :133.
[9] Kodama T.Proposal for new indexes describing the degree of hysteresis and those applications to the ZrMn2-H2systems[J].J.Alloys Compd., 1998, 278 (1-2) :194.
[10] Reule H, Hirscher M, Weihardt A, Kronm��ller H.Hydrogen desorption properties of mechanically alloyed MgH2composite materials[J].J.Alloys Compd., 2000, 305:246.
[11] Zuttel A, Wenger P, Rentsch S, Sudan P, Mauron P, Emmenegger C.LiBH4a new hydrogen storage material[J].J.Power Sources, 2003, 118:1.
[12] Zuttel A, Rentisch S.Hydrogen storage properties of LiBH4[J].Journal of Alloys and Compounds, 2003:356-357, 515.
[13] Friedrichs O, Buchter F, Borgschulte A, Remhofa A, Zwickyb C, Maurona Ph, Bielmanna M, Z��ttela A.Direct synthesis of LiBH4and LiBD4 from the elements[J].Acta Mater, 2008, 56 (5) :949.
[14] Vajo J J, Skeith S L, Mertens F.Reversible storage of hydrogen in destabilized LiBH4[J].Phys.Chem.B, 2005, 109:3719.
[15] Vajo J J, Salguero T T, Gross A F, Skeith S L, Olson G L.Thermodyamie destabilization and reaction kineties in light metal hydride systems[J].Journal of Alloys and Compounds, 2007, 446-447:409.
[16] Wan X F, Markmaitree T, Osborn W.Nanoengineering-enabled solid state hydrogen up take and release in the LiBH4plus MgHz system[J].J.Phys.Chem.C, 2008, 101 (41) :1005.
[17] Vajo J J, Olson G L.Hydrogen storage in destabilized chemical systems[J].Scr.Mater., 2007, 56:829.
[18] Nakamori Y, Miwa K, Ninomiya A, Li H, Ohba N, Towata S, Z��ttel A, Orimo S.Correlation between thermodynamical stabilities of metal borohydrides and cation electronegatives:first-principles calculations and experiments[J].Phys.Rev.B, 2006, 74 (4) :045126.
[19] Orimo S, Nakamori Y, Kitahara G, Miwa K, Ohba N, Towata S, Z��ttel A.Dehydriding and rehydriding reac-tions of LiBH4[J].J.Alloys Compd., 2005, 404-406:427.
[20] Xia L S, Zhu S H.Mechanism of dehydrogenation of Al-LiBH4system[J].Chinese Journal of Rare Metals, 2013, 37 (4) :511. (������, ������.Al-LiBH4��ϵ�������ܵĻ����о�[J].ϡ�н���, 2013, 37 (4) :511.
[21] Hagemann H, Longhini M, Kaminski J W, Wesolowski T A, Cern��R, Penin N, S�irby M H, Hauback B C, Severa G, Jensen C M.LiSc (BH4) 4:a novel salt of Li+and discrete Sc (BH4) 4complex anions[J].J.Phys.Chem.A, 2008, 112 (33) :7551.
[22] Yin L C, Wang P, Fang Z Z, Cheng H M.Thermodynamically tuning LiBH4by fluorine anion doping for hydrogen storage:a density functional study[J].Chem.Phys.Lett., 2008, 450:318.
[23] Kostka J, Lohstroh W, Fichtner M, Hahn H.Diborane release from LIBH4/Siliea gel mixtures and the effect of additives[J].Journal of Physical Chemistry C, 2007, 111 (37) :14026.
[24] Yu X B, Grant D M, Walker G S.Low-temperature dehydrogenation of LiBH4through destabilization with TiO2[J].J.Phys.Chem.C, 2008, 112:11059.
[25] Guo W W.Investigation on There Hydrogenation and Dehydrogenation of LiBH4by Adding Single-Walled Carbon Nanotubes[D].Shenyang:Shenyang University, 2010.58. (������.����SWNTS��LiBH4����������Ӱ����о�[D].����:������ѧ, 2010.58.)
[26] Au M, Jurgensen A R, SPeneer W A, Anton D L, Pinkerton F E.Stability and reversibility of lithium borohydrides doped by metal halides and hydrides[J].Journal of Physical Chemistry C, 2008, 112 (47) :18661.
[27] Fang Z Z, Ma L P, Kang X D, Wang P J, Wang P, Cheng H M.In situ formation and rapid decomposition of Ti (BH4) 3by mechanical milling LiBH4with TiF3[J].Applied Physics Letters, 2009, 94 (4) :342.
[28] Opalka S M, Tang X, Laube B L, Vanders Purt T H.Experimental and theoretical screening of nanoscale oxide reactivity with LiBH4[J].Nanotechnology, 2009, 20 (20) :16949.
[29] Gross A F, Vajo J J, Vanatta S L, Olson G L.Enhanced hydrogen storage kinetics of LiBH4in nanoporous carbon scaffolds[J].Acta Mater., 2008, 112:5651.
[30] Fang Z Z, Wang P, Rufford T E, Kang X D, Lu G Q, Cheng H M.Kinetic and thermodynamic based improvements of lithium borohydride incorporated into activated carbon[J].Acta Mater., 2008, 56 (20) :6257.
[31] Zhang Y, Zhang W S, Wang A Q, Sun L X, Fan M Q, Chu H L, Sun J C, Zhang T.LiBH4nanoparticles supported by disordered mesoporous carbon:hydrogen storage performances and destabilization mechanisms[J].Int.J.Hydrogen Energy, 2007, 32:3976.
[32] Yu X B, Wu Z, Chen Q R, Li Z L, Weng B C, Huang T S.Improved hydrogen storage properties of LiBH4destabilized by carbon[J].Applied Physics Letters, 2007, 90 (3) :034106-3.