不同晶相MnO2催化剂的NH3-SCO反应性能
来源期刊:稀有金属2021年第2期
论文作者:马俊洋 刘丹丹 王丽 黄泱 郭耘
文章页码:177 - 186
关键词:不同晶相;MnO2;NH3-SCO;隧道结构;
摘 要:以柴油车尾气净化过程中氨逃逸的治理为背景,采用水热合成法制备了不同晶相(α-,β-和δ-)MnO2、并考察晶相结构对低温氨气选择性催化氧化(NH3-SCO)反应性能的影响;并运用多种手段,如X射线衍射(XRD)、扫描电子显微镜(SEM)、氮气低温吸-脱附、X射线光电子能谱(XPS)、氢气程序升温还原(H2-TPR)、氧气程序升温脱附(O2-TPD)、氨气程序升温脱附(NH3-TPD)等对催化剂的组织结构、化学状态和氧化还原性能进行表征。研究结果发现MnO2的晶相结构和隧道结构与氨气选择性催化氧化反应性能密切相关。具有独特的[2×2]隧道结构的α-MnO2具有最佳的反应性能,NH3可在175℃实现全转化且N2选择性为94%,其在120℃时的反应速率是具有层状结构δ-MnO2的12倍。α-MnO2表面具有较高的Mn3+/Mn4+比有利于催化剂氧化还原性能的提高和对氧的活化,丰富的酸中心和酸量有助于对NH3吸附和活化;二者的共同作用使得该催化剂具有良好的反应性能。
网络首发时间: 2019-09-23 15:53
稀有金属 2021,45(02),177-186 DOI:10.13373/j.cnki.cjrm.xy19050035
马俊洋 刘丹丹 王丽 黄泱 郭耘
以柴油车尾气净化过程中氨逃逸的治理为背景,采用水热合成法制备了不同晶相(α-,β-和δ-)MnO2、并考察晶相结构对低温氨气选择性催化氧化(NH3-SCO)反应性能的影响;并运用多种手段,如X射线衍射(XRD)、扫描电子显微镜(SEM)、氮气低温吸-脱附、X射线光电子能谱(XPS)、氢气程序升温还原(H2-TPR)、氧气程序升温脱附(O2-TPD)、氨气程序升温脱附(NH3-TPD)等对催化剂的组织结构、化学状态和氧化还原性能进行表征。研究结果发现MnO2的晶相结构和隧道结构与氨气选择性催化氧化反应性能密切相关。具有独特的[2×2]隧道结构的α-MnO2具有最佳的反应性能,NH3可在175℃实现全转化且N2选择性为94%,其在120℃时的反应速率是具有层状结构δ-MnO2的12倍。α-MnO2表面具有较高的Mn3+/Mn4+比有利于催化剂氧化还原性能的提高和对氧的活化,丰富的酸中心和酸量有助于对NH3吸附和活化;二者的共同作用使得该催化剂具有良好的反应性能。
中图分类号: TQ426;X734.2
作者简介:马俊洋(1991-),男,河南南阳人,硕士研究生,研究方向:环境催化,E-mail:173409656@qq.com;;*王丽,副教授,电话:021-64253703,E-mail:wangli@ecust.edu.cn;
收稿日期:2019-05-31
基金:上海浦江计划项目(18PJD019)资助;
Ma Junyang Liu DANDan Wang Li Huang Yang Guo Yun
Key Laboratory for Advanced Materials and Research Institute of Industrial Catalysis,College of Chemistry and Molecular Engineering,East China University of Science and Technology
China Tabacoo Zhejing Industrial Co.Ltd.
Abstract:
With the increase of automobiles,the emission of NOx worsensed the atmosphere in the case of photochemical smog and acid rain.How to efficiently remove NOx became urgent for environment protection.Although NH3 selective catalytic reduction of NOx was a mature technology for reducing NOx emission.To efficiently remove NOx,the over stoichiometric NH3 in application resulted in the NH3 slip causing serious environmental pollution and endangered human health.NH3 slip could be avoided by ammonia selective catalytic oxidation(NH3-SCO) technology, which could convert NH3 into N2 and H2 O in an oxidizing atmosphere.MnO2 had been widely used in catalytic fields because of its good low-temperature catalytic activity,and its reaction performance was closely related with crystal phase structure.Mn-based catalysts with different crystallization phases,α-,β-and δ-MnO2 prepared by hydrothermal synthesis,were investigated for NH3-SCO.The physical and chemical properties of the catalysts were characterized by X-ray diffraction(XRD),scanning electron microscope(SEM),N2 adsorption-desorption and X-ray photoelectron spectroscopy(XPS).Meanwhile,the redox property was tested by oxygen temperature programmed desorption(O2-TPD) and H2 temperature programmed reduction(H2-TPR),and acid by ammonia temperature programmed desorption(NH3-TPD).According to the test results,the order of catalyst activity and N2 selectivity followed the sequences:α-MnO2> β-MnO2>δ-MnO2.Complete conversion of NH3 were achieved on α-MnO2 at175℃.with 94% N2 selectivity,and the by-products were N2 O and NO.The reaction rates(120 ℃) and low reaction energy also confirmed α-MnO2 was most active in NH3-SCO,whose reaction rate was 12 times higher than that of δ-MnO2.Considering the byproducts,it was worth mentioning that except N2 O and NO,NO2 was also detected on β-MnO2 and δ-MnO2.SEM results showed that MnO2 with different crystalline phase,α-,β-and δ-MnO2 were in the form of nanowire with(2×2) tunnel structure,nano rod with(1×1)tunnel structure and flowerlike with layered stack structure,respectively.The particle size of δ-MnO2 was 12.4 nm,while it was up to23.2 nm on β-MnO2.XPS displayed that the ratio of Mn3+/Mn4+ on α-MnO2 was up to 2.24 with the lowest average of oxidation state(AOS) of Mn(3.49),and the ratio was only 0.79 on δ-MnO2 with the highest average of oxidation state(AOS) of Mn(3.83).The increase in the Mn oxidation state led to the decrease in the amount of adsorbed oxygen.In the H2-TPR profiles,it was found that α-MnO2 had the lowest onset reduction temperature indicating the easily reducible property of α-MnO2.Compared with the O2-TPD profiles of β-MnO2,it was found that the onset temperature for O2 desorption was much lower on α-MnO2 and δ-MnO2.Furthermore,a broad and intensive O2 desorption peak was found showing the high amount of adsorbed oxygen species on α-MnO2.Acidity and amounts played an important role in ammonia adsorption and activation,so NH3-TPD were conducted.It was shown in the NH3-TPD results that the distribution of acid sites and the acid amount were closely related with the crystalline phases.Strong acid sites and the highest total acid amount were found on β-MnO2,in contrast,the lowest total acid amount with even distribution of strong and weak acid sites were detected on δ-MnO2.The increase in the highest total acid amount were beneficial to ammonia adsorption,and the optimum acid strength would further favor ammonia activation.Based on the test and characterization results,nanowire β-MnO2 with(2×2) tunnel structure had higher ratio of Mn3+/Mn4+ which was beneficial to the improvement in redox and oxygen activation.Meanwhile,different kinds of acid center and abundant acid amount on the surface favored the adsorption and activation of NH3.So,the combination of the two properties made α-MnO2 own the high performance in NH3-SCO.
Keyword:
different crystallization phases; manganese dioxide; NH3-SCO; channel structure;
Received: 2019-05-31
氮氧化物(NOx)是大气污染主要成分之一,主要来源于固定源和移动源的尾气排放,用氨选择性催化还原(NH3-SCR)NOx技术可有效地消除NOx
锰是一种常见的过渡金属,因其多种可变价态而具有较好的催化性能。Mn O2是众多锰氧化合物之一,基本组成单元是Mn O6八面体,可通过共棱或共角的连接方式形成不同晶相结构的Mn O2,如α-,β-和δ-Mn O2
不同晶相的Mn O2催化剂的隧道结构不同,进而也决定了孔道结构中不同阳离子的存在
图1 不同晶相Mn O2的晶体结构
Fig.1 Crystal structure of Mn O2in different phases
(a)α-Mn O2;(b)β-Mn O2;(c)δ-Mn O2
不同晶相Mn O2的物理化学性质不同,其在不同反应中表现出来的性能也不相同。Shi等
以上可知,具有不同晶相结构Mn O2的反应性能与催化反应体系密切相关;因此需要进一步研究Mn O2晶相结构对NH3-SCO的影响。本文采用水热法制备了不同晶相的α-,β-和δ-Mn O2,研究晶相结构不同对NH3-SCO反应的影响;并通过多种手段对其结构、化学性质、氧化还原性能进行表征,以期建立反应性能和结构之间的关系。
1 实验
1.1 催化剂的制备
α-Mn O2:称取1.4 g KMn O4和2.25 g Mn SO4・H2O溶解于去离子水中,在160℃下水热反应12 h,冷却后抽滤、洗涤,60℃干燥12 h,350℃空气焙烧3 h。β-Mn O2:称取0.5 g KMn O4和2.5 g Mn SO4・H2O溶解于去离子水中,在140℃下水热反应12 h,冷却后抽滤、洗涤,100℃干燥12 h,350℃空气焙烧3 h。δ-Mn O2是由2.8 g KMn O4和0.5 g Mn SO4・H2O水热合成,其他反应条件与制备β-Mn O2一致。
1.2 催化剂活性评价
称取0.1 g催化剂放入直径为4 mm的石英反应管中,通入500×10-6NH3和5%O2,Ar为平衡气,气体流量为200 ml・min-1。反应气体浓度分析采用NEXUS6700-FTIR红外光谱仪进行。
NH3的转化率(NH3conversion)和N2,N2O,NOx选择性(N2selectivity,NO selectivity,NOxselectivity)计算公式如下:
1.3 催化剂的表征
1.3.1 X射线衍射(XRD)
样品的XRD表征在Bruker D8 Focus型X射线衍射仪器上进行。入射光源采用Cu靶Kα射线(λ=0.15406 nm),管电压40 k V,管电流40 m A,广角衍射的扫描范围为2θ=10°~80°,扫描速率为6(°)・min-1,扫描步幅为0.02°。
1.3.2 N2低温吸脱附(N2adsorption-desorption)
氮气低温吸附脱附曲线在NOVA 4200e Surface Area&Pore Size型比表面积吸附仪上进行,温度为-196℃。样品在测试前均在180℃真空脱气6 h。
1.3.3 扫描电子显微镜(SEM)
SEM在Hitachi公司的扫描电子显微镜S-3400N上测得,电子加速电压为5~30 k V。样品通过干撒法进行制样,样品测试前要进行镀金处理。
1.3.4 H2程序升温还原(H2-TPR)
H2-TPR表征在天津鹏翔科技有限公司制造的装置上进行。称取25 mg的250~375μm样品置于U形石英微型反应器中,其中反应气为10%H2/N2混合气(40 ml・min-1),待基线稳定后以10℃・min-1程序升温至600℃,采用热导检测器(TCD)记录程序升温中H2的浓度变化,并以商业Cu O为标准计算耗氢量。
1.3.5 O2程序升温脱附(O2-TPD)
样品的O2-TPD表征在Auto-Chem II装置上进行。将25 mg催化剂在20%O2/He(40 ml・min-1)、400℃预处理1 h,然后降温至50℃;然后Ar吹扫到基线稳定。以10°C・min-1的升温速率升温至800℃,使用HPR-20 QIC质谱记录O2(质子数/电荷数的比值(m/z)=32)的信号。
1.3.6 NH3程序升温脱附(NH3-TPD)
NH3-TPD在天津鹏翔科技有限公司的催化剂表征实验装置上测定。取25 mg催化剂置于U型石英管中,在50ml・min-1Ar气氛中以10°C・min-1升温至催化剂的焙烧温度,预处理1 h,降至室温后吸附10%NH3/Ar(50 ml・min-1)1 h,再在室温下用Ar吹扫1.5 h除去弱吸附的NH3,待基线平稳后,以10°C・min-1升温至800°C,TCD检测器记录脱附的NH3。
1.3.7 X射线光电子能谱(XPS)
样品表面元素分析是在美国Thermo ESCALAB 250Xi仪器上进行检测。光源使用单色Al Kα靶(hv=1486.6 e V),功率150 W,能量分析器固定透过能为30 e V,数据经过校正处理,样品C 1s主峰的结合能定在284.8 e V。
2 结果与讨论
2.1 不同晶相Mn O2对NH3-SCO催化反应性能的影响
图2为不同晶相Mn O2的NH3-SCO反应的NH3转化率,N2以及副产物NO2,N2O和NO的选择性曲线图。催化剂在NH3转化率为90%的温度(T90)和N2选择性见表1。其中,活性最好的α-Mn O2的T90比活性最差的δ-Mn O2低了130℃左右,N2选择性高了近40%,α-Mn O2在175℃实现NH3的全转化,N2选择性高达94%;而δ-Mn O2的NH3全转化温度则高于300℃,其N2选择性随着反应温度显著下降。对尾气进行分析可知,其含氮副产物主要有N2O,NO和NO2,其副产物分布与Mn O2晶相有关。另外,副产物种类及含量的不同可能与NH3反应路径不同相关。
在排除内外扩散的影响条件下,进行了动力学相关实验,通过Arrhenius曲线得到反应的本征活化能,结果见表1及图3。
通过比较反应温度在120℃时的反应速率,发现α-Mn O2的反应速率(4.98×10-7mol・g-1・s-1);是δ-Mn O2反应速率的12倍。为了排除比表面积对反应性能的影响,计算了比活性(见表1),发现α-Mn O2具有最高的比活性。
比较催化剂的表观活化能(Ea)发现δ-Mn O2的活化能低于α-Mn O2活化能,这与不同晶相Mn O2的反应速率顺序矛盾,这是由于Mn O2在反应过程中存在补偿效应所致。
为了验证补偿效应是否存在,将ln A和Ea之间的对应关系进行了研究,其中A为指前因子。研究发现ln A和Ea满足Cremer-constable关系式,其中,m为斜率,c为常数(图4)
图2 不同晶相Mn O2对NH3-SCO的反应活性
Fig.2 NH3-SCO activity of Mn O2catalysts with different crystallization phases
(a)NH3conversion and N2selectivity;(b)N2O selectivity;(c)NO2selectivity;(d)NO selectivity
图3 不同晶相Mn O2催化剂的Arrhenius曲线
Fig.3 Arrhenius curves of Mn O2catalysts with different crys-tallization phases
这也验证了不同晶相Mn O2在反应过程中确实存在补偿效应。
图4 Mn O2催化剂在NH3催化氧化反应中的ln A与Ea之间的关联
Fig.4 ln A as a function of Eafor NH3oxidation on Mn O2cata-lysts
2.2 催化剂表征
2.2.1 XRD分析
图5为不同晶相Mn O2催化剂的XRD谱图。通过与标准卡片对比,图5(1)的特征衍射峰应于四方晶系α-Mn O2(JCPDS 44-0141),晶胞参数为a=0.9785 nm,c=0.2863 nm。图5(2)的特征衍射峰对应于四方晶系β-Mn O2(JCPDS 24-0735),晶胞参数为a=0.44 nm,c=0.2874 nm。图5(3)的特征衍射峰对应于单斜相的δ-Mn O2(JCP-DS80-1098),晶胞参数为a=0.5149 nm,b=0.2843nm,c=0.7176 nm。
可以看出,β-Mn O2的结晶度高,晶型完好。相反,α-和δ-Mn O2的衍射峰强度都较低且峰形较宽,结晶度相对较差,说明其表面缺陷较多。根据Scherrer方程计算出Mn O2的平均晶粒大小,结果见表1。β-Mn O2的晶粒尺寸最大(23.1 nm)。δ-Mn O2具有最小的晶粒尺寸(12.4 nm),而α-Mn O2的晶粒尺寸介于两者之间,为19.6 nm。
2.2.2 SEM和BET分析
图5 不同晶相Mn O2的XRD谱图
Fig.5 XRD patterns of Mn O2with different crystallization phases
表1 不同晶型Mn O2的比表面积(SBET),晶粒尺寸及动力学参数 下载原图
Table 1 Specific surface area(SBET),crystal size,and kinetic parameters of Mn O2catalysts with different crystal structures
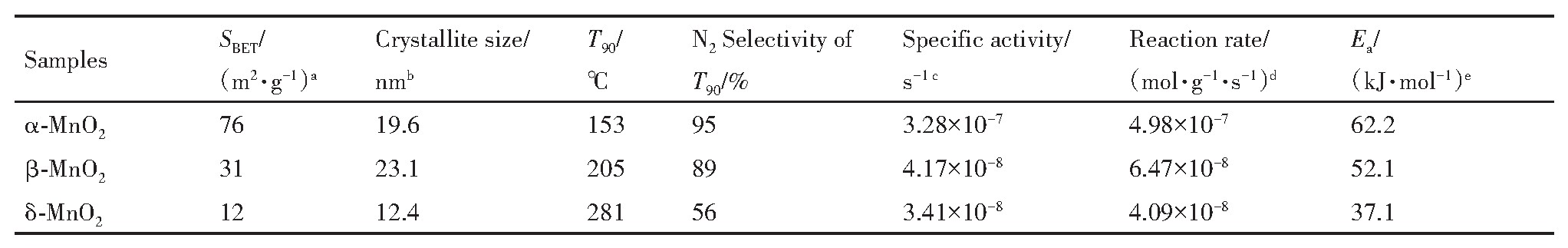
aMeasured by N2absorption desorption experiment,bCalculated from Scherrer equation,c-dSpecific activity and reaction rate at 120℃,eActivation energy is measured by kinetic experiments
不同晶相Mn O2的SEM结果见图6。α-Mn O2呈现为不规则的纳米线,直径为32~53 nm,长度为1.5~3.0μm。与α-Mn O2相比,β-Mn O2纳米棒状的直径大(50~110 nm)、长度小(0.5~1.6μm)。与α-和β-Mn O2不同,δ-Mn O2表现为大小为0.4~0.6μm花球状的纳米颗粒。由于Mn O6八面体的不同连接方式形成了不同隧道结构的Mn O2相,可以推测Mn O2的隧道结构以及形貌是影响其催化活性的重要因素之一。
具有一维结构的Mn O2(α-和β-Mn O2)比二维层状δ-Mn O2更有利于NH3的选择性催化氧化反应。对于同为一维结构的Mn O2,α-Mn O2的孔道尺寸大于β-Mn O2,更有利于NH3和O2的吸附活化,从而表现出较好的催化活性。在以下部分中继续讨论其他因素的影响。
此外,由表1可知,纳米线α-Mn O2的比表面积为76 m2?g-1,远高于其他晶相Mn O2的比表面积;δ-Mn O2比表面积约为β-Mn O2的比表面积的1/3。催化剂的比表面积越高越则暴露的活性位越多,从而有利于反应的发生。
2.2.3 NH3-TPD表征
催化剂表面酸性对NH3-SCO催化反应起着重要的作用,通过NH3-TPD探究不同晶相Mn O2的表面酸中心的分布及酸浓度情况,结果见图7。
在100~600℃的温度区间观察到NH3在不同温度区间的脱附峰,其中100~300℃低温区脱附峰归属为吸附于弱酸位上的NH3脱附峰;而300~600℃高温区脱附峰归属为吸附于中强酸位上的NH3脱附峰
图6 不同晶相Mn O2的SEM图
Fig.6 SEM images of Mn O2with different crystallization phases
(a1,a2)α-Mn O2;(b1,b2)β-Mn O2;(c1,c2)δ-Mn O2
图7 不同晶相的Mn O2的NH3-TPD谱图
Fig.7 NH3-TPD patterns of Mn O2with different crystallization phases
α-Mn O2和δ-Mn O2在低温区和高温区均检测到NH3的脱附峰,表明催化剂表面存在不同强度的酸中心。β-Mn O2仅在高温区出现NH3的脱附峰,表明其表面以强酸中心为主。对于NH3-SCO反应,NH3的吸附和活化是反应的第一步
对NH3的脱附峰进行积分,并将δ-Mn O2脱附峰面积定义为1;将其他催化剂的脱附峰面积与之相比,得到相对酸量,结果见表2。由结果可知,α-Mn O2比δ-Mn O2具有更高的酸浓度。这与Dai等
此外,对于α-Mn O2和δ-Mn O2,其弱酸中心与强酸中心的分布不同,其中α-Mn O2弱酸中心与强酸中心分布均匀,而δ-Mn O2表面的弱酸中心更高。β-Mn O2表面以强酸中心为主,其与NH3之间的相互作用强反而不利于活化;相反,α-Mn O2和δ-Mn O2表面具有不同强度的酸中心则有利于NH3的活化。
2.2.4 H2-TPR和O2-TPD表征
表2 催化剂的耗氢量,Mn的平均氧化态,相对氧/酸浓度以及XPS结果 下载原图
Table 2 H2consumption,AOS of Mn,relative concentration of oxygen/aicd,and XPS results of catalysts
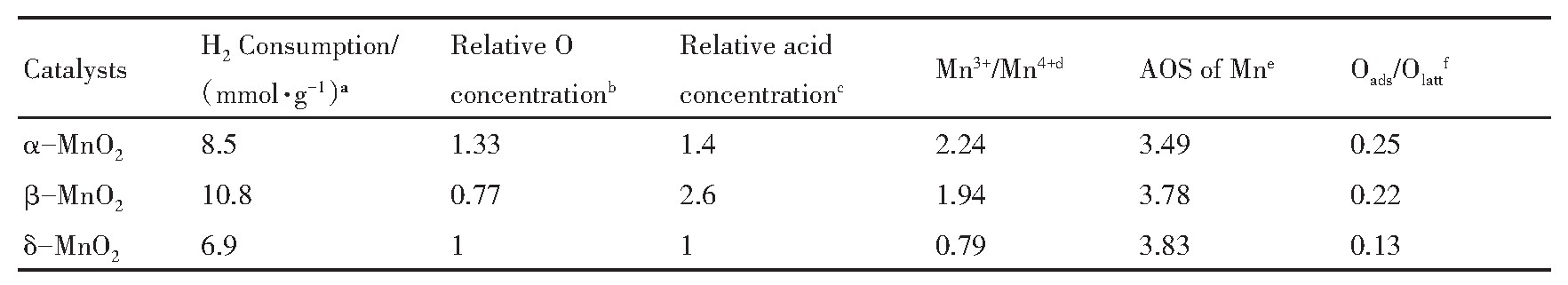
aH2consumption of catalyst obtained by H2-TPR,bRelative O concentration of catalyst obtained by O2-TPD,cRelative acidconcentration of catalyst obtained from NH3-TPD,d-fComes from XPS data
除表面酸碱性外,催化剂的氧化还原能力以及对氧气活化能力与催化剂的反应性能密切相关
根据文献报道
由图8(a)可知,α-Mn O2在338℃出现了强还原峰并伴有肩膀峰(316℃);通过卷积分处理发现峰面积比约为1∶1,因此其还原过程为Mn O2→Mn2O3→Mn O。且还原过程有部分重叠。而β-Mn O2
在343和442℃处出现了两个明显的还原峰,且还原峰面积比约为2∶1,其还原路径为Mn O2→Mn3O4→Mn O。δ-Mn O2仅在350℃处出现一个还原峰,表明其还原成Mn2O3或Mn3O4中间产物再还原成Mn O的还原过程发生完全重叠、或者由Mn O2一步还原到Mn O
由图8(b)可知,不同晶相的Mn O2在400℃以下氧的脱附峰强度不同,该温度段的氧脱附峰是参与表面反应的表面吸附氧的脱附峰
另外,α-Mn O2对应的起始脱附峰温度较低,表明其表面吸附氧可在较低温度脱附,进而有利于氧化反应的进行。
2.2.5 XPS表征
为了探究催化剂表面Mn和O元素的化学组成和状态,对不同晶相Mn O2进行了XPS表征。
图8 不同晶相的Mn O2的H2-TPR和O2-TPD谱图
Fig.8 H2-TPR(a)and O2-TPD(b)profiles of Mn O2with different crystallization phases
图9 不同晶相Mn O2的Mn 2p3/2和O 1s的XPS谱图
Fig.9 (a)Mn 2p3/2and(b)O 1s XPS spectra of Mn O2with different crystallization phases
由图9(a)可知,催化剂表面存在3种状态的Mn物种,结合能为(643.5±0.1),(642.3±0.2)和(641.2±0.1)e V的峰分别对应于Mn4+,Mn3+和Mn2+物种
由图9(b)所示O 1s的XPS谱图中发现催化剂表面存在3种不同类型的氧物种。结合能为529.0~530.1 e V的峰归属于与锰结合的晶格氧(O2-:标记为Oα);结合能为531.4 e V的峰归属于表面化学吸附氧物种(如以-OH和CO32-形式存在的O22-和O-:标记为Oβ)
3 结论
通过水热法制备了α-Mn O2,β-Mn O2和δ-Mn O2,发现Mn O2的晶相结构对NH3-SCO反应性能影响显著,催化剂的活性和N2选择性从高到低的顺序为:α-Mn O2>β-Mn O2>δ-Mn O2。具有[2×2]隧道结构的α-Mn O2在175℃实现NH3的全转化、且N2选择性高达94%。其反应速率(120℃)是具有层状结构δ-Mn O2的12倍。具有独特的隧道结构[2×2]α-Mn O2纳米线其Mn3+/Mn4+比例高有利于提高对氧的活化、而丰富的酸中心和酸量有利于NH3吸附和活化;二者的共同作用使得α-Mn O2具有良好的NH3选择性氧化的能力。
参考文献

