诺氟沙星-壳聚糖微球的制备及释药性能
薛昌刚,童春义,肖苏尧,王 贝,俞丹密,唐冬英,刘选明
(湖南大学 生命科学与技术研究院,化学生物传感与计量学国家重点实验室,湖南 长沙,410082)
摘 要:利用乳液-化学交联法,用水溶性壳聚糖(CS)与诺氟沙星(NFX)制备诺氟沙星-壳聚糖微球(NFX-CSM)。根据正交实验设计,考察投料比、交联剂用量、转速和反应温度对质量指标的影响,选出最佳制备工艺条件;利用扫描电镜,红外光谱和Zeta电位仪对载药微球进行表征;用药物溶出度仪检测NFX-CSM在不同pH值环境下的释药速率,并考察不同交联剂用量和投料比((m(CS)?m(NFX))所制备的载药微球对释药速率的影响;将大肠杆菌与NFX-CSM共培养,检测载药微球的抗菌效果。研究结果表明:在最佳制备工艺条件下,制得载药微球的平均粒径约为4 μm,球形圆整,分散性好,载药量和包封率分别为4.9%和42.3%;载药微球在不同pH值环境下均对药物有良好的缓释效果,其释药速率随交联剂用量的增加和投料比的增大而变小;NFX在CSM的协同抗菌作用下,抗菌效果明显增强。
关键词:诺氟沙星;壳聚糖;微球;抗菌性;协同作用
中图分类号:O636.1;R978.1 文献标识码:A 文章编号:1672-7207(2008)03-0480-06
Preparation of norfloxacin-chitosan microsphere and
its drug release property
XUE Chang-gang, TONG Chun-yi, XIAO Su-yao, WANG Bei, YU Dan-mi,
TANG Dong-ying, LIU Xuan-ming
(Insitute of Life Science and Technology, State Key Laboratory of Chemo/Biosensing and Chemometrics,
Hunan University, Changsha 410082, China)
Abstract: Norfloxacin(NFX)-chitosan(CS) microsphere(NFX-CSM) was prepared by using water-soluble CS and NFX with emulsification and cross-linking process. Orthogonal design based on 4 factors: the feed ratio of CS to NFX, dosage of crosslinker, stirring speed and temperature, was studied to determine the optimum preparing technique of microsphere. NFX-CSM was characterized via scanning electron microscope, Fourier transform infrared spectrometer and Zeta potential measurement. The release speed of NFX was determined under different pH conditions with the dissolution apparatus. Effects of dosage of crosslinker and feed ratio of CS to NFX on drug release were examined. Antibacterial property was tested while E. coli and NFX-CSM were co-cultured. The results show that NFX-CSM has good shape and dispersibility with the average particle size of about 4 μm; the drug loading and drug encapsulation efficiency of NFX-CSM are 4.9% and 42.3%, respectively; the sustained release is remarkable under different pH conditions; the drug release speed is decreased with the increase of feed ratio of CS to NFX and dosage of crosslinker. The antibacterial effect of NFX is improved obviously in the synergetic action of CS microsphere.
Key words: norfloxacin; chitosan; microsphere; antibacterial property; synergetic action
诺氟沙星属于氟喹诺酮类抗菌药,具有广谱抗菌作用,是最常用的肠道类抗菌药品之一,对大肠杆菌、痢疾杆菌等革兰阴性菌有高度抗菌活性。但是,诺氟沙星几乎不溶于水、乙醇、甲醇和乙醚,而易溶于盐酸和氢氧化钠,其脂溶性较差,药物穿透能力不强,生物利用度低[1]。口服诺氟沙星时,它首先在胃中大量溶解,到达肠道后药物利用率不高,在临床应用上有时造成给药量较大而引起多种副作用[2-3],主要表现在对消化系统、肝脏、血液系统、神经系统、肾脏系统、关节等的毒性。近年来,有研究报道通过添加不同的缓释辅料来改善氟喹诺酮类药物的副作用,常用的材料主要有醋酸纤维、PEG、聚乳酸等生物可降解材料[4],但是将抗菌性能优良的壳聚糖分子制成微球作为载体来装载诺氟沙星的研究报道很少。
壳聚糖具有生物可降解性和良好的生物相容性,是一种常用的天然药物、基因载体材料[5-10]。壳聚糖具有很强的亲水性,在酸溶液中膨胀形成胶体,可以减缓所载药物在胃液中的扩散及溶出,从而使更多的药物进入肠道中,因此,可以作为结肠耙向药物载 体[11]。壳聚糖及其衍生物本身又具有优异的广谱抗菌性,当制成纳米粒时,抗菌性能递增[12]。水溶性壳聚糖是壳聚糖经羧化改性而制成,与普通壳聚糖相比,其生物相容性更好,更易降解,性质更稳定,抑菌活性更优[13],作为药物载体时,不降低pH值敏感药物的抗菌活性[14],因此,水溶性壳聚糖适合作为具有pH值敏感特性的诺氟沙星的药物载体。在此,本文作者用诺氟沙星和水溶性壳聚糖制备诺氟沙星-壳聚糖微球,并对载药微球进行药物释放和体外抗菌性能的检测。
1 实 验
1.1 试剂与仪器
药品和试剂为:诺氟沙星(NFX,购自Sigma公司);水溶性壳聚糖(CS,平均相对分子质量为5 000,浙江玉环县海洋生物化学有限公司生产);其他药品和试剂均为分析纯;大肠杆菌由本实验室提供。
仪器为:JSM-5600LV扫描电子显微镜(日本JEOL电子公司制造);WQF-410型傅里叶变换红外光谱仪(北京瑞利分析仪器公司制造);Zetasizer 3000Hs电位粒度分析仪(英国Malvern公司制造);5810R高速离心机(德国Eppendorf公司制造);Himac CR 22G高速低温离心机(日本Hitachi公司制造);Rcz-6c1药物溶出度仪(上海黄海药检仪器厂制造);UV-1600紫外可见分光光度计(北京瑞利分析仪器公司制造);超纯水系统(美国Millipore公司制造)。
1.2 诺氟沙星-壳聚糖微球(NFX-CSM)的制备
称取0.25 g水溶性CS,溶于8 mL超纯水中,轻微振荡至溶液清亮。称取一定量NFX溶于2 mL 0.1 mol/L的盐酸溶液中,待完全溶解后,将NFX的盐酸溶液加入到CS水溶液中,搅拌使其混合均匀。混合物缓慢加入到盛有100 mL石蜡油的三颈烧瓶中,以2%的Span80作为乳化剂,高速搅拌30 min,形成稳定的微乳 液,然后,加入一定量的戊二醛作为交联剂,搅拌反应3 h。用丙酮破乳、离心,然后,用无水乙醇和丙酮交替洗涤沉淀并离心,沉淀冷冻干燥,得到橙黄色粉末(NFX-CSM)。采用同样方法,不加药物,制得空白壳聚糖微球(CSM)。
1.3 样品的表征及性能检测
1.3.1 NFX-CSM形貌及结构表征
采用扫描电子显微镜(SEM)对NFX-CSM样品形貌进行观察;用傅里叶变换红外光谱仪(FTIR)对NFX-CSM样品进行红外光谱测试。
1.3.2 CSM在酸溶液中的电位检测
将CSM溶于弱酸中,用Zeta电位仪检测其电位。
1.3.3 NFX-CSM载药量和包封率的检测
将NFX-CSM加入到50 mL 0.1 mol/L的盐酸溶液中,于80 ℃水浴加热,待NFX-CSM完全降解后,用紫外-可见分光光度计检测NFX的含量,以CSM为对照,检测波长为277 nm。以纯NFX的盐酸溶液 (0.1 mol/L)作标准曲线,标准吸收曲线方程为:Y=111.885X+0.010 05(线性相关系数r=0.999 8)。载药量S1和包封率S2的计算式如下:

1.3.4 NFX-CSM释药速率检测
配制3种不同pH值的缓冲液,考察载药微球在不同释放介质中的释药情况。介质分别为:pH=2.0的酸性缓冲液(模拟胃液环境);pH=7.2的PBS磷酸盐缓冲液(模拟结肠环境);pH=9.0的弱碱缓冲液(模拟大肠环境)。在药物溶出仪上固定4个容积为250 mL的溶出杯,分别加入不同的释放介质溶液各100 mL,以50 mg NFX在pH=2.0介质中的释放情况作为参照,其他3个溶出杯各加入50 mg NFX-CSM,在37 ℃以100 r/min转速搅拌,定时取出3 mL释放液,测其吸光度,每次取液后补充等量相应介质溶液,然后,根据标准曲线方程计算其浓度,绘制累计释药率-时间曲线。另外,考察不同交联剂用量和不同投料比制备的微球对释药速率的影响。
1.3.5 药物缓释对大肠杆菌生长的影响
取200 mL活化后的大肠杆菌菌液,加入到20 mL LB液体培养基中,然后,加入一定量的NFX-CSM溶液,振荡培养,每隔30 min取100 mL共培养菌液,用紫外分光光度计检测OD600值,以载药微球中相同量的NFX和CSM作为对照。OD值越大,表示大肠杆菌浓度越高,生长越旺盛,药物的抗菌作用越弱,假设不加任何药物,大肠杆菌的OD值为A0,加入药物后的OD值为A1,则药物对细菌的抑制率η为:
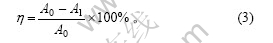
然后,根据抑制率比较NFX和NFX-CSM的抗菌效果。
2 结果与讨论
2.1 正交实验优选最佳工艺
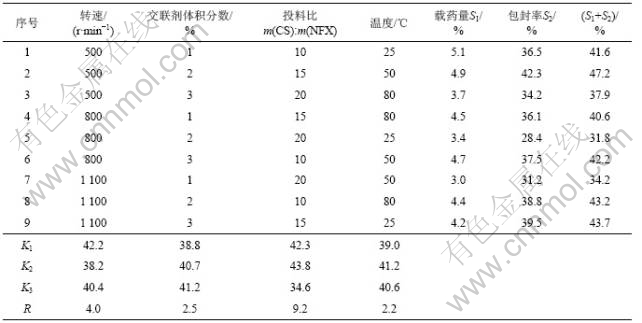
在单因素考察法的基础上,选定投料比(m(CS)?m(NFX))、交联剂在反应体系中所占体积分数、转速和反应温度4个因素,各分3个水平,按L9(34)正交实验设计要求,对不同因素和水平列出9种组合进行分析(见表1)。根据微球的载药量(S1)和包封率(S2)综合评价(S1+S2),选出最佳制备工艺条件。由表1中的级差R可知,各因素对载药微球的载药量和包封率综合影响由大至小依次为:投料比,转速,交联剂用量,反应温度。根据4个考察因素的K1,K2和K3得知,选定转速为500 r/min、交联剂体积分数为3%、投料比为15?1、温度为50 ℃为最佳制备工艺条件,进行实验验证,计算得到载药量和包封分别为4.9%和42.8%。以下实验所用NFX-CSM均按该反应条件制得。
表 1 正交实验设计结果
Table 1 Results of orthogonal experiment
2.2 NFX-CSM的表征
载药微球NFX-CSM的SEM照片如图1所示。可见,微球粒径主要分布在2~5 μm之间,平均约为4 μm,球形圆整,分散性较好。而空白CS微球在弱酸溶液中带少量正电荷,电位为11.2 mV(如图2所示),这是因为在酸性溶液中,微球上的―NH2与H+结合,形成质子化胺 ―NH3+。

图1 NFX-CSM的扫描电镜照片
Fig.1 SEM micrograph of NFX-CSM
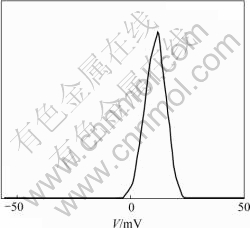
图2 CSM在弱酸溶液中的电位图
Fig.2 Image of potential of CSM in weak acid solution
2.3 红外光谱分析
图3所示分别为CSM,NFX和NFX-CSM在4 000~ 400 cm-1区域的FTIR光谱。可见,CSM特征吸收峰在 1 653 cm-1(C=O伸缩振动)、1 568 cm-1(C=N伸缩振动,这是CS被戊二醛交联后所形成的Schiff碱的特征峰)、1 066 cm-1和1 027 cm-1(CS吡喃环中C-H的弯曲振动)处。NFX特征吸收峰在1 728 cm-1和1 619 cm-1处,分别为羧基上的羰基振动吸收峰和环上的羰基振动吸收峰,在819 cm-1和746 cm-1处的峰为CF=CH中的C―H的面外变形振动峰,1 259 cm-1处的峰为C―N伸缩振动峰。从图3所示的NFX-CSM红外光谱可以看出在1 374 cm-1处出现NFX的吸收峰,这表明NFX被CS包裹后削弱了NFX的分子间的作用力,吸收峰发生了偏移。在曲线3中,1 653 cm-1和1 568 cm-1处CSM的吸收峰消失,而在1 637 cm-1处出现了较强的特征吸收峰,1 066 cm-1处峰移向低波数1 060 cm-1,619 cm-1处峰移向低波数607 cm-1,而1 027 cm-1的吸收峰明显减弱。与曲线1和2比较,曲线3没有出现新的特征峰,而CSM的主要特征峰都出现红移,表明NFX与CSM之间没有生成新键,而主要是以物理包埋的方式结合。
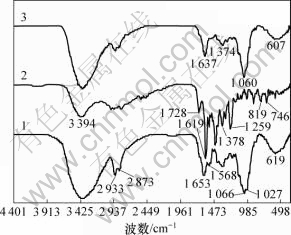
1―CSM;2―NFX;3―NFX-CSM
图3 CSM,NFX和NFX-CSM的红外吸收光谱
Fig.3 FTIR spectra of CSM, NFX and NFX-CSM
2.4 载药微球的释药性能检测
2.4.1 不同交联剂用量对载药微球释药速率的影响
图4所示为戊二醛在反应体系所占体积分数分别为1%,2%和3%时,载药微球在PBS中的释药曲线。可见,戊二醛所占比例越大,载药微球释药速率越慢。这是因为交联剂用量越多,制备的壳聚糖微球骨架密度越大,药物分子被包裹得越紧密,形成的微通道越少,导致小分子药物的释放扩散阻力增大。若交联剂用量过小,则制备的壳聚糖微球的骨架密度比较低,药物主要分布在微球的表面,无法有效提高载体缓释药物的效果。

φ(戊二醛)/%:1―1;2―2;3―3
图4 不同交联剂用量制备的NFX-CSM释药曲线
Fig.4 Drug release curves of NFX-CSM with different dosages of crosslinker
2.4.2 不同投料比制备的载药微球对释药速率的影响
图5所示为CS与NFX投料比不同时制备的载药微球的释药速率。可见,当m(CS)?m(NFX)为10?1时,在释药的前5 h内,释药率为41.1%;而当m(CS)?m(NFX)为15?1和20?1时,释药率分别为30.6%和24.4%。这是因为CS量越多,药物被包裹的越紧密,药物的释放速率越慢,载药微球的缓释效果越明显。
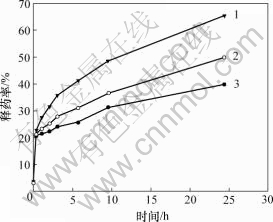
m(CS)?m(NFX):1―10?1;2―15?1;3―20?1
图5 CS与NFX不同投料比制备的载药微球释药曲线
Fig.5 Drug release curves of NFX-CSM with different feed ratios of CS to NFX
2.4.3 NFX-CSM在3种pH值环境下的药物释放检测
图6所示为载药微球在不同pH值环境下的释药结果。可见,NFX-CSM在3种不同的释放介质下,均对药物有良好的缓释效果:在pH=2.0和pH=9.0的介质中,药物释放50%所用时间分别为5 h和9 h,而在PBS缓冲液中为24.5 h,表明制备的NFX-CSM在模拟体内环境下具有缓慢释放药物的作用,这将延长药物在体内的作用时间,提高药物的利用率。而纯NFX在pH=2.0的介质中,经过0.3 h,释药率已达到95%以上。
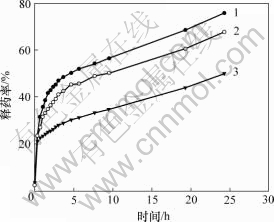
1―pH=2.0;2―pH=9.0;3―PBS缓冲液
图6 NFX-CSM在不同释放介质中的释药曲线
Fig.6 Drug release curves of NFX-CSM in different media
NFX-CSM在介质中的释药速率主要取决于以下2个因素:一是微球在溶液中的溶胀机制,溶胀速度越快,药物的释放速率越快。在酸性溶液中,微球表面上有质子化胺―NH3+,由于静电排斥作用,使得水凝胶各网格之间的空隙增大,孔道畅通,使渗透性增强,因而释药速率较大;而在碱性和中性条件下,―NH2基团依附于微球表面,使得孔道堵塞,渗透性降低,因而释药速率较慢,这可以解释药物在pH=2.0介质中的释放速率大于在pH=9.0介质中的释放速率的原因;二是药物在不同pH值介质中溶解度的影响,因为NFX为两性药物,易溶于酸和碱,而难溶于水等溶剂,所以,在微球溶胀条件相差不大的情况下,溶解度越大,药物的释放速率越快。因此,药物在pH=9.0的弱碱缓冲液中的释放速率大于在PBS中的释放速率。
口服NFX,药物在经过胃部时,在胃酸pH值的影响下,迅速大量溶解,无法稳定有效地到达肠道抗 菌,利用率不高,这种突释现象可能是造成诺氟沙星在临床应用中给药量大的原因之一;而NFX-CSM在经过胃部时,由于药物被包裹,不能迅速溶解于胃酸中,阻止或延缓了药物释放,而到达肠道后,壳聚糖可以被结肠中菌群产生的酶所分解而释放所载有的药 物[11],同时,壳聚糖的生物黏附性可使载药微球黏附于结肠黏膜,从而延长药物作用时间,提高疗效[15]。
2.5 NFX-CSM对大肠杆菌的生长抑制效果
载药微球与大肠杆菌共培养,检测不同作用时段的细菌致死情况,结果如图7所示。可见,纯NFX在前6 h抗菌效果明显,但是6 h后其作用逐渐减弱,到 28.5 h时,细菌抑制率已经降到30%以下;而NFX-CSM在前6 h的抗菌效果比纯NFX的低,但是,随着作用时间的延长,其效果逐渐增强,到55 h时,其细菌抑制率达到85%左右。其原因主要是在实验前期(6 h内),NFX- CSM中的药物释放量少,对细菌的抑制作用弱,随着时间的延长,NFX-CSM中的药物不断溶出,抗菌作用不断增强,特别是14 h后,效果明显优于NFX,到55 h时,药物几乎全部溶出,对细菌的生长抑制率达到了最高值。由此可见,NFX-CSM对药物的缓释效果,保证了NFX在细菌培养液中的浓度,延长了药物对细菌的生长抑制作用时间,并且NFX在CSM的协同抗菌作用下,明显提高了药物对细菌的作用效果。
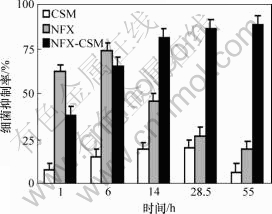
图7 CSM, NFX以及NFX-CSM对大肠杆菌的生长抑制率
Fig.7 Growth inhibition ratios to coliform of CSM, NFX and NFX-CSM
3 结 论
a. 用乳液-化学交联法,根据正交优化设计,制得球形圆整,分散性好,平均粒径约为4 μm的NFX-CSM,药物与壳聚糖之间主要以物理包埋的方式结合。
b. NFX-CSM在模拟不同人体部位体液的释放环境下,均对药物有良好的缓释效果;另外,微球的释药速率随交联剂用量的增加和投料比m(CS)?m(NFX)的增大而变慢。
c. NFX在CSM的协同抗菌作用下,明显提高了药物对细菌的作用效果,表明所制备的CSM是一种有潜力的抗菌缓释材料,这也为水溶性壳聚糖的进一步研究开发提供了理论和应用基础。
参考文献:
[1] 李秉超, 付田霞, 徐清海. Ce-诺氟沙星配合物的制备及其抗菌活性[J]. 辽宁化工, 2000, 29(6): 341-343.
LI Bing-chao, FU Tian-xia, XU Qing-hai. Preparation and antibacterical activity of new complex between Ce and norfloxacin[J]. Liaoning Chemical Industry, 2000, 29(6): 341-343.
[2] Stahlmann R, Lode H. Fluoroquinolones in the elderly: Safety considerations[J]. Drugs Aging, 2003, 20(4): 289-302.
[3] 谢景超. 氟喹诺酮类药物的副作用[J]. 中南药学, 2005, 3(6): 375-378.
XIE Jing-chao. The side effects of fluoroquinolones[J]. Central South Pharmacy, 2005, 3(6): 375-378.
[4] 钱 凤, 朱耀斌, 李健和. 氟喹诺酮类药物近代剂型的开发与应用[J]. 药学实践杂志, 2001, 19(3): 154-156.
QIAN Feng, ZHU Yao-bin, LI Jian-he. The development and applications of modern formulation about fluoroquinolones[J]. Journal of Pharmaceutical Practice, 2001, 19(3): 154-156.
[5] 夏金兰, 王 春, 聂珍媛, 等. 羧甲基壳聚糖银噻苯咪唑的制备及其抑菌性能[J]. 中南大学学报: 自然科学版, 2005, 36(1): 34-37.
XIA Jin-lan, WANG-Chun, NIE Zhen-yuan, et al. Preparation and antimicrobial activity of carboxymethyl chitosan-Ag- tiabendazole[J]. Journal of Central South University: Science and Technology, 2005, 36(1): 34-37.
[6] Janes K A, Fresneau M P, Marazuela A, et al. Chitosan nanoparticles as delivery systems for doxorubicin[J]. Journal of Controlled Release, 2001, 73(2): 255-267.
[7] Shikata F, Tokumitsu H, Ichikawa H, et al. In vitro cellular accumulation of gadolinium incorporated into chitosan nanoparticles designed for neutron-capture therapy of cancer[J]. Eur J Pharm Biopharm, 2002, 53(1): 57-63.
[8] Fennessey S F, Farris R J. Fabrication of aligned and molecularly oriented electrospun polyacrylonitrile nanofibers and the mechanical behavior of their twisted yarns[J]. Polymer, 2004, 45(12): 4217-4225.
[9] 李和平, 阮建明, 黄伯云, 等. 磁性壳聚糖纳米粒子的制备及表征[J]. 中南大学学报: 自然科学版, 2004, 35(2): 175-179.
LI He-ping, RUAN Jian-ming, HUANG Bai-yun, et al. Preparation and characterization of magnetic chitosan nanoparticles[J]. Journal of Central South University: Science and Technology, 2004, 35(2): 175-179.
[10] 张阳德, 张彦琼, 陈记稷, 等. 壳聚糖-碳纳米粒的制备及其体外性质的研究[J]. 中国现代医学杂志, 2006, 16(6): 801-806.
ZHANG Yang-de, ZHANG Yan-qiong, CEHN JI-ji, et al. Preparation and in vitro evaluation of chitosan-carbon nanoparticles[J]. China Journal of Modern Medicine, 2006, 16(6): 801-806.
[11] 李国锋, 陈建海, 刘立捷, 等. 结肠菌群触发型5-氨基水杨酸壳聚糖胶囊大鼠体内的吸收与分布研究[J]. 第一军医大学学报, 2003, 23(5): 431-434.
LI Guo-feng, CHEN Jian-hai, LIU Li-jie, et al. Absorption and distribution of 5-aminosalicylic acid from its chitosan capsule degraded by colon bacteria-released enzymes in rats[J]. Journal of First Military Medical University, 2003, 23(5): 431-434.
[12] 丁德润, 沈 勇. 壳聚糖衍生物及其纳米粒的抗菌性能研究[J]. 印染, 2005, 31(14): 12-14.
DING De-run, SHEN Yong. Antibacterial finishing with chitosan derivatives and their nanoparticles[J]. Dyeing and Finishing, 2005, 31(14): 12-14.
[13] 杨宇民, 马振祥, 尹继成, 等. 系列水溶性壳聚糖衍生物的抑菌性能研究[J]. 中国公共卫生, 2005, 21(9): 1080-1081.
YANG Yu-min, MA Zhen-xiang, YIN Ji-cheng, et al. Study on antimicrobial activity of chitosan water soluble derivatives[J]. Chin J Public Health, 2005, 21(9): 1080-1081.
[14] 尹承慧, 侯春林, 徐 皓, 等. 羧甲基壳聚糖/环丙沙星植入缓释微球防治局部感染的实验研究[J]. 第二军医大学学报, 2005, 26(1): 72-74.
YIN Cheng-hui, HOU Chun-lin, XU Hao, et al. Prevention and treatment of local infection using implantable sustained release ciprofloxacin/carboxmethyl chitosan microspheres[J]. Academic Journal of Second Military Medical University, 2005, 26(1): 72-74.
[15] 李 扬, 王 强, 钱 方, 等. 左氧氟沙星羧甲基壳聚糖微球在大鼠体内结肠靶向释药的研究[J]. 中国新药杂志, 2006, 15(17): 1455-1457.
LI Yang, WANG Qiang, QIAN Fang, et al. Colon-target drug delivery of levofloxacin microshperes in rats[J]. Chinese Journal of New Drugs, 2006, 15(17): 1455-1457.
收稿日期:2007-07-26;修回日期:2007-09-29
基金项目:湖南省生物纳米技术重大科技专项基金资助项目(03NKY1001);国家“985工程”(二期)平台建设项目(2005年)
通信作者:刘选明(1963-),男,湖南新宁人,教授,博士生导师,从事生物纳米技术与生化分析研究;电话:0731-8821721;E-mail: sw_xml@hnu.cn