编号:1004-0609(2015)-07-1897-07
层状Li0.5Na0.5CoO2的合成及显微结构
周 然1,王 琛1,梁 钰1,石逸扬1,艾延龄1, 2
(1. 中南大学 材料科学与工程学院,长沙 410083;
2. 中南大学 有色金属材料科学与工程教育部重点实验室,长沙 410083)
摘 要:为了研究具有α-NaFeO2结构的复杂钴氧化物原子排列规律,采用固相反应合成了Li0.5Na0.5CoO2多晶粉末,并利用X射线衍射(XRD)、扫描电子显微分析(SEM)和透射电子显微分析(TEM)等检测手段对其形貌、晶体结构等进行了表征。结果表明:一般处理状态下,Li0.5Na0.5CoO2为片状,其晶体结构与层状LiCoO2相似,但在某些处理状态下通过TEM观察到沿[0001]带轴衍射花样中出现菱面体晶系中应该消光{10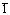 0}的晶面族。这说明Li0.5Na0.5CoO2的晶体结构已经由菱面体结构转变成六方结构。
0}的晶面族。这说明Li0.5Na0.5CoO2的晶体结构已经由菱面体结构转变成六方结构。
关键词: Li0.5Na0.5CoO2;电子衍射;晶体结构;合成
中图分类号: O614.11;O766 文献标志码:A
Synthesis and microstructure of layered cobaltite Li0.5Na0.5CoO2
ZHOU Ran1, WANG Chen1, LIANG Yu1, SHI Yi-yang1, AI Yan-ling1, 2
(1. School of Materials Science and Engineering, Central South University, Changsha 410083, China;
2. Key Laboratory of Nonferrous Materials Science and Engineering, Ministry of Education,
Central South University, Changsha 410083, China)
Abstract: In order to research the structure of complex cobalt oxide compounds with the similar crystallographic features of α-NaFeO2, the solid state reaction was used to prepare the Li0.5Na0.5CoO2 , whose crystal structure and morphology were characterized by X-ray diffractometry (XRD), scanning electron microscopy(SEM),transmission electron microscopy (TEM). The results show that, under normal conditions, the platelet-like Li0.5Na0.5CoO2 and layered LiCoO2(R M) have similar crystal structures. However, the extinction spots of crystal-plane {10
M) have similar crystal structures. However, the extinction spots of crystal-plane {10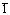 0} of rhombohedral R
0} of rhombohedral R m space group in [0001] zone axis is detected in TEM patterns, which indicates that the crystal structure of Li0.5Na0.5CoO2 has transformed from rhombohedra system to hexagonal system.
m space group in [0001] zone axis is detected in TEM patterns, which indicates that the crystal structure of Li0.5Na0.5CoO2 has transformed from rhombohedra system to hexagonal system.
Key words: Li0.5Na0.5CoO2; electron diffraction; crystal structure; synthesis
近年来,层状碱金属钴氧化合物AxCoO2(A=Li,Na)吸引了科研工作者的极大兴趣。层状LixCoO2早已作为电极材料广泛用于二次锂离子电池中[1-2],并通过不同原子位掺杂获得较好的电循环性能[3-5];而NaxCoO2拥有多种层状结构,也已用作钠离子电池电极材料[6-7],同时表现出极其优良的热电性,其低温超导性也引起了广泛研究[8-10]。因此,研究者们通过制备Li+、Na+共生的碱金属钴氧化合物来研究层状AxCoO2微观结构与宏观性质之间的关系。BALSYS等[11]最先制备出Li和Na摩尔比接近1:1的稳定化合物Li0.43Na0.36CoO1.96,通过中子粉末衍射确定其空间群为P63/mmc,晶格常数a=2.839 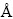 ,c=20.36
,c=20.36 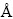 。化合物中O离子以A―B―C―A―A―C―B―A方式堆垛,每个单胞包括4个CoO2层,Li离子和Na离子分层排列在CoO2层两侧。SEMENOVA等[12-13]在此基础上研究了具有P63/mmc结构LixNayCoO2(x≈y≈0.5)的制备条件及结构特征,发现940~1000 ℃为最佳的温度合成范围,并用拉曼光谱证实Li0.43Na0.36CoO1.96中O3-LiCoO2和P2-NaxCoO2的存在。随后,研究者对LixNayCoO2的结构也进行了深入研究。MESILOV等[14]通过X射线吸收光谱分析发现LixNayCoO2中越靠近材料表面,Li和Na摩尔比越接近化学计量数。BERTHELOT等[15]采用过高温X射线衍射仪观测LixNayCoO2相合成过程,发现具有OPP9- (Li/Na/Na)CoO2的新结构。而对于LixNayCoO2性能研究中,REN等[16]在室温下观测到Li0.48Na0.35CoO2的热电势达到180 μV/K,远高于LiCoO2和NaxCoO2单相的。BOS等[17]在此基础上研究发现,随着碱金属(Li和Na)的减少,LixNayCoO2的热电势也减少。
。化合物中O离子以A―B―C―A―A―C―B―A方式堆垛,每个单胞包括4个CoO2层,Li离子和Na离子分层排列在CoO2层两侧。SEMENOVA等[12-13]在此基础上研究了具有P63/mmc结构LixNayCoO2(x≈y≈0.5)的制备条件及结构特征,发现940~1000 ℃为最佳的温度合成范围,并用拉曼光谱证实Li0.43Na0.36CoO1.96中O3-LiCoO2和P2-NaxCoO2的存在。随后,研究者对LixNayCoO2的结构也进行了深入研究。MESILOV等[14]通过X射线吸收光谱分析发现LixNayCoO2中越靠近材料表面,Li和Na摩尔比越接近化学计量数。BERTHELOT等[15]采用过高温X射线衍射仪观测LixNayCoO2相合成过程,发现具有OPP9- (Li/Na/Na)CoO2的新结构。而对于LixNayCoO2性能研究中,REN等[16]在室温下观测到Li0.48Na0.35CoO2的热电势达到180 μV/K,远高于LiCoO2和NaxCoO2单相的。BOS等[17]在此基础上研究发现,随着碱金属(Li和Na)的减少,LixNayCoO2的热电势也减少。
本文作者采用固相合成方法在较低温度750 ℃合成名义成分为Li0.5Na0.5CoO2的单相碱金属钴氧化合物,并用多种分析方法进行微观表征,探究其与六方晶系Li0.48Na0.35CoO2的关系,为研究晶体结构与性质提供依据。
1 实验
1.1 Li0.5Na0.5CoO2的固相合成及热分析
Li0.5Na0.5CoO2是通过NaCoO2、Li2CO3和碱式碳酸钴粉末按一定比例混合烧结而成。原料先在500 ℃下预烧结1 h,再快速升温至750 ℃分别烧结8~12 h,产物随炉冷却得到分析样品。NaCoO2通过Na2O2与Co3O4在500 ℃烧结1 h制备得到。考虑挥发效应,原料配比时Li和Na适当过量,并在每次烧结前,对样品进行长时间研磨。同时,参照高虹等[18]的方法,以碱式碳酸钴和碳酸锂为原料在750 ℃烧结10 h制备的LiCoO2作为对照样品。
使用日本理学会TAS100 热分析仪器对原料粉末进行示差扫描量热(DSC)分析和热重分析(TG),测试温度范围为25~800 ℃ ,升温速率为10 ℃/min,气氛为空气。
1.2 Li0.5Na0.5CoO2的形貌和晶体结构分析
使用日本理学会Rigaku D/Max 2500 型衍射仪对不同粉末样品进行X射线衍射(XRD)物相分析。使用FEI公司 Sirion 200 场发射扫描电镜(SEM)对样品进行微观形貌观察。利用PS-6真空型电感耦合等离子体原子发射光谱仪(ICP-ASS)对Li0.5Na0.5CoO2以及LiCoO2进行Li和Na含量分析。透射电镜试样是将粉末样品在铜网支撑的微栅上制得,使用FEI公司TECNAI G2 F20场发射透射电镜(加速电压200kV)进行电子衍射和高分辨图像等透射电子显微分析(TEM)。
2 结果与讨论
2.1 Li0.5Na0.5CoO2的低温合成温度范围
NaCoO2、Li2CO3和碱式碳酸钴粉末固相反应合成Li0.5Na0.5CoO2的示差扫描量热曲线和质量损失曲线如图1所示。曲线中有3个明显的吸热峰,对应温度约为80、300和490 ℃。80 ℃的吸热峰是样品中水分蒸发造成的。碱式碳酸钴在300 ℃左右发生分解,造成了第二个吸热峰,由于碳酸盐分解释放大量CO2,与此温度对应的TG曲线出现了明显质量损失。正常情况下,Li2CO3的分解温度约为700 ℃,但由于碱式碳酸钴分解产生的高活性Co3O4具有催化作用,能使其在450 ℃开始分解,500 ℃左右就能够大量分解,反应为DSC曲线中第三个吸热峰,此时Li2CO3的分解也对应了质量损失曲线下行。
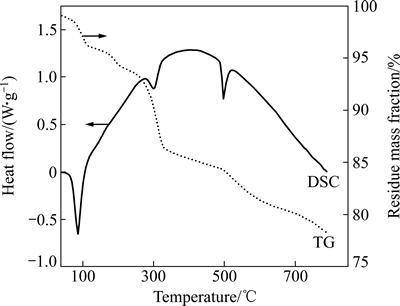
图1 NaCoO2、Li2CO3和碱式碳酸钴混合物的TG和DSC曲线
Fig. 1 TG and DSC curves of mixture including NaCoO2, Li2CO3 and basic cobaltous carbonate
2.2 Li0.5Na0.5CoO2的X射线衍射分析
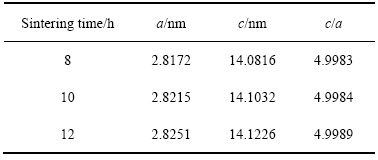
图2所示为Li0.5Na0.5CoO2在不同烧结工艺下得到的样品的XRD谱。对比固相烧结的LiCoO2标准样XRD峰可知,不同烧结时间后Li0.5Na0.5CoO2样品材料特征峰尖锐,基本保持LiCoO2晶体结构特征。在750 ℃烧结8 h后,样品中观察到Co3O4衍射峰,而在10和12 h的衍射样中,Co3O4峰值已经消失,材料衍射峰(006)和(102)及(108)和(110)均分裂完好,晶化程度较高,无明显杂峰,表明10 h以上的烧结制度已能制备较纯单相多晶粉末样品。参考LiCoO2晶体学数据(a=2.8146,c=14.0537,R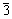 M)[19],采用Rietveld法计算不同烧结时间的Li0.5Na0.5CoO2的晶格参数a、c以及c/a值,如表1所列。随烧结时间的增加,Li0.5Na0.5CoO2的晶格参数均随之增加,c轴晶格参数的增速快于a轴的。相对于LiCoO2的XRD谱,Li0.5Na0.5CoO2的XRD谱整体左移,说明结构中有离子被更大半径的离子代替。烧结8 h试样中(006)晶面衍射峰并不明显,随烧结时间的延长衍射强度逐渐增加,并出现宽化。这很可能是由于烧结过程LiCoO2中3a位的Li+被Na+取代造成的。层状LiCoO2的(006)晶面只有Li+占位,而由于引入了原子序数和离子半径更大的Na+,Li0.5Na0.5CoO2的(006)面衍射能力更强,同时,Na+取代造成了晶格畸变,产生衍射峰宽化。
M)[19],采用Rietveld法计算不同烧结时间的Li0.5Na0.5CoO2的晶格参数a、c以及c/a值,如表1所列。随烧结时间的增加,Li0.5Na0.5CoO2的晶格参数均随之增加,c轴晶格参数的增速快于a轴的。相对于LiCoO2的XRD谱,Li0.5Na0.5CoO2的XRD谱整体左移,说明结构中有离子被更大半径的离子代替。烧结8 h试样中(006)晶面衍射峰并不明显,随烧结时间的延长衍射强度逐渐增加,并出现宽化。这很可能是由于烧结过程LiCoO2中3a位的Li+被Na+取代造成的。层状LiCoO2的(006)晶面只有Li+占位,而由于引入了原子序数和离子半径更大的Na+,Li0.5Na0.5CoO2的(006)面衍射能力更强,同时,Na+取代造成了晶格畸变,产生衍射峰宽化。
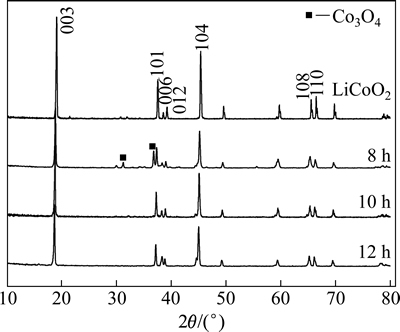
图2 750 ℃下不同烧结时长Li0.5Na0.5CoO2的XRD谱
Fig. 2 XRD patterns of Li0.5Na0.5CoO2 at 750 ℃ for different sintering time
表1 750 ℃烧结不同时间合成的Li0.5Na0.5CoO2的晶胞参数a、c值以及c/a比值
Table 1 Lattice parameters of a, c and c/a ratio of Li0.5Na0.5CoO2 synthesized at 750 ℃ for different sintering time
2.3 Li0.5Na0.5CoO2的成分分析及形貌特征
利用电感耦合等离子体原子吸收光谱(ICP-AAS)对不同烧结时间的Li0.5Na0.5CoO2进行锂和钠的精确含量进行测定,其结果列于表2中。从表2可以发现,经过长时间的烧结,钠元素挥发较多,锂离子挥发较为稳定,当烧结时间为10~12 h时,基本不变。
图3所示为经不同时间烧结合成的Li0.5Na0.5CoO2层状相的SEM像。从图3可以看出,合成的颗粒形状为片状,但是颗粒状态区别较大。烧结8 h样品的SEM像中颗粒较小,但比较规整;烧结10 h样品的颗粒大小很不均匀,部分颗粒明显增大;而烧结12 h的样品中,大颗粒数量明显增多,最大颗粒半径可达3 μm左右。图2中,与标准LiCoO2的XRD谱相比,不同烧结时间后,Li0.5Na0.5CoO2的XRD衍射峰(006)峰宽较大,随着烧结时间延长,没有明显减少的趋势,而由图3的SEM像可以判断,造成XRD衍射峰峰宽较大的原因很有可能不是颗粒过小,而是晶格发生畸变。
表2 750 ℃不同烧结时间后合成的Li0.5Na0.5CoO2的Li和Na 含量
Table 2 Li and Na content in Li0.5Na0.5CoO2 synthesized at 750 ℃ for different sintering time
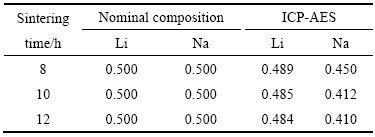

图3 750 ℃下不同烧结时间的Li0.5Na0.5CoO2的SEM像
Fig. 3 SEM images of Li0.5Na0.5CoO2 synthesized at 750 ℃ for different sintering time
2.4 Li0.5Na0.5CoO2的电子显微分析
图4所示为LiCoO2和烧结12 h合成的Li0.5Na0.5CoO2沿[0001]晶带轴下的电子衍射花样及高分辨照片,其中电子衍射花样是根据LiCoO2晶格常数标定后的结果。图4(a)所示为LiCoO2沿[0001]带轴的电子衍射花样,满足菱面体点阵消光规律。而图4(b)中,Li0.5Na0.5CoO2沿[0001]带轴的电子衍射花样出现了菱面体点阵中原本消光的{10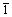 0}晶面族斑点。图4(c)所示为烧结12 h Li0.5Na0.5CoO2在某个区域下沿[0001]带轴的高分辨像及傅立叶转变花样,图4(d)所示为同种材料另外一个区域沿[0001]带轴的电子衍射花样及高分辨像,这些区域的花样中都出现了{10
0}晶面族斑点。图4(c)所示为烧结12 h Li0.5Na0.5CoO2在某个区域下沿[0001]带轴的高分辨像及傅立叶转变花样,图4(d)所示为同种材料另外一个区域沿[0001]带轴的电子衍射花样及高分辨像,这些区域的花样中都出现了{10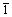 0}晶面族斑点,说明在这种烧结工艺下,绝大部分晶粒已经转变成了与LiCoO2不同的晶体结构。从图4(c)和(d)所示的衍射花样还可以看出,在某些特殊区域,甚至出现了沿[10
0}晶面族斑点,说明在这种烧结工艺下,绝大部分晶粒已经转变成了与LiCoO2不同的晶体结构。从图4(c)和(d)所示的衍射花样还可以看出,在某些特殊区域,甚至出现了沿[10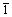 0]方向的两倍周期有序,对于这些局部区域的有序,本文作者正在进一步研究中,但对于未出现有序的晶体结构,经过分析与模拟后,其晶体结构是可以确定的。
0]方向的两倍周期有序,对于这些局部区域的有序,本文作者正在进一步研究中,但对于未出现有序的晶体结构,经过分析与模拟后,其晶体结构是可以确定的。
由表2的ICP-AAS结果说明固相反应过程烧损较小,因此,{10 0}晶面族衍射斑点的出现不是由于反应中成分变化等原因引起的结构改变,而是由晶体内部自身原子排列规律变化造成的。WANG等[20]研究HL-LiCoO2晶体结构时也曾发现相似衍射斑点,认为是由原本分层的Li和Co原子混排造成的,考虑到Li2CO3晶体结构及本实验制备Li0.5Na0.5CoO2原料的特点,这种可能性应该不大,因为层状LiCoO2中, Li原子半径较小,较易从氧四面体中脱离。根据TAKAHASHI等[21]的数据进行计算,O-Co-O层氧原子间距为1.985
0}晶面族衍射斑点的出现不是由于反应中成分变化等原因引起的结构改变,而是由晶体内部自身原子排列规律变化造成的。WANG等[20]研究HL-LiCoO2晶体结构时也曾发现相似衍射斑点,认为是由原本分层的Li和Co原子混排造成的,考虑到Li2CO3晶体结构及本实验制备Li0.5Na0.5CoO2原料的特点,这种可能性应该不大,因为层状LiCoO2中, Li原子半径较小,较易从氧四面体中脱离。根据TAKAHASHI等[21]的数据进行计算,O-Co-O层氧原子间距为1.985  ,O-Na-O层间距为3.221
,O-Na-O层间距为3.221  ,相对而言,O-Na-O原子层更容易引入新的原子,同时,从表2可知,反应过程中Na原子烧损较多,边缘可能存在较多空位和位错等缺陷,游离的Li原子便利用了这些缺陷进入Na原子层,并随反应时间延长在Na原子间扩散。通过上述分析可知,Li0.5Na0.5CoO2中出现Li、Na原子混合层是大概率事件。
,相对而言,O-Na-O原子层更容易引入新的原子,同时,从表2可知,反应过程中Na原子烧损较多,边缘可能存在较多空位和位错等缺陷,游离的Li原子便利用了这些缺陷进入Na原子层,并随反应时间延长在Na原子间扩散。通过上述分析可知,Li0.5Na0.5CoO2中出现Li、Na原子混合层是大概率事件。
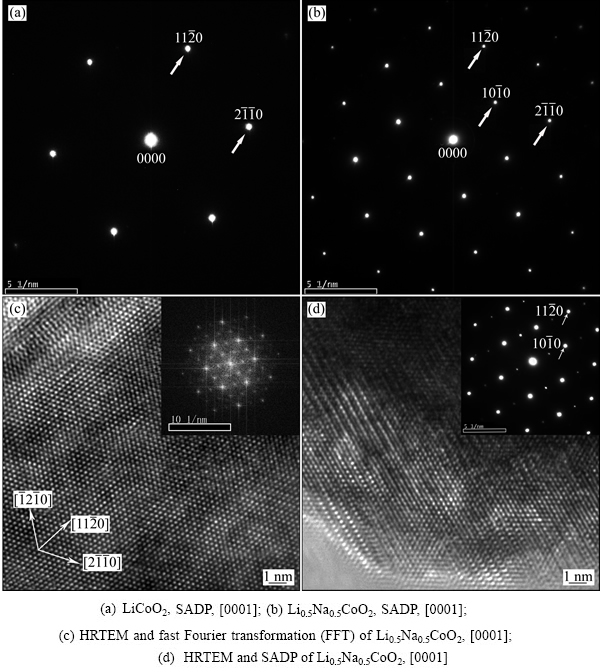
图4 Li0.5Na0.5CoO2的选区电子衍射花样及高分辨像
Fig. 4 Selected area diffraction pattern (SADP) and high resolution transmission electron microscopy (HRTEM)
基于以上判断以及XRD结果中Li0.5Na0.5CoO2与LiCoO2衍射花样基本相似的事实,结合晶体学方面的知识,采用CrystalMaker软件建立了一个如图5(a)所示的模型,其点阵常数及原子占位参考Co-O层由共边的钴氧八面体组成,Li很难进去取代Co。本实验中制备的Li0.5Na0.5CoO2原料为NaCoO2、Li2CO3和碱式碳酸钴,NaCoO2也属R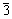 m空间群,Na占3a位, Co、O原子的Wyckoff位置与LiCoO2的完全相同;Li2CO3分解生成的Li2O为Fm
m空间群,Na占3a位, Co、O原子的Wyckoff位置与LiCoO2的完全相同;Li2CO3分解生成的Li2O为Fm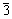 m结构,Li原子占据氧四面体中心;碱式碳酸钴可分解尖晶石结构的Co3O4,其中Co2+占据氧四面体中心,Co3+占据氧八面体中心,这些氧八面体也是以共边方式相连,与LiCoO2的CoO2层排列形式一致。因此,随着固相反应进行,Co和O原子很可能在氧充足的条件下迅速形成CoO2层,而由HOLZAPFEL等[19]的LiCoO2数据建立的模型中CoO2层位置及堆垛方式不变,由于Na原子引入,原3a位的原子以 Li-Na-Li(Na)-Li-Na-Li (Na)…方式堆垛,这种结果使得晶体已经不能满足菱面体点阵的平移对称规律,晶体的结构为简单六方,但其晶格常数与R
m结构,Li原子占据氧四面体中心;碱式碳酸钴可分解尖晶石结构的Co3O4,其中Co2+占据氧四面体中心,Co3+占据氧八面体中心,这些氧八面体也是以共边方式相连,与LiCoO2的CoO2层排列形式一致。因此,随着固相反应进行,Co和O原子很可能在氧充足的条件下迅速形成CoO2层,而由HOLZAPFEL等[19]的LiCoO2数据建立的模型中CoO2层位置及堆垛方式不变,由于Na原子引入,原3a位的原子以 Li-Na-Li(Na)-Li-Na-Li (Na)…方式堆垛,这种结果使得晶体已经不能满足菱面体点阵的平移对称规律,晶体的结构为简单六方,但其晶格常数与R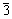 m的LiCoO2用六角座标表示时基本相同,因为只有这样粉末多晶衍射结果才有可能与LiCoO2的花样相近。根据这个模型计算出的XRD粉末衍射花样与[0001]带轴电子衍射花样如图5(b)和(c)所示,其中图5(b)中上部分所示为烧结12 h的 Li0.5Na0.5CoO2样品的粉末XRD谱,曲线为计算出来的结果。对比X射线实验与计算结果可以看出,除了小角度的(001)、(002)晶面衍射峰外,其他峰值匹配较好。(001)和(002)峰之所以检测不到,这是因为(001)晶面衍射峰角度较小,同时,在计算结果中这两个衍射峰的强度也不超过3%,所以,在实验结果中观察不到是正常的。计算出来的[0001]带轴电子衍射花样出现了明显的{10
m的LiCoO2用六角座标表示时基本相同,因为只有这样粉末多晶衍射结果才有可能与LiCoO2的花样相近。根据这个模型计算出的XRD粉末衍射花样与[0001]带轴电子衍射花样如图5(b)和(c)所示,其中图5(b)中上部分所示为烧结12 h的 Li0.5Na0.5CoO2样品的粉末XRD谱,曲线为计算出来的结果。对比X射线实验与计算结果可以看出,除了小角度的(001)、(002)晶面衍射峰外,其他峰值匹配较好。(001)和(002)峰之所以检测不到,这是因为(001)晶面衍射峰角度较小,同时,在计算结果中这两个衍射峰的强度也不超过3%,所以,在实验结果中观察不到是正常的。计算出来的[0001]带轴电子衍射花样出现了明显的{10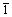 0}晶面族斑点,但强度较实验结果偏低,考虑到实际情况存在二次衍射及动力学效应,该结果也是正常的。由此可以断定,烧结12 h的Li0.5Na0.5CoO2样品的晶体结构应该已经转变成了简单六方结构。
0}晶面族斑点,但强度较实验结果偏低,考虑到实际情况存在二次衍射及动力学效应,该结果也是正常的。由此可以断定,烧结12 h的Li0.5Na0.5CoO2样品的晶体结构应该已经转变成了简单六方结构。
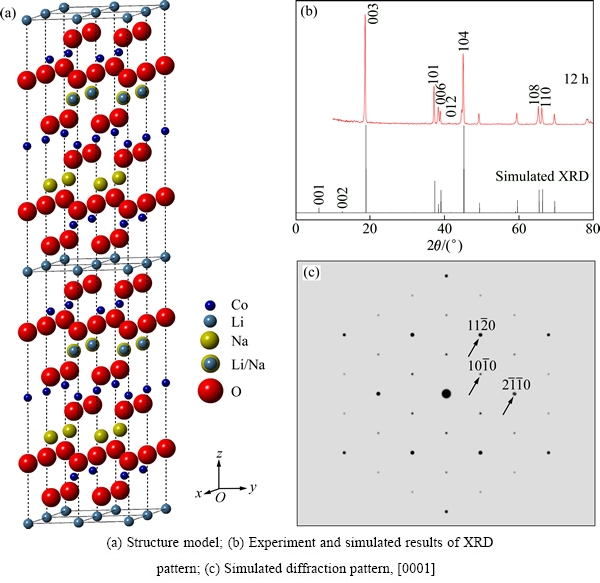
图5 Li0.5Na0.5CoO2的层状结构模型与模拟结果
Fig. 5 Structure model and simulated results of Li0.5Na0.5CoO2
3 结论
1) 采用固相合成法制备了单相Li0.5Na0.5CoO2多晶粉末,其结晶度高、烧损量少,XRD衍射花样及晶格常数与层状LiCoO2相近。
2) Li0.5Na0.5CoO2多晶粉末呈片状,晶粒随烧结时间增加而长大,最大的颗粒半径为2~3 μm。
3) Li0.5Na0.5CoO2多晶粉末沿[0001]带轴出现原本消光的{10 0}晶面族电子衍射斑点,并存在局部两倍周期有序。晶体结构转变为六方结构,其中Co和O原子沿c轴保持六方最密堆积,Li和Na原子以Li-Na-Li/Na-Li-Na-Li/Na…方式堆垛。
0}晶面族电子衍射斑点,并存在局部两倍周期有序。晶体结构转变为六方结构,其中Co和O原子沿c轴保持六方最密堆积,Li和Na原子以Li-Na-Li/Na-Li-Na-Li/Na…方式堆垛。
REFERENCES
[1] 张卫民, 杨永会, 孙思修, 刘兆平, 宋新宇. 二次锂离子电池正极活性材料―LiCoO2制备研究进展[J]. 无机化学学报, 2000, 16(6): 873-878.
ZHANG Wei-min, YANG Yong-hui, SUN Si-xiu, LIU Zhao-ping, SONG Xin-yu. Progresses in preparation study of positive electrode material―lithium cobaltate used for lithium ion battery[J]. Chinese Journal of Inorganic Chemistry, 2000, 16(6): 873-878.
[2] MEGAHED S, EBNER W. Lithium-ion battery for electronic applications[J]. Journal of Power Sources, 1995, 54(1): 155-162.
[3] 李普良, 徐 舜, 习小明. 锂离子电池正极材料LiCoO2合成方法及其掺杂研究进展[J]. 矿业工程, 2004, 24(1): 84-88.
LI Pu-liang, XU Shun, XI Xiao-ming. Synthesizing methods if Lithium-ion battery cathode material LiCoO2 and its advances in doping research[J]. Mining and Metallurgical Engineering, 2004, 24(1): 84-88.
[4] 肖 劲, 曾雷英, 彭忠东, 赵 浩, 胡国荣. 锂离子电池正极材料LiNi0.5Mn0.5O2的循环性能[J]. 中国有色金属学报, 2006,16(8): 1439-1444.
XIAO Jin, ZENG Lei-ying, PENG Zhong-dong, ZHAO Hao, HU Guo-rong. Cycle performance of LiNi0.5Mn0.5O2 as cathode material for lithium secondary batteries[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(8): 1439-1444.
[5] 李义兵, 陈白珍, 徐 徽, 石西昌, 胡拥军, 陈 亚. Li(Mnl/3Nil/3C01/3)1-yMyO2(M=AI, Mg, Ti)正极材料的制备及性能[J]. 中国有色金属学报, 2006,16(8): 1474-1479.
LI Yi-bing, CHEN Bai-zhen, XU Hui, SHI Xi-chang, HU Yong-jun, CHEN Ya. Preparation and behavior of cathode material Li(Mnl/3Nil/3Col/3)1-yMO2(M=Al, Mg, Ti)[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(8): 1474-1479.
[6] VICIU L, BOS W, ZANDBERGEN H, HUANG Q, FOO M, ISHIWATA S, RAMIREZ A, LEE M, ONG N, CAVA R. Crystal structure and elementary properties of NaxCoO2 (x=0.32, 0.51, 0.6, 0.75, and 0.92) in the three-layer NaCoO2 family[J]. Physical Review B, 2006, 73(17): 17410401-17410410.
[7] 胡英瑛, 温兆银, 芮 琨, 吴相伟. 钠电池的研究与开发现状[J]. 储能科学与技术, 2013, 2(2): 81-90.
HU Ying-ying, WEN Zhao-yin, RUI Kun, WU Xiang-wei. State-of-the-art research and development status of sodium batteries[J]. Energy Storage Science and Technology, 2013, 2(2): 81-90.
[8] BRACONNIER J, DELMAS C, FOUASSIER C, HAGENMULLER P. Comportment electrochimique des phases NaxCoO2[J]. Materials Research Bulletin, 1980, 15(12): 1797-1804. (in French)
[9] TAKADA K, SAKURAI H, TAKAYAMA- MUROMACHI E, IZUMI F, DILANIAN R, SASAKI T. Superconductivity in two-dimensional CoO2 layers[J]. Nature, 2003, 422(6927): 53-55.
[10] FOO M, WANG Y, WATAUCHI S, ZANDBERGEN H, HE T, CAVA R, ONG N. Charge ordering, commensurability, and metallicity in the phase diagram of the layeredNaxCoO2[J]. Physical Review Letter, 2004, 92(24): 7001-7004.
[11] BALSYS R, DAVID R. The structure of Li0.43Na0.36CoO1.96 using neutron powder diffraction[J]. Solid State Ionics, 1994, 69(1): 69-74.
[12] SEMENOVAA A, SAMIGULLINA R, SHALAEVA E, KOUROV N, KELLERMAN G. Studies on formation and decomposition of the layered cobaltite LixNayCoO2[J]. International Journal of Inorganic Chemistry, 2011, 2011(1): 1-11.
[13] SEMENOVAA A, KELLERMAN G, BAKLANOVA I, PERELYAEVA L, VOVKOTRUB E. Raman spectroscopy study of sodium-lithium cobaltite[J]. Chemical Physics Letters, 2010, 491: 169-171.
[14] MESILOV V, GALAKHOV V, SEMENOVA A, KELLERMAN D, ELOKHINA L. X-ray spectra and specific features of the structure of lithium-sodium cobaltite LixNayCoO2[J]. Physics of the Solid State, 53(2): 271-275.
[15] BERTHELOT R, POLLET M, CARLIER D, DELMAS C. Reinvestigation of the OP4-(Li/Na)CoO2-layered system and first evidence of the (Li/Na/Na)CoO2 phase with OPP9 oxygen stacking[J]. Inorganic Chemistry, 2011, 50(1): 2420-2430.
[16] REN Z, SHEN J, JIANG S, CHEN X, FENG C, XU Z, CAO G. Enhanced thermopower in an intergrowth cobalt oxide Li0.48Na0.35CoO2[J]. Journal of Physics: Condensed Matter, 2006, 18(29): 379-384.
[17] BOS J, HERTZ J, MOROSAN E, CAVA R. Magnetic and thermoelectric properties of layered LixNayCoO2[J]. Journal of Solid State Chemistry, 2007, 180(11): 3211-3217.
[18] 高 虹, 瞿玉春, 瞿秀静. 锂离子电池阴极材料LiCoO2的合成[J]. 中国有色金属学报, 1998,8(1): 185-187.
GAO Hong, ZHAI Yu-chun, ZHAI Xiu-jing. Preparation of LiCoO2 as cathode in secondary lithium battery[J]. The Chinese Journal of Nonferrous Metals, 1998,8(1): 185-187.
[19] HOLZAPFEL M, HAAK C. Lithium conductors of the system LiCo(1-x)Fe(x)O2 preparation and structural investigation[J]. Journal of Solid State Chemistry, 2001, 156(2): 470-479.
[20] WANG H, JANG Y. TEM study of electrochemical cycling-induced damage and disorder in LiCoO2 cathodes for rechargeable lithium batteries[J]. Journal of the Electrochemical Society, 1999, 146(2): 473-480.
[21] TAKAHASHI Y, GOTOH Y, AKIMOTO J. Single-crystal growth, crystal and electronic structure of NaCoO2[J]. Journal of Solid State Chemistry, 2003, 172(1): 22-26.
(编辑 龙怀中)
基金项目:长沙市科技计划资助项目(K 1005011-11)
收稿日期:2014-02-04;修订日期:2015-05-20
通信作者:艾延龄,副教授,博士;电话:13787182335;E-mail:ylai@csu.edu.cn