NaOH-Na2S熔盐法处理分银渣
田庆华,程利振,袁廷刚,辛云涛,郭学益
(中南大学 冶金与环境学院,湖南 长沙,410083)
摘要:采用NaOH-Na2S熔盐体系处理分银渣,并对熔炼过程进行研究,考察碱渣比、盐渣比、熔炼温度和熔炼时间对金属元素锑、锡、砷的分离以及对铅、铋、金、银富集效果的影响。研究结果表明:熔炼的优化条件为:碱渣比和盐渣比分别为0.4和2.0,熔炼温度500 ℃、熔炼时间60 min。在此优化条件下,熔炼产物经浸出后,金属元素锑、锡和砷浸出率分别达到87.7%,95.5%和63.0%,铅、铋、金和银不浸出,富集到浸出渣中。
关键词:分银渣;熔炼;浸出;富集
中图分类号:TF814;TF818 文献标志码:A 文章编号:1672-7207(2014)08-2553-06
Processing of silver separated residue by NaOH-Na2S molten salt method
TIAN Qinghua, CHENG Lizhen, YUAN Tinggang, XIN Yuntao, GUO Xueyi
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: The processing of silver separated residue (SSR) by NaOH-Na2S molten salt method was investigated. The effects of the mass ratio of NaOH to SSR, the mass ratio of Na2S・9H2O to SSR, smelting temperature and smelting time were studied on the leaching efficiencies of Sb, Sn and As, and the precipitations of Pb, Bi, Au and Ag into residue were also discussed. The results show that the optimum conditions of the process are determined as follows: the mass ratio of NaOH to SSR is 0.4, the mass ratio of Na2S・9H2O to SSR is 2.0, the smelting temperature is 500 ℃, and the smelting time is 60 min. The leaching rates of Sb, Sn and As reach 87.7%, 95.5% and 63.0%, respectively, while other metal elements, such as Pb, Bi, Au and Ag are left in the residue.
Key words: silver separated residue; smelting; leaching; enrichment
分银渣是铜阳极泥经过提取大部分的铜、硒、金、银后留下的残渣。由于分银渣中含有大量的金属铅、锡、锑、铋和一部分贵金属,故处理分银渣时,不仅要回收铅、锡、锑和铋,还要使贵金属富集,从而有利于资源综合利用和环境保护[1-4]。目前对于分银渣的研究主要集中在国内,普遍采用酸法浸出,即采用盐酸、硫酸、硝酸分离其中的某些金属。李义兵等[5-7]采用HCl-NaCl体系同时提取铅和锑以及采用亚硫酸钠和硫代硫酸钠从分银渣中提取银;孙文达[8]研究了用氯化法提取金并富集铂、钯的工艺。酸法浸出选择性差,浸出液中杂质含量高,不利于后续工艺的提取。关于熔盐体系的研究,有报道采用碱浸[9-10]、碱熔[11]回收锡冶炼工艺中的锡泥、锡渣、锡中矿;Brostow等[12-18]采用硫化碱水溶液预处理富银矿、电路板污泥、黝铜矿以及复杂辉锑矿等。通过硫化碱解离其矿物结构,金属锡、锑和砷等进入到溶液中,浸出液成分相对单一[19-21],贵金属富集到浸出渣中。实验研究表明:碱法浸出体系选择性虽高,但金属浸出率偏究低,浸出渣中待分离元素含量偏高,仍需后续处理,且碱性浸出液体积量大,后续处理困难。低温碱性熔炼[22]是在相对低的熔融温度条件下的碱性介质中,将某些难回收金属元素形态转型为易于后续分离提取的金属形态,包括熔融温度下的氧化、还原和固化、硫化等,从而应用于分解含氧酸盐矿以及从精矿或尾渣中分离酸性或者两性物质的反应过程,过程温度低、清洁、低碳、适宜处理多金属复杂物料[22]。为了同时分离分银渣中的锡、锑、砷以及富集铅、铋、金和银,缩短工艺流程,降低碱耗,提高资源利用率,保护环境,本文作者采用NaOH-Na2S熔炼体系处理分银渣,对熔炼过程的工艺条件进行系统研究,以期为分银渣的清洁回收提供实验和理论依据。
1 实验
1.1 实验原料
实验所用主要原料阳极泥分银渣为国内某厂阳极泥经过硫酸化焙烧―分铜浸出―氯化分金―氨浸分银工艺提取其中金、银、铂、钯等金属后所留下残渣,其主要成分见表 1。从表1可以看出:原料中铅、锡、锑、铋的品位较高,含有少量的贵金属金和银。图1所示为分银渣的XRD谱。由图 1可以看出:原料中的Pb和Sb主要以Pb7Sb8S19,Pb5(AsO4)3Cl,Pb5Ag3S24和Sb2O3的形式存在,金属Sn和Bi主要以SnO2和Bi2O3的形式存在。实验所用的NaOH,Na2S・9H2O以及实验分析所用的试剂均为分析纯。
表1 实验用分银渣主要成分(质量分数)
Table 1 Compositions of silver separated residue in experiment %
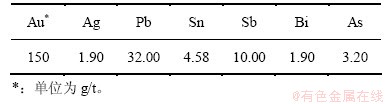
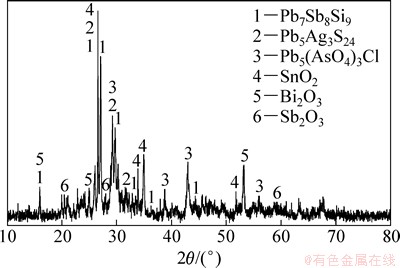
图1 分银渣的XRD光谱
Fig. 1 XRD pattern of silver separated residue
1.2 实验装置
实验装置主要包括SRJX箱式电炉、DF-101S型集热式恒温磁力搅拌器、循环水式真空泵和电热恒温鼓风干燥箱等。
1.3 实验过程
取10 g烘干磨细(粒径<150 μm)的分银渣,与一定量的NaOH和Na2S・9H2O浆化混匀后装入刚玉坩埚中,放进电炉中在设定温度下进行熔炼反应,反应结束后,取出刚玉坩埚在空气中自然冷却,所得熔炼产物在固定的条件下加入烧杯中水浸,固定浸出温度80 ℃、浸出时间60 min、液固比4:1和搅拌速度300 r/min,经液固分离后,量取浸出液体积,然后取样分析。
熔炼过程各主要金属元素的浸出率为
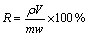 (1)
(1)
式中:R为各种元素的浸出率,%;ρ为溶液中金属的质量浓度,g/L;V为浸出液的体积,L;m为分银渣的质量,g;w为分银渣中各元素的质量分数,%。
1.4 分析表征
利用美国 Baird 公司生产的PS-6 真空型电感耦合等离子体原子发射光谱仪(ICP-AES)和原子吸收分光光度计(AAS)分析浸出液中Pb,Sn,Sb,Bi,As,Au和Ag的含量,用日本理学生产的3014Z型X线衍射分析仪(XRD)测定分银渣和浸出渣的物相及晶体结构等特征。利用德国PW-1404型X荧光光度计(XRF)分析分银渣和浸出渣各元素含量。
2 结果与讨论
2.1 未添加硫化钠时碱渣比对金属浸出率的影响
当熔炼温度为500 ℃和熔炼时间为90 min时,不同碱渣比对分银渣中金属浸出率影响如图2所示。由图2可见:当碱渣比增加到1.0时,锡、锑和砷的浸出率分别为84%,49%和0.66%,过程中铋不浸出;当碱渣比小于1.0时,铅的浸出率很低,在碱渣比大于1.0时,浸出率增加了5%左右;砷的浸出率相对稳定。熔炼过程主要发生以下反应:
SnO2+2NaOH=Na2SnO3+H2O(g) ↑ (2)
3SnS2+6NaOH=2Na2SnS3+Na2SnO3+H2O(g) ↑ (3)
Pb5(AsO4)3Cl+12NaOH=5Na2PbO2+3Na3AsO4+NaCl+10H2O(g)↑ (4)
Bi2O3+6NaOH=2Na3BiO3+3H2O(g)↑ (5)
由式(2)和(3)可知:分银渣中SnO2和SnS2与熔融碱反应生成了易溶于碱性溶液的Na2SnO3和Na2SnS3,且随碱渣比增加,浸出率增加。分银渣中的Sb2S3极易氧化[23],当其粒度为0.1 mm时,着火点为200 ℃,故反应式(6)在500 ℃条件下很容易进行,生成的Sb2O3微溶于碱,因此锑浸出率低。
2Sb2S3+9O2= 2Sb2O3+6SO2 (6)
由图2可知:当溶液中锡和砷浸出率稳定后,NaOH才与铅和铋反应生成可溶性盐类,反应式见式(4)和式(5),生成的Na2PbO2随着溶液中碱渣比增加到1.2时,铅浸出率为7.4%,而生成的Na3BiO3在浸出过程中很容易水解为Bi(OH)3沉淀进入渣中,故铋在溶液中不浸出;过程中金和银均不浸出。因此,选择碱渣比1.0作为后续实验条件。
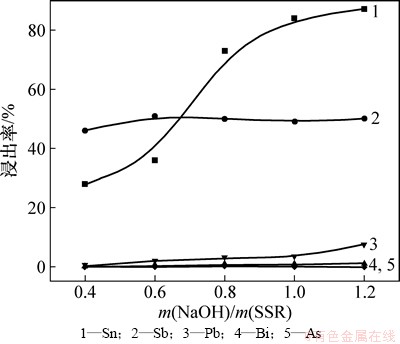
图2 NaOH与分银渣质量比对金属浸出率的影响
Fig. 2 Effect of mass ratio of NaOH to SSR on leaching rate of metals
2.2 盐渣比对金属浸出率影响
根据低价锑酸盐在硫化钠碱性溶液中易于溶解,而铋酸钠和铅酸钠在硫化钠碱性溶液中生成了溶度积更小的硫化铋和硫化铅沉淀,从而使得锑、锡和砷进入溶液,而铅、铋及金、银进入渣中,后续研究拟利用添加硫化钠彻底分离铅、铋、金、银和锑、锡、砷。
当固定碱渣比为1.0,熔炼温度为500 ℃和熔炼时间为90 min时,考察不同盐渣比对分银渣中金属浸出率的影响,如图3所示。由图3可见:当盐渣比从0.8增加到1.0时,锡的浸出率从76%增加到86%,原因是Na2S・9H2O与分银渣中的SnS2进行了反应,反应式见式(7);继续增加Na2S用量时,锡浸出率稳定在85%左右;随着盐渣比的增加,金属锑浸出率在盐渣比0.8~1.8之间快速上升,这是因为Na2S在熔炼过程中与金属锑的硫化物以及氧化物生成了Na3SbS3等易溶于硫化碱水溶液的钠盐,反应式见式(8);而按照式(4)和式(5)反应生成的Na2PbO2和Na3BiO3与 Na2S・9H2O分别按式(9)和式(10)反应生成了PbS和Bi2S3,PbS和Bi2S3在硫化钠碱性溶液中溶度积均在10-4以下[23],故在溶液中检测不到铅、铋、金和银。
SnS2+2Na2S=2Na4SnS4 (7)
2Sb2O3+6Na2S+3H2O=2Na3SbS3+6NaOH (8)
Na2PbO2+Na2S+2H2O=PbS↓+4NaOH (9)
2Na3BiO3+3Na2S+6H2O=Bi2S3↓+12NaOH (10)
当盐渣比为2.0时,锡和锑浸出率最高,分别为90%和85%左右,而砷浸出率比较稳定,为56%左右,铅、铋、金和银均不浸出,因此,选择盐渣比2.0作为后续实验条件。
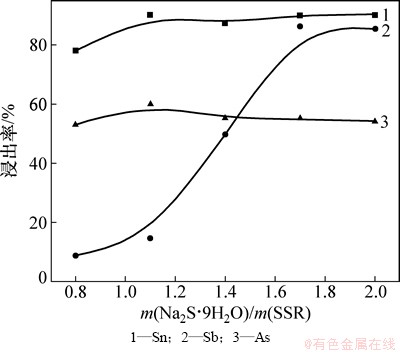
图3 Na2S・9H2O与分银渣质量比对金属浸出率的影响
Fig. 3 Effect of mass ratio of Na2S・9H2O to SSR on leaching rate of metals
2.3 添加硫化钠时碱渣比对金属浸出率影响
为了研究分银渣中金属锡、锑、砷与铅、铋、金、银在碱性熔炼过程中与碱反应程度,进一步考察了当固定盐渣比为2.0,熔炼温度为500 ℃和熔炼时间为90 min时,不同碱渣比对分银渣中金属浸出率的影响,如图4所示。由图4可见:当碱渣比从0.2增加到0.4时,锡、锑和砷的浸出率分别从88%,77%和58%增加到95%,89%和62%,碱渣比继续增加时,锡、锑和砷浸出率基本无变化,铅、铋、金和银均不浸出。因此选择碱渣比0.4作为后续实验条件。
2.4 熔炼温度对金属浸出率的影响
当固定碱渣比为0.4,盐渣比为2.0和熔炼时间为90 min时,考察不同熔炼温度对分银渣中金属浸出率影响,如图5所示。由图5可见:当熔炼温度从300 ℃升高到500 ℃时,水溶液浸出后金属锡的浸出率从87%增加到92%,砷浸出率波动不大,浸出率为63% 左右;当熔炼温度从300 ℃升高到400 ℃时,锑浸出率从82%减少到75%,而当熔炼温度从400 ℃升高到500 ℃时,锑浸出率从75%增加到89%;锑浸出率波动的原因是:分银渣中的Sb2S3及低价氧化锑在380 ℃左右时易生成Sb2O4,而Sb2O4需要更高的反应温度,才能与硫化钠碱性熔体进行反应[24],故当熔炼温度从400 ℃升高到500 ℃时,水溶液浸出后,锑浸出率从75%增加到89%。此过程中铅、铋、金和银均不浸出,选择熔炼温度500 ℃作为后续实验条件。
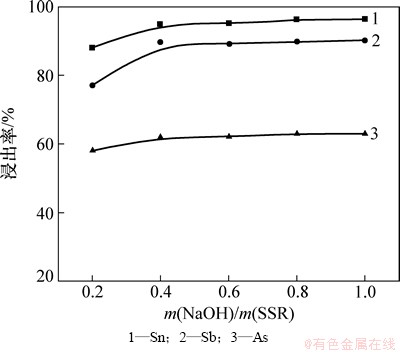
图4 NaOH与分银渣质量比对金属浸出率的影响 (固定盐渣比2:1)
Fig. 4 Effect of mass ratio of NaOH to SSR on leaching rate of metals (m(Na2S・9H2O)/m(SSR)=2:1)
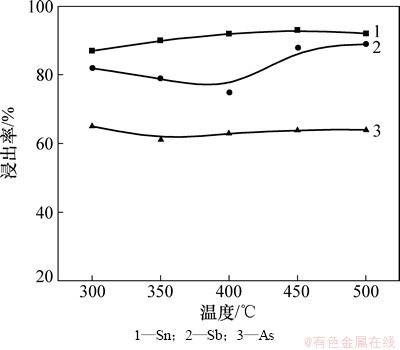
图5 熔炼温度对分银渣金属浸出率的影响
Fig. 5 Effect of smelting temperature on metals leaching rate of SSR
2.5 熔炼时间对金属浸出率的影响
当固定碱渣比为0.4、盐渣比为2.0和熔炼温度为500 ℃时,不同熔炼时间对分银渣中金属浸出率的影响,如图6所示。由图6可见:当熔炼时间从20 min增加到60 min时,锡、锑和砷的浸出率分别从55%,77%和60%增加到94%,85%和65%,改变熔炼时间对锡浸出率影响较锑和砷明显;当熔炼时间从60 min增加到100 min时,3种金属浸出率均未得到明显提高,说明熔炼反应过程在60 min内可以完成。此过程中铅、铋、金和银不浸出,因此选择熔炼时间60 min作为后续实验条件。
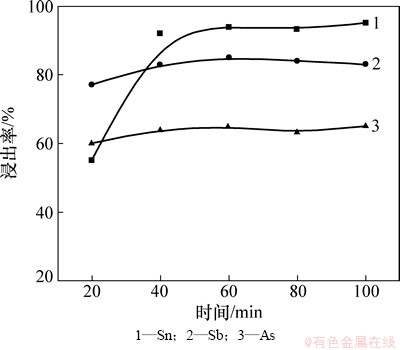
图6 熔炼时间对分银渣金属浸出率的影响
Fig. 6 Effect of smelting time on metals leaching rate of SSR
2.6 碱性熔炼优化条件实验
综合各因素实验的较佳条件进行5组平行优化实验,当熔炼温度为500 ℃、熔炼时间为60 min、碱渣比为0.4和盐渣比2.0时,锑、锡和砷的平均浸出率分别为 87.7%,95.5%和63.0%,从而实现锑、锡、砷和铅、铋、金、银的分离。在优化条件下浸出渣中金属质量分数分别如表2所示,浸出渣中富集了几乎全部的铅、铋、金和银。图7所示为在优化条件下得到的浸出渣的XRD分析结果。从图7可知,浸出渣物相结构比起原料变得更单一,主要为铅、铋的硫化物PbS,Pb0.816Bi0.123S,以及银的单质金属态(Ag0.7Fe0.3)。此外,固定最佳碱渣比和盐渣比直接浸出分银渣,锑、锡和砷的浸出率仅为26%,13%和51%,说明经过NaOH-Na2S熔盐体系熔炼过程处理能够显著提高分银渣中金属锑和锡的浸出率。
表2 优化条件下浸出渣主要成分(质量分数)
Table 2 Main chemical components of leaching residue under optimum conditions %

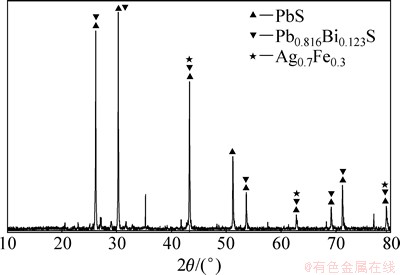
图7 浸出渣的XRD光谱
Fig. 7 XRD patterns of leaching residue
3 结论
(1) 采用NaOH-Na2S熔盐体系处理分银渣,并对熔炼过程进行研究,熔炼产物经浸出后,分银渣中金属元素锑、锡、砷和铅、铋、金、银得到了高效选择性的分离,锑、锡和砷进入溶液中,铅、铋、金和银在浸出渣中富集。
(2) NaOH-Na2S熔盐体系处理分银渣最佳工艺条件如下:当熔炼温度为500 ℃、熔炼时间为60 min、碱渣比和盐渣比分别为0.4和2.0时,锑、锡和砷浸出率分别达到了87.7%,95.5%和63.0%,铅、铋、金和银富集到浸出渣中。
(3) 浸出渣主要物相主要为硫化铅、硫化铋及银单质形态。
参考文献:
[1] 黎鼎鑫, 王永录. 贵金属提取与精炼[M]. 长沙: 中南大学出版社, 2003: 377-393.
LI Dingxin, WANG Yonglu. Extraction and refining of precious metal[M]. Changsha: Central South University, 2003: 377-393.
[2] 吴艳新. 从铜阳极泥分银渣中综合回收利用锡的研究[D]. 赣州: 江西理工大学冶金与化学学院, 2013: 5-12.
WU Yanxin. Study on the comprehensive recovery of tin from silver-separated residue[D]. Ganzhou: Jiangxi University of Science and Technology. School of Metallurgical and Chemistry Engineering, 2013: 5-12.
[3] 安娟. 分银渣中有价元素高效回收利用新工艺[D]. 长沙: 中南大学冶金科学与工程学院, 2012: 1-15.
AN Juan. New technology of efficient recycling of valuable elements in silver separating residue[D]. Changsha: Central South University. School of Metallurgy Science and Engineering, 2012: 1-15.
[4] 诸向东, 汪洋, 李仕雄, 等. 分银渣中有价金属高效回收利用[J]. 矿冶工程, 2012, 32(6): 86-89.
ZHU Xiangdong, WANG Yang, LI Shixiong, et al. Efficient recycling of valuable metals from silver separating residue[J]. Mining and Metallurgy Engineer, 2012, 32(6): 86-89.
[5] 李义兵, 陈白珍, 王之平, 等. 分银渣铅锑浸出工艺研究[J]. 有色金属(冶炼部分), 2004(5): 9-11.
LI Yibing, CHEN Baizhen, WANG Zhiping, et al. Study on leaching process of lead and antimony from silver separated residue[J]. Nonferrous Metals (Extractive Metallurgy), 2004(5): 9-11.
[6] 李义兵, 陈白珍, 龚竹青, 等. 用亚硫酸钠从分银渣中浸出银[J]. 湿法冶金, 2003, 22(1): 34-37.
LI Yibing, CHEN Baizhen, GONG Zhuqing, et al. Leaching of Ag from residue containing silver with sodium sulfite[J]. Hydrometallurgy of China, 2003, 22(1): 34-37.
[7] 张钦发, 龚竹青, 陈白珍. 用硫代硫酸钠从分银渣中提取银[J]. 贵金属, 2003, 24(1): 5-9.
ZHANG Qianfa, GONG Zhuqing, CHEN Baizhen. Extracting Ag from residue containing silver with Na2S2O3[J]. Precious Metals, 2003, 24(1): 5-9.
[8] 孙文达. 分银渣中贵金属的回收[J]. 铜业工程, 2008(1): 35-36.
SUN Wenda. Precious metals recovery in silver separating residue[J]. Copper Engineering, 2008(1): 35-36.
[9] 张荣良, 丘克强. 从含锡渣中提取锡制取锡酸钠的研究[J]. 矿冶, 2008, 17(1): 35-41.
ZHANG Rongliang, QIU Keqiang. Research on extracting tin and preparation of sodium stannate from slag containing tin[J]. Mining & Metallurgy, 2008, 17(1): 35-41.
[10] 曹学增, 陈爱英. 电镀锡渣制备氯化亚锡和锡酸钠[J]. 应用化工, 2002, 31(3): 38-40.
CAO Xuezeng, CHEN Aiying. Preparation of tin dichloride and sodium stannate from electroplatet in wasteslug[J]. Applied Chemical Industry, 2002, 31(3): 38-40.
[11] 谢克强. 锡中矿提取锡的新工艺研究[J]. 有色金属设计, 1999, 26(1): 20-24.
XIE Keqiang. A new technology research on extracting tin from tin separation middlings[J]. Nonferrous Metals Design, 1999, 26(1): 20-24.
[12] Brostow W, Gahutishvili M, Gigauri R, et al. Separation of natural trivalent oxides of arsenic and antimony[J]. Chemical Engineering Journal, 2010, 159(3): 24-26.
[13] Bala P, Achimovi O M. Selective leaching of antimony and arsenic from mechanically activated tetrahedrite, jamesonite and enargite[J]. International Journal of Mineral Processing, 2006, 81(1): 44-50.
[14] Kuchar D, Fukuta T, Onyango M S, et al. Sulfidation treatment of copper-containing plating sludge towards copper resource recovery[J]. Journal of Hazardous Materials, 2006, 138(1): 86-94.
[15] Kuchar D, Fukuta T, Onyango M S, et al. Sulfidation treatment of molten incineration fly ashes with Na2S for zinc, lead and copper resource recovery[J]. Chemosphere, 2007, 67(8): 1518-1525.
[16] Ubaldini S, Veglio F, Fornari P, et al. Process flow-sheet for gold and antimony recovery from stibnite[J]. Hydrometallurgy, 2000, 57(3): 187-199.
[17] Li Y H, Liu Z H, Li Q H, et al. Removal of arsenic from Waelz zinc oxide using a mixed NaOH-Na2S leach[J]. Hydrometallurgy, 2011, 108(3/4): 165-170.
[18] Celep O, Alp I, Deveci H. Improved gold and silver extraction from a refractory antimony ore by pretreatment with alkaline sulphide leach[J]. Hydrometallurgy, 2011, 105(3/4): 234-239.
[19] Tongamp W, Takasaki Y, Shibayama A. Precipitation of arsenic as Na3AsS4 from Cu3AsS4-NaHS-NaOH leach solutions[J]. Hydrometallurgy, 2010, 105(1/2): 42-46.
[20] Tongamp W, Takasaki Y, Shibayama A. Arsenic removal from copper ores and concentrates through alkaline leaching in NaHS media[J]. Hydrometallurgy, 2009, 98(3/4): 213-218.
[21] Samuel A A, Sandstrom A. Selective leaching of arsenic and antimony from a tetrahedrite rich complex[J]. Minerals Engineering, 2010, 23(15): 1227-1236.
[22] 赵由才, 张承龙, 蒋家超. 碱介质湿法冶金技术[M]. 北京: 冶金工业出版社, 2009: 10-16.
ZHAO Youcai, ZHANG Chenglong, JIANG Jiachao. The hydrometallurgical technology in alkaline media[M]. Beijing: Metallurgical Industry Press, 2009: 10-16.
[23] 赵瑞荣, 石西昌.锑冶金物理化学[M]. 长沙: 中南大学出版社, 2006: 10-15.
ZHAO Ruirong, SHI Xichang. The metallurgical physical chemistry of antimony[M]. Changsha: Central South University, 2006: 10-15.
[24] 雷霆, 朱从杰,张汉平. 锑冶金[M]. 北京: 冶金工业出版社, 2009: 255-258.
LEI Ting, ZHU Congjie, ZHANG Hanping. Antimony metallurgy[M]. Beijing: Metallurgical Industry Press, 2009: 255-258.
(编辑 赵俊)
收稿日期:2013-09-26;修回日期:2013-12-10
基金项目:国家自然科学基金重点资助项目(51234009)
通信作者:郭学益(1966-),男,湖南长沙人,博士,教授,从事难冶有色金属提取、资源循环利用及环境材料制备研究;电话:0731-88877863;E-mail:xyguo@csu.edu.cn