文章编号:1004-0609(2013)10-2868-07
锂离子筛前驱体Li4Mn5O12的制备及性能
许 惠1, 2,陈昌国1,宋应华2,卓 琳2
(1. 重庆大学 化学化工学院,重庆 400030;
2. 重庆工商大学 环境与生物工程学院,重庆 400067)
摘 要:以水热法自制γ-MnOOH和LiOH・H2O为原料,在较低温度下固相反应制备出尖晶石型Li4Mn5O12,经酸浸脱锂后得到对Li+具有特殊选择性的MnO2离子筛。研究该离子筛对Li+的吸附性能和选择性,并用XRD、SEM和FT-IR等和Li+选择性吸附研究固相反应工艺对离子筛材料结构、化学组成及离子交换性质的影响。结果表明:煅烧时间对前驱体的生成有较大影响,由400 ℃煅烧32 h所得的前驱体为纯相Li4Mn5O12化合物,经酸浸脱锂后的离子筛仍保持与前驱体相同的尖晶石结构;锰源γ-MnOOH、前驱体Li4Mn5O12和离子筛MnO2均为低维棒状结构形貌;离子筛对锂的吸附速率符合一级动力学Lagergren方程,饱和吸附容量为40.2 mg/g,并具有较好的Li+选择性。
关键词:Li4Mn5O12;离子筛;前驱体;吸附
中图分类号:TQ174 文献标志码:A
Synthesis and properties of lithium ion-sieve precursor Li4Mn5O12
XU Hui1, 2, CHEN Chang-guo1, SONG Ying-hua2, ZHUO Lin2
(1. College of Chemistry and Chemical Engineering, Chongqing University, Chongqing 400030, China;
2. School of Environmental and Biological Engineering, Chongqing Technology and Business University, Chongqing 400067, China)
Abstract: Spinel-type Li4Mn5O12 precursors were synthesized from γ-MnOOH self-prepared by hydro-thermal method and LiOH・H2O by low temperature solid-phase reaction. Furthermore, MnO2 ion-sieves with Li+ selective adsorption property were prepared by the acid treatment process to extract Li+ from the spinel Li4Mn5O12 precursor. The effects of solid-phase reaction process on the structure, chemical composition and ion-exchange property of the ion-sieve material were investigated by XRD, SEM, FT-IR and Li+ selective adsorption measurements. The results show that calcination time has the considerable effect on the precursor. The precursor synthesized at 400 ℃ for 32 h is a pure Li4Mn5O12. Final MnO2 ion-sieve and Li4Mn5O12 precursor have a low-dimensional rod-like morphology link γ-MnOOH and share the same structure of spinel. The adsorption rate of ion-sieve is consistent with the pseudo-first order kinetic equation of Lagergren. The Li+ saturated adsorption capacity is 40.2 mg/g, and the ion-sieve shows good Li+ selection.
Key words: Li4Mn5O12; ion-sieve; precursor; adsorption
锂在国民经济、国防建设,尤其是新能源等领域应用广泛。我国拥有全球少有的盐湖锂资源,开发盐湖卤水提锂技术,是我国锂生产行业的研究热点。但盐湖卤水中微量的Li+与大量的Mg2+共存,且由于Mg2+、Li+性质十分相近,使Li+、Mg2+分离十分困难,是盐湖卤水提锂尚未解决的重大技术瓶颈。利用高选择性吸附剂进行Li+的分离富集,被公认为是从低浓度卤水中提取锂最有前途的方法[1-4]。因此,研究高性能锂吸附材料是解决这一技术瓶颈的关键。
目前,研究较多的正尖晶石型LiMn2O4因其Mn―O骨架构成了有利于Li+嵌入和脱出的四面体与八面体三维内部空间结构,且在Li+嵌入和脱出后仍维系结构不变,除被用作锂离子二次电池正极材料外[5-6],亦被广泛研究用作锂吸附材料[7-10]。但由于该LiMn2O4中锰的平均化合价为3.5,在酸浸脱除Li+过程中,LiMn2O4中的Mn3+易发生歧化反应[11],生成Mn4+和Mn2+,Mn4+留在尖晶石骨架中,Mn2+进入溶液,Mn2+的溶解导致尖晶石结构被破坏,离子筛的循环稳定性差是目前锂锰氧化物作为离子筛应用存在的关键问题。富锂型Li4Mn5O12因过量的锂离子取代锰离子,其Mn的存在价态皆为+4价,提高了锂锰氧化物中锰的存在价态,可有效抑制Mn的溶损、提高尖晶石结构的稳定性,因而成为最有开发前途的锂吸附材料[12]。
由于Li4Mn5O12不稳定,在空气中温度超过500 ℃分解成LiMn2O4和Li2MnO3[13],纯相Li4Mn5O12的合成较困难。目前,Li4Mn5O12的制备方法主要有熔盐 法、高温固相反应法、水热-高温固相反应法等。其中,熔盐法[14-15]反应时间长,锂盐浪废大;高温固相法[16-17]需要在氧气气氛下进行,反应条件苛刻;水热-低温固相反应[12, 18]作为一种软化学方法,工艺简单,操作可控,引起了人们的关注。
本文作者以水热法自制的γ-MnOOH为锰源,通过低温固相反应制备出纯相Li4Mn5O12前驱体,并经酸浸脱锂后得到MnO2离子筛。与现已研究的锂锰氧化物锂离子筛合成技术相比,本研究方法具有合成方法较简单、目标材料酸溶损率低、选择性高、饱和吸附容量大的特点。
1 实验
1.1 材料的制备
1.1.1 γ-MnOOH的制备
称取10 g分析纯KMnO4于反应釜中,按化学计量加入一定量体积分数为5%乙醇溶液,在120 ℃下水热反应14 h,自然冷却后将产物过滤洗涤,在60 ℃下干燥后得到γ-MnOOH,记为MO。
1.1.2 锂离子筛的制备
将制得的γ-MnOOH(MO)按摩尔比n(Li)/n(Mn)= 0.80加入LiOH・H2O,并加入适量乙醇溶液将原料进行湿法混合,在90 ℃水浴加热下搅拌直至溶液蒸干,再在110 ℃烘箱中彻底干燥,然后在马弗炉中于400 ℃下煅烧不同时间(12 h、18 h、24 h、32 h),得到离子筛前驱体,分别记为LMO-12、LMO-18、LMO-24和LMO-32。将2 g离子筛前驱体LMO-32,放入置有200 mL、0.5 mol/L盐酸溶液的具塞三角烧瓶中,在25 ℃下恒温振荡浸取5 h,过滤、洗涤、干燥得到离子筛SMO,用原子吸收光谱仪测定滤液中的Li+及Mn2+浓度。
1.2 结构与形貌分析与表征
采用德国Bruker公司生产的D8 ADVANCE型X射线衍射仪对各产物进行晶相分析,其中XRD的分析条件如下:Cu Kα靶,扫描电压40 kV,电流30 mA,扫描范围10°~80°,扫描速度10 (°)/min。采用英国OXFORD公司生产的TESCAN VEGAII型扫描电子显微镜对各产物进行形貌观察。采用美国PE公司生产的Spectrum I型傅立叶红外分析仪进行红外光谱分析,KBr压片,波数范围450~4 000 cm-1。
采用EDTA络合滴定法测定锰总量,采用草酸钠-高锰酸钾返滴定法[19]测定锰的平均化合价;采用日本日立公司生产的Z5000原子吸收光谱法测定溶液中Li+和微量Mn2+的浓度。
1.3 吸附实验
1.3.1 吸附动力学
准确称取1.0 g离子筛粉末置入具塞三角烧瓶中,加入0.5 g/L的LiCl溶液200 mL,滴加2 mol/L NaOH溶液保持溶液pH在8.0左右,在25 ℃下恒温振荡,在不同的时间取上层清液,采用原子吸收光谱仪测定吸附前后溶液中锂离子的浓度变化。锂离子筛对锂的吸附容量qt(mg/g)可由式(1)计算得到:
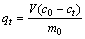 (1)
(1)
式中:V为吸附Li+溶液的体积,L;c0和ct分别表示开始吸附和t时刻Li+的浓度,mg/L;m0为离子筛MnO2的质量,g。
1.3.2 共存金属离子的分配系数(选择性)实验
将0.5 g离子筛分别置入含50 mL浓度均为20 mmol/L Li+、Na+、K+、Ca2+和Mg2+的具塞三角烧瓶中,用氨水-氯化铵缓冲溶液调节溶液pH=8.0,在25 ℃下恒温振荡,2 d后达到平衡,静置取上清液,用原子吸收光谱仪测定各离子的浓度。被吸附的各金属离子的分配系数(Kd)和选择性系数(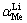 )(Me为Na+、K+、Ca2+、Mg2+)分别由式(2)及(3)计算得到:
)(Me为Na+、K+、Ca2+、Mg2+)分别由式(2)及(3)计算得到:
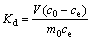 (2)
(2)
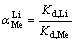 (3)
(3)
式中:ce表示吸附达到平衡时各离子的浓度,mg/L。
2 结果与讨论
2.1 前驱体的制备
图1所示为γ-MnOOH与氢氧化锂的混合物在 400 ℃静态空气中分别煅烧不同时间(12 h、18 h、24 h、32 h)获得锂锰氧前驱体(LMO)的XRD谱。
由图1可见,煅烧时间对目标产物的生成有较大影响。当煅烧时间为12 h时,样品在2θ=23.1o、28.8o与33.5o处出现了少量方铁锰矿Mn2O3晶相(JCPDS 24―0508),表明反应还未进行完全;随着反应时间的延长,所得目标产品的特征峰均与标准Li4Mn5O12相吻合(JCPDS 46―0810),属纯立方相,空间点群结构为Fd3m(227),且衍射峰的强度随着煅烧时间的延长而增大,峰型更加尖锐,特别是(400)晶面特征峰的强度随着煅烧时间的延长逐渐增强。
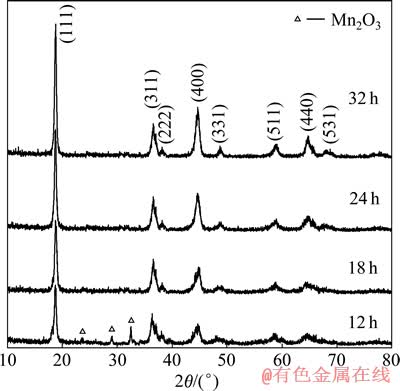
图1 不同煅烧时间下制备的Li4Mn5O12前驱体的XRD谱
Fig. 1 XRD patterns of Li4Mn5O12 precursors calcined at 400 ℃ for different times
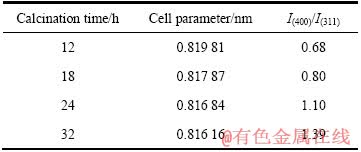
表1所列为不同时间所得样品的晶胞参数和I(400)与I(311)的强度比值。富锂型Li4Mn5O12可以表示为Li[Li0.33Mn1.67]O4,过量的Li+将占据锰所在16d位置[20],从表1可以看出,所合成样品的晶胞参数明显小于正尖晶石LiMn2O4的晶胞参数(0.823 80 nm),这是由于Li+占据部分八面体16d位置,从而引起锰的平均化合价增大,即Mn4+浓度增大。锰的价态越高,对阴离子O2-的极化作用越大,则锰与氧原子形成的骨架越紧密,从而导致晶胞收缩变小[18]。另外,特征峰(400)与(311)的强度比值反映材料中Li+占据部分八面体16d位置的情况[21],比值越大,表明占据八面体16d位置的Li+量越多,导致(400)晶面的生长速度超过 (311)晶面的生长速度,使得结构转向更加有序的八面体结构,从而可以有效抑制Jahn-Teller效应[22]。随着煅烧时间的增加,样品的I(400)/I(311)逐渐增大,说明随着反应时间增加,Li取代16d位置的Mn越多。
表1 400 ℃、不同煅烧时间下制备的前驱体的晶体结构参数
Table 1 Cell parameters of precursors calcined at 400 ℃ for different times
研究400 ℃煅烧不同时间(12 h、18 h、24 h、32 h)获得锂锰氧前驱体(LMO)中锰的质量分数及平均化合价,结果见表2。
表2 400 ℃不同煅烧时间下制备的前驱体中锰的含量及平均化合物
Table 2 Mn content and average valence of precursors calcined at 400 ℃ for different times
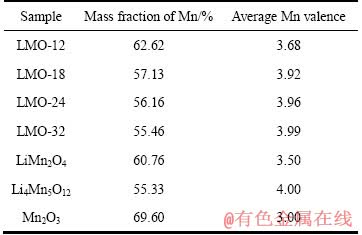
由表2可以看出,400 ℃煅烧12 h所得样品的化合价最低,且锰的质量分数最高,主要是样品中含有Mn2O3杂相的缘故,而其他煅烧时间(18 h、24 h、32 h)获得锂锰氧前驱体中锰的平均化合价均较高,超过3.9,接近于4,这说明前驱体中Mn3+含量大大降低,这将有助于降低材料在酸浸过程中锰的溶损,提高材料的稳定性。同时,锰的总量介于正尖晶石LiMn2O4和Li4Mn5O12中锰的总量之间,表明这些产物不是纯相的富锂型尖晶石相Li4Mn5O12。其中,于400 ℃煅烧32 h所得的前驱体中锰的总量及锰的平均化合价最接近于富锂型尖晶石相 Li4Mn5O12的,几乎可以认为是纯相的Li4Mn5O12化合物。
2.2 离子筛的制备
2.2.1 酸浸处理制备离子筛
将400 ℃煅烧32 h所得前驱体LMO采用0.5 mol/L的稀盐酸酸浸处理制备相应的离子筛SMO。化学分析表明,前驱体Li4Mn5O12中锂的脱出率为98%,锰的溶损率为0.8%,显示出较好的化学稳定性。图2所示为前驱体及相应离子筛SMO的XRD谱。
从图 2 中可以看出,经酸处理后的样品SMO为纯的立方相λ-MnO2 (JCPDS 44-0992),对比酸浸脱锂前后样品的XRD谱可以看出,经酸处理后样品的特征峰强度减弱,且经酸处理后的离子筛的衍射峰2θ角较前驱体的向右发生了一定的偏移,表明Li+脱出后样品的晶胞发生了收缩,但仍保持着与前驱体相同的尖晶石结构,这表明在酸浸脱锂过程中Mn―O骨架非常稳定。
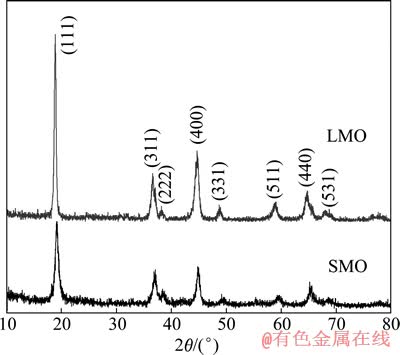
图2 前驱体LMO和离子筛SMO的XRD谱
Fig. 2 XRD patterns of precursor LMO and ion-sieve SMO
2.2.2 形貌分析
图3所示为用扫描电镜观察到的各产物的微观形貌。从图3(a)可以看出,水热合成的γ-MnOOH为低维棒状的结构形貌,其直径在300 nm左右,长约5 μm,但不均匀。从图3(b)可以看出,经过煅烧所得的前驱体LMO仍然保持锰源的棒状结构形貌。由图3(c)可知,经酸处理后所得样品SMO与前驱体形貌相似,说明在酸洗后锂吸附剂的微观结构几乎不变,这也是锂离子筛能吸附锂的重要基础。只是酸浸后离子筛的棒状颗粒变得不光滑,似乎颗粒表面产生了溶解。

图3 不同样品的SEM像
Fig. 3 SEM images of different samples
2.2.3 红外光谱分析
图4所示为前驱体LMO和离子筛SMO的红外光谱。图中在1 100~2 500 cm-1范围内出现的吸收峰为背景峰(由于样品在空气气氛中测定)。
由图4可以看出,经过酸处理的离子筛SMO与前驱体LMO出峰位置基本相同,在630 cm-1及520 cm-1处出现的吸收峰可归属为Mn―O和Li―O特征振动峰,在3 430 cm-1附近出现的吸收峰为吸附水的伸缩振动峰,但对于SMO,在 910 cm-1附近出现了H质子的晶格藕合振动峰,该数据与文献[23]相同的结果,这说明在LMO转型为锂离子筛SMO的酸浸过程中,Li+从尖晶石骨架中溶出,同时H+进入了晶格,可以推测酸浸过程中发生了Li+-H+离子交换反应。
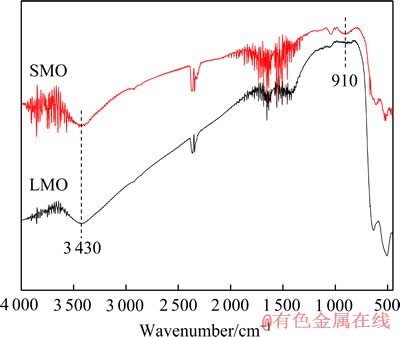
图4 前驱体LMO及离子筛SMO的FT-IR谱
Fig. 4 FT-IR spectra of precursor LMO and ion-sieve SMO
2.3 离子筛的吸附性能
2.3.1 离子筛的吸附动力学
图5(a)所示为SMO离子筛在常温下吸附动力学曲线。结果表明,锂吸附容量随着吸附时间的延长而增加。在起始阶段,离子交换进行得较快,12 h吸附容量可达到37 mg/g。随着吸附的进行,容量增长减慢,达到20 h后,吸附基本达到平衡,此时的吸附容量为40.2 mg/g。
根据王禄[24]提出的离子筛的理论最大锂交换能力以8 a位一个当量的嵌入锂来计算,约为6.5 mmol/g,即45 mg/g左右。在本研究中,所得离子筛饱和吸附容量达到40 mg/g,表现出较好的锂吸附性能和较大的吸附容量。
图5(b)所示为根据Lagergren方程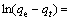
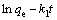 的模拟曲线,其中qe为离子筛的吸附容量,mg/g;k1为Lagergren吸附速度常数,s-1。由图5(b)可知,在吸附达到平衡之前,离子筛吸附速率符合一级动力学Lagergren 方程,吸附速率常数k1=6.71×10-5 s-1,该数值比文献[18]报道的吸附速率常数(3.29×10-4 s-1)小了5倍左右。
的模拟曲线,其中qe为离子筛的吸附容量,mg/g;k1为Lagergren吸附速度常数,s-1。由图5(b)可知,在吸附达到平衡之前,离子筛吸附速率符合一级动力学Lagergren 方程,吸附速率常数k1=6.71×10-5 s-1,该数值比文献[18]报道的吸附速率常数(3.29×10-4 s-1)小了5倍左右。
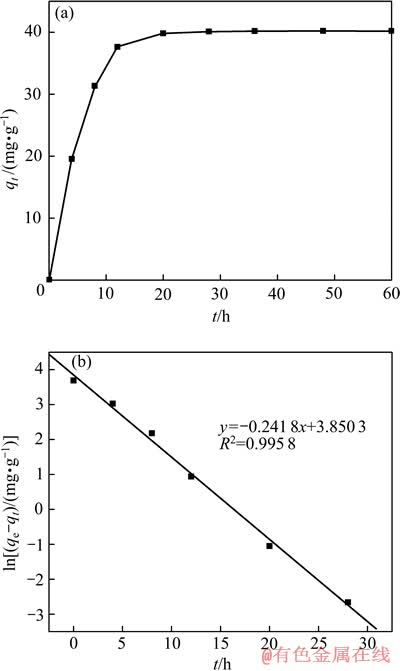
图5 离子筛吸附动力学曲线及Lagergren拟合曲线
Fig. 5 Adsorption kinetics curves of SMO (a) and simulated curve according to Lagergren equation (b)
2.3.2 共存金属离子的分配系数(选择性)
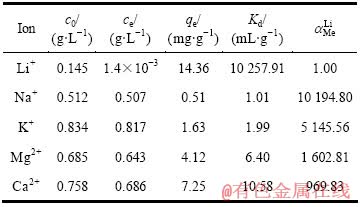
由于卤水中Li+ 通常与大量的碱金属离子和碱土金属离子共存,因此,选择性是离子筛最关键的技术特性。在静态吸附条件下,离子筛对卤水中主要杂质离子K+、Na+、Ca2+和Mg2+的吸附性和选择性研究结果见表3。
分配系数Kd是与离子筛的吸附容量qe有关的参数。吸附容量qe越大,则Kd也越大。分离因素是衡量离子筛对Li+及其他碱金属离子、碱土金属离子分离程度的参数,对Li+的吸附容量越大,对其他离子吸附容量越小,则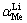 增大。由表3可见,离子筛SMO对碱金属及碱土金属离子的分配系数Kd由大到小的顺序为Li+、Ca2+、Mg2+、K+、Na+,分离因素
增大。由表3可见,离子筛SMO对碱金属及碱土金属离子的分配系数Kd由大到小的顺序为Li+、Ca2+、Mg2+、K+、Na+,分离因素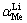 由小到大的顺序为Li+、Ca2+、Mg2+、K+、Na+,这表明离子筛对锂离子具有较高的选择性。同时离子筛的分配系数Kd, Li=10 257.91,与文献[18]报道的分离系数具有相同的数量级。离子筛对Li+的高选择 性主要是因为λ-MnO2具有三维通道,其孔道尺寸和Li+的半径相同,适合Li+的嵌入,即吸附过程中Li+可以进入三维通道中,而其他金属离子的离子半径较大,只能吸附在离子筛表面位置[18]。
由小到大的顺序为Li+、Ca2+、Mg2+、K+、Na+,这表明离子筛对锂离子具有较高的选择性。同时离子筛的分配系数Kd, Li=10 257.91,与文献[18]报道的分离系数具有相同的数量级。离子筛对Li+的高选择 性主要是因为λ-MnO2具有三维通道,其孔道尺寸和Li+的半径相同,适合Li+的嵌入,即吸附过程中Li+可以进入三维通道中,而其他金属离子的离子半径较大,只能吸附在离子筛表面位置[18]。
表3 金属离子在SMO离子筛上的Kd和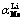
Table 3 Kd and 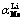 for metal ions on SMO ion-sieve
for metal ions on SMO ion-sieve
3 结论
1) 通过水热-低温固相反应制备了Li4Mn5O12前驱体。400 ℃煅烧32 h所得的前驱体几乎为纯相的Li4Mn5O12化合物,当用0.5 mol/L盐酸作为锂浸脱剂时,Li4Mn5O12前驱体的锰溶损率为0.8%,表现出较好的结构稳定性。
2) 常温下在0.5 g/L LiCl 溶液中离子筛的饱和吸附容量为 40.2 mg/g,分配系数为10 257.91 mL/g,表现出较高的Li+选择性。
REFERENCES
[1] TSUCHIYA S, NAKATANI Y, LBRAHIM R, OGAWA S. Highly efficient separation of lithium chloride from seawater[J]. Journal of the American Chemical Society, 2002, 124: 4936-4937.
[2] CHUNG K S, LEE J C, KIM W K, KIM S B, CHO K Y. Inorganic adsorbent containing polymeric membrane reservoir for the recovery of lithium from seawater[J]. Journal of Membrane Science, 2008, 325: 503-508.
[3] 董殿权, 张凤宝, 张国亮, 刘亦凡. Li4Ti5Ol2的合成及对Li+的离子交换动力学[J]. 物理化学学报, 2007, 23(6): 950-954.
DONG Dian-quan, ZHANG Feng-bao, ZHANG Guo-liang, LIU Yi-fang. Synthesis of Li4Ti5O12 and its exchange kinetics with Li+[J]. Acta Physico-Chimica Sinica, 2007, 23(6): 950-954.
[4] 刘骆峰, 张雨山, 黄西平, 张家凯, 王玉琪. 海水卤水提锂高效吸附剂的合成及应用研究[J]. 化学工业与工程, 2010, 27(2): 138-143.
LIU Luo-feng, ZHANG Yu-shang, HUANG Xi-ping, ZHANG Jia-kai, WANG Yu-qi. Synthesis and application of efficient adsorbent for lithium extraction from seawater and brines[J]. Chemical Industry and Engineering, 2010, 27(2): 138-143.
[5] ZHENG J P, CRAIN D J, ROY D. Kinetic aspects of Li intercalation in mechano-chemically processed cathode materials for lithium ion batteries: Electrochemical characterization of ball-milled LiMn2O4[J]. Solid State Ionics, 2011, 196: 48-58.
[6] 王英平, 王先友, 隗小山, 魏启亮, 杨秀康, 杨顺毅, 舒洪波, 白艳松, 吴 强. 以Mn3O4为前驱体制备尖晶石型LiMn2O4及其性能[J]. 中国有色金属学报, 2012, 22(8): 2276-2282.
WANG Ying-ping, WANG Xian-you, KUI Xiao-shan, WEI Qi-liang, YANG Xiu-kang, YANG Shun-yi, SHU Hong-bo, BAI Yan-song, WU Qiang. Preparation process and performance of spinel LiMn2O4 using Mn3O4 as precursor[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(8): 2276-2282.
[7]  C. Preparation and characterization of LiMn2O4 ion-sieve with high Li+ adsorption rate by ultrasonic spray pyrolysis[J]. Solid State Ionics, 2010, 181: 1425-1428.
C. Preparation and characterization of LiMn2O4 ion-sieve with high Li+ adsorption rate by ultrasonic spray pyrolysis[J]. Solid State Ionics, 2010, 181: 1425-1428.
[8] MA Li-wen, CHEN Bai-zhen, CHEN Yan, SHI Chan-xi. Preparation, characterization and adsorptive properties of foam-type lithium adsorbent[J]. Microporous and Mesoporous Materials, 2011, 142: 147-153.
[9] 王 禄, 马 伟, 韩 梅, 韩长功. 高效锂离子筛吸附剂MnO2・0.5H2O的软化学合成及吸附性能研究[J]. 化学学报, 2007, 65(12): 1135-1139.
WANG Lu, MA Wei, HANG Mei, HANG Chang-gong. Soft chemical synthesis and adsorption properties of MnO2・0.5H2O, a high performance ion sieve for lithium[J]. Acta Chimica Sinica, 2007, 65(12): 1135-1139.
[10] 马立文, 陈白珍, 石昌西, 冯大伟. 富锂锂锰氧化物的制备及其在溶液中的抽Li+/吸Li+性能[J]. 无机化学学报, 2011, 27(4): 697-703.
MA Li-wen, CHEN Bai-zhen, SHI Xi-chang, FENG Da-wei. Preparation and Li+ extraction/adsorption properties of lithium- rich manganese oxide in aqueous solution[J]. Chinese Journal of Inorganic Chemistry,2011, 27(4): 697-703.
[11] FENG Q, MIYAI Y, KANOH H. Li+ extraction/insertion with spinel-type lithium manganese oxides: Characterization of redox-type and ion-exchang-type site[J]. Langmuir, 1992, 8: 1861-1667.
[12] SUN Shu-ying, SONG Xing-fu, ZHANG Qin-hui, WANG Jin, YU Jian-guo. Lithium extraction/insertion process on cubic Li-Mn-O precursors with different Li/Mn ratio and morphology[J]. Adsorption, 2011, 17: 881-887.
[13] LI Y M, MAKITA Y, LIN Z Z, LIN S M, NAGAOKA N, YANG X J. Synthesis and characterization of lithium manganese oxides with core-shell Li4Mn5O12@Li2MnO3 structure as lithium battery electrode materials[J]. Solid State Ionics, 2011, 196: 34-40.
[14] YANG X J, KANOH H, TANG W P, OOI K. Synthesis of Li1.33Mn1.67O4 spinels with different morphologies and their ion adsorptivities after delithiation[J]. Journal of Materials Chemistry, 2000, 10: 1903-1909.
[15] YANG X J, TANG W P, KANOH H, OOI K. Synthesis of lithium manganese oxide in different lithium-containing fluxes[J]. Journal of Materials Chemistry, 1999, 9: 2683-2690.
[16] TAKADA T, HAYAKAWA H, AKIBA E. Preparation and crystal structure refinement of Li4Mn5O12 by the rietveld method[J]. Journal of Solid State Chemistry, 1995, 115(2): 420-426.
[17] ZHANG Y C, WANG H, WANG B, YAN H, AHNIYAZ A, YOSHIMURA M. Low temperature synthesis of nanocrystalline Li4Mn5O12 by a hydrothermal method[J]. Materials Research Bulletin, 2002, 37: 1411-1417.
[18] 孙淑英, 张钦辉, 于建国. 低维纳米立方相Li4Mn5O12的制备及锂吸附性能[J]. 无机材料学报, 2010, 25(6): 626-629.
SUN Shu-ying, ZHNAG Qin-hui, YU Jian-guo. Preparation and lithium adsorption properties of low-dimensional cubic Li4Mn5O12 nanostructure[J]. Journal of Inorganic Materials, 2010, 25(6): 626-629.
[19] 陈永熙, 周立娟, 郭丽萍. 锂锰氧化物中锰的平均化合价的测定研究[J]. 武汉理工大学学报, 2001, 23(10): 1-3.
CHEN Yong-xi, ZHOU Li-juan, GUO Li-pin. The research on the determination of average Mn valency in lithium manganese oxide[J]. Journal of Wuhan University of Technology, 2001, 23(10): 1-3.
[20] AITCHISON P, AMMUNDSEN B, BELL T, JONE D J. Proton insertion in spinel lithium manganates and the effect of manganese substitution[J]. Physica B: Condensed Matter, 2000, 276/278: 847-848.
[21] WANG Lu, MA Wei, LIU Ru, LI Hai-yan, MENG Chang-gong. Correlation between Li+ adsorption capacity and the preparation conditions of spinel lithium manganese precursor[J]. Solid State Ionics, 2006, 177: 1421-1427.
[22] KIM J, MANTHIRAM A. Low temperature synthesis and electrode properties of Li4Mn5O12[J]. Journal of the Electrochemical Society, 1998, 145(4): L53-L55.
[23] AMMUNDSEN B, AITCHISON P, BURNS G R, BELL T. Proton insertion and lithium-proton exchange in spinel lithium manganates[J]. Solid State Ionics, 1997, 97: 269-276.
[24] 王 禄. 尖晶石型锰氧化物离子筛制备及提锂性能[D]. 大连: 大连理工大学, 2008: 94-95.
WANG Lu. Preparation and lithium uptake properties of lithium ion sieves derived from spinel-type manganese[D]. Dalian: Dalian University of Technology, 2008: 94-95.
(编辑 陈卫萍)
基金项目:重庆市科委自然科学基金计划资助项目(CSTC2011JJA50004);重庆市教委科学技术研究项目(KJ100723)
收稿日期:2012-12-22;修订日期:2013-08-09
通信作者:陈昌国,教授,博士;电话:023-65106053;E-mail: cgchen@cqu.edu.cn