

基于感染风险评价模型的隔离病房气流组织模拟研究
谢军龙1,吴鑫1,郭晓亮1,侯佳鑫1,段梅子1,王飞飞2,徐新华2,高乃平3
(1. 华中科技大学 能源与动力工程学院,湖北 武汉,430074;
2. 华中科技大学 环境科学与工程学院,湖北 武汉,430074;
3. 同济大学 机械与能源工程学院,上海,200092)
摘要:为了降低隔离病房内的感染风险,根据隔离病房内医护人员感染风险及气流组织流场计算的特征,在随机非阈值Dose-response模型的基础上,改进并建立Medical Staff Dose-response感染风险评价模型,并将该评价模型应用在CFD仿真过程中,得到隔离病房在不同送风形式、温度、湿度及换气次数下的医护人员感染风险值,从而分析主要气流组织因素对感染风险值的影响。研究结果表明:送风形式对医护人员呼吸区域感染风险值影响较大。在患者咳嗽后1 000 s内,湿度与感染风险值呈负相关,而温度与感染风险值间无明显规律。
关键词:隔离病房;感染风险;气流组织;数值模拟
中图分类号:TU834 文献标志码:A 开放科学(资源服务)标识码(OSID)
文章编号:1672-7207(2021)06-1798-11
Simulation of air distribution in isolation ward based on infection risk assessment model
XIE Junlong1, WU Xin1, GUO Xiaoliang1, HOU Jiaxin1, DUAN Meizi1,
WANG Feifei2, XU Xinhua2, GAO Naiping3
(1. School of Energy and Power Engineering, Huazhong University of Science and Technology, Wuhan 430074, China;
2. School of Environmental Science and Engineering, Huazhong University of Science and Technology, Wuhan 430074, China;
3. School of Mechanical and Energy Engineering, Tongji University, Shanghai 200092, China)
Abstract: To reduce the infection risk of isolation ward, an assessment model of Medical Staff Dose-response (MSDR) infection risk based on the random non-threshold Dose-response model was improved and built with the consideration of infection risk of medical staff and air distribution calculation characteristics. Accordingly, the MSDR model was applied in the CFD simulation to evaluate the infection risk with major parameters of air distribution, including ventilation type, temperature, humidity and ventilation rate. The results show that the ventilation type prevails on the infection risk of medical staff in the respiratory area. Moreover, humidity is negatively correlated with the infection risk within 1 000 s after the onset of cough. Comparably, the temperature change does not affect the infection risk obviously.
Key words: isolation ward; risk of infection; air distribution; numerical simulation
医院是人发生交叉感染的高风险场所[1],许多感染通过空气中的病原体[2]传播。病原体一旦离开感染者,其去向取决于多种复杂的因素[3],无论是在整个房间里[4],还是在源患者和脆弱个体周围的微环境中[5],气流组织是最重要的因素之一。李安桂等[6]研究了不同送风模式下病房室的内病原微生物的排除效果;凌继红等[7]通过实验研究了气流组织对负压隔离病房排污效率的影响;张桉康等[8]研究了不同气流组织条件下呼气区域的飞沫个数及飞沫排除效果;郑晓红等[9]针对个性化通风系统下病房的排污效率及吸入空气质量指数进行了研究;LIU等[10]主要研究了热均匀和分层环境中的浓度分布及最大直接暴露距离来评估暴露风险;YU等[11]从病毒清除能力的角度探讨了综合医院病房通风设计策略的有效性。目前,人们主要利用计算流体力学(CFD)对隔离病房内气流组织进行仿真,但仅从流动角度对病房内感染风险值初步进行定性分析,未能结合病原体传播途径及特性对感染风险值进行定量分析。为了对感染风险值进行定量分析,人们基于随机非阈值Dose-response模型[12],考虑病原体的传播途径、粒径特性等因素对感染风险值进行评价[13]。但其都是通过实验或者数值模拟后得到某点病原体浓度分布后再进行感染风险值计算,都未将该模型应用在CFD仿真过程中以得到任意时刻的感染风险值。
因此,为了在气流组织流场计算过程中对隔离病房内感染风险值进行定量分析,本文作者在随机非阈值Dose-response模型上加以改进,提出Medical Staff Dose-response模型(简称MSDR模型)。MSDR模型可结合CFD仿真过程分析隔离病房在不同气流组织参数下对医护人员感染风险值的影响,为隔离病房气流组织设计提供参考。
1 MSDR模型建立
1.1 随机非阈值Dose-response模型
SZE等[12]提出的随机非阈值Dose-response模型公式为

 (1)
(1)
式中:PI(x, to)为在to时间内于x位置处的感染风险值即感染概率;to为暴露时间,h;m为病原体总个数;v(x, t)j为第j个粒径病原体的体积分数;fs为咳嗽频率;p为呼吸量,m3/h;c为初始病原体浓度; 为病原体在空气中的存活能力参数;rj为第j个粒径病原体的传染性参数;βj为第j个粒径病原体在肺泡区域的沉积分数;rj与βj为与病原体的粒径有关的参数。
为病原体在空气中的存活能力参数;rj为第j个粒径病原体的传染性参数;βj为第j个粒径病原体在肺泡区域的沉积分数;rj与βj为与病原体的粒径有关的参数。
随机非阈值Dose-response模型关注的是房间内某个点的感染风险,但是医护人员是在一个相对固定的区域内呼吸,其余区域的暴露水平对医护人员感染风险影响较小。只分析某点的感染风险值不能全面反映医护人员的感染风险值。所以,随机非阈值Dose-response模型不利于对医护人员的感染风险进行评价。随机非阈值Dose-response模型虽然考虑了咳嗽频率,但只是简单叠加。而患者在一段时间内并不是均匀咳嗽的,有可能前一段时间咳嗽比较频繁,后一段时间基本不咳嗽,且第二次及以后的咳嗽对呼吸区域内的暴露水平有很大影响。因此,这会导致得到的暴露水平与实际的暴露水平有差异。
1.2 MSDR模型
MSDR模型从以下4个方面对随机非阈值Dose-response模型进行改进。
1) 可同时对医护人员的呼吸区域和时间进行积分,从而得到医护人员呼吸区域的感染风险值。这表明将医护人员呼吸区域的感染风险值作为评价指标是合理可行的,其更能表征医护人员的感染风险值。
2) 在实际过程中,患者咳嗽是无规律的,咳嗽频率难以统计与预测,在对医护人员感染风险值进行评价时会带来较大处理难度。因此,MSDR模型简化了时域上的处理过程,消除咳嗽频率不规律性对医护人员感染风险值的影响,只对单次咳嗽的呼吸区域内咳嗽液滴进行研究。
3) 咳嗽液滴粒径对感染风险值影响较大,且咳嗽液滴在隔离病房内传播扩散过程中,因蒸发作用,自身粒径会发生变化,所以,在对医护人员进行感染风险评价时,不可忽略咳嗽液滴的蒸发效应。MSDR模型在CFD仿真过程中可实现对呼吸区域内咳嗽液滴的循环,实时监测咳嗽液滴粒径,从而在感染风险评价模型中应考虑液滴蒸发效应。
4) 鉴于气流组织流场非稳态计算过程中采用变时间步长求解,因此,为了便于对计算结果进行统计,本模型将观察时间离散为多个时间步进行积分。
通过以上分析,对式(1)进行修改,即可得MSDR模型公式。
MSDR模型只考虑医护人员呼吸区域的感染风险,因此,该模型第j个粒径病原体的体积分数可表示为
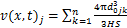 (2)
(2)
MSDR模型将观察时间离散为多个时间步长,因此,该模型对时间积分可表示为
 (3)
(3)
式中:d0jk为第k个在当前步长的初始直径为第j个粒径的病原体直径,m;Δti为第i个时间步长;H为呼吸区域的竖直高度,该模型隔离病房距地面1.3~1.5 m[14]高度区域为医护人员的呼吸区域高度,即呼吸区域高H=0.2 m;S为医护人员呼吸区域的水平面积,即为房间的占地面积,m2。
通过以上分析,可得医护人员的感染风险评价MSDR模型公式为

 (4)
(4)
2 MSDR模型数值应用
在对MSDR模型进行数值应用时,其正确性不仅取决于MSDR模型参数,还取决于咳嗽液滴蒸发扩散模型。咳嗽液滴蒸发扩散模型直接决定了医护人员感染风险值。因此,需要对咳嗽液滴蒸发扩散模型及MSDR模型参数进行正确、合理设置。
2.1 咳嗽液滴蒸发扩散模型设置
根据本文中患者的嘴部长×宽为0.02 m×0.02 m,若咳嗽时的气流速度最大为9 m/s,则喷出的最大空气体积流率为0.003 6 m3/s,咳嗽时的咳嗽液滴的最大质量流率为1.9×10-6 kg/s,咳嗽液滴的密度取1 003 kg/m3,则咳嗽液滴的体积流率为1.894×10-9 m3/s,咳嗽液滴所占的体积分数为5.26×10-7,远小于10%,颗粒物中心的相对间距与粒径之比为99[15]。本文所设置的咳嗽液滴初始参数都参考以上数值。对于本文咳嗽液滴扩散传播的研究可认为是稀疏两相流,可忽略颗粒-颗粒之间的相互作用。为了简化计算,实现模拟过程,本文对咳嗽液滴扩散过程进行简化,对咳嗽液滴进行了以下4点假设:
1) 咳嗽液滴间不发生碰撞、破碎与凝并现象;
2) 咳嗽液滴与壁面间的碰撞为完全弹性碰撞;
3) 咳嗽液滴仅考虑重力、单曳力及热泳力[16];
4) 咳嗽液滴离开嘴部后开始蒸发直至无水分,在蒸发过程中咳嗽液滴保持为球状[17]。
采用离散相模型(DPM)对咳嗽液滴的蒸发扩散进行模拟计算;湍流模型选择RNG k-ε模型;采用隐式Simple算法耦合压力和速度场,计算变量均采用二阶迎风差分格式;壁面设置为标准壁面函数;能量方程收敛残差标准为10-6,其他变量收敛残差标准为10-4。
2.2 模型准确性验证
咳嗽液滴蒸发扩散模型主要用于模拟咳嗽液滴在隔离病房内的扩散传播,在此基础上定量分析因咳嗽液滴扩散特性而扩散到医护人员呼吸区域所导致的交叉感染风险值。咳嗽液滴扩散特性的准确性对本文计算结果的正确性起到决定性作用,针对该模型对咳嗽液滴的扩散特性进行了准确性验证,将该模型在CHAO等[18]相同实验条件下进行模拟计算,并将可反映咳嗽液滴扩散特性的均方位移与实验结果进行比较,如图1所示(其中,Y2为Y坐标二次方的平均值,即为均方位移)。

图1 不同粒径下咳嗽液滴均方位移的数值模拟与实验结果对比
Fig. 1 Comparison of numerical simulation and experimental results of mean azimuth shift of cough droplets with different particle sizes
由图1可知:数值模拟结果与实验结果变化趋势相似,吻合较好。由咳嗽液滴的均方位移和时间可得粒径为28 μm的咳嗽液滴在该段时间内扩散系数的模拟值与实验值分别约为0.010 150 m2/s和0.010 950 m2/s,粒径为45 μm的咳嗽液滴在该段时间内扩散系数的模拟值与实验值分别约为0.000 195 m2/s和0.000 180 m2/s[18],模拟值与实验值的相对误差分别为7.9%和7.7%。因为在模拟过程中忽略了咳嗽液滴在实际扩散过程中可能黏附空气中的颗粒物、咳嗽液滴之间的相互作用等,与实验值会有误差,但都在可接受的误差范围内。相对于整个隔离病房的面积而言,咳嗽液滴在某一时刻扩散位置的模拟值与实验值误差是比较小的,其误差带来的咳嗽液滴在整个房间内扩散特征差异基本可忽略不计,本模型能较好地反映咳嗽液滴在病房内的扩散特性。
2.3 物理模型设置
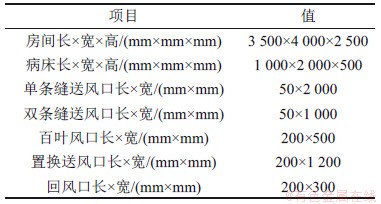
针对单人隔离病房,在MSDR模型基础上,对隔离病房内患者咳嗽1次后的室内的气流组织进行模拟,分析不同气流组织因素对MSDR的影响。其中4种送风形式分别为单条缝对侧上送下回、双条缝异侧上送下回、百叶对侧上送下回和格栅对侧下送上回,在下面分析中分别用A,B,C和D表示,送、回风口的布置如图2所示。隔离病房以及风口的具体尺寸见表1。

图2 送风形式方案设计
Fig. 2 Scheme design of air supply form
表1 隔离病房及各风口尺寸
Table 1 Dimensions of isolation ward and each diffuser
2.4 MSDR模型参数确定
MSDR模型适用于分析呼吸道传染性疾病的感染风险。目前,对流感病毒的研究比较全面,可获得流感病毒初始浓度、存活能力等参数,因此,本文针对医护人员流感病毒的感染风险值进行模拟分析。结合相关研究:将医护人员呼吸量设为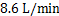 [19];液滴中的流感病毒初始浓度根据文献[20]设为
[19];液滴中的流感病毒初始浓度根据文献[20]设为 PFU/L。流感病毒的存活能力按下式处理:
PFU/L。流感病毒的存活能力按下式处理:
 (5)
(5)
传染性表达取值为[13]
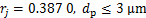
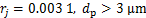
病原体粒径与其在肺泡区域的沉积关系[21]按下式处理:
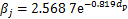 (6)
(6)
2.5 MSDR模型数值应用流程
MSDR模型在数值应用的流程为:先通过稳态计算得到各送风形式的初始稳定流场,然后通过非稳态方法模拟咳嗽液滴在隔离病房内传播扩散过程。在咳嗽过程中(0~0.4 s),患者嘴巴模型边界条件设置为速度进口条件。咳嗽结束后,将患者嘴巴模型边界条件设置为壁面条件,并保持此状态直至计算结束。在非稳态模拟过程中,加载并运行根据MSDR模型相关公式以及关键参数编写的感染风险评价UDF(User Defined Functions,用户自定义函数),即可得到相应的感染风险值。MSDR模型计算流程如图3所示。

图3 MSDR模型计算流程
Fig. 3 MSDR model calculation process
3 气流组织因素对MSDR影响分析
3.1 送风形式对MSDR影响分析
对以上4种送风形式进行模拟,并对不同送风形式下隔离病房内医护人员的呼吸区域感染风险值进行计算。
图4和图5所示分别为病房内的X截面(病房长的中截面)及Z=0.3 m截面(距离病房地板0.3 m截面)的速度等值线图。由图4和图5可知:在4种送风形式下,病房内的速度分布不同。其中采用格栅对侧下送上回送风形式时,病房内的风速比较低,其分布比较均匀。气流从病房底部进风口水平射入房间后,沿房间地板向进风口相反方向运动,主气流受到回风口抽吸作用,带着患者产生的大部分咳嗽液滴直接从回风口排出,而其他气流在室内热源产生的热气流提升作用下向上运动,并带着其余小部分咳嗽液滴向四周扩散,最后从房间顶部排到室外;而在其余3种送风形式下,气流从房间顶部送风口射入,由于送风速度较大,所以,送风口附近的速度梯度比较大,气流搅动较大。在单条缝对侧上送下回送风和双条缝异侧上送下回送风形式下,射入房间内的气流在重力作用下气流下沉,并向四周扩散,裹挟着部分咳嗽液滴向咳嗽反方向从回风口流出。而在百叶对侧上送下回送风形式下,气流从送风口斜向下射入,所以,气流撞击到障碍物后向上扩散,后又受到回风口抽吸作用裹挟部分咳嗽液滴向下运动,从而排出室外。

图4 X截面速度等值线图
Fig. 4 Velocity contour maps of X section

图5 Z=0.3 m截面速度等值线图
Fig. 5 Velocity contour maps of Z=0.3 m
图6~9所示分别为4种送风形式下的咳嗽液滴扩散图,由图6~9可知:在4种送风形式下,咳嗽液滴在病房内的分布不同,所以,病房内每个位置的感染风险值也不同。当t<10 s时,在格栅对侧下送上回和双条缝异侧上送下回送风形式下,医护人员呼吸区域内的咳嗽液滴数目明显比其余2种送风形式的高。但是当t=10~1 000 s时,格栅对侧下送上回送风形式下的医护人员呼吸区域的咳嗽液滴数目减少,当t=50 s时,呼吸区域的咳嗽液滴数目明显比其余3种送风形式的少,到t=1 000 s时,呼吸区域基本无咳嗽液滴。而其余3种送风形式在t=10 s后,呼吸区域的咳嗽液滴数目还在增加,其液滴数目及其增加量最多的是双条缝异侧上送下回送风形式。

图6 单条缝对侧上送下回送风液滴扩散图
Fig. 6 Droplet diffusion diagrams at air supply mode of up-supply and down-return on opposite side of single seam

图7 双条缝异侧上送下回送风液滴扩散图
Fig. 7 Droplet diffusion diagrams at air supply mode of up-supply and down-return on opposite side of double seam

图8 百叶对侧上送下回送风液滴扩散图
Fig. 8 Droplet diffusion diagrams at air supply mode of up-supply and down-returnon opposite side of louver

图9 格栅对侧下送上回送风液滴扩散图
Fig. 9 Droplet diffusion diagrams at air supply mode of down-return and up-supply on opposite side of grille
图10所示为4种送风形式下的MSDR分析图,由图10可知:当t<10 s时,格栅对侧下送上回和双条缝异侧上送下回送风形式下,医护人员的感染风险值明显比其余2种送风形式的高。但是当t= 10~1 000 s时,格栅对侧下送上回送风形式下的医护人员呼吸区域的感染风险值基本不变而其余3种送风形式增加幅度比较大。随时间的延长,其余3种送风方式与格栅对侧下送上回送风形式下的感染风险差值变大。当t=600 s时,4种送风形式下的感染风险值都基本维持稳定,其余3种送风形式的感染风险值是格栅对侧下送上回送风形式下医护人员呼吸区域感染风险值的6.7~12.5倍。这与咳嗽液滴在呼吸区域分布规律相符,因此,用MSDR模型计算医护人员呼吸区域感染风险值是准确的、可行的。
出现这种现象是因为格栅对侧下送上回送风形式的回风口在呼吸区域上方,送风口在呼吸区域下方,又因为咳嗽液滴粒径越小,其重力就越小,在医护人员肺泡区域的沉积分数就越大,传染性越强。所以,当t=0~20 s时,在格栅对侧下送上回送风形式下,患者刚喷出的较小粒径咳嗽液滴大部分被裹挟到医护人员的呼吸区域,其感染风险值也就最大。但是,随通风时间变长,格栅对侧下送上回送风形式下的病房内较小粒径咳嗽液滴大部分已被排出室外,悬浮在呼吸区域内的小粒径咳嗽液滴已经很少,且较大咳嗽液滴基本沉降至地面,所以,医护人员呼吸区域的感染风险值趋于平缓。而其余3种送风方式回风口均在房间下部,气流总体方向与咳嗽液滴扩散方向相反,所以,咳嗽液滴到达医护人员呼吸区域所需时间较长。因此,咳嗽液滴入射初期,其感染风险值较小;随室内流场的搅动,咳嗽液滴容易被气流裹挟到病房医护人员的呼吸区域,不易被排出室外,从而导致感染风险值不断增大。

图10 不同送风形式的MSDR分析
Fig. 10 MSDR analysis of different air supply forms

图11 不同湿度条件下的MSDR分析
Fig. 11 MSDR analysis at different humidity conditions
因为本研究只对隔离病房进行一次咳嗽液滴的入射,所以,在咳嗽液滴基本被排出室外及沉降到地面后,医护人员呼吸区域的咳嗽液滴数趋于零,因此,当t=1 000 s时,医护人员感染风险值也趋于平稳,基本不变。
3.2 温湿度对MSDR影响分析
选用感染风险值较小的格栅对侧下送上回送风形式为例,分别模拟分析30%,40%,50%,60%和70%相对湿度环境下及18,20,22,24和26 ℃送风温度下医护人员呼吸区域的感染风险值。不同送风湿度和温度的MSDR分析结果分别如图11和图12所示。
由图11和图12可知:温度和湿度送风条件的变化对医护人员呼吸区域的感染风险值影响较小。虽然温度和湿度送风条件对咳嗽液滴蒸发的影响较大,但是对咳嗽液滴扩散的影响较小。本文的感染风险评价实质是对医护人员呼吸区域内的咳嗽液滴数目以及咳嗽液滴的粒径、感染性等相关特性进行综合分析。其中,咳嗽液滴的扩散相对咳嗽液滴因蒸发效应引起的粒径变化对医护人员感染风险值的影响较大。这是因为咳嗽液滴本身粒径较小,蒸发时间较短,所以,温度和湿度引起咳嗽液滴蒸发时间及粒径变化值差异非常小,温度和湿度送风条件对医护人员呼吸区域的感染风险值影响较小。
但在患者咳嗽后1 000 s内,湿度变化引起感染风险值的变化明显比温度的变化大,而且湿度与感染风险值有着明显的对应关系:医护人员呼吸区域的感染风险值随湿度的减小而增大。因为病房内湿度越小,咳嗽液滴蒸发速度就会越快,咳嗽液滴粒径变小的速度也就越快,在某种程度上增加了病房内较小粒径咳嗽液滴的占比,而较小粒径咳嗽液滴在肺泡区域有着较大的沉积分数与传染性。因此,在患者发生咳嗽后1 000 s内,湿度越低,医护人员的感染风险值越大。

图12 不同温度条件下的MSDR分析
Fig.12 MSDR analysis at different temperatures

图13 定风速下的MSDR分析
Fig. 13 MSDR analysis at constant wind speed
3.3 换气次数对MSDR影响分析
通过调节送风风速以及风口尺寸以实现每小时换气次数的改变,其模拟结果分别如图13和图14所示。

图14 定风口下的MSDR分析
Fig. 14 MSDR analysis at fixed tuyere
由图13可知:在定风速下,随每小时换气次数增多,液滴排除能力不断增强,但是当每小时换气次数过多时,气流组织对咳嗽液滴的影响不再明显增大,当每小时换气次数增大到16次/h后,咳嗽液滴排除能力不再随每小时换气次数的增多有明显变化。但是,较多的换气次数排除液滴的能力较强,时效性较好,所以,当t=100 s时,医护人员感染风险值基本已达到峰值并保持稳定。而较少的换气次数的咳嗽液滴排除液滴的能力较弱,因此,在t=100 s时感染风险值仍有显著增加。在t=1 000 s时,每小时换气次数为24次/h的感染风险值是8次/h的47%。
由图14可知:在定风口条件下,增大风速对排除液滴效果的增益不明显,甚至会有所下降,每小时换气次数为12次/h的风险值明显比其他情况的高。这是因为风速增大加剧了液滴在病房内的四处扩散,因此,感染风险值没有随之减小,反而有所增加。
4 结论
1) 送风形式对医护人员呼吸区域感染风险值影响较大,当感染风险值稳定时,其余3种送风形式医护人员呼吸区域感染风险值为格栅对侧下送上回送风形式下的6.7~12.5倍。
2) 在格栅对侧下送上回送风形式下,患者咳嗽后1 000 s内,湿度与感染风险值呈负相关,而温度与感染风险值间无明显的规律;在定风速条件下,医护人员感染风险值随每小时换气次数的增加而增大;在定风口条件下,每小时换气次数(风速)过少或者过多都会使感染风险值增大。
参考文献:
[1] VILLAFRUELA J M, OLMEDO I, BERLANGA F A, et al. Assessment of displacement ventilation systems in airborne infection risk in hospital rooms[J]. PLoS One, 2019, 14(1): e0211390.
[2] KOWALSKI W. Hospital airborne infection control[M]. Boca Raton: CRC Press, 2012: 27.
[3] HAMODA M F, MAHMOUD H. Microbiological characteristics of indoor air bioaerosols in a waste paper recycling factory[J]. International Journal of Environmental Science and Technology, 2019, 16(6): 2601-2610.
[4] 李海英, 周叶, 邓启红. 热与污染物在不同建筑楼层间的传输行为与分布特性[J]. 中南大学学报(自然科学版), 2013, 44(12): 5125-5132.
LI Haiying, ZHOU Ye, DENG Qihong. Transport of heat and air pollutants across different floors in high-rise buildings[J]. Journal of Central South University(Science and Technology), 2013, 44(12): 5125-5132.
[5] STOCKWELL R E, BALLARD E L, O'ROURKE P, et al. Indoor hospital air and the impact of ventilation on bioaerosols: a systematic review[J]. Journal of Hospital Infection, 2019, 103(2): 175-184.
[6] 李安桂, 张莹, 韩欧, 等. 隔离病房的环境保障与气流组织有效性[J]. 暖通空调, 2020, 50(6): 26-34.
LI Angui, ZHANG Ying, HAN Ou, et al. Effectiveness of air distribution and pollutant control in isolation wards[J]. Heating Ventilating & Air Conditioning, 2020, 50(6): 26-34.
[7] 凌继红, 于会洋, 李猛, 等. 气流组织对负压隔离病房排污效率的影响[J]. 天津大学学报(自然科学与工程技术版), 2014, 47(2): 174-179.
LING Jihong, YU Huiyang, LI Meng, et al. Effects of air flow distribution on contaminant removal efficiency in an infectious isolation room[J]. Journal of Tianjin University(Science and Technology), 2014, 47(2): 174-179.
[8] 张桉康, 张华玲, 刘鹏. 普通病房飞沫污染物传播特性与评价[J]. 重庆大学学报, 2021, 44(3): 82-92.
ZHANG Ankang, ZHANG Hualing, LIU Peng. General wards droplets pollutants propagation characteristics and evaluation[J]. Journal of Chongqing University, 2021, 44(3): 82-92.
[9] 郑晓红, 钱华, 刘荔. 新型个性化通风系统预防传染病传播数值研究[J]. 中南大学学报(自然科学版), 2011, 42(12): 3905-3911.
ZHENG Xiaohong, QIAN Hua, LIU Li. Numerical study on a new personalized ventilation system application in cross infection prevention[J]. Journal of Central South University(Science and Technology), 2011, 42(12): 3905-3911.
[10] LIU Fan, ZHANG Chongyang, QIAN Hua, et al. Direct or indirect exposure of exhaled contaminants in stratified environments using an integral model of an expiratory jet[J]. Indoor Air, 2019, 29(4): 591-603.
[11] YU H C, MUI K W, WONG L T, et al. Ventilation of general hospital wards for mitigating infection risks of three kinds of viruses including middle east respiratory syndrome coronavirus[J]. Indoor and Built Environment, 2017, 26(4): 514-527.
[12] SZE TO G N, WAN M P, CHAO C Y H, et al. A methodology for estimating airborne virus exposures in indoor environments using the spatial distribution of expiratory aerosols and virus viability characteristics[J]. Indoor Air, 2008, 18(5): 425-438.
[13] 廖悦. 高海拔地区供暖病房飞沫污染物的传播及风险评价[D]. 重庆: 重庆大学, 2017: 75-87.
LIAO Yue. The transmission of droplets contaminants in heating wards of high altitude region and risk assessment[D]. Chongqing: Chongqing University, 2017: 75-87.
[14] MURAKAMI S. Analysis and design of micro-climate around the human body with respiration by CFD[J]. Indoor Air, 2004, 14: 144-156.
[15] 高军. 下送风房间气溶胶颗粒动力学与跟随性的理论及应用研究[D]. 上海: 同济大学, 2009: 6-8.
GAO Jun. Theory and application of aerosol particle dynamics and tracking in downward air supply chamber[D]. Shanghai: Tongji University, 2009: 6-8.
[16] WEI Jianjian, LI Yuguo. Enhanced spread of expiratory droplets by turbulence in a cough jet[J]. Building and Environment, 2015, 93: 86-96.
[17] 汪新智, 任安星, 武永吉, 等. 基于欧拉-拉格朗日方法的携病毒飞沫扩散过程的数值模拟[J]. 自然杂志, 2020, 42(3): 239-248.
WANG Xinzhi, REN Anxing, WU Yongji, et al. Numerical simulation of cough droplets transmission based on Euler-Lagrange method[J]. Chinese Journal of Nature, 2020, 42(3): 239-248.
[18] CHAO C Y H, WAN M P. A study of the dispersion of expiratory aerosols in unidirectional downward and ceiling-return type airflows using a multiphase approach[J]. Indoor Air, 2006, 16(4): 296-312.
[19] 刘平, 王贝贝, 赵秀阁, 等. 我国成人呼吸量研究[J]. 环境与健康杂志, 2014, 31(11): 953-956.
LIU Ping, WANG Beibei, ZHAO Xiuge, et al. Research on inhalation rate of Chinese adults[J]. Journal of Environment and Health, 2014, 31(11): 953-956.
[20] YANG W, MARR L C. Dynamics of airborne influenza a viruses indoors and dependence on humidity[J]. PloS One, 2011, 6(6): e21481.
[21] LIPPMANN M, ALBERT R E. The effect of particle size on the regional deposition of inhaled aerosols in the human respiratory tract[J]. American Industrial Hygiene Association journal, 1969, 30(3): 257-275.
(编辑 刘锦伟)
收稿日期: 2020 -11 -19; 修回日期: 2021 -01 -03
基金项目(Foundation item):国家自然科学基金资助项目(51878462);武汉市科技计划项目(2020020601012229) (Project(51878462) supported by the National Natural Science Foundation of China; Project(2020020601012229) supported by the Science and Technology Planning Program of Wuhan)
通信作者:谢军龙,博士,研究员,从事空气品质计算仿真,暖通空调与制冷等研究;E-mail: hustxjl@163.com
DOI: 10.11817/j.issn.1672-7207.2021.06.009
引用格式:谢军龙, 吴鑫, 郭晓亮, 等. 基于感染风险评价模型的隔离病房气流组织模拟研究[J]. 中南大学学报(自然科学版), 2021, 52(6): 1798-1808.
Citation:XIE Junlong, WU Xin, GUO Xiaoliang, et al. Simulation of air distribution in isolation ward based on infection risk assessment model[J]. Journal of Central South University(Science and Technology), 2021, 52(6): 1798-1808.