������ʱ��: 2016-08-04 16:59
ϡ�н��� 2017,41(12),1369-1373 DOI:10.13373/j.cnki.cjrm.xy16060019
�����Ȼ������۳�����TiCl3��Һ�Ʊ���Ӧ��
���춫 ��� �ΰ��� �°���
�ʸּ����о�Ժ����˾������Դ�ۺ����ù����ص�ʵ����
�ʸּ�����ҵ�������ι�˾
ժ Ҫ��
���Ȼ��������������ѵ�ԭ��, ���Ѳ�ҵ���е���Ҫ�м��Ʒ, ���е�VOCl3��Ӱ�캣����O�����Ͳ���Ӳ��, ���, �����Ȼ��ѳ�����ʹ�á����۳�����������������, ����������TiCl3��Һ, �������Ծ����Ȼ�������Ӱ��ϴ��ҹ���δϵͳ����TiCl3��Һ�Ʊ�����, �������۳���Ч���������ȶ��Բ������TiCl3��Һ�Ʊ���������ѧ����;�о�����������ҺŨ�ȡ�����ͨ����������¶�ͣ��ʱ�䡢�����ﴦ����ʽ��Cl2, N2���Ʒ����ȶ�TiCl3��Һ�Ʊ����̼�������Ӱ��, �õ��˽��Ź��ղ���, ��չ���ȶ����顣�����ʾ:��������������Ӧ, �������Ȼ��ѷ�Ӧ����TiCl3��0.33AlCl3;TiCl3��Һ�Ʊ����Ź��ղ���Ϊ:��������ҺŨ��1.1%1.4% (��������) ;����������������������, Cl2/Al (������) Ϊ0.71.1;����¶�ͣ��ʱ��68 min;����ѹ��170200 kPa, ����Ϊ57 m3��h-1, ����ѹ��Ϊ120150 kPa, ����Ϊ810 m3��h-1�������Ż����ղ����Ʊ���TiCl3��Һ��������, TiCl3����8.9%10.1%, AlCl3����3.5%4.2%, �ɽ������Ȼ�����VOCl3������0.15%0.20%������0.0003%��
�ؼ��ʣ�
���Ȼ���;���۳���;TiCl3��Һ;TiCl3��0.33AlCl3;
��ͼ����ţ� TQ134.11
����飺���춫 (1984-) , ��, ����������, ˶ʿ�о���, ������ʦ, �о�����:��ұ��, ������Դ�ۺ�����;E-mail:mqd2005041@126.com;;�ΰ���, ���ڼ�������ʦ;�绰:08123380801;E-mail:Heanxi56@163.com;
�ո����ڣ�2016-06-14
���������ص�����о���չ�ƻ� (2013CB632606) ����;
Preparation and Application of TiCl3 Slurry Used in Al-Powder Vanadium Removal of Crude TiCl4
Miao Qingdong Li Kaihua He Anxi Chen Aixiang
State Key Laboratory of Vanadium and Titanium Comprehensive Utilization, Pangang Group Research Institute Co.Ltd.
Pangang Group Titanium Co.Ltd.
Abstract��
Pure TiCl4 is raw material of titanium sponge production and important intermediate product in titanium industrial chain.VOCl3 has an effect on O content and HB of titanium sponge, so rough TiCl4 must be used after vanadium removal.Removing vanadium by aluminum power was the mainstream technique and vanadium removal material was TiCl3 slurry so its quality had a significant impact on quality of pure TiCl4.TiCl3 slurry preparation method has not been mastered systematically in China, so the effect and operation stability of vanadium removal by aluminum power was poor.Thermodynamic property of preparation process of TiCl3 slurry was calculated.Effect of factors (concentration of aluminum powder suspension, Cl2 amount, maximum temperature retention time, condensate treatment and control method of Cl2 and N2) on TiCl3 slurry preparation process and quality was researched.The optimum process parameters and control method were obtained, and then the stability test was carried out.The result showed that aluminum powder reacted with Cl2 first, then reacted with TiCl4, and TiCl3��0.33 AlCl3 was generated.The optimum process parameters of TiCl3 slurry preparation process were: concentration of aluminum powder suspension was 1.1% ~ 1.4% (mass fraction) ; amount of Cl2 should be controlled in accordance with aluminum powder amount, Cl2/Al mass ratio was 0.7 ~ 1.1; maximum temperature retention time was 6 ~ 8 min; N2 pressure was170 ~ 200 k Pa, flow rate was 5 ~ 7 m3��h-1, Cl2 pressure was 120 ~ 150 kPa, flow rate was 8 ~ 10 m3��h-1.TiCl3 slurry quality prepared by optimum process parameters was good, and the TiCl3 content was 8.9% ~ 10.1% and AlCl3 content was 3.5% 4.2%.VOCl3 content in crude could be reduced from 0.15% ~ 0.20% to 0.0003% after vanadium removing operation by TiCl3 slurry.
Keyword��
TiCl4; vanadium removal by aluminum powder; TiCl3 slurry; TiCl3��0.33AlCl3;
Received�� 2016-06-14
���б�ǿ�ȸߡ���ʴ�������ŵ�������ں��պ��졢����ұ���ҽ�Ƶ���ҵ[1,2,3,4,5]�����Ȼ����������ѵ�ԭ��, ��������������������ҪӰ�졣���������ӹ���, ������Ҫ��:VOCl3, Si Cl4, Fe Cl3��Al Cl3��[6,7]����ȥ�е������Ȼ��Ѳ���ϴ����ʼ����ѷdz�����, �������������ϴ�[8]��
��ҵ������������:���۳�����ͭ˿�������л��������H2S����[9,10,11,12]��ͭ˿��������Ʒ������, ��Ч�ʵ͡��ɱ��ߡ�����ѹ�����ձ������������л��������, �÷��ɱ���, ���ܴ�, �������ȶ��Բ�, ��Ʒ�������ߡ�H2S������Ч�ʸߡ��ɱ���, ��������HCl��ʴ�豸, ��Ʒ�������ߡ���������Ҳ������۳�����, �ҹ�����ʹ��, �÷���Ʒ������, �ɻ��շ�, �ɱ�����, ����ʵ�ֹ�ģ������[13,14,15]���ۺϿ��Dz�Ʒ�������������ɱ����ɲ����Ե�ָ��, ���۳������Ǵ����Ȼ��ѳ������Ź��շ�����
���۳�������Ϊ����:1.Ti Cl3��Һ�Ʊ�;2.Ti Cl3��Һ���������Ti Cl3��Һ�Ʊ��Ǻ��ļ���, Ti Cl3��Һ����Ӱ�����Ч���;����ԡ������о�Ti Cl3��Һ�Ʊ����ղ����Ϳ��Ʒ�����������Ӱ��, �õ��Ż����ղ���������Ti Cl3��Һ�ij���Ч����
1 ʵ��
1.1 ԭ��
Ti Cl3��Һ�Ʊ����̿��ܷ����ķ�Ӧ��:
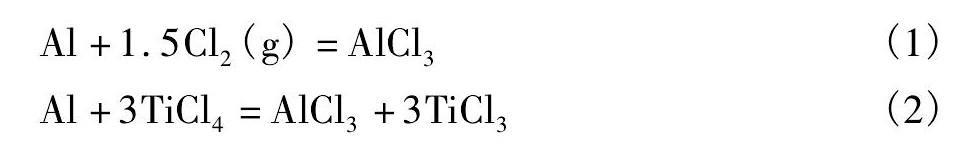
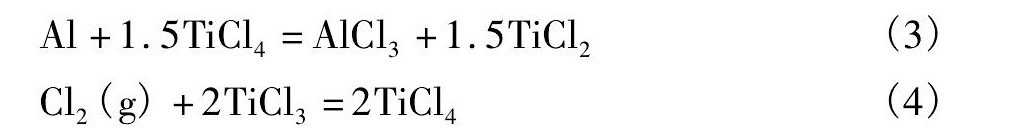
��HSC���������˷�Ӧ (1) ~ (4) ������˹������ (��Ʀ�rGm��) (��ͼ1��ʾ) , �������, 0~200�淶Χ��, ��Ӧ (1) ~ (4) �Ħ�rGm��Ϊ��ֵ, ���Է���Ӧ, ��������������Ӧ����Al Cl3, ǿ���ȷ�Ӧ, ��ϵ�¶�����, Ϊ��Ӧ2�ṩ�¶�����, ����Ti Cl3��Al Cl3, Ti Cl3��Al Cl3��ͬ��������Ti Cl3��0.33Al Cl3, �������dz����Լ�[16,17,18]��ֵ��ע���������������Ti Cl3��Ӧ����Ti Cl4����Ti Cl3Ũ�Ƚ���, �����Ti Cl3��Һ�Ʊ�������Ӧ�ϸ��������������
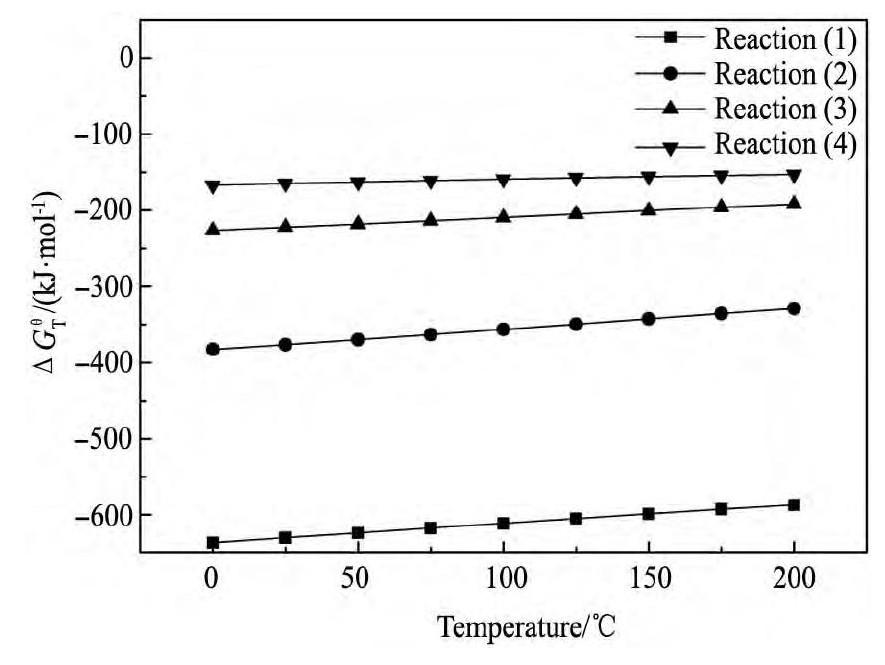
ͼ1 ��Ӧ (1) ~ (4) �Ħ�rGm��-T�Ĺ�ϵFig.1 Relationship between��rGm��-T of Reaction (1) ~ (4)
1.2 ����
��ʵ������������������װ��, ����������ͼ2��ʾ, ��Ӧ���ݻ�Ϊ0.9 m3��ʵ�������, �Ƚ������Ȼ��Ѽ��뷴Ӧ�� (����Ϊ1Cr18Ni9Ti) ��, ���ø�ѹ (��ˮ������������) ���������뷴Ӧ��, ����������̵�������, ����30 min (�����ٶ�1390 r��min-1) ��ͨ�������͵����������, ���������۷�Ӧ����, ��ϵ�¶�����, ���¶ȴ�100��ֹͣͨ����, ���������Ȼ��ѷ�Ӧ, ����Ti Cl3��Al Cl3, �¶ȼ�������, ���¶ȿ�ʼ�½�ʱ, ��Ӧ���, ����8~10 min�Ӿ����Ȼ�������ʼҺλ, ����5~10 min, Ti Cl3��Һ�Ʊ����̽�����
1.3 ԭ��
�����Ȼ���:ij�����ѳ��Բ�, ������1��ʾ;����:�, ��Ҫ�������2��ʾ;����������:�����͵�����Ҫ�������3��ʾ��
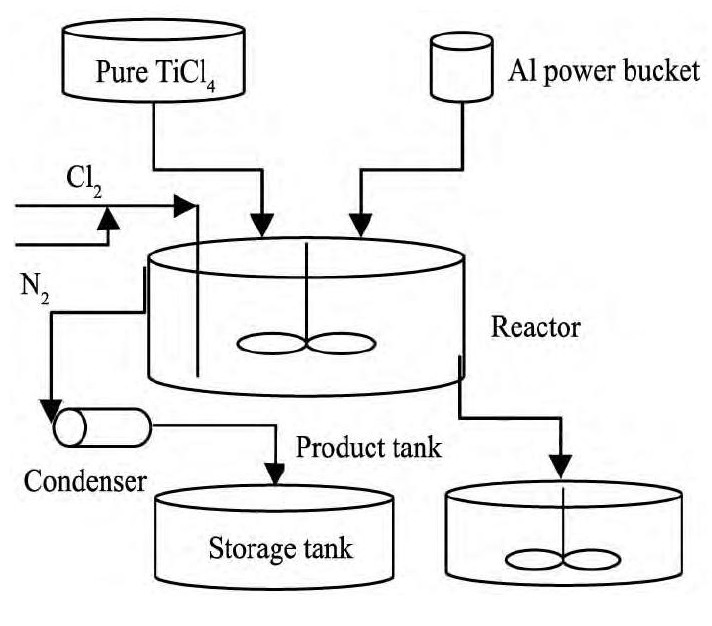
ͼ2 Ti Cl3��Һ�Ʊ�����Fig.2 Ti Cl3slurry preparation process
��1 �����Ȼ��ѻ�ѧ���Table 1Chemical composition of pure Ti Cl4 (%, mass fraction) ����ԭͼ

��1 �����Ȼ��ѻ�ѧ���Table 1Chemical composition of pure Ti Cl4 (%, mass fraction)
��2 ��������Table 2 Aluminum powder properties ����ԭͼ

��2 ��������Table 2 Aluminum powder properties
��3 ��������������Table 3 Cl2, N2properties ����ԭͼ

��3 ��������������Table 3 Cl2, N2properties
1.4 ��ⷽ�����豸
1.4.1 ���Ȼ���������Ԫ�ؼ��
�������ܽ�ϡ�����Ȼ���, ϡ�ͱ�Ϊ1��50 (�����) , ���õ����ϵ�������ԭ�ӷ�������� (ICP-AES) ������������Ԫ�غ�����
1.4.2 ���Ȼ�����Ti Cl3���
������ԭ�ζ���, �ζ��Լ�Ϊ����������Һ��
1.4.3 Ti Cl3��Һ������̬Al Cl3�ļ��
�������Ļ���120��ʱ����Ti Cl3��Һ (ת��3000r��min-1, ʱ��5 min) , �ϲ�Ϊ��Һ, �²�Ϊ������, ����ICP-AES��������Һ��Al Cl3����, ���ݹ�Һ���������õ�����̬Al Cl3��������Ҫ����ͼ���豸���4��ʾ��
2 ���������
��������ʵ��, �Ϻõ�Ti Cl3��Һ��������: (1) Ti Cl3Ũ��:8%~10%; (2) Al Cl3Ũ��<4.5%; (3) �� (Ti Cl3+Al Cl3) �Q14%��
��4 ��Ҫ�����豸Table 4 Main equipment ����ԭͼ

��4 ��Ҫ�����豸Table 4 Main equipment
2.1 ������ȵ�Ӱ��
�����뾫���Ȼ�����ȶ�Ti Cl3��Һ����Ӱ����ͼ3���������������, Ti Cl3, Al Cl3���������������Ϊ1%ʱ, Ti Cl3Ũ��Ϊ5.7%, Ti Cl3����ƫ��, ���������Ҫ���������Ϊ1.45%ʱ, Ti Cl3��Al Cl3�����ֱ�Ϊ10.9%��4.75%, Ti Cl3��������Ҫ��, ��Al Cl3����ƫ��, ͬʱ�� (Ti Cl3+Al Cl3) =15.65>14%, ���Ϲ������������, ������ȿ�����1.1%~1.4%��
2.2 Cl2ͨ������Ӱ��
��������Ti Cl3��Һ������Ӱ����ͼ4��ʾ����Cl2/Al����, Ti Cl3������������С, Al Cl3��������������ȶ���������ƫС, ���������۷�Ӧ��������, �¶ȵ�, ���������Ȼ��ѷ�Ӧ��, ������������, ͬ����Ӧʱ����Al Cl3��Ti Cl3�����͡�����������, ��ϵ�¶�����, ���������Ȼ��ѷ�Ӧ���ʼӿ�, Al Cl3��Ti Cl3��������ÿ�����������̶�, �ʷ�Ӧ������Al Cl3����һ�¡���Cl2/Al>1.1ʱ, ����ͨ����, ������������������, ���������Ȼ��ѷ�Ӧ��������, Ti Cl3Ũ�Ƚ��͡�ͬʱ����ѧ����������, ��������Ti Cl3��Ӧ, ����Ti Cl3�������͡��ۺϿ���Ti Cl3��Һ�����ͷ�Ӧ���ʵ�����, Cl2/Al��Ӧ������0.7~1.1��Χ�ڡ�
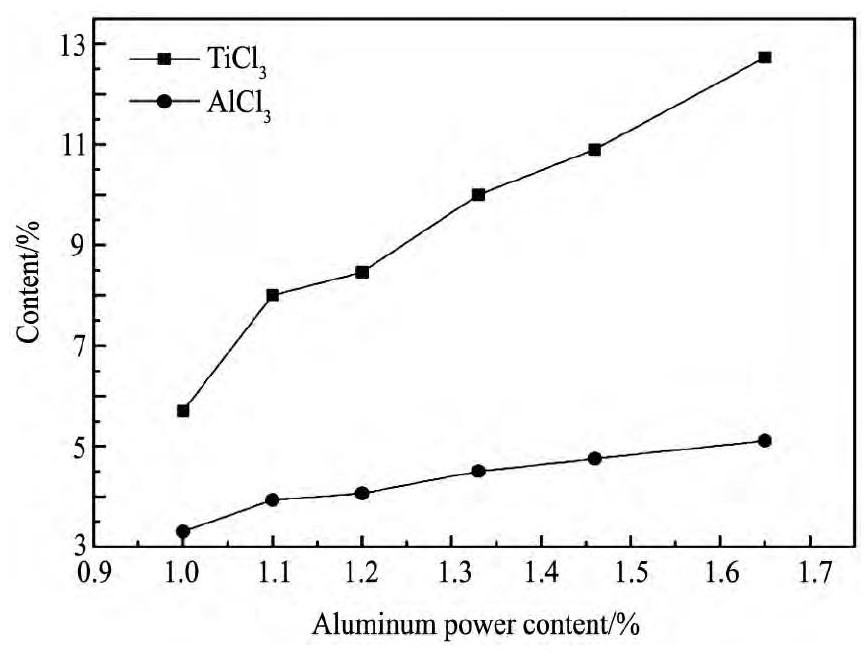
ͼ3 ������ȶ�Ti Cl3, Al Cl3����Ӱ��Fig.3 Effect of Al powder ratio on Ti Cl3, Al Cl3content
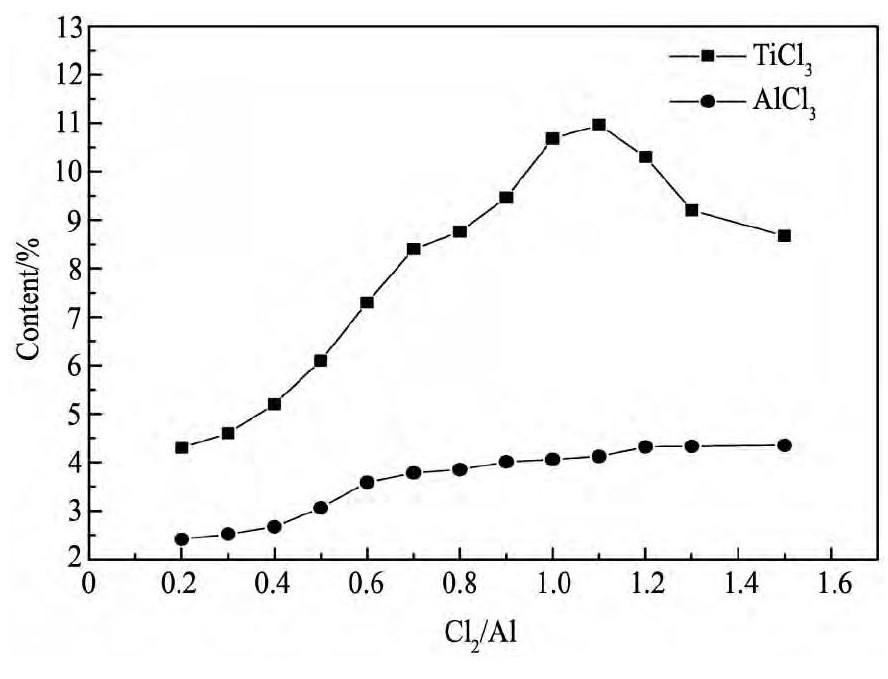
ͼ4 Cl2/Al��Ti Cl3, Al Cl3������Ӱ��Fig.4 Effect of Cl2/Al on Ti Cl3, Al Cl3content
2.3 ����¶�ͣ��ʱ���Ӱ��
����¶�ͣ��ʱ���Ti Cl3��Һ������Ӱ����ͼ5��ʾ����ͣ��ʱ���ӳ�, Ti Cl3��Al Cl3Ũ������, ������С, ������Al Cl3�����������, ͣ��ʱ��Ϊ8 minʱ, ���ͷ���Ϊ37.4%����Ӧ������¶�ʱ, ��Ӧ���, ��Ti Cl3��Al Cl3Ũ�Ȼ������䡣��ʱTi Cl3��Al Cl3�γ������Ti Cl3��0.33Al Cl3�Ĺ������ڽ��� (Ti Cl3��0.33Al Cl3�е�Al Cl3�����ܳ�����Һ��) , ��ͣ��ʱ���ӳ�, Ti Cl3��0.33Al Cl3����������, ����̬Al Cl3��������, �����ڲ�Ʒ��Al Cl3���ơ��ۺϿ�������̬Al Cl3�����ͷ�Ӧ����, ����¶�ͣ��ʱ��Ӧ������6~8 minΪ�ˡ�
2.4 �������Ӱ��
Ti Cl3��Һ�Ʊ���������¶ȴ�135~140��, �ҷ�Ӧ����Ϊ��ѹ, ���Ȼ��ѺͲ���Al Cl3�ӷ����������ޡ���������ʾ������������̬Al Cl3ƽ��������0.6%, ���2.0%���ֱ����������;����Ȼ��Ѳ���Ti Cl3��Һ�Ʊ������е�������ʧ���о��������Ӱ�졣�����ʾ, ���þ����Ȼ�������������, Ti Cl3����û�б仯, Al Cl3������3.80%������3.35%, �����ڲ�Ʒ��Al Cl3�������ơ�
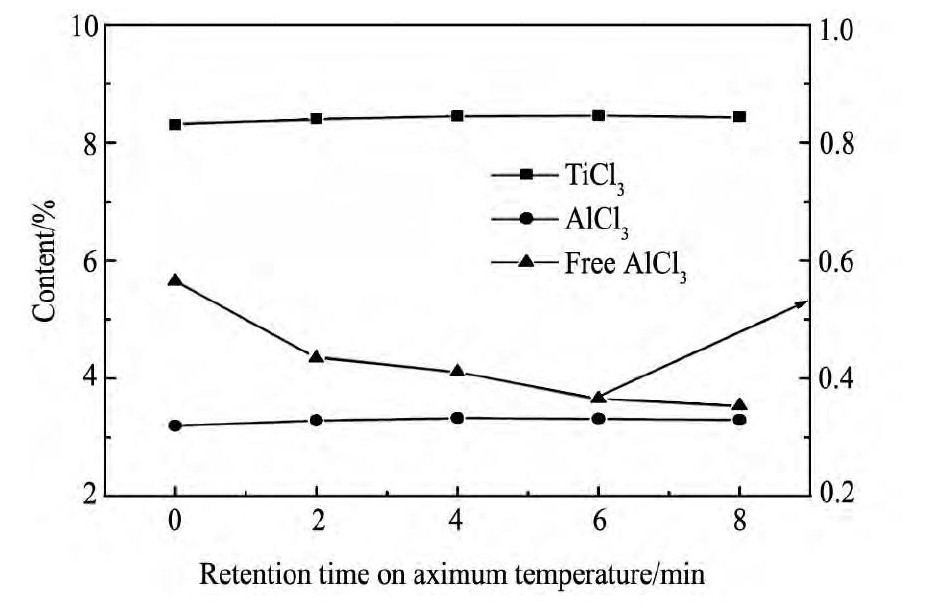
ͼ5 ����¶�ͣ��ʱ���Ti Cl3, Al Cl3������Ӱ��Fig.5 Effect of maximum temperature retention time on Ti Cl3, Al Cl3content
2.5 N2��Ӱ��
Ti Cl3��Һ�Ʊ�Ӧͨ�뵪��, ������������Ϻ���뷴Ӧ�ޡ�������Ҫ����:1.ϡ����������������������Ӧ�ٶ�, ��ֹ��Ӧ����������ȫ�¹�;2.����������, �ٽ����Ͻ���, ��֤������������ֻ�ϡ��������ݱ���, ��ͨ����ʱ, �����������ķ�Ӧ�ٶ���ͨ�뵪��ʱ��40~45����
�������ʵ��, �����������Ŀ��Ʒ���Ϊ:�����������ֱ���ô�ѹ����С������Сѹ�������������Ʒ���������������Ч��֤���ϳ�ֽӴ���Ӧͬʱ�ɱ�������ѹ�����㵼�����������������͵��������Ŀ��Ʋ������5��ʾ��
���ô˿��Ʒ����ɱ�֤���������۷�Ӧƽ�Ƚ���, ͬʱ�ɷ�ֹ����ѹ�����ߵ������������������뷴Ӧ��ϵ��
��5 �����͵������Ʋ���Table 5 Control parameters of Cl2and N2 ����ԭͼ
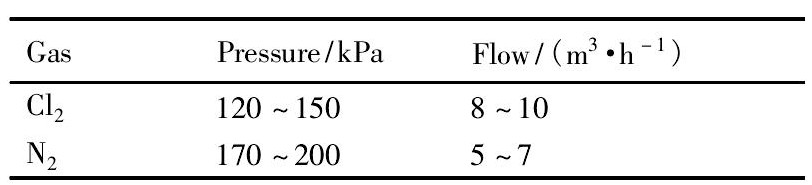
��5 �����͵������Ʋ���Table 5 Control parameters of Cl2and N2
2.6 �ȶ����鼰����Ч��
�����Ż����ղ�����չ�ȶ���ҵ����, �ȶ�����ͼ��ѽ�Һ�Ʊ������볣��������ͬ, �ͼ��ѽ�ҺӦ���������ij�����ѳ���ҵ�������װ��, �����õ���ȷ�ʽ, ����Ϊ600~800k W, �����ݻ�Ϊ9 m3, ����������Ϊ��ʽ��, ������Ϊ32�顣���ղ���Ϊ:�������1.25%, Cl2/Al 1.0, ����¶�ͣ��ʱ��8 min, ����ѹ��190 k Pa, ����6.5 m3��h-1, ����ѹ��145 k Pa, ����9.8 m3��h-1��Ti Cl3��Һ�Ʊ������ȶ��ܿ�, Ti Cl3����8.9%~10.1%, Al Cl3����3.5%~4.2%����Ti Cl3��Һ����VOCl3����Ϊ0.15%~0.20%�Ĵ����Ȼ���, Ti Cl3��Һ���Ϊ�����Ȼ��ѵ�7% (������) , VOCl3��Al Cl3�����ֱ�Ϊ0.0003%��0.0006%, �ﵽ�й���ɫ������ҵ�� (YS/T655-2007) ��һ��ƷҪ��
3 ����
1.���۳�������Ч�ɷ���Ti Cl3��0.33Al Cl3������ѧ�������, ������Ϊԭ���Ʊ�Ti Cl3��Һ�ķ�Ӧ������:������������Ӧ, ���ɵ�Al Cl3, �ų�����, Ϊ���������Ȼ��ѵķ�Ӧ�ṩ��������Ti Cl3��0.33Al Cl3��
2.�Ʊ�Ti Cl3��Һ���Ź��ղ���Ϊ:�����뾫���Ȼ��ѱ���1.1%~1.4% (������) , �����������ۼ���������, Cl2/Al�� (������) 0.7~1.1, ����¶�ͣ��ʱ��6~8 min, N2ѹ��170~200 k Pa, ����5~7 m3��h-1, Cl2ѹ��120~150 k Pa, ����Ϊ8~10 m3��h-1��
3.�ȶ������Ʊ���Ti Cl3��Һ��������, Ti Cl3����8.9%~10.1%, Al Cl3����3.5%~4.2%, ��ҵӦ�ñ���Ti Cl3��Һ������Ȼ������ (������) Ϊ7%ʱ�ɽ������Ȼ�����VOCl3������0.15%~0.20%������0.0003%��
�����
[1] Zheng L, Li D, He C C, Chen Q Q, Deng Z H, Tong S H.Microstructure of Ti-Mo-Si coating laser cladding on titanium alloy[J].Chinese Journal of Rare Metals, 2016, 40 (11) :1094. (֣��, �, �شϴ�, ��ٻٻ, ������, ͯ�ۻ�.�ѺϽ���漤���۸�Ti-Mo-SiͿ����֯�о�[J].ϡ�н���, 2016, 40 (11) :1094.)
[2] Valiev R Z, Semenova I P, Latysh V V, Rock H, Lowe T C, Petruzelka J.Nanostructured titanium for biomedical application[J].Advanced Engineering Material, 2008, 10 (8) :1.
[3] Miao Q D, Sheng Z, Li K H.Study of source and trend of manganese in titanium sponge[J].Light Metals, 2016, (8) :47. (���춫, ʢ, ���.���������̵���Դ�������о�[J].�����, 2016, (8) :47.)
[4] Eldon R P, James A H.Extractive metallurgy of titanium:a review of the state of heart and evolving production techniques[J].JOM, 1983, 35 (6) :60.
[5] Bhowmik S, Benedictus R, Poulis J A, Bonin H W, Bui V T.High-performance nanoadhesive bonding of titanium for areospace and space applications[J].International Journal of Adhesion&Adhesives, 2009, 29:259.
[6] Zhang J, Wu X.Development of process sponge titanium[J].Titanium Industry Progress, 2006, 23 (2) :8. (�Ž�, ����.�����⺣��������������״[J].�ѹ�ҵ��չ, 2006, 23 (2) :8.)
[7] Weil K S, Hovanski Y, Lavender C A.Effects of Ti Cl4purity on the sinterability of Armstrong-processed Ti powder[J].Journal of Alloys and Compounds, 2009, 473:L39.
[8] Li Y J, Sun H M, Xu W C.Status of process for removing vanadium from tetrachloride titanium and its development trends[J].Modern Chemical Industry, 2007, 27 (6) :24. (���Ǿ�, �ﻢ��, ��ΰ��.�����Ȼ��ѳ���������״����չ����[J].�ִ�����, 2007, 27 (6) :24.)
[9] John B G, Michael M L.Process for purifying titanium tetrachloride[P].United Stated Patent:US20020179427A1, 2002.
[10] Sun K, Ma Y Y, Dong A G.Separation of impurity vanadium from Ti Cl4by means of adsorption[J].Rare Metals, 1999, 18 (2) :129.
[11] Yang J P, Liu J, Chen T X, Zhang P.Study on process of vanadium removal from crude titanium tetrachloride by carbon compounds[J].Chemical Industry Times, 2008, 22 (10) :53. (���, ����, ������, ��ƽ.��Ti Cl4�л���������о�[J].����ʱ��, 2008, 22 (10) :53.)
[12] Chu L Z, Yu J, Li M X, Li W.Development on technology of removing vanadium from raw titanium tetrachloride[J].Chemical Intermediate, 2009, (10) :12. (����־, �ھ�, ������, ��.�����Ȼ��ѳ������ս�չ[J].�����м���, 2009, (10) :12.)
[13] Xu C, Yuan Z F, Wang X Q.Preparation of Ti Cl4with the titanium slag containing magnesia and calcia in a combined fluidized bed[J].Chinese J.Chem.Engin., 2006, 14 (3) :281.
[14] Luo J H, He H L.Development status of vanadium removal process from crude titanium tetrachloride[J].Nonferrous Metals (Extractive Metallurgy) , 2015, (5) :44. (��, �λ���.�����Ȼ��ѳ������շ�չ��״[J].��ɫ���� (ұ������) , 2015, (5) :44.)
[15] Yu J, Chen T X, Zhang P.Present situation and evolution on process of vanadium removal from rough titanium tetrachloride[J].Guizhou Chemical Industry, 2007, 32 (3) :22. (�ھ�, ������, ��ƽ.�����Ȼ��ѳ������ռ���չ[J].���ݻ���, 2007, 32 (3) :22.)
[16] Winter G.Purification of vanadium-containing Ti Cl3by heating with Ti Cl3��0.33Al Cl3[P].United Stated Patent:3871874, 1975.
[17] Isoo S, Takeshi S, Koichi T.Process for activating catalyst component useful for polymerizing propylene[P].United Stated Patent:3923687, 1975.
[18] Guo G L, Tang Y Q.A study on surface structure of3Ti Cl3��Al Cl3catalysts system[J].China Science (Series B) , 1987, (4) :355.