文章编号:1004-0609(2010)03-0522-07
RuO2・nH2O薄膜的制备以及物相演变和伏安特性
刘 泓,甘卫平,郭桂全,刘继宇,李 祥,郑 峰
(中南大学 材料科学与工程学院,长沙 410083)
摘 要:以RuCl3・3H2O水溶液为电沉积液,采用直流?示差脉冲组合电沉积技术,通过后续热处理工艺制备超级电容器用钽基RuO2・nH2O薄膜电极材料。用X射线衍射仪 (XRD)、红外光谱仪 (FTIR)、差热分析仪 (DTA)、扫描电镜 (SEM)和电化学分析仪,研究前驱体RuCl3・cH2O转化为RuO2・nH2O的物相演变行为以及微观组织形貌和循环伏安性能。结果表明:随着热处理温度升高,前驱体RuCl3・cH2O通过4步反应转变成RuO2・nH2O薄膜;该薄膜经历从无定形向晶体结构的转变。经300 ℃热处理的RuO2・nH2O薄膜电极材料的单位面积质量为2.5 mg/cm2,比电容达到512 F/g;当电压扫描速率从5 mV/s增加到250 mV/s 时,其比电容下降34%。
关键词:水合氧化钌;薄膜材料;热处理;超级电容器;物相演变
中图分类号:TG154.5 文献标识码:A
Preparation, phase transition and cyclic voltammetric properties of RuO2・nH2O film
LIU Hong, GAN Wei-ping, GUO Gui-quan, LIU Ji-yu, LI Xiang, ZHENG Feng
(School of Materials Science and Engineering, Central South University, Changsha 410083, China)
Abstract: As a good electrode material for supercapacitor, RuO2・nH2O film was deposited on tantalum foils in aqueous solution of RuCl3・3H2O by galvanostatic-differential pulse voltammetry and heat treatment. The phase transition, surface morphology and cyclic voltammetric performance from precursor RuCl3・cH2O to amorphous and crystalline RuO2・nH2O of the developed film were studied with X-ray diffractometer (XRD), infrared spectrometer (FTIR), differential thermal analyzer (DTA), scanning electron microscope (SEM) and electrochemical analyzer, respectively. The results show that the precursor RuCl3・3H2O film transforms into RuO2・nH2O through four reactions, including one from amorphous to crystal phase change with the increase of temperature. After being heat treated at 300 ℃, surface mass of the RuO2・nH2O film electrode material is 2.5 mg/cm2 with a specific capacitance of 512 F/g. The specific capacitance of the RuO2・nH2O film decreases by 38% when the voltage scan rate increases from 5 mV/s to 250 mV/s.
Key words: RuO2・nH2O; film material; heat treatment; supercapacitor; phase evolution
随着高端电子设备朝小型化、轻量化、高可靠性、长寿命的方向发展,电子器件中的电容器必须向容量大、体积小、功率密度高和脉冲放电性能优异的方向发展[1]。传统的电容器已经不能满足高端电子设备的要求。超级电容器的比功率是蓄电池的数十倍,比能量是物理电容器的数百倍[2],而且具有充放电效率高、能够持续放出大电流[3?4]、不需要维护保养和寿命长等性能,正在被广泛地应用于航空航天、电子信息技术、绿色环保能源工业、电动汽车等领域。研究超级电容器有着极其广阔的应用前景和重要的战略意义。
根据电荷的储存机理,超级电容器可分为双电层电容器和法拉第准(赝)电容器。双电层电容器使用碳素材料作为电极[5?6],比电容为200 F/g左右。法拉第准电容器使用RuO2[7]、MnO2[8]、NiO[9]和SnO2[10]等金属氧化物作为电极,通过法拉第氧化还原反应完成充放电。其中,RuO2・H2O电极材料的比电容高达700 F/g[7],比电容大约是碳电极的3倍,比功率比碳电极的大1个数量级;在硫酸电解液中性能稳定,充放电性能优异且循环寿命长。因此,RuO2・H2O是目前应用于高比能超级电容器性能最优异的电极材料,已显示出非常重要的地位和广阔的应用前景[11]。
RuO2・H2O电极的性能是直接影响超级电容器整体性能的主要因素。RuO2・H2O占超级电容器制造成本的50%以上。不同形态结构的RuO2・H2O的比电容相差很大。对于微孔结构的RuO2・H2O电极材料,电极深层的活性物质能参与快速可逆的氧化还原反应;与晶体结构的RuO2相比,质子更容易在无定形的RuO2・H2O中自由扩散。因此,无定形的RuO2・H2O电极材料具有更大的比电容。目前,制备氧化钌电极材料的方法有电沉积法[11?13]、涂敷热分解法[14]、Sol-gel法[3, 15]和CVD法[16]等。采用涂敷热分解等高温方法制备RuO2电极材料,薄膜的结合水含量较低,影响电容特性,且RuO2的用量较大;用Sol-gel法制备RuO2,薄膜附着力较差;CVD法制备RuO2薄膜,反应时间长,不宜批量生产;电沉积法设备要求低,采用RuCl3・3H2O水溶液为电沉积液制备RuO2・H2O薄膜,成本相对较低。电沉积法制备的初生薄膜成分为RuCl3・cH2O,附着力较差,比电容较小,需要经过热处理将其转变为RuO2・nH2O,以便改善附着力和提高比电容[13]。但是,若处理温度过高会使RuO2・nH2O晶化,导致比电容快速降低。为此,本文作者采用电沉积法制备RuO2・nH2O薄膜材料,研究在钽基RuO2・nH2O薄膜制备过程中前驱体转变为RuO2・nH2O的物相演变行为;研究热处理过程中RuO2・nH2O由无定形结构向晶体结构演变的规律和RuO2・nH2O的循环伏安性能。
1 实验
1.1 钽箔基体的预处理
将纯度为99.95%的金属钽箔切成尺寸为15 mm×15 mm×0.1 mm的样品,用金相砂纸打磨抛光,丙酮除油,碱液加热到70~80 ℃后浸泡10 min,混合酸清洗40 s,再用去离子水超声波清洗后保存备用。
1.2 钽基氧化钌薄膜的制备
首先,配制3 mmol/L RuCl3・3H2O和200 mmol/L NaNO3的混合溶液,经充分搅拌后静置待用;然后,以石墨为阳极,金属钽片为阴极,采用直流?示差脉冲组合电沉积技术,先用3 mA/ cm2的直流电流密度沉积0.5 h,然后采用示差脉冲电流沉积2.5 h,电压脉冲宽度为10 s,脉冲周期为20 s,振幅为0.02 mA/cm2,每点电流增益为0.01 mA/cm2,终止电流密度为6 mA/cm2。沉积获得RuCl3・cH2O薄膜前驱体,经自然凉干,在0.5 mol/L的RuCl3・3H2O异丙醇溶液中提拉,然后,分别经过100、150、200、300、400和500 ℃处理,保温时间为2 h,升温速率为10 ℃/s。
1.3 性能测试
分别采用D-MAX 2500X射线衍射仪、Nicolet 380红外光谱仪、SEM (Sirion 200) 扫描电镜和STA 49C差热分析仪对薄膜材料的晶体结构、官能团、微观形貌和热分解过程进行分析。用CHI 660C电化学测试仪对薄膜的电化学性能进行测试,采用铂片电极作为辅助电极,硫酸亚汞电极作为参比电极,钽基RuO2・nH2O薄膜作为工作电极,电解液为0.5 mol/ L的H2SO4溶液。
2 结果与讨论
2.1 表面形貌
电沉积制备的RuCl3・cH2O薄膜前驱体与钽基片的结合力较弱,需要通过热处理使RuCl3・cH2O转变成RuO2・nH2O,完成成分和结构转变,提高附着力,增强薄膜的电容稳定性。若热处理温度过高,会减少RuO2・nH2O的结晶水含量,晶化严重,降低薄膜的比电容[7]。实验证明,薄膜的最佳热处理温度为300 ℃。图1所示为薄膜在热处理前、后的SEM像。自然晾干后的薄膜微观形貌如图1(a)所示,其表面呈现出均匀的絮凝状微孔结构,附着力低,在溶液中浸泡会脱落。将自然晾干的薄膜以6 ℃/min升温至300 ℃后保温 1 h,然后随炉冷却,结构由原来的絮凝状微孔转变成为小于15 μm的缩水板块状结构(图1(b)),薄膜的单位质量由5.4 mg/cm2降低到2.5 mg/cm2,薄膜在溶液中浸泡不会脱落而且电学性能稳定。图1(c)所示为图1(b) 的横截面图。由图1(c)可以看出,薄膜厚度约为5.6 μm。热处理改变薄膜的形貌,提高薄膜的附着力。

图1 薄膜自然晾干和热处理后正面及其横截面的SEM像
Fig.1 SEM images of film: (a) After being dried in air; (b) After being heat treated at 300 ℃ for 2 h; (c) Cross section of (b)
2.2 RuO2・nH2O的物相演变过程
薄膜中的初始成分是异丙醇和RuCl3・cH2O,经过300 ℃热处理后,转变为RuO2・nH2O。通过X射线仪、红外光谱仪、差热分析仪检测分析薄膜从RuCl3・cH2O转变成RuO2・nH2O的机理,研究薄膜材料各成分在热处理过程中的转变过程。
图2所示为不同温度处理后薄膜的XRD谱。由图2可以看出,在150 ℃以下处理的薄膜的XRD谱中不存在晶体衍射峰,以非晶态存在;当处理温度高于200 ℃时,薄膜的XRD谱中存在Ru和RuO2 2种晶体的特征衍射峰;当处理温度为200 ℃时,Ru晶体的特征衍射峰窄而强,而RuO2的特征衍射峰比较宽;随着温度的升高,Ru晶体的特征衍射峰变弱,RuO2的特征衍射峰变得窄而尖。X射线衍射分析结果说明,在升温过程中,Ru晶体先增多后减少,而RuO2在不断地产生,并且经历从非晶态向晶态的转变。

图2 不同温度处理的薄膜的XRD谱
Fig.2 XRD patterns of film materials treated at different temperatures
薄膜在300 ℃和100 ℃处理后的红外光谱图如图3所示。由图3可看出,波数为3 412.77 cm?1和3 138.5 cm?1的波峰对应的是经300 ℃热处理的薄膜的结晶水的反对称和对称伸缩振动[17];波数为3 444.04 cm?1的波峰对应的是经100 ℃热处理的薄膜的结晶水的峰,从峰的特征可看出结晶水在100 ℃比在300 ℃多;波数为1 617.44 cm?1和1 400.65 cm?1的波峰对应的是羧酸盐中羧酸根的伸缩振动峰,前者是―COO?的反对称伸缩振动峰,峰形宽,很强,后者是―COO?的对称伸缩振动峰,强度稍弱,峰形尖锐,这些都是典型的羧酸盐中羧酸根的特征峰。两峰的波数差大于200 cm?1,

图3 不同温度热处理薄膜的红外光谱图
Fig.3 Infrared spectra of film materials treated at different temperatures
说明羧酸根是单齿键合的。在2 065 cm?1和1 655 cm?1附近没有出现吸收峰,表明样品中不存在自由羧酸。波数为599.76 cm?1和500.31 cm?1的波峰是Ru―O的特征峰。薄膜经100 ℃和300 ℃处理后,其红外光谱中不存在醇的特征峰,表明此时已经不存在异丙醇,红外谱峰出现的位置一样,只是强度有变化,即红外谱峰对应物质的成分的相对量发生了变化。由此可以推断,随着温度的升高,薄膜中的异丙醇一部分受热挥发,另一部分被氧化成羧酸盐;水合氧化钌结晶水的含量随着温度升高而不断减少,反应贯穿整个热处理过程。
从XRD谱和红外光谱图的分析可知:随着温度的升高,RuCl3・cH2O转化成RuO2・nH2O,在150 ℃时RuO2・nH2O以非晶态存在;在200 ℃时已经向晶态转变,异丙醇被氧化,以羧酸盐形式存在;在100 ℃时羧酸盐已经开始产生。将薄膜在异丙醇溶液中提拉后在室温下放置5~10 min,然后在空气气氛下进行薄膜的DTA测试,结果如图4所示。由图4可以看出,在126.8 ℃前为吸热趋势,而在126.8 ℃后为放热趋势,在220 ℃左右放热和吸热达到平衡状态,在126.8 ℃到220 ℃之间存在2个吸热反应。结合图2所示的XRD谱和图3所示的红外光谱图可以推测出,薄膜在热处理过程中由RuCl3・cH2O转变成RuO2・nH2O的步骤和机理。在200 ℃以下的DTA吸热峰分别对应着以下不同的反应步骤。
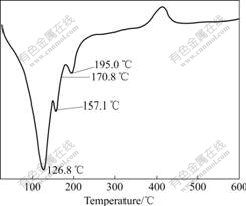
图4 薄膜在空气中的DTA曲线
Fig.4 DTA curve of film in air
1) 异丙醇挥发
异丙醇在室温下容易挥发,沸点是82.5 ℃,所以,薄膜的DTA曲线从室温到126.8 ℃处于吸热状态,对应的是异丙醇的挥发。查“Lange’s Handbook of Chemistry”得知,每摩尔异丙醇挥发吸收的热量为41.4 kJ[18]。
2) 形成单质钌
从126.8 ℃到220 ℃,薄膜的DTA曲线整体处于放热状态。分析XRD谱可知,单质Ru来源于RuCl3・cH2O的还原,在200 ℃,单质钌的特征峰最强,含量最多。分析红外光谱图可知,异丙醇被氧化,以羧酸盐形式存在,在100 ℃时羧酸盐已经开始产生。由于RuCl3・cH2O的强氧化性,将异丙醇被氧化成羧酸,从而产生单质钌,所以,对应126.8 ℃到220 ℃放热状态存在的反应为

反应(1)每生成1 mol单质钌放出的热量为312.6 kJ。
3) RuCl3・cH2O转化为RuO2・nH2O
从126.8 ℃到220 ℃的放热过程中,存在2个吸热反应。通过X射线衍射分析可知,在150 ℃时薄膜以非晶态存在,推测157.1 ℃吸热峰对应的反应为

反应(2)每生成1 mol RuO2・nH2O吸收的热量为30.21 kJ。
4) RuO2・nH2O转化为RuO2
物质从非晶转变为晶体有一个固定的起始温度。通过X射线衍射分析可知,晶体RuO2在200 ℃ 已经产生,因此,对应于195.0 ℃产生的吸热峰的反应为

2.3 循环伏安性能
利用三电极体系测定300 ℃热处理的薄膜在不同扫描速率的循环伏安图如图5所示。由图5可看出,循环伏安曲线呈现方形特征,表现出良好的充、放电性能。在充、放电过程中,RuO2・nH2O与电解液发生质子交换,产生法拉第氧化还原反应[19?20]:


图5 薄膜在不同扫描速率下的循环伏安图
Fig.5 Cyclic voltammetric curves of film as function of scan rate
RuO2・nH2O的法拉第反应包含连续、可逆转化的多个氧化还原反应,表现出良好的法拉第赝电容特性。随着扫描速率的增加,氧化峰向高电位偏移,还原峰向低电位偏移。在?0.6 V至0.6 V的范围内有3个氧化还原反应峰,是多重氧化还原过程叠加的结果,分别对应着Ru(Ⅱ)/Ru(Ⅲ)、Ru(Ⅲ)/Ru(Ⅳ)和Ru(Ⅳ)/Ru(Ⅴ) 之间的转化[21]。第1个氧化峰在低扫描速率时十分明显,在高扫描速率时第2个氧化峰明显。
循环伏安图的第1和第2个氧化峰的峰值电流与扫描速率之间的关系如图6所示。由图6可以看出,第1个氧化峰的峰值电流随扫描速率的增加缓慢增大,第2个氧化峰的峰值电流随扫描速率增加线性增大。根据图5和6的分析,可以推测:Ru(Ⅱ)/Ru(Ⅲ)之间的反应在较慢的电位扫描速率时才能进行得较充分,而Ru(Ⅲ)/Ru(Ⅳ)之间的反应在高电位扫描速率下也能完成快速的充、放电。

图6 薄膜的比电容和循环伏安峰值电流与电压扫描速率的关系
Fig.6 Relationships among voltage scan rate and specific capacitance and peak current of cyclic voltammetry of film
薄膜的比电容可以通过下述公式进行计算:
 (5)
(5)
式中:Cp为比电容;i为响应电流的微分值;s为扫描速率;m为薄膜的质量。
根据公式(5)计算不同扫描速率下的比电容,结果如图6所示,可以看出比电容与扫描速率之间的变化关系。当电压扫描速率从5 mV/s增加到250 mV/s时,比电容从512 F/g下降到327 F/g,下降了34%。随着扫描速率的增加,比电容下降趋势先快后慢,这主要是由于Ru(Ⅱ)/Ru(Ⅲ)之间的反应在高的扫描速率下不能快速完成充、放电所致。
图7所示为薄膜电极材料经不同热处理后比电容与循环次数的关系。由图7可以看出:1) 薄膜电极材料的热处理温度低于200 ℃时,在充、放电的前10次循环中,薄膜材料的比电容快速下降,随着循环次数的增加,比电容趋于稳定;2) 热处理温度越高,薄膜材料的比电容越稳定,经100、150、200、300、400和500 ℃热处理的薄膜材料在120次充、放电循环后,比电容分别保持30%、40%、72%、97%、99%和99%;3) 随着热处理温度的升高,薄膜材料的比电容经历先升后降的趋势,在300 ℃时,薄膜材料具有较高的比电容且循环充、放电稳定性良好。

图7 热处理温度对薄膜电极材料比电容的影响
Fig.7 Effects of heat treatment temperature on specific capacitance of film electron materials
经较低温度热处理薄膜的比电容低而且不稳定,随着热处理的温度升高,薄膜材料的比电容呈先升后降的趋势。从RuO2・nH2O的相转变过程分析可以知道,这主要是因为随着热处理温度的升高,薄膜电极材料中RuCl3・3H2O转化为RuO2・nH2O的比例增加,附着力更强,有利于提高薄膜材料的比电容;随着温度的升高RuO2・nH2O的结晶水的含量不断减少[7],离子间距不断缩小,晶体的晶粒尺寸逐渐变大,质子的扩散只发生在无定形氧化钌之间,而且取决于钌离子的间距,晶体的点阵结构阻止质子的扩散,从而抑制RuO2・nH2O薄膜与电解液界面发生的法拉第氧化还原反应,降低薄膜材料的比电容。
3 结论
1) 随着温度的升高,RuCl3・cH2O向晶态RuO2・nH2O薄膜转变。在150 ℃以下,RuO2・nH2O以非晶态存在,在200 ℃以上向晶态转变,存在单质Ru和RuO2 2种晶体。随着温度的升高,单质Ru晶体先增多后减少,晶态RuO2不断增多。
2) 随着温度的升高,RuCl3・cH2O薄膜发生异丙醇挥发、形成非晶态RuO2・nH2O、形成单质钌和RuO2・nH2O失去结晶水4个反应而转化为晶态RuO2。
3) 经300 ℃热处理的薄膜单位面积质量为2.5 mg/cm2,厚度约为5.6 μm,综合性能最佳。薄膜的比电容随着扫描速率的增加而下降;当电压扫描速率从5 mV/s增加到250 mV/s时,比电容从512 F/g下降到327 F/g,下降34%。
4) 随着温度的升高,薄膜的比电容先升后降;当热处理温度高于200 ℃时,薄膜的比电容稳定性较好, 经100 ℃和300 ℃热处理的薄膜在120次充、放电循环后比电容分别保持30%和97%。
REFERENCES
[1] JUN L, SIVAKKUMAR S R, JANG M K, JONG H K, SEONG M J, DONG Y K. Carbon nanofibre/hydrous RuO2 nanocomposite electrodes for supercapacitors[J]. Journal of Power Sources, 2007, 168: 546?552.
[2] LIU X R, PETER G P. Ru oxide supercapacitors with high loadings and high power and energy densities[J]. Journal of Power Sources, 2008, 176: 410?416.
[3] HU C C, WANG C C, CHANG K H. A comparison study of the capacitive behavior for sol-gel-derived and co-annealed ruthenium-tin oxide composites[J]. Electrochimica Acta, 2007, 52: 2691?2700.
[4] GODFREY S, BRANKO N P. Performance optimization of a battery-capacitor hybrid system[J]. Journal of Power Sources, 2004, 134: 130?138.
[5] STAITI P, LUFRANO F. A study of the electrochemical behaviour of electrodes in operating solid-state supercapacitors [J]. Electrochimica Acta, 2007, 53: 710?719.
[6] HU C C, SU J H, WEN T C. Modification of multi-walled carbon nanotubes for electric double-layer capacitors: Tube opening and surface functionalization [J]. Journal of Physics and Chemistry of Solids, 2007, 68: 2353?2362.
[7] ZHENG J P, XIN Y. characterization of RuO2?nH2O with various water contents[J]. Journal of Power Sources, 2002, 110: 86?90.
[8] TAKUYA S, VINAY G, NORIO M. Effects of electrochemical-deposition method and microstructure on the capacitive characteristics of nano-sized manganese oxide[J]. Electrochimica Acta, 2006, 51: 4412?4419.
[9] FERNANDO P, JOAQUIN I, TERESA A C, CARLOS P, ROSA M R, JOSE M A, JOSE M R. RuO2・xH2O/NiO composites as electrodes for electrochemical capacitors: Effect of the RuO2 content and the thermal treatment on the specific capacitance[J]. Electrochimica Acta, 2006, 51: 4693?4700.
[10] HWANG S W, HYUN S H. Synthesis and characterization of tin oxide/carbon aero gel composite electrodes for electrochemical supercapacitors[J]. Journal of Power Sources, 2007, 172: 451?459.
[11] MONDAL S K, MUNICHANDRAIAH N. Anodic deposition of porous RuO2 on stainless steel for supercapacitor studies at high current densities[J]. Journal of Power Sources 2008, 175: 657?663.
[12] HAN J H, LEE S W, CHOI G J, LEE S Y, HWANG C S, DUSSARRAT C, GATINEAU J. Chemical vapor deposition of Ru thin films with an enhanced morphology, thermal stability, and electrical properties using a RuO precursor[J]. Chemistry of Materials, 2009, 21: 207?209.
[13] 甘卫平, 黎小辉, 欧定斌, 覃政辉. 退火温度对钽基RuO2・nH2O 电沉积薄膜电容性能的影响[J]. 中南大学学报: 自然科学版, 2006, 37(4): 660?664.
GAN Wei-ping, LI Xiao-hui, OU Ding-bin, QIN Zheng-hui. Effect of annealing temperature on capacitance of ruthenium oxide films deposited on tantalum substrate[J]. Journal of Central South University: Science and Technology, 2006, 37(4): 660?664.
[14] DAVID E. Improved capacitor using amorphous RuO2[M]. Florida: Evans Capacitor Company, 2000.
[15] 亓淑艳, 冯 静, 闫 俊, 侯相钰, 张密林. 海胆球形和纳米线形MnO2 制备及其超级电容特性[J]. 中国有色金属学报, 2008, 18(1): 113?117.
QI Shu-yan, FENG Jing, YAN Jun, HOU Xiang-yu, ZHANG Mi-lin. Hydrothermal synthesis and supercapacitor properties of urchin sphere and nanowire MnO2[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(1): 113?117.
[16] GUJAR T P, SHINDE V R, LOKHANDE C D, KIM W Y. Spray deposited amorphous RuO2 for an effective use in electrochemical supercapacitor[J]. Electrochemistry Communications, 2007, 9: 504?510.
[17] 李良超, 郝仕油, 林秋月. 水杨酸锰的热分解机理及纳米氧化锰形貌[J]. 中国有色金属学报, 2004, 14(12): 2114?2119.
LI Liang-chao, HAO Shi-you, LIN Qiu-yue. Thermal decomposition mechanism of manganese salicylate and shape of nanometric manganese oxide[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(12): 2114?2119.
[18] DEAN JA. Lange’s handbook of chemistry[M]. New York: McGraw-Hill Inc, 1972, 642.
[19] PATAKE V D, LOKHANDE C D. Chemical synthesis of nano-porous ruthenium oxide (RuO2) thin films for supercapacitor application[J]. Applied Surface Science, 2008, 254: 2820?2824.
[20] MARIJAN V, DUNJA C. Electrochemical quartz crystal microbalance study of electrodeposited ruthenium[J]. Journal of Electroanalytical Chemistry, 1999, 474: 167?173.
[21] KVASTEK K, HORVAT V. Electrochemical properties of hydrous ruthenium oxide films formed and measured at different potentials[J]. Journal of Electroanalytical Chemistry, 2001, 511: 65?78.
基金项目:国家高技术研究发展计划资助项目(2007AA03Z240);湖南省重大专项资助项目(2009FJ1002-3);米塔尔基金资助项目(07MX18)
收稿日期:2009-04-16;修订日期:2009-09-16
通信作者:刘 泓,博士研究生;电话:0731-88830248;E-mail: chinaliuhong@yahoo.com.cn
(编辑 杨 华)