文章编号: 1004-0609(2006)06-1094-06
源自硫化矿区的氧化亚铁硫杆菌新菌系的鉴定
杨 宇1, 2, 彭 宏1, 万民熙1, 邱冠周1, 2, 黄菊芳1, 2, 胡岳华1, 2
(1. 中南大学 资源加工与生物工程学院, 长沙 410083;
2.中南大学 生物冶金教育部重点实验室, 长沙 410083)
摘 要: 从广西铜坑矿区多金属复杂硫化矿矿坑水中分离得到了一株嗜酸氧化亚铁硫杆菌(暂命名为TK), 该菌株为革兰氏阴性细菌, 短杆状, 菌体大小为(0.4±0.1) μm×(1.4±0.2) μm, 最适生长温度为25~30℃, 最适pH值为2.0, 化能自养型, 能利用亚铁、 单质硫和葡萄糖生长, 不能利用硫代硫酸钠、 蛋白胨生长。 测定其亚铁和元素硫的氧化能力, 并考察它对铁闪锌矿的浸出效果。 以16SrDNA序列同源性为基础构建了包括15株已报道菌种和其他菌属菌株作为外来群在内的系统发育树。 结果表明: TK菌株处于单独的一个分支内, 与嗜酸氧化亚铁硫杆菌株D2最为相似, 相似性为98.67%, 推测TK菌株为嗜酸氧化亚铁硫杆菌的一个新菌系。 该菌系的分离为嗜酸氧化亚铁硫杆菌多样性和生态分布研究提供了一种新材料。
关键词: 嗜酸氧化亚铁硫杆菌; 生物浸出; 系统发育树; 16SrDNA 中图分类号: Q939
文献标识码: A
Identification of new-subspecies
Acidithiobacillus ferrooxidans strain from complex sulfide mines
YANG Yu1, 2, PENG Hong1, WAN Ming-xi1, QIU Guan-zhou1, 2,
HUANG Ju-fang1, 2, HU Yue-hua1, 2
(1. School of Minerals Processing and Bioengineering,Central South University, Changsha 410083, China;
2. Key Laboratory of Biometallurgy of Ministry of Education,Central South University, Changsha 410083, China)
Abstract: An Acidithiobacillus ferrooxidans strain TK was isolated from the Tong Ken area, Guangxi province in China. The cell of TK strain is Gram negative and rod-shaped in (0.4±0.1) μm×(1.4±0.2) μm. The optimum growth temperature is 25-30℃, and the optimum growth pH is 2.0. The TK strain can grow autographically by using Fe2+, sulfur, glucose as sole energy sources, however, can not grow with NaS2O3 and peptone. The oxidation of Fe2+, sulfur and bioleaching marmatite with this strain was studied. A phylogenetic tree was constructed by comparing with the published 16SrDNA sequences of the relative bacteria species. In the phylogenetic tree, the TK strain is in a new branch which has the closest relative to the Acidithiobacillus ferrooxidans strain D2 with 98.67% sequence similarity. These results reveal that the TK strain may be a new strain of Acidithiobacillus ferrooxidans. It offers a new material in order to study the polymorphism and bionomics of bioleahing microbes.
Key words: Acidithiobacillus ferrooxidans(A.f); bioleaching; phylogenetic tree; 16SrDNA
嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans, 简称A.f菌), 是一种化能自养, 专性好氧, 嗜酸革兰氏阴性菌, 以自身细胞分裂的形式进行繁殖, 可以固定空气中的CO2, 以氧化Fe2+、 S0及S2-的化合物等来获得生长过程所需的能量[1, 2]。 自从1947年由Colmer和Hinkle首先分离纯化并命名以来, 一直是在生物浸出及其他如煤脱硫方面最主要的细菌之一, 受到国内外研究者的重视和研究[2-7]。
嗜酸氧化亚铁硫杆菌广泛生存于土壤、 海水、 淡水、 垃圾、 硫磺矿泉和沉积硫内, 尤以金属硫化矿或煤矿的酸性矿坑水中最为常见[3]。 但各地的A.f菌呈现出复杂的多样性, 国内外的研究均表明, 来源不同的嗜酸氧化亚铁硫杆菌菌株对金属硫化矿物的浸出效果明显不同[1, 3]。 因此采集不同样点的水样, 以分离纯化各种适应于不同底物作用的嗜酸氧化亚铁硫杆菌, 对了解不同地域和环境下A.f菌的多样性(包括种群多样性、 系统发育多样性和功能多样性)和生态演化规律, 进一步解析微生物冶金的群落结构和功能, 以及开发高效浸矿菌株有重要意义[8]。
本文作者从广西大厂铜坑矿区的某废矿坑的水样中, 分离纯化了一株铁硫氧化细菌, 进一步的生理生化显示为嗜酸氧化亚铁硫杆菌, 同时考察其浸矿能力, 这可能揭示嗜酸氧化亚铁硫杆菌分布多样性同浸矿环境的相互关联。
1 实验
1.1 菌种分离
菌株由广西大厂铜坑矿区的矿坑水中分离得到, 故暂命名为TK。 矿区中矿石为多金属复杂硫化矿石, 主要矿物有: 铁闪锌矿、 黄铁矿、 锡石。 矿坑水温度为25℃左右, pH值为6.6, 呈弱酸性。 将采集到的酸性水样先用9K液体培养基[9]富集培养, 待培养基的pH值下降到1.0左右, 用梯度稀释法在改进的9K固体培养基[10]涂布, 再用平板划线法分离。
1.2 培养基
采用的液体培养基(9K)配方如下: (NH4)2SO4 3g/L, KCl 0.1g/L, K2HPO4 0.5g/L, MgSO4・7H2O 0.5g/L, Ca(NO3)2 0.01g/L, FeSO4・7H2O 44.7g/L, pH1.8~2.0。 分离培养基为改进的9K固体培养基, 即在每升9K液体培养基中加入琼脂15g, KSCN 15.4g, pH2.0~2.2。 基础培养基为不加FeSO4的9K培养基。
1.3 生理生化特性
最适温度: TK菌株都以相同的菌量接种到9K液体培养基中, 分别置于不同的温度的条件下, 培养3d, 用血球计数板计数, 测定不同温度下TK的生长状况。
最适初始pH值: 用1mol/L的硫酸将9K液体培养基调至不同pH值, 接种相同的菌量, 培养3d, 用血球计数板计数, 测定不同pH条件下菌的生长状况。 能量利用特性: 基础培养基(不加Fe2+的9K培养基)中分别加入蛋白胨0.1%, 葡萄糖0.1%, 硫磺5%, 硫代硫酸钠1%, 七水合硫酸亚铁14.7%, 七水合硫酸亚铁14.7%+ 蛋白胨0.1%, 七水合硫酸亚铁14.7%+ 葡萄糖0.1%。 其中硫代硫酸钠、 七水合硫酸亚铁14.7%过滤除菌后加入培养基, 硫磺隔水蒸煮1h灭菌, 再加入培养基。 以TK菌株悬液接种, 每培养3d传代一次。 连续传代3次, 涂片并在显微镜下观察菌的生长情况。
1.4 电镜观察
30℃液体培养细菌至对数生长期, 收集菌体, 经革兰氏染色后在光学显微镜下观察。 将菌体涂布在小块盖玻片上, 自然晾干后, 再用导电胶贴于圆形贴片上, 喷金后在扫描电镜下观察。
1.5 亚铁和硫氧化活性测定
亚铁氧化活性测定: 取TK菌株的液体培养物, 用5×104 mol/L的K2Cr2O7对其中的Fe2+进行滴定。 每隔一段时间(一般为3~4h)取0.5mL菌液, 用蒸馏水(或者1%稀硫酸)稀释10倍, 再取其中的1mL滴定, 每次进行3次重复, 然后取其平均值作为滴定值。 滴定用1∶1的硫磷酸作为络合剂, 用0.2%二苯胺磺酸钠作指示剂, 滴定至亮紫色即到滴定终点。 硫氧化活性测定: 将TK菌株接种到只添加了单质硫的基础培养基(硫浓度为5%)中, 通过pH值的变化来考察TK菌株的硫氧化活性。
1.6 浸矿实验
矿样为铁闪锌矿, 粒度分布为104~147μm。 接种量为10%, 调节初始菌浓度为1.0×10-7 cell/mL, 浸矿条件: 矿样量5%, 160r/min, 30℃。
1.7 基因组提取及16SrDNA扩增
对纯化后培养的菌株使用Sangon公司的UNIQ-10柱式基因组DNA抽提试剂盒提取基因组DNA。 扩增体系50μL组成为: 33μL无菌水、 10×PCR buffer 5μL、 10×dNTPs 5μL、 引物FC27和RC1492各2μL、 Taq DNA聚合酶 1μL、 TK菌株的基因组DNA 2μL。 扩增程序: 94℃, 5min; 94℃, 1min; 55℃, 1min; 72℃, 3min(共30个循环); 72℃, 10min。 PCR引物为通用引物[9]如下: 正向引物(FC27)为5’-AGAGTTTGATCCTGGCTCAG-3’, 反向引物(RC1492)为5’-TACGGCTACCTTGTTACGACTT-3’。
1.8 16SrDNA测序及分析
采用克隆测序技术。 克隆试剂盒为上海生工的PCR产物克隆试剂盒SK2212。 载体选用pUCm-T, 蓝白筛选后所得的重组克隆交由北京三博远志生物技术有限责任公司测序。 序列已经提交到GenBank(登录号: DQ062114), 并将该16SrDNA序列与GenBank核酸序列数据库进行序列比较, 用clustalx1.8软件进行全序列比对[11], 并构建系统发育树。
2 结果与讨论
2.1 菌株形态与生理生化特性
菌株是革兰氏阴性细菌, 短杆状, 菌体大小为(0.4±0.1)μm×(1.4±0.2)μm。 在改进的9K固体培养基, 菌落呈圆形, 表面干燥, 直径约为0.6~1.0mm, 边缘不规则, 中央呈浅褐色(图1)。 最适生长温度为25~30℃, 最适pH值为2.0。 可以利用亚铁、 单质硫和葡萄糖生长, 且在亚铁葡萄糖混合培养基中也能生长; 不能利用蛋白胨生长, 且在亚铁蛋白胨混合培养基中不能生长(表1)。 考察葡萄糖和蛋白胨对TK菌株生长的影响, 适当加大了硫酸亚铁+蛋白胨混合培养基、 硫酸亚铁+葡萄糖混合培养基中蛋白胨、 葡萄糖的含量, 表明蛋白胨、 葡萄糖对TK菌株的生长都是抑制作用。 图2所示为在温度30℃, pH值1.8的9K液体培养基中, TK菌株的生长曲线。
表1 TK菌株能源利用特性
Table 1 Characteristics of TK strain with different substrates


图1 TK菌株的菌落形态和透射电镜像
Fig.1 Colony of TK and scanning electron micrograph

图2 TK菌株的生长曲线
Fig.2 Growth curve of TK strain
2.2 亚铁和硫氧化活性
2.2.1 亚铁氧化活性
TK菌株有较强的亚铁氧化活性, 能够氧化9K培养基中的Fe2+成为Fe3+来获取生命所需的能量, 实验表明亚铁氧化活性是与细菌的生长相关, 8h时该菌的亚铁氧化率较低, 和空白对照无明显差别, 这是细菌转移到新的环境后的一个适应过程, 生长繁殖处于诱导期; 随着培养时间的增加, 该菌开始进入缓慢生长期, 亚铁氧化率慢慢提高, 与空白对照差异显著; 34h时进入了对数生长期, 亚铁氧化率也急剧增高, 说明了亚铁氧化活性与细菌的生长密切相关, 细菌的生长越快, 亚铁氧化活性越强[12]。 52h亚铁氧化率达到99.5%。 虽然TK菌株利用Fe2+为能源生长, 但与一般微生物所具有的生长规律一致[13]。
图3所示为TK菌株在温度为30℃, pH值为2.0的9K培养基中的亚铁氧化率曲线。 其中: TK曲线代表接种TK菌株的培养基中Fe2+氧化随时间的变化, Control曲线为空白对照。
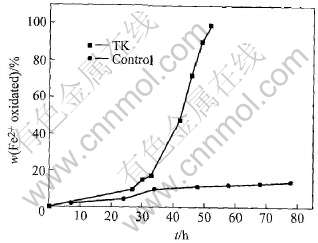
图3 TK菌株的亚铁氧化率曲线
Fig.3 Ferrous ion oxidation curves by TK strain(control: without cells)
2.2.2 硫氧化活性
接种3d后, pH值开始下降; 3~18d之间, 细菌产酸速度加快, 故pH值显著下降, 此阶段菌处于对数生长期; 18d以后, pH值变化不明显, 此时菌已处于平稳期。 在生长代谢过程中, 细菌以元素硫为能源, 氧化生成硫酸, 导致培养基的pH值下降, 由初始2.3降到1.0, 表明该菌具有较强的硫氧化活性。
图4所示为TK菌株接种添加了单质硫的基础培养基(硫浓度为5%)21d内, 培养基pH值随时间的变化。 图5所示为相应的培养过程中, 在第9、 15和21d细菌菌数变化的柱型图。
2.3 浸矿实验
铁闪锌矿的浸矿试验, 证实了TK菌株具有浸矿能力, 能对锌离子有一定的浸出效果, 但效果不是很明显, 可能是由于该菌株未经驯化所致和矿石成分较复杂的原因[4]。 开始阶段, TK菌株对铁闪锌矿的浸出速度比较稳定, 随时间变化不显著, 浸出锌离子的浓度维持在比无菌对照高出150mg/L左右的水平上, 但25d 以后, 锌的浸出率呈现出加快的趋势, 由于细菌能够吸附在矿石表面能对矿物产生腐蚀电化学作用来加快浸矿速度。 27d后, 细菌浸出的锌离子浓度达到650mg/L, 而无菌对照只有392mg/L, 如图6所示。 其中Control为无菌对照。 铁闪锌矿的浸矿试验中, 接种10%的未经过驯化的TK菌株能提高锌的浸出速率。

图4 TK菌硫氧化过程pH值的变化
Fig.4 Variation of pH value in sulfur oxidation by TK strain
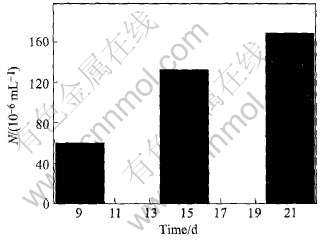
图5 TK菌硫源菌数变化柱形图
Fig.5 Population number of TK strain with sulfur substrate
2.4 16SrDNA序列分析与系统发育树
染色体DNA用PCR扩增出16SrDNA并进行测序, 序列长度为1199bp, Genbank中的序列登录号为DQ062114。 以16SrDNA 序列同源性为基础构建系统发育树(图7)。 TK菌株单独位于系统发育树一个新的分支中, 与目前Genbank中已有记录的其他菌株相比, 最相近的为D2(登记序列号AFE278723)相似度98.67%, 与标准株ATCC23270(登记序列号AF465604)相似度为97.68%。 数据显示菌株TK为嗜酸氧化亚铁硫杆菌的一个新菌系[14, 15]。 该菌株的分离为嗜酸氧化亚铁硫杆菌多样性和生态分布研究提供了一种新材料, 同时通过其他功能基因的研究也揭示了嗜酸氧化亚铁硫杆菌生态多样性的特点[16, 17], 这对浸矿细菌的遗传分类学研究具有一定的意义。
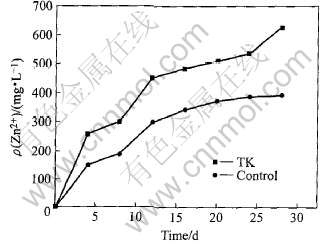
图6 TK菌株对铁闪锌矿中的锌的浸出
Fig.6 Zinc extraction from marmatite concentrate by TK strain

图7 TK菌株的16SrDNA序列系统发育树
Fig.7 Phylogenetic tree derived from 16SrDNA sequence of TK strain
3 结论
1) 从广西铜坑矿区多金属复杂硫化矿矿坑水中分离得到了一株嗜酸氧化亚铁硫杆菌TK, 为革兰氏阴性菌, 短杆状, 菌体大小为(0.4±0.1) μm×(1.4±0.2) μm。 最适生长温度为25~30℃, 最适pH值为2.0。
2) 该菌株能利用亚铁、 单质硫和葡萄糖生长, 不能利用蛋白胨生长。 混合培养基中, 蛋白胨、 葡萄糖对TK菌株的生长起抑制作用。 该菌株具有很强的亚铁氧化活性, 52h亚铁氧化率达到99.5%; 也具有很强的硫氧化活性, 在15d以后导致培养基的pH值由初始的pH 2.3降到pH 1.0。 亚铁氧化活性和硫氧化活性的活性强弱都与菌所处生长期相关。 TK菌株对铁闪锌矿浸出, 在27d, 细菌浸出的锌离子浓度达到650mg/L, 而无菌对照只有392mg/L, 说明菌株具有浸出硫化矿的能力。
3) 16SrDNA系统发育树的构建表明菌株TK为嗜酸氧化亚铁硫杆菌一个新菌系, 与目前Genbank中已有记录的其他菌株相比, 最相近的为D2(登记序列号: AFE278723)相似度98.67%。
REFERENCES
[1]Kelly D P, Wood A P. Reclassification of some species of Thiobacillus to the newly designated genera Acidithiobacillus gen. nov., Halothiobacillus gen. nov. and Thermithiobacillus gen. nov.[J]. International Journal of Systematic and Evolutionary Microbiology, 2000, 50: 489-500.
[2]Temple K L, Colmer A R. The autotrophic oxidation of iron by a new bacterium Thiobacillus ferrooxidans[J]. Journal of Bacteriolgy, 1951, 61: 605-611.
[3]Rawlings D E. Heavy metal mining using microbes[J]. Annual Review Microbiology, 2002, 56: 65-91.
[4]SHI Shao-yuan, FANG Zhao-heng. Bioleaching of marmatite flotation concentrate by Acidithiobacillus ferrooxidans[J]. Hydrometallurgy, 2004, 75: 1-10.
[5]Nestor D, Valdivia U, Chaves A P. Mechanisms of bioleaching of a refractory mineral of gold with Thiobacillus ferrooxidans[J]. International Journal of Mineral Processing, 2001, 62: 187-198.
[6]Brierley J A, Brierley C L. Present and future commercial applications of biohydrometallurgy[J]. Hydrometallurgy, 2001, 59: 233-239.
[7]Acharya C, Kar R N, Sukla L B. Bacterial removal of sulphur from three different coals[J]. Fuel, 2001, 80: 2207-2216.
[8]Baker B J, Banfield J F. Microbial communities in acid mine drainage[J]. FEMS Microbiology Ecology, 2003, 44: 139-152.
[9]Silverman M P, Lundgren D C. Study on the chemoautotrophic iron bacterium ferrobacillus ferrooxidans(Ⅰ): an improved medium and harvesting procedure for securing high cell yield[J]. Journal of Bacteriology, 1959, 77: 642-647.
[10]张在海, 邱冠周, 胡岳华, 等. 氧化亚铁硫杆菌的菌落分离研究[J]. 矿产综合利用, 2002, 1: 19-23.
ZHANG Zai-hai, QIU Guan-zhou, HU Yue-hua, et al. The investigation of the colony isolation of thiobacillus ferrooxidans[J]. Multipurpose Utilization of Mineral Resource, 2002, 1: 19-23.
[11]Thompson J D, Gibson T J, Plewniak F, et al. The ClustalX windows interface: flexible strategies for multiple sequence alignment aided by quality analysis tools[J]. Nucleic Acids Research, 1997, 24: 4876-4882.
[12]Ageeva S N, Kondrat’eva T F, Karavaiko G I. Phenotypic Characteristics of Thiobacillus ferrooxidans Strains[J]. Microbiology, 2001, 70(2): 186-194.
[13]Prescott L M, Harley J P, Klein D A. Microbiology[M]. 4th ed. New York: McGraw-Hill, 1999. 115-117.
[14]Karavaiko G I, Turova T P, Kondrateva T F, et al. Phylogenetic heterogeneity of the species Acidithiobacillus ferrooxidans[J]. Journal of Systematic and Evolutionary Microbiology, 2003, 53: 113-119.
[15]Rawlings D E. The molecular genetics of Thiobacillus ferrooxidans and other mesophilic, acidophilic, chemolithotrophic, iron- or sulfur-oxidizing bacteria[J]. Hydrometallurgy, 2001, 59: 187-201.
[16]杨宇, 彭宏, 孙斌, 等. 嗜酸氧化亚铁硫杆菌亚铁氧化酶基因分子多态性研究[J]. 遗传, 2005, 27(5): 787-791.
YANG Yu, PENG Hong, SUN Bin, et al. Molecular diversity of the gene encoding Fe(Ⅱ)-oxidizing enzyme in Acidithiobacillus ferrooxidans[J]. Hereditas, 2005, 27(5): 787-791.
[17]PENG Hong, YANG Yu, HU Yue-hua, et al. Structure analysis of 16SrDNA sequences from strains of Acidithiobacillus ferrooxidans[]. Journal of Biochemistry and Molecular Biology, 2006, 39(2): 178-182.
基金项目: 国家创新研究群体科学基金资助项目(50321402);国家重点基础研究发展规划资助项目(2004CB619201)
收稿日期: 2005-08-09; 修订日期: 2005-11-08
通讯作者: 胡岳华, 教授; 电话: 8877216; E-mail:hyh@mail.csu.edu.cn
(编辑陈爱华)