ʯú���������ᷰ�������о�
��Դ�ڿ���ϡ�н���2012���5��
�������ߣ���� ���̿� �뽨�� Ѧ���� ����
����ҳ�룺804 - 810
�ؼ��ʣ�ʯú;����;����ѧ;��ȡ;����������;
ժ Ҫ����ʯú��̼����������ֵ�������Ϊ�о�������"����+����������,����Һ���ص�pHֵ����ԭ��������ȡ�ͷ���ȡ,����ȡҺ������������γ�����"������ȡ���������������ղ���:����������С��37��m��100%������������Ϊ50%������������Ϊ4%��Һ�̱�Ϊ2.5��1�������¶�Ϊ90�桢����ʱ��Ϊ7 h�������½���,��12.5%P204+5%TBP+82.5%�ǻ�ú��Ϊ�л��ࡢˮ��pHֵΪ2�����Ϊ2��1������������ȡ��1.5 mol.L-1����������������ȡ����������ȡ�ͷ���ȡ���������:�������̾�����ѧ����,���ۻ��Ϊ46.26kJ.mol-1,���ڻ�ѧ��Ӧ���ƹ���;���ܻ����ʴ�75%����;V2O5��Ʒ���ȴ���99%,����GB3283-1987����Ҫ��;ȫ���̼�����������,��ˮ��������ѭ��ʹ���ʴ�97%����,���������ڽ���,����������ᷰ���ա�
ϡ�н��� 2012,36(05),804-810
��� ���̿� �뽨�� ������ Ѧ���� ����
���������Ƽ���ѧұ��ѧԺ
������ɫ�����о�Ժ
��������ҵ�ɷ�����˾
��ʯú��̼����������ֵ�������Ϊ�о������á�����+����������,����Һ���ص�pHֵ����ԭ��������ȡ�ͷ���ȡ,����ȡҺ������������γ����ȡ�������ȡ���������������ղ���:����������С��37��m(100%)����������Ϊ50%������������Ϊ4%��Һ�̱�Ϊ2.5��1�������¶�Ϊ90�桢����ʱ��Ϊ7 h�������½���,��12.5%P204+5%TBP+82.5%�ǻ�ú��Ϊ�л��ࡢˮ��pHֵΪ2�����Ϊ2��1������������ȡ��1.5 mol.L-1����������������ȡ����������ȡ�ͷ���ȡ���������:�������̾�����ѧ����,���ۻ��Ϊ46.26kJ.mol-1,���ڻ�ѧ��Ӧ���ƹ���;���ܻ����ʴ�75%����;V2O5��Ʒ���ȴ���99%,����GB3283-1987����Ҫ��;ȫ���̼�����������,��ˮ��������ѭ��ʹ���ʴ�97%����,���������ڽ���,����������ᷰ���ա�
��ͼ����ţ� TF841.3
����飺���(1963-),��,ɽ��������,��ʿ�о���,������;�о�����:����ұ��(E-mail:zhujun_tiger@126.com);
�ո����ڣ�2012-03-14
��������ʡ�Ƽ��������ص���Ŀ(2011KTDZ01)����;
Abstract��
The stone coal removed carbon by roasting was taken and calorific values were used as the study object.Leaching by sulfuric acid+aid-leaching agent,extracting and anti-extracting after regulating pH and reduction treatment,anti-extraction liquid produced V2O5 after oxidation by acid ammonium salt precipitation of vanadium processes.The results demonstrated that vanadium total recovery rate was more than 75%,the purity of the V2O5 product was higher than 99%,in line with GB3283-1987 quality requirements,the whole process was almost no waste gas emission,recycling rate of waste water reached above 97% after treatment,the waster slag could be used for building materials,the process was a clean type of the vanadium extraction process.
Keyword��
stone coal; leaching; acid leaching kinetics; solvent extraction; V2O5;
Received�� 2012-03-14
ʯú���ں�̼��ҳ��, ���нṹ���ܡ� �ҷָߡ� �Ż����������͵��ص�, �ҹ�ʯúԶ��������2��108 t, Լ��ʮ��֮�ŷֲ�������������, ��Ʒλ�༯����0.1%��0.5%֮��
���, ����ǹ���Ӧ����Ϊ�㷺�� ������Ƶ�ʯú��ȡ������֮һ
1 ʵ ��
1.1 ���պ��ԭ�����ʷ���
�ۺ϶�Ԫ�ط�����(��1), �����������(��2)��X���������(��3)���������֪, ʯӢ�Ǵ����ϵ���Ҫ������ɳɷ�, ����ǷǾ���ṹ��� ����5.02%�ķ�������̬������̼������, ���ַ�����Ƕ̬���������ܵĹ��������С� ʯú���ᄃ����̼�������ƻ�, ���ַ��ӿ������ͷų���, ͬʱ, �ͼ۷��������ɸ۷�������, �����γ�һ�����Ŀ����Է�����, ����������νṹ�ȶ�, ������ͬ����ʽȡ��Al3+������������е�V(��)���ٲ��ֱ��ͷų�����
1.2 ʵ�鷽��
�ᷰ���հ���: ����+������������ ����+�������к͡� ��м��ԭ�� ��ȡ������ȡ�� ������������ ������γ����� ���յȲ��衣 �����ʡ� ��ȡ�ʺͳ����ʵļ�����ò�����, ��ʽ(1), ʽ(2)��ʽ(3)��ʾ��
��(������)
E(��ȡ��)
������
2 ���������
2.1 �� ��
���������ʷ�����֪, �����еķ�����������ʽ����, ���ȡһ����ǿ����ʩ�������� �������Ũ���������������DZ������ǿ���ֶΡ� Ϊ�˽�һ��ȷ����ѵĽ������ղ���, ������һ������֤����, ���ڶ���ѧ���۷����Ļ�����̽���˽�������ѧ�ķ�Ӧ�ٶȿ��Ʋ��衣
2.1.1 ��������ʵ��
ʵ������: ���ϸ�ĥ������ΪС��37 ��m(100%), ����������Ϊ4%(�����ϵ�������), Һ�̱�2.5��1, �����¶�90 ��, ����ʱ��7 h, �����ٶ�250 r��min-1, �ֱ�仯������������ ������������ ����ʱ��ͽ����¶�, �������ֱ��ͼ1��4��
��ͼ1��֪, ʯú�����մ�����, ����Ҫ�ϸ����������ſ���ʵ������Ľ����ʡ� ���������仯��35%ʱ, ���������Ӻܿ�, ��Ҫ�Ǹ۷�����������ܷ����α�����, 35%��50%ʱ, ���������ٷŻ�, �������������ƻ��������ζ��ܳ���, Ũ������, �����H+���뾧����û��������ӵĿ�����, �����ʳ����������ȶ��� ������Ũ�ȹ���, ���豸Ҫ���ϸ�, ��Һ�е�������Ũ������, �Ʊ�Ҫ���Ӻ����кʹ���ʱ�������ʵ�����,ͬʱ�д������������ܳ�, �����˺����븻������ѹ���� �ʱ�����ѡ��50%������������
��1 ��Ԫ�ط��� (%, ��������)
Table 1 Multi-element analysis (%, mass fraction)
| V2O5 | Al2O3 | TFe | CaO | K2O | SiO2 | MgO | S |
| 0.94 | 8.37 | 4.41 | 5.92 | 3.69 | 56.70 | 4.14 | 2.11 |
��2 ��������� (%)
Table 2 Vanadium phase analysis (%)
| Free oxide V2O5 | Aluminosilicate V2O5 | Carbonaceous V2O5 | Total |
| 0.21 | 0.68 | 0.047 | 0.937 |
| 22.41 | 72.57 | 5.02 | 100 |
��3 X����������� (%)
Table 3 XRD analysis (%)
| Components | Quartz | Hematite | Anhydrite | Apatite | Illite | Potassium feldspar | Amorphous phase | Other |
| Content | 55 | 5 | 7 | 2 | 8 | 7 | 15 | 1 |

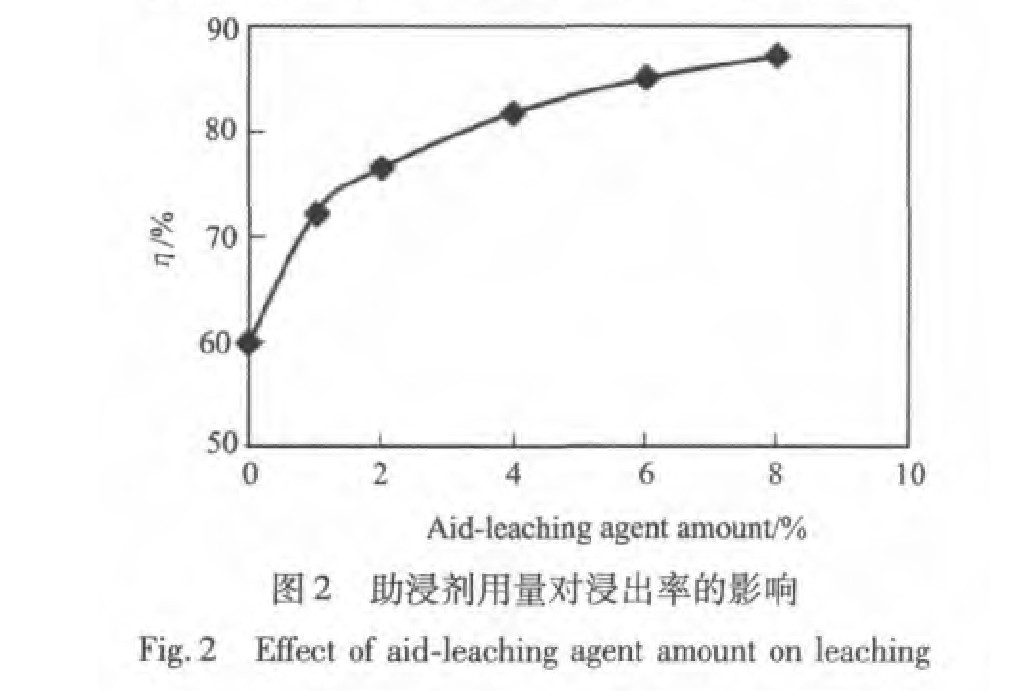

��ͼ2��֪, ����ʹ���������ʱ, �����ʽ�Ϊ60%, ��ʵ����������, �������ǻ���60%�� ����������������, ������������ߡ� �����������û���ͬ����һ��, �����ƻ����ᄃ��, ��������ھ����еķ�����������Ӵ����ʡ� ������Ũ�Ȳ���̫���������, ��������Һ��H+��Ũ��, ����������, ���������P�����Է��������������ַ�Ӧ, �����в��ֹ��������еķ�û���ͷų���, ����������������, �൱�������H+��Ũ��, �����˾����ƻ��Ŀ�����, ʹ���������ߡ� ���������۸�, �ۺϿ���, ������������Ϊ4%��
��ͼ3�ɼ�, 5��7 h, ��������������, 7 h�Ժ�, ������Ϊ84%, ���ȶ��� ��������������+��������ϵ��, 7 h�Ѵﵽ�˷��Ľ�����Ӧƽ��ʱ�䡣
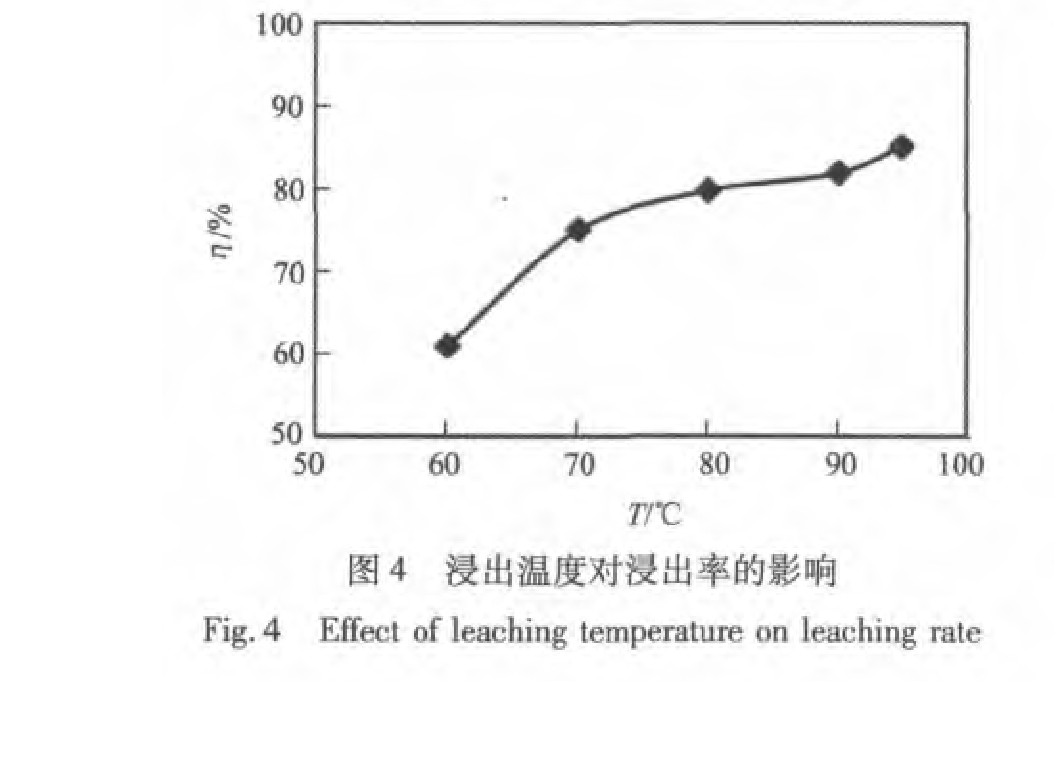
��ͼ4�ɼ�, ���¶ȵ�����, �����ʳ���������, �¶�Խ��, ��Ӧ�ٶ�Խ��, ���Ľ�����Ҳ��֮��ߡ� �ۺϽ�������ɱ��� �ܺġ� �豸�������������й�, ��ʵ����ƽ����¶�Ϊ90 �档
2.1.2 ��֤ʵ��
�������ʵ����, ѡ�������֤ʵ������: ��̼��������Ϊ-400Ŀ(100%), ��������Ϊ50%, ����������Ϊ4%, L��S=2.5��1, T=90 ��, t=7 h, r=250 r��min-1, ���������ۺ�ƽ������, �빤ҵ������50 L�´ɷ�Ӧ���н���, ��������ͬ��������, ������4��ʾ��
�ɱ�4��֪, �ۺ�ƽ��ʵ���з����ܽ������ȶ�, ƽ��ֵΪ82.90%, ��ƫ���Ϊ0.6, ˵��, �ڱ�ʵ�����ʵ�������½�������ᷰ����һ�����ظ��Լ�������; �빤ҵʵ���з����ܽ����ʻ����ȶ���84%����, ������֡� ��Ӧ�����ص�ԭ��, �빤ҵ�����ձ���ۺ������һ���ٷֵ�����, ͬʱҲ֤���˽��������ʺ��ڴ��౺�����ϵĴ�����
2.1.3 ��������ѧ����
���ݽ�������ѧ����ԭ����֪, ������Ӧ��Һ�̶��෴Ӧ, ���ϵ��͵ĺ�����ģ��; ����������Ҫ��Ϊ��ɢ�� ������ ��ѧ��Ӧ�ȼ�����, �䷴Ӧ���ʵĴ�С��Һ�ഫ�ʿ��ƹ��̡� ��Ĥ��ɢ���ƹ��̼���ѧ��Ӧ���ƹ������߾���; ���ٽ���������, ���Ժ���Һ�ഫ�ʹ��̶Խ�����Ӧ���ʵ�Ӱ��, ������ʵ���֤���˵�, �������������Թ��̵��жϿ��ɱ��ۻ��ȷ��, ��ɢ���̿���ʱ, ���ۻ��һ��С��12 kJ��mol-1, ��ѧ��Ӧ����ʱ, ���ۻ��һ�����42 kJ��mol-1
��4 ��֤ʵ���� (%)
Table 4 Results of verifying test (%)
| Groups | 1 | 2 | 3 | 4 | 5 | Average | Standard deviation |
| Total leaching rate of parallel tests | 81.91 | 84.04 | 82.98 | 83.05 | 82.53 | 82.90 | 0.60 |
| Total leaching rate of semi-industrial | 84.04 | 83.66 | 83.90 | 84.11 | 83.92 | 83.93 | 0.58 |
1-(1-��)1/3=kt (4)
ʽ��, kΪ���۷�Ӧ�ٶȳ�����
ͬʱ, ��һ������Ũ����(����������������ʵ��), ̽�ֲ�ͬ����ʱ�����¶ȶԽ����ʵ�Ӱ��, �����ͼ5, ����������1-(1-��)1/3��t��ͼ6�� ��T�����Ĺ�ϵ��1-(1-��)1/3��t�����ֱ�߹�ϵ(���ϵ��������0.90), �Խ�����Ӧ�������з���, ���ݻ������ϡ�������ģ�͡�, ��������������Ӧ���ӻ�ѧ��Ӧ���ƶ���ѧ���̡� Ϊ�˽�һ��ȷ��, ����Arrhennius����:
k=Ae-E/RT (5)
��ʽ(5)����ȡ�����õ�:
lnk=lnA-E/RT (6)
ʽ��, TΪ����ѧ�¶�, EΪ���ۻ��, RΪ���峣��, AΪ���鳣����
��ͼ5, 6��ʽ(4)���lnk, ����lnk��1/T��ͼ7�� ����
ͼ5 �Ǻͷ�Ӧʱ��Ĺ�ϵ
Fig.5 Relationship of �� and reaction time
ͼ6 1-(1-��)1/3�뷴Ӧʱ���ϵ
Fig.6 Relationship of 1-(1-��)1/3 and reaction time
(1)y=0.024x+0.301,R2=0.923;(2)y=0.022x+0.276,R2=0.947;(3)y=0.014x+0.306,R2=0.902;(4)y=0.009x+0.304,R2=0.942;(5)y=0.005x+0.232,R2=0.972
2.2 �� ��
�����۽��������������ļ۷����ӱ���ȡ, ����ȡǰ�辡���������۽������ӵĺ����� ����Һ���京�϶�����������, ����ǿ������ȡ�����������Ӽ���������ȡ, �ɲ�����; ������Һ�е���������������нϸߵĵ�ɼ���С�İ뾶�������뷰����, ����, ��ȡǰ�轫���������ӻ�ԭΪ����������ȡ�Ķ���������; ����Һ�еķ���Ҫ�Է�������(VO2+)��ʽ����, ���ױ���ȡ(��ʽ8), ��VO2+���������ϵ�, ��۷��뻹ԭΪ�ļ۷�
ͼ7 lnk��1/T��ϵ
Fig.7 Relationship of lnk and 1/T
nVO2++m[HA]2=(VO)nA2n[HA]2(m-n)+2nH+ (8)
ʽ��: HA����P204��
P204����ǿ���Ի�����(pH=2)����, ������ҺpHֵԶԶС��1, ���ñ���������ʯ�����кͻص�pHֵ, Ȼ�������м��ԭ���顣 ������, ����Һ��Fe3+��ռ������0.53%, VO2+�����dz��͡�
2.2.1 ��ȡ��������
��������: ˮ��pH=2, P204�������Ϊ12.5%(ռ�л��������), �л��������100 ml, ���Vo/Va=2/1, ��ʱ��3 min, ���÷ֲ�ʱ��2 min, ������ȡ, �����л�����TBP��������Է���ȡ�ʵ�Ӱ��, ��������ͼ8��ʾ��
��ͼ8��֪, TBP��P204��ȡ�ļ۷������Ե�Э������, ����ʹ��P204��ȡʱ, ����ֲ㻺��(1 min)���������������, ����TBP��, ��ȡ��������98.5%�������ȶ�, �ֲ�ʱ����ٵ� 30 s֮���������������, �ϲ���ɫ, �²�dz��ɫ�� ��ѡ��TBP�������5%, ���л������Ϊ12.5%P204(��ȡ��)+5%TBP(Э�ͼ�)+82.5%�ǻ�ú��(ϡ�ͼ�)��
����������, ������Һ��ʼpHֵ�Է���ȡ�ʼ�����ʧ�ʵ�Ӱ��, �����ͼ9, 10��
����ȡԭ����ʽ(8)������֪, �����Խ�������ȡ�������ӽ�������, ������ȡ���̵Ľ���, ���������ͷŵ���Һ��, ��ʹ��ҺpHֵ����[22]:
ͼ8 �л�����TBP��������Է���ȡ�ʵ�Ӱ��
Fig.8 Effect of organic phase TBP volume fraction on extraction of vanadium
lgD=lgK+mlg[HA]+2pH (9)
E=D/(D+Vo/Va) (10)
ʽ��: DΪ����ϵ��; KΪƽ�ⳣ��, EΪ��ȡ��, %��
����ͼ9��֪: ����ȡ����ˮ��pHֵ��������, pHֵ����2��, ����ȡ�������ȶ�, ��Ȼ, pH, D��E 3��֮������ȹ�ϵ�� ����, ��ͼ10��֪, ��pHֵ�����ͬʱ����ʧ��Ҳ������, pH=4, ����ʧ�ʸߴ�30%, ��ΪFe3+, Al3+, SiO
2.2.2 ����ȡ��������
����McCabe-Thiele��ͼ��, ��Vo/Va=4/1�� ����ȡ������Ũ��1.5 mol��L-1�� ��3 min�� �����л���V2O5����Ũ�Ȳ�ͬ�����»��Ʒ���ȡ������(ͼ11)�� ��3����������ȡ��,����ȡҺ�з�Ũ�ȴﵽ12.72 g��L-1, ƶ�л����з�Ũ��С��0.51 g��L-1, ����ȡ�ʴ���96%��


ͼ11 ����ȡ������
Fig.11 Stripping isotherm of vanadium
2.3 ����������
��������: NaClO3������Ϊ��Һ��V2O5���ʵ�����0.45��, ����������ԭ��λΪ800��1000 mV, 65 ��������1.5 h����, ��Һ������ɫ��Ϊ���ɫ; ����15%��ˮ�ص�pH=2.0, ������ 95 ��, ����2 h, ����0.5 h; ��2���ڳ���ĸҺ��ȥ����ˮϴ�Ӻ��3��, 525 ��������2 h, ��Ʒ�ɷּ���5�� ��Ҫ��Ӧʽ����:
3V2O2(SO4)2+NaClO3+3H2O=
3(VO3)2SO4+NaCl+3H2SO4 (11)
6(VO2)2SO4+(NH4)2SO4+(7+n)H2O=
(NH4)2V12��O31��nH2O��+7H2SO4 (12)
(NH4)2V12��O31��nH2O=6V2O5+2NH3��+H2O�� (13)
��5 ��Ʒ�и��ɷֵĺ��� (%, ��������)
Table 3 Composition of product (%, mass fraction)
| Composition | V2O5 | Si | Fe | P | S | As | Na2O+ K2O |
| Product | 99.12 | 0.02 | 0.22 | 0.046 | - | 0.0088 | 0.325 |
| GB3283-87 | ��98.00 | ��0.25 | ��0.30 | ��0.05 | ��0.03 | ��0.02 | ��1.50 |
����ĸҺ�������, ϴ��ˮ���ô��ѷ����հ���, ��Һ����������������Һ��ѭ��ʹ��, �ʳ����η���ʧ�ʿɺ��Բ���, �������պ����������3��ϴ��Һ��Ӧ, �����������Һ��
3 �� ��
1. ������+�������������ᷰ���������ڴ�������, �����ʸ���82%, �������鼰����ѧ����, ȷ����ѧ��Ӧ����Ϊ������Ӧ���̵���Ҫ���Ʋ��衣
2. ����Һ�����ص�pHֵ����м��ԭ������, ��3��������ȡ, V2O5��ȡ�ʴ���99.0%, ��Ũ��Ϊ1.5 mol��L-1��������Һ���з���ȡ, ��3����������ȡ, V2O5����ȡ�ʴ���97.0%, �������ø÷���������Ч������, ��������γ�����, ���ò�Ʒ��V2O5������������98%, ����GB3283-1987����Ҫ��
3. �������������������Ͽ�ȫ����������, ��Һѭ��ʹ�û���������, ѭ��ʹ���ʴﵽ97%����, ����������������ڽ��ġ� ��·�ȷ���, ����ȷ�������������ڴӴ����������ᷰ, ���ڻ���������ա�
�����

