光化学还原过程中纳米TiO2表面Hg(Ⅱ)的吸附与脱附
司士辉1, 杨政鹏1, 刘 波2
(1. 中南大学 化学化工学院, 长沙 410083;
2. 深圳大学 应用化学系, 深圳 518060)
摘 要: 采用石英晶体微天平现场技术研究了Hg(Ⅱ)离子在纳米TiO2表面的吸附及光化学还原过程。 结果表明: Hg(Ⅱ)离子借助于纳米TiO2表面羟基发生吸附, 吸附平衡常数约为3.9×105L/mol, 且 Hg(Ⅱ)离子的吸附量受溶液的pH值、 浓度和共存阴离子的影响; 在pH值为4的HgCl2溶液中, Hg(Ⅱ)离子在纳米TiO2上的饱和吸附量约为0.85mmol/g; 在UV光照射下, 初始阶段TiO2表面水光解产生的质子可使吸附的 Hg(Ⅱ)离子从TiO2表面脱附下来, 而且Hg(Ⅱ)浓度和pH值越大, 脱附现象越明显; 随后Hg(Ⅱ)光还原沉积逐渐占主导地位, 且光沉积速率受Hg(Ⅱ)浓度、 溶液pH值和有机物加入的影响。
关键词: 纳米TiO2; 吸附; 光化学还原; 石英晶体微天平 中图分类号: O614.24+3
文献标识码: A
Adsorption and desorption of Hg(Ⅱ) at surface of nanocrystalline TiO2 during photochemical reduction process
SI Shi-hui1, YANG Zheng-peng1, LIU Bo2
(1. School of Chemistry and Chemical Engineering,Central South University, Changsha 410083, China;
2. Department of Applied Chemistry, Shenzhen University, Shenzhen 518060, China)
Abstract: In-situ technique of quartz crystal microbalance (QCM) was used to investigate the adsorption and the photochemical reduction process of Hg(Ⅱ) at the surface of nanocrystalline TiO2. The results show the Hg(Ⅱ) is adsorbed onto the surface of nanocrystalline TiO2 by hydroxyl groups, and the adsorption equilibrium constant is about 3.9×105L/mol based on the pseudo-first-order kinetic model. The adsorption amount of Hg(Ⅱ) at the surface of TiO2 is affected by pH value, concentration of Hg(Ⅱ) and coexisting anions, and the saturated adsorption amount of Hg(Ⅱ) is approximately 0.85mmol/g at pH of 4. During the initial stage of UV illumination, the protons produced in photodegradative reactions of water can cause the desorption of adsorbed Hg(Ⅱ) from the surface of TiO2 . The degree of desorption increases with the increase of both the concentration of Hg(Ⅱ) and pH value of solution. Then, the photochemical deposit reaction of Hg from the solution strengths and the rate of Hg photodeposition are influenced by the concentration of Hg(Ⅱ), pH value and added organics.
Key words: nano titanium dioxide; adsorption; photoreduction; quartz crystal microbalance
环境中Hg浓度高于5×10-9时对人畜有很强的毒害性, 特别是有机汞类化合物比无机汞类化合物毒性更大, 例如CH3Hg+对中枢神经有致命的影响[1] 。 汞类化合物无法直接进行化学或生物降解, 目前常见除去废水中汞的方法有活性炭吸附法[2], 离子交换法[3]和沉淀法[4]等。 然而这些方法需要耗费能量或消耗大量的化学物质。 近年来的研究表明, 采用纳米半导体光催化剂如TiO2光化学, 消除环境污染物是一种十分有效地净化技术。 纳米TiO2在光照下, 分别在导带和价带产生激发态电子和空穴, 它们能够在半导体或内表面上引发各种氧化还原反应[5-8]。
物质在金属氧化物表面的吸附机制通常涉及到路易斯酸碱反应或自由基作用的氧化还原反应[9]。 最近的光电化学技术、 FTIR和质谱等方法已用来研究有机物在纳米TiO2表面的吸附行为[10,11]。 纳米TiO2光催化还原清除重金属离子的研究已有报道[12], 但重金属离子光催化沉积机制及其影响因素有待进一步研究。
[BJ(,,,][BJ)] 第15卷第9期 司士辉, 等: 光化学还原过程中纳米TiO2表面Hg(Ⅱ)的吸附与脱附 石英晶体微天平(QCM)是一种灵敏的质量传感器, 可以现场监测发生在电极表面的微小质量变化, 例如单层和多层的沉积/溶解, 修饰层的物质迁移以及吸附动力学等[13]。 该技术也已用于监测半导体电极/溶液界面的光诱导物质迁移过程[14-16]。 本文作者借助石英晶体微天平技术研究了纳米TiO2表面上Hg(Ⅱ)的吸附及光还原沉积过程。
1 实验
1.1 试剂与仪器
锐钛矿型纳米TiO2(粒径为25nm)溶胶, 其它试剂均为分析纯。 高纯水用于清洗和配制所有溶液。 石英晶体微天平设备(自制)及Protek C3100可编程通用计数器。
1.2 纳米TiO2膜的制备
石英晶体的金电极用2mol/L NaOH溶液处理20min, 然后用水清洗。 将电极水平固定好, 用旋转涂膜法制备纳米TiO2膜, 根据TiO2膜修饰前后测得的石英晶体(AT切, 9MHz)的频率变化可估测石英晶体上沉积的TiO2膜厚约为0.6μm, 制备的TiO2膜在300℃下烘烤1h以增加膜的稳定性。
1.3 QCM测定
修饰有TiO2膜的石英晶体单面触液, 两个电极导线连接到IC-TTL振荡器上。 整个检测设备放置在金属箱中以避免周围的电磁干扰。 可编程通用计数器监测频率, 记录的数据储存于计算机中。 空调控制室温于20℃, 在黑暗中进行Hg(Ⅱ)的吸附实验。 修饰有TiO2膜的压电石英晶体在空白溶液中待频率稳定后, 于2s内注入一定体积的HgCl2溶液, 并记录整个过程的频率变化。
在纳米TiO2半导体光化学实验中, UV光通过检测池的一个石英窗口照射到TiO2膜, 监测整个过程的QCM频率信号。 用HNO3(0.1mol/L)和NaOH(0.1mol/L)调节溶液的pH值。
2 结果和讨论
2.1 Hg(Ⅱ)在纳米TiO2上的吸附行为
物质在纳米半导体光催化剂TiO2表面的光化学机制与其在纳米粒表面的吸附行为有关, 物质的吸附形式(物理吸附或化学吸附)及强弱程度对其光反应路径和速率有很大影响[17]。 本文作者借助QCM现场技术探讨了在纳米TiO2膜上Hg(Ⅱ)的吸附行为。
2.1.1 吸附动力学过程
图1所示为pH=4的溶液加入检测池后QCM的频率变化。 从图1可看出, HgCl2 在Au电极上及KCl在TiO2表面没有吸附发生, 但HgCl2在TiO2膜电极上有明显的吸附且达到吸附平衡需要一个较长过程。 由于TiO2表面存在大量―OH基团, 该吸附现象的实质是TiO2的羟基与Hg(Ⅱ)发生配位作用, 其反应式为
>Ti―OH+Hg2+→>Ti―OH…Hg2+(1)
其吸附平衡常数可由下述方法估算。 对于物质在电极表面上的吸附过程, 溶液中吸附物质的浓度可假定不变, 吸附反应可用准一级动力学模型来描述[18]:

根据反应速率的定义, 可将该反应的动力学方程描述如下:
d[MP]/dt=k1[M][P]-k2[MP](3)
式中 k1和k2分别为缔合常数和离解常数。 由于QCM的频率变化值Δf(Δf=f0-f)与[MP]成比例, Δfm-Δf(Δfm为频率变化最大值)与[M]成比例, 式(3)可改写为
d(Δf)/dt=k1c(Δfm-Δf)-k2(Δf)(4)
即:
d(Δf)/dt=-(k1c+k2)(Δf)+k1c(Δfm)(5)
式中 c为溶液中Hg(Ⅱ)的浓度(吸附过程中变化较小, 可认为是一常数)。 以d(Δf)/dt对Δf作图(对应于图1的曲线c)得到一条直线(见图2), 由其斜率(l=-k1c-k2)和截距(d=k1cΔfm)可求得动力学常数k1和k2, 进而求得反应式(1)的吸附平衡常数K。
K=k1/k2(6)
计算求得的吸附平衡常数为3.9×105L/mol。

图1 溶液加入检测池后QCM的频率变化
Fig.1 Frequency changes of QCM after solution added to detector cell
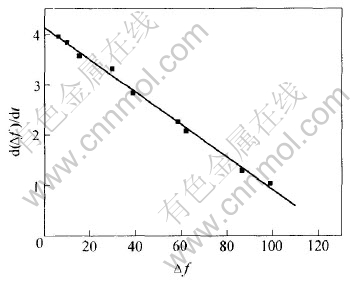
图2 d(Δf)/dt与Δf关系图
Fig.2 Plot of d(Δf)/dt vs Δf corresponding to curve c in Fig.1
2.1.2 pH值、 浓度及共存阴离子对Hg(Ⅱ) 在纳米TiO2上吸附的影响
由于TiO2膜在pH值较低时不稳定, 而在pH值较高时, Hg(Ⅱ)易沉淀, 本文作者用QCM测定了pH为1~6时Hg(Ⅱ)的吸附量(见图3)。 在pH值较低时, Hg(Ⅱ)的吸附量较小; 随着pH值增大, Hg(Ⅱ)的吸附量也随之增大。 此外, 当pH值一定时, 吸附量随HgCl2浓度的增大而增大。 TiO2的表面电荷随溶液pH改变而变化, pH值下降可减少表面负电荷增加正电荷, 就锐钛矿型TiO2而言, 等电荷点的pH值(pHzpc)大约为5 [19]。 当溶液pH值低于pHzpc时, TiO2表面吸附活性点的羟基会与质子发生反应:
>Ti-OH+H+→>Ti-OH+2(7)
因此, 表面的质子化与去质子化平衡影响了Hg(Ⅱ)在TiO2表面的吸附行为。
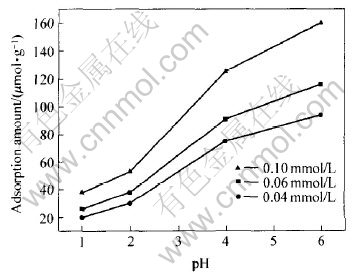
图3 pH值对Hg(Ⅱ)吸附的影响
Fig.3 Effect of pH value on amount of adsorbed Hg(Ⅱ)
共存阴离子对Hg(Ⅱ)的吸附影响如表1所列。 从表中可看出, NO-3和SO2-4共存时QCM的频率均有所下降(表面质量增加), 且SO2-4的下降幅度较大。 其原因可能来自两个方面: 1) NO-3 和SO2-4直接吸附于电极表面; 2) NO-3和SO2-4聚集于电极表面, 减少了电极表面的正电荷, 增加了负电荷, 从而使Hg(Ⅱ)在电极表面的吸附量增加, 结果导致QCM频率下降。 Cl-和SCN-共存时, QCM的频率则均有较大幅度的上升, 且SCN-的上升幅度大于Cl-的, 由于Cl-和SCN-分别与Hg(Ⅱ)发生配位作用所致。
Hg2++Cl--HgCl+ k1=5.5×106
Hg2++2Cl--HgCl2 k2=1.7×1013
Hg2++3Cl--HgCl-3 k3=1.2×1014
Hg2++4Cl--HgCl2-4 k4=1.2×1015
Hg2++2SCN--Hg(SCN)2
k′2=3.0×1017
Hg2++4SCN--Hg(SCN)2-4
k′4=2.1×1021
生成稳定的配合物, 使一部分Hg(Ⅱ)从纳米TiO2表面脱附下来, 即TiO2表面上Hg(Ⅱ)的吸附量减少, 因而QCM的频率上升。 由于Hg(Ⅱ)与SCN-的稳定常数明显高于Cl-的稳定常数, 因而SCN-更易使吸附的Hg(Ⅱ)从纳米TiO2表面脱附下来, 从而使得频率上升幅度更大。
表1 阴离子对Hg(Ⅱ)吸附的影响
Table 1 Effect of anions on adsorption of Hg(Ⅱ)*

2.2 纳米TiO2光化学过程中吸附Hg(Ⅱ)的脱附
2.2.1 光化学过程中纳米TiO2膜质量的变化
在UV光下, TiO2受到激发产生了光生电子和正穴[12]:
TiO2+hv→h+vb+e-cb(8)
2H2O+4h+vb→O2+4H+(9)
Hg(Ⅱ)随后可发生下述光化学还原反应:
Hg2+ads+e-cb→Hg+ads(10)
Hg+ads+e-cb→Hg0surf(11)
图4所示为不同浓度HgCl2溶液UV光照下覆盖TiO2膜的QCM频率变化。 图5所示为UV光照下覆盖TiO2膜不同pH值溶液的QCM频率变化。 由图4和5可见, 在UV光照的初始阶段, QCM的频率均有所上升, 然后随时间逐渐下降。 但在KCl溶液中未观察到该现象, 表明UV光的温度效应或TiO2表面其它性质变化很小, 不会导致QCM产生频率响应, 频率的变化主要反映了膜表面质量的变化。 UV光照初始阶段QCM的频率上升表明吸附的Hg(Ⅱ)发生了脱附。 这是由于在UV光照下纳米TiO2表面光化学氧化反应主要是水分子发生了光化学氧化, 该过程产生质子, 进而置换了吸附在纳米TiO2上的Hg(Ⅱ), 其反应为
>Ti-OH…Hg2++H+→ Hg2++>Ti-OH+2(13)
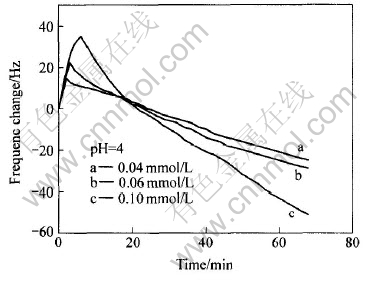
图4 不同浓度HgCl2溶液中UV光照下覆盖TiO2膜的QCM频率变化
Fig.4 Frequency changes of QCM for different concentrations of HgCl2 solution with TiO2 films during UV illumination

图5 不同pH值溶液中UV光照下覆盖有TiO2膜QCM频率变化
Fig.5 Frequency change of QCM for HgCl2 solution at different initial pH values with TiO2 films during UV illumination
结果使TiO2上的Hg(Ⅱ)吸附量减小, 频率上升。 随后, 由于Hg(Ⅱ)的光还原沉积占主导地位, 电极表面质量增加, 频率又下降。
2.2.2 浓度、 pH值和有机物对Hg(Ⅱ)光还原沉积速率的影响
从图4和5中还可看出, 在光照初始阶段, Hg(Ⅱ)浓度和pH值越大, 频率上升幅度就越大, 且时间延续得越长。 这是由于Hg(Ⅱ)浓度和pH值较大时, Hg(Ⅱ)在纳米TiO2上的吸附量较大, 有利于与光解产生的质子进行置换, 结果使得较多的Hg(Ⅱ)从纳米TiO2表面脱附下来, 因而QCM频率上升的幅度较大, 延续的时间较长。 随后QCM频率的下降表明, Hg(Ⅱ)在TiO2电极上光还原沉积为主要反应过程。 Hg(Ⅱ)浓度和pH越大, 曲线下降越快; 相反, Hg(Ⅱ)浓度和pH越小, 曲线则下降较平缓。 这说明浓度和pH越大越有利于Hg(Ⅱ)的光还原沉积, 这是由于Hg(Ⅱ)浓度大时, 单位时间内扩散到电极表面的Hg(Ⅱ)量较大, 使得Hg(Ⅱ)的还原速率相对较大, 因而频率下降越快所致。 而pH较大时, 纳米TiO2上Hg(Ⅱ)的吸附量较大, 有利于与光电子发生还原反应, 使得Hg(Ⅱ)的光还原沉积速率较大。
有机物对Hg(Ⅱ)光还原有很大影响, 其结果如表2所列。 从表2中可看出, 在0.08mmol/L HgCl2溶液(pH=4)中加入有机物(8mmol/L)后于UV光照下反应35min, Hg(Ⅱ) 光还原沉积量明显增大, 且有机物还原性越强, Hg(Ⅱ)光还原沉积量越大。 由于半导体光生正穴氧化有机物后减小了与电子再复合几率, 因而产生了较多的光生电子, 有利于Hg(Ⅱ)的还原。
表2 有机物对Hg(Ⅱ)光还原的影响
Table 2 Effect of different organism on photo-reduction of Hg(Ⅱ)*

3 结论
1) Hg(Ⅱ)离子在纳米TiO2表面的吸附动力学过程可用准一级方程描述, 吸附平衡常数约为3.9×105L/mol, 且 Hg(Ⅱ)离子的吸附量受溶液的pH值、 浓度和共存阴离子的影响。
2) UV光照下, 初始阶段TiO2表面水光解产生的质子可使吸附的 Hg(Ⅱ)离子从TiO2表面脱附下来, 且Hg(Ⅱ)浓度和pH越大, 脱附现象越明显。 随后Hg(Ⅱ)光还原沉积逐渐占主导地位, 且光沉积速率受Hg(Ⅱ)浓度、 溶液pH和加入有机物的影响。
REFERENCES
[1]Litter M I. Heterogeneous photocatalysis:transition metal ions in photocatalytic systems[J]. Appl Catal B, 1999, 23(2): 89-114.
[2]Namasivayam C, Periasamy K. Bicarbonate-treated peanut hull carbon for mercury(Ⅱ) removal from aqueous solution[J]. Water Res, 1993, 27(11): 1663-1668.
[3]Osteen A B, Bibler J. Treatment of radioactive laboratory waste for mercury removal[J]. Water Air Soil Pollut, 1991, 56(1): 63-74.
[4]Ghazy S E. Removal of cadmium, lead, mercury, tin, antimony, and arsenic from prinking and seawaters by colloid precipitate flotation[J]. Sep Sci Technol, 1995, 30(3): 933-947.
[5]Fox M A, Dulay M T. Heterogeneous photocatalysis[J]. Chem Rev, 1993, 93(1): 341-357.
[6]Linsebigler A L, Lu G, Yates J T. Photocatalysis on TiO2 surface: principles mechanisms and selected results[J]. Chem Rev, 1995, 95(3): 735-758.
[7]MA Shu-zhen, LIAO Fu-hui, XU Ming-yuan, et al. Effect of microstructure, grain size, and rare earth doping on the electrorheological performance of nanosized particle materials[J]. J Mater Chem, 2003, 13(12): 3096-3102.
[8]阎建辉, 黄可龙, 司士辉, 等. 单分散纳米TiO2光催化剂的水解-凝胶制备法[J]. 中国有色金属学报, 2003, 13(3): 788-792.
YAN Jian-hui, HUANG Ke-long, SI Shi-hui, et al. Preparation of photocatalytic activity nanosized TiO2 by hydrolysis-sol method[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(3): 788-792.
[9]Calatayud M, Markovits A, Menetrey M, et al. Adsorption on perfect and reduced surfaces of metal oxi-des[J]. Catalysis Today, 2003, 85(2): 125-143.
[10]Raskó J, Kecskés T, Kiss J. Adsorption and reaction of formaldehyde on TiO2-supported Rh catalysts studied by FTIR and mass spectrometry[J]. J of Catalysis, 2004, 226(1): 183-191.
[11]JIANG Dian-lu, ZHAO Hui-jun, ZHANG Shan-qing, et al. Photoelectrochemical measurement of phthalic acid adsorption on porous TiO2 film electrodes[J]. J of Photochemistry and Photobiology A: Chemistry , 2003, 156(3): 201-206.
[12]Wang X L, Pehkonen S O, Ajayk K, et al. Photocatalytic reduction of Hg(Ⅱ) on two commercial TiO2 catalysis[J]. Electrochimica Acta, 2004, 49(9): 1435-1444.
[13]Butty D A, Ward M D. Measurement of interfacial processes at electrode surfaces with the electrochemical quartz crystal microbalance[J]. Chem Rev, 92(6): 1355-1379.
[14]Lyon L A, Hupp J T. Energetics of semiconductor electrode/solution interfaces: EQCM evidence for charge-compensating cation adsorption and intercalation during accumulation layer formation in the titanium dioxide/aletonitrice system[J]. J Phys Chem, 1995, 99(43): 15718-15720.
[15]Lemon B I, Hupp J T. Photochemical quartz crystal microbalance study of the nanocrystalline titanium dioxide semiconductor electrode/water interface: simultaneous photoaccumulation of electrons and protons[J]. J Phys Chem, 1996, 100(35): 14578-14580.
[16]Myung N, Wei C, Tacconi N R, et al. Photoelectrochemical quartz crystal microgravimetry. Development and use as an in-situ photoelectrode corrosion and stabilization probe[J]. J Electroanal Chem, 1993, 359(2): 307-313.
[17]Hug S J, Sulzberger B. In situ fourier transform infrared spectroscopic evidence for the formation of several different surface complexes of oxalate on TiO2 in the aqueous phase[J]. Langmuir, 1994, 10(10): 3587-3597.
[18]SI Shi-hui, FUNG Ying-sing, SI Li, et al. Study of adsorption behavior of bilirubin on human-albumin monolayer using piezoelectric crystal[J]. J of Colloid and Interface Science, 2002, 253(1): 47-52.
[19]Oliva F Y, Avalle L B, Cámara O R, et al. Adsorption of human serum albumin (HSA) onto colloidal TiO2 particles, Part Ⅰ[J]. J of Colloid and Interface Science, 2003, 261(2): 299-311.
(编辑李艳红)
基金项目: 国家高技术研究发展计划资助项目(2001AA218041); 国家自然科学基金资助项目(20475065)
收稿日期: 2005-03-04; 修订日期: 2005-06-10
作者简介: 司士辉(1967-), 男, 教授, 博士.
通讯作者: 司士辉, 电话: 0731-8836993; E-mail: sishihui@mail.csu.edu.cn