���±��: 1004-0609(2006)10-1806-06
������������������Ӽ������ü��������
������1, ������2, ������3
(1. ͭ��ѧԺ ����, ͭ�� 244000; 2. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ, ��ɳ 410083;
3. ���ϴ�ѧ ��Ϣ��ѧ�빤��ѧԺ, ��ɳ 410083)
ժ Ҫ: �о���������������������ᡢ ���� ��ʪ����Ӱ��������, ���������������������Ӽ�����ص��·����� �������: ͨ����������λ������ؿɵó��ڲ�ͬ�������ʱ, ���Ӽ�������Ŀ���, �Ӷ��ڸ����������������������������������������, ʹ������������ȶ������5%, ƽ������Ч�����1%��
�ؼ���: �����; ���Ӽ�; ��������λ; ���
��ͼ�����: TF1; TP205 ���ױ�ʶ��: A
Role of additive in nickel electrolysis cathodic process and its on-line control
GAO Tian-xing, LI Shi-xiong, LIU Ai-xin
(1. Department of educational Administration, Tonglin Academy, Tonglin 244009, China;
2. School of Metallurgical Science and Engineering, Central South University,
Changsha 410083, China;
3. School of Information Science and Engineering, Central South University,
Changsha 410083, China)
Abstract: The influence and effect of boracic acid, glue and wetting agent during nickel electrolysis cathodic process were studied and the method of on-line control in nickel electrolysis cathodic process was also put forward. The results show that through on-line control of cathodic overpotential, the optimum amount of additives can be determined under different electrolysis conditions and separated quality, and glabrous of cathodic nickel can be raised efficiently in complicated nickel electrolysis. This enhances the stability of zero-sized nickel production by 5% and average current efficiency by 1%.
Key words: nickel electrolysis; additives; cathodic overpotential; control
�ڲ�ͬ������������͵����ܶ���, ���ҺӦ��ȡ��ͬ��pHֵ�� һ�������, pHֵ��, ��������������, �׳�����; pHֵ����, �����������ӷ���ˮ��, Ӱ���������[1]�� Ϊ��, �����ڵ��Һ����Ϊ����������ֵ��ҺpHֵ���ȶ�, ��ֹ������ˮ�⡣ ����, ����Ĵ��ڻ����Լ�������������Ĵ���, ʹ���������ƽ���⻬�� ��������������泤����ʱ, ��ͨ��������ʪ�������ơ� �����������������ӻ�צ��, ��̴�������Ĥ, ���������������·, Ӱ���Ʒ����, �����ܺ�ʱ, ��ͨ���ӽ������ơ�
������������������, ���Һ�ɷ֡� ��ҺpHֵ�� ���ӵ���ɢ�� ʼ��Ƭ������ ���Һ���¶ȡ� ���������ܶȵȵ�����������������ߵ����������������Ҫ���ء� ����Щ��������ȶ��������仯ʱ, Ҫ������������ؼ�ȡ�������Ӽ��Ե��Һ����������ء�
Ŀǰ����ⶼ�Ǹ��������������״���˹��ж����Ӽ��ļ�����, �ⲻ�����ͺ����, ���ҵ������IJ�����, �����ij���������ǰ�����������3g/dm3����, ��������4~6g/dm3, ����[2]��H2BO3�ļ�������Ϊ5~20g/dm3, �����ǵ����Һ�ɷֲ����� �����ܶȸı䡢 ���Һ�¶Ȳ��ȡ� ���Ӽ������б�ʱ, ���Ӽ��Ŀ��ƿ��˹����ڸ��������ա� ���, �б�Ҫ�о���������������и������Ӽ��֮���������ϵ, �Լ�����������ϵ�Ե����ᾧ�ȵ绯ѧ����֮������ϵ, �����������ϵ��Ѱ��һ�����߿������Ӽ����·�������װ�á�
1 ʵ��
1.1 Ni-H2Oϵ��λpHͼ�ⶨ
Ni-H2Oϵ��λpHͼ�ⶨ[3, 4]װ���ɴ����������� ��ȼ�pHS-2�͡� �����λ��ơ� ����ء� ������ ���缫�� �ʹ��缫�������缫����ɡ� �̶��¶�25��, �ⶨ��ͬ����Ũ������Һ��pHֵ�� ��λֵ, ����������ֲ���Ni-H2Oϵ��λ��pH���ߡ�
1.2 ��̬�������߲ⶨ
��̬���������ö���λ���ⶨ[5]�� ʵ��װ���ɺ��λ�� XFD-8�ͳ���Ƶ�źŷ������� X-Y������¼�Ǽ�UJ-1�͵�λ�����ɡ� ʵ��ʹ�þ���ɰо��Ĥ��H�Ͳ�������, �о��缫Ϊֱ��2.6mm������, ��A-B������ڲ������ж���, ��Ķ���Ϊ�о��缫�Ĺ�����, ɨ���ٶ�Ϊ9.0mV/min, �����缫Ϊ���������Ƭ, �αȵ缫Ϊ���ʹ��缫;���ط����ڳ������²����Զ�����ʵ���¶ȡ�
1.3 �����
�����[6]���������������, ����ʼ��Ƭ������, ��������-�Ȼ�����Һ�����Һ, ����������Һ�����Ĥ�ڵ�������, ��55�桢 200A/m2�ĵ����������������������ϳ���, �����Ҹ߳�������Һ��20~30mm, �Է��������ܽ��������������Ⱦ����, ���������ܽ����������Һ����������
2 ���������
2.1 ��������������г��õ����Ӽ�
2.1.1 ����
1) Ni-H2Oϵ��λ��pH����
25����Ni-H2Oϵ��λ��pH������ͼ1��ʾ�� ͼ��ͬʱ������˹���ƽ�����Һ������Ũ�ȷֱ�Ϊ1�� 10-2�� 10-4��10-6mol/dm3ʱ��4���λ��pH�ߡ�
��ͼ1��֪, ���ߣj���ߢ��ཻ��pHֵ����, H+��������Ni2+�������ϻ�ԭ�ŵ�, �����
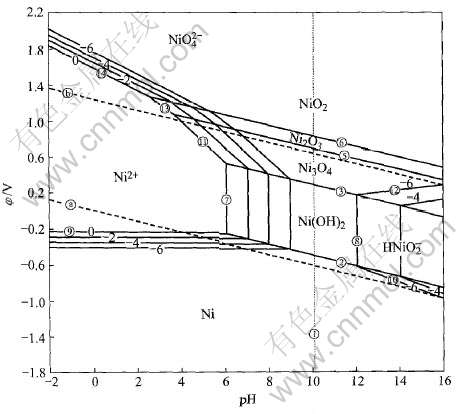
ͼ1 25��ʱNi-H2Oϵ��λ��pH����
Fig.1 Potential��pH curves of Ni-H2O system at 25��
ҺpH�������ߣj���ߢ��ཻ��pHֵ����, ��(H+/ H2)����������, Ni2+��������H+������ ������ҺpH���߽������Ni(OH)2����, Ҳ���ܵõ����ܶȺϸ���������� ͼ1�е�����Ϊ��ͬNi2+Ũ�ȵĶ���, ��ֵ��С, Ni2+ˮ���pH����; Ϊ��ʹNi2+������H+��ʼ����, Ҫ����ҺpH���ߡ� ��ҵ������Ϊ�˽����һì��, ����H3BO3�������, �Կ����ʵ���pHֵ��
2) ��������û���
H3BO3����Һ��ֻ�����H+��BO3-3��������, ������Һ��pHֵ�½�(���������)ʱ, ������H+�ͷ������з�Ӧ: 3H++BO3-3[FY]H3BO3, �Ӷ���������Һ��H+Ũ��, ʹpHֵ������ά��ԭ����ֵ����; �����Һ��pHֵ������(����Ƚ���)ʱ, ��������·�Ӧ: H3BO3[FY]3H++BO3-3, H++OH-[FY]H2O, �Ӷ�������OH-Ũ��, ʹpHֵ�����ܱ��ֲ��䡣
�ڹ�ҵ����������, ͨ����������Һ��pHֵ�ɱ�֤Ni2+����H+�������ϻ�ԭ, �������ܱ�֤H+�������ϲ���ԭ, ��Ϊ�������һ���ĵ����ܶ�(��180~250A/m2)�½��С� �������ڼ���, ������������������ʵ�ʵ�λ��Ni2+��ƽ���λҪ��һЩ, ���յ���H+�������ķŵ��������ӡ� ����H+������������������NiHȻ�����, ����NiH��NiH���ϲ���H2�Ĺ����ǽ����ѵIJ���, �����������������NiH�Ļ��ۡ�
�������¶�Ϊ65��, �����ܶ�Ϊ200A/m2, ��Һ���ΪNiSO4180g/dm3�� NiCl2 69g/dm3�� H3BO3 5g/dm3�� pH 2.0�������Ƶõ�������, ����900�������������, ��ò�ͬ��ȵ���������H2�������ڱ�1��
��1 ��ͬ�����������H2�ĺ���
Table 1 Content of H2 in cathodic nickel with different thicknesses

NiH�����ɼ�����, ������������������Ӧ��; ���Һ�е��л����ܽ��͵��Һ�������������ʪ��, ʹ���������������ɵ����������������������, �������������������, ��Ӧ������������ʱ��������������, ������������������Ч�ʡ�
ͼ2��ʾΪ�������IJ��ּ������ߡ� ��ͼ��֪, ������1�ﵽ�������, ����Ũ�����Ӱ��, ����1�ĵ������λ�ĸ���Ѹ�ٽ���, ������һ���̶���һ���ĸ���λ�µ�������, ������ĵ���������H+�ŵ�����ġ� ����3Ϊ��KCl��Һ, һ��ʼ��û�н������������ĵ���, ������1��������ʱ, ����3�����㼸��ͬ������, ˵����ΪH+�ŵ����¡� ����, ����������, ���������H+�ŵ�ʹ��������H+ƶ��, ��ʹpH����, ��֮�����˴������3NiSO4��4Ni(OH)2���������コ������, ��������������, ���������������ɡ�
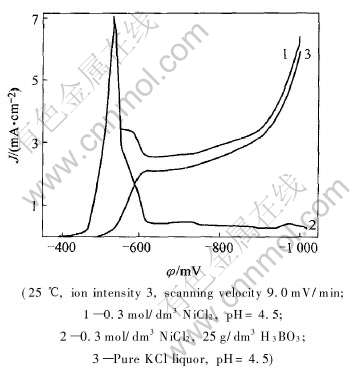
ͼ2 ���������ּ�������
Fig.2 Part of polarized curves of nickel cathodic
����2����Һ��������, ����������������ŵ������������������, ������zH3BO3��Ni(OH)2�Ľ�������, �������Ӵ�������, ���ױ�����������, �Ӷ��������������������ᄃ�峤����к�����, ����, ���ỹ����ʹH+�ŵ�Ĺ���λ����, H+�ŵ��λԽ��, H2��������, ��H+�ŵ��������, ��ͼ2����2�ĵ�����ʾ�� �ھ����������, ���������谭�������, ����2�ĵ�������û�л���, �����Ա����½������ơ� ����, ���������˵, �������һ���̶��ϼ����������Ĵ���, ʹ���������ƽ���⻬��
2.1.2 ��
1) �ý����Ƶ������������
���ʵ��֤��, �ڵ��Һ�����ӽ���������Ni2+�������ĵ���������Ϸŵ�, ��ֹ���ɴִ����ӡ� ���Һ�к���50~100mg/dm3������ʱ, ֻҪ�ڵ��Һ������40mg/dm3��, �Ϳ��Է�ֹ����������, �õ�ƽ���⻬���������� ʵ�黹֤��, �����ຬ������100mg/dm3ʱ, ��Ҫ�Ľ�Ũ����ӦҪ���ӡ�
2) �����軯����
���¶�60��, ���Һ���ΪNi2+ 65g/dm3�� Cl- 40g/dm3�� Na+ 35g/dm3�� pH 5������, �ⶨ�˲�ͬ��Ũ�������缫��Ӧ���������ܶ�J0, ������ڱ�2�� �ɼ�, ���Ž�Ũ������, ���������ܶȿɽ��ʹ�4��������֮�ࡣ ��֤������Ni2+��ԭ��ǿ�ҵ��軯���á�
��2 ��ͬ��Ũ�������缫�Ľ��������ܶ�
Table 2 Exchanged current density under different glue concentrations

3) ����ֹ�����ӵĻ���
�ڵ������������, �缫��Ӧ�ٶ�Ϊ
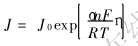
����ʽ��֪, ��T�� �Ǻͦ��㶨������, Ni2+�ŵ��ٶ�J(�ɿ����ǵ�������������ٶ�)�뽻�������ܶ�J0������, �ɼ�, ֻҪ����J0, �Ϳ��Խ���Ni2+�Ļ�ԭ�ٶȡ�
���Խ��������ܶȵ�Ӱ��ʵ�����, �ڵ��Һ�����ӽ���ʹ���������ܶ�J0����Ƚ���, ����Ũ��Ϊ100mg/dm3, Ni2+�ŵ��ٶ�ֻΪԭ�������֮����
������Ϊ, �ڽ�����ʱ, �缫����������ķ�Ӧ�ٶ��ǵ缫ƽ�洦�����֮���� δ����ʱ, �缫���������, ���ڼ�˷ŵ�, Ni2+�ŵ��ٶȱ��ڵ缫ƽ��ȴҪ��103���� �ɴ˿ɼ�, �����������������, ʹ�������ٶȱȵ缫ƽ�洦��, �Ӷ�����Ni��ᾧ����, �õ�ƽ���� �⻬�ĵ������
2.1.3 ��ʪ��(�����������)
������ʪ��(�����������)��ʹ��Һ�ı�������Ѹ�ٽ���, ��������С, ���Һ�Ե缫�������ʪ�Ժ�, ���ɵ������������������渽��, ���������ﲻ�����ס� ����ʪ��Ũ�ȴﵽ20mg/dm3ʱ, ��������������������Сֵ, �������ʪ���ڵ缫����������ﵽ���͡� �����������, ���������Ľ�������Һ�¶����30��������൱�� ���, �����Һ���л���ʱ, ����������ʪ���Ƿ�ֹ��������������Ч������
2.2 ��������λ���������Ƶ�ʵ��Ӧ��
2.2.1 ���Ӽ�Ũ������������λ�Ĺ�ϵ
�ִ��绯ѧ�о�����[7-14], ������������������, ���Һ�ɷ֡� ��ҺpHֵ�� ���Ӽ�Ũ�ȡ� ������ɢ����ѧ�� ���Һ���¶����ȴ��ݡ� ���������ܶȡ� ʼ��Ƭ�������Ǿ�����������������Ĺؼ��� ���������Ĺ�ͬ�������������ĵ缫��λ����������λ��������
��������λͨ����ָ, ������ƽ���λ��ȥ�����������λ�IJ�ֵ�� ��������Ϊ�������� �ȶ������������ɺ��뾧�������Ĺ���, �ض�����������λ����ij�ֻ�����, ijԪ�ص�ƽ���λ�����������������ʵ缫�����Ԫ����������ĵ�λ� ���������¶ȡ� �����ܶȵ���������ȶ���ʱ��, ��������λ�ǵ��Һ�и������ʺ����Ӽ�Ũ�ȶ��������ṹӰ��IJ����� ��ij������Ũ����, �ڲ�ͬ�ĵ�⼼������(�� �¶ȡ� �����ܶȡ� ��������Ũ�ȵ�)�Լ���ͬ���������Ӽ�ʱ, ��������λ�Ĵ�С�ǵ��Һ���ʵ�ʵʱ��ӳ�� Ϊ��, ���߷����˽����缫������ͨ����������λ���߿������Ӽ��ķ�����װ��[15]�� �о�����, ���ø�ר�������ⶨ���������ϵ��Һ����������λ, ���Կ���ȷ��ָʾ�����Һ������, �����ݼ��ĵ绯ѧ����ȷ�����Ӽ������ֵ, �Ӷ����߿����������������̡�
�ڵ��Һ�¶�55��, ѭ���ٶ�660mL/min�� Ni2+ 50g/dm3�� NaCl 90g/dm3�� 40g/dm3 H2SO4��������, ��������Ӽ����ᡢ ���� ����������ڲ�ͬŨ���¶���������λӰ���ϵ����ֵ���ڱ�3��
�ɱ�3��֪, ����ͽ���Ϊ������ƽ����, �乲ͬ�ص���ʹ��������λѸ�����ӡ� ���ڽ���ʹ������������ڵ�(��Ӱ�������ѧ�ɷ�)Ӱ�������������, ���������ƽ�������û�����Ϊ���ҺpHֵ�Ļ������H+�ŵ�����Ƽ�, �ʵ����������Ӳ����ص������, �������ἴ��ά���������������С� ����, ��������������Ҫ���Ӽ�, ����뷽���ͼ������Ŀ��ƶԵ���������������Ҫ��
��3 ���Ӽ�Ũ������������λ�Ĺ�ϵ
Table 3 Relationship between concentration of additives and cathodic overpotential
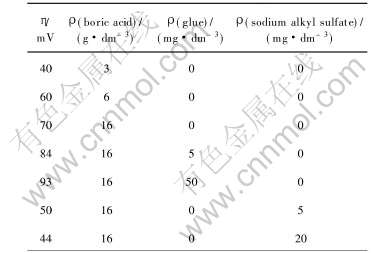
����Һ���л���ʱ, ����������Ƿ�ֹ���������������Ӽ�, �ɱ�3��֪, ������������ε�����, ��������λ���͡�
2.2.2 ������������������Ӽ�Ũ������صķ�����װ��
����ijһ����������˵, ��ͨ����������λ�������, �õ�һ����ѵ���������λ, �ٸ��������������λ����������������������Ӽ�Ũ�ȵ������ϵͳ��
����̿�����Ϊ: ���Ƚ����Ӽ��ܽ��ڲ�, ����һ���ٶȽ��������Һ�Ľ�Һϵͳ, �ڵ��Һ�������۵Ĺ�����, ͨ������װ�ó�ȡ������Һ������������λ������ǽ�������⡣ ������������λ���������DZ�, ����ѹ���λ�Ƚ�, ���ⶨ����������λ������ѹ���λʱ, �����DZ��Զ�����ִ�����Ӵ����Ӽ�������; ���ⶨ����������λ������ѹ���λʱ, �����DZ��Զ�����ִ�����������Ӽ�������; ���ⶨ����������λ����ѹ���λ���ʱ, �����DZ��ȶ����Ӽ����������䡣
������ǵ���Һ����ϵ�еĽ�Һϵͳ, ���¶�Ҳ�͵��۵�һ�¡� �������������Һ�ijɷ����¶Ⱥ�ϵ�е��۵��Һ�ijɷ����¶���ͬ, ����, ������Ǽ����������̴��������е��������ĵ�ᾧ������
2.2.3 �������������������λ�Ĺ�ϵ
ͼ3��ʾΪ�������������������λ�Ĺ�ϵ�� ��ͼ��֪, ������������λ�����, �������������, ����������λΪ51.23mVʱ, ���������Ϊ93.50%(��������), ����������λΪ61.35mVʱ, ���������Ϊ98.6%�� ����, ����������λ������61mV�������������Ӽ�Ũ�ȶ������ƵĻ���, ����������λ����59mVʱ, �������Ӽ�����, ����������λ����63mVʱ, �������Ӽ�������
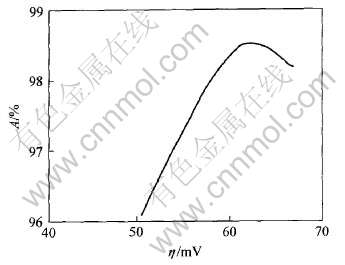
ͼ3 �������������������λ�Ĺ�ϵ
Fig.3 Relationship between percent zero-sized nickel(A) and cathodic overpotential(��)
2.2.4 ��������λ�����Ч�ʵĹ�ϵ
ͼ4��ʾΪ����Ч������������λ�Ĺ�ϵ�� ��ͼ��֪, ����Ч������������λ�������߱仯, �����ߵ����, ����������λΪ55mVʱ, ����Ч��Ϊ97.58%; ������������λ������, ����������λΪ61.25mVʱ, ����Ч��Ϊ98.60%�� �������������������λ, ����Ч�ʷ�������������λ�����Ӷ����͡�
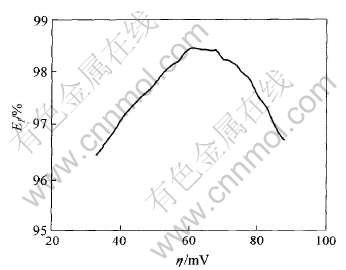
ͼ4 ����Ч������������λ�Ĺ�ϵ
Fig.4 Relationship between current efficiency(EI) and cathodic overpotential(��)
REFERENCES
[1]�Ź���. ����ұ����Ͷ����ļ�������[J]. ��ɫұ��, 1998(3): 30-33.
ZHANG Guo-zhu. Technology modification in Fukang Smelter[J]. Non-ferrous Smelting, 1998(3): 30-33.
[2]������. ��ұ��[M]. ��ɳ: ���ϴ�ѧ������, 2005: 111.
PENG Rong-qiu. Nickel Metallurgy[M]. Changsha: Central South Univerisity Press, 2005: 111.
[3]����. �ü�������Ƶ�λ��pHͼ��һ���·���[J]. ��ɫ����, 1990, 42(2): 48-52.
LI Yang. A new computer method for drawing potential PH diagram[J]. Nonferrous Metals, 1990, 42(2): 48-52.
[4]������. �����ݿ������ӵ��������ϵ��λ��pHͼͨ��ϵͳ[J]. �������Ӧ�û�ѧ, 1985, 2(4): 50-53.
WANG Pei-ming. Complex system with database for potential PH diagram system[J]. Computers and Applied Chemistry, 1985, 2(4): 50-53.
[5]�����, �°���. ұ��绯ѧ�о�����[M]. ��ɳ: ���Ϲ�ҵ��ѧ������, 1990: 73-87.
SHU Yu-de, CHEN Bai-zhen. Metallurgy Electrochemistry Research Approach[M]. Changsha: Central South University of Technology Press, 1990: 73-87.
[6]�κ��, ������. ��ɫ������ȡұ���ֲ�ͭ��[M]. ����: ұ��ҵ������, 2000: 611-622.
REN Hong-jiu, WANG Li-chuan. Nonferrous Metal Refine Metallurgical Manual Copper Nickel[M]. Beijing: Metallurgy Industry Press, 2000: 611-622.
[7]Knuutila K. The effect of organic additives on the electrocrystallization of copper[A]. The Electrorefining and Winning of Copper[C]. Denver Colorado: The Metallurgical Society Inc, 1984: 129-143.
[8]������, ������. ���Һ������п�����̵�Ӱ�켰�����߿���[J]. �й���ɫ����ѧ��, 1998, 8(3): 319-322.
LI Shi-xiong, LIU Ai-xin. Effect of electrolyte quality on zinc electrodeposition and on-line control[J]. The Chinese Journal of Nonferrous Metals, 1998, 8(3): 319-322.
[9]Suarez D F. The effect of organic additives on the electrocrystallization of copper[A]. The Electrorefining and Winning of Copper[C]. Denver, Colorado: The Metallurgical Society Inc, 1984: 145-170.
[10]������, ������. Ǧ�������е��Һ��������ص�ԭ����ʵ��[J]. ��ұ����, 1998, 18(3): 47-49.
LI Shi-xiong, LIU Ai-xin. The principle and pratical on electrolyte quality on-line control aluminum electrolysis[J]. Mining and Metallurgical Engineering, 1998, 18(3): 47-49.
[11]Kerby R C, Jankola W A, Claesseens P L, et al. Proceeding of International Symposium on Electro-metallurgical Plant Praticep[C]. Canada: Pergamon Press, 1990: 309-322.
[12]Robert C, Kerby P. Method and Apparatus for Controlling the Quality of Electrolytes[P]. US 4324621A, 1982-07-18.
[13]������, л��Ԫ, ����߶, ��. ͭ������Ӽ��Ĺ�ҵ���[J]. �й���ɫ����ѧ��, 2004, 14(1): 131-138.
LI Shi-xiong, XIE Da-yuan, LIN Sheng-dao. Industrial control of copper electrolysis additive[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(1): 131-138.
[14]������, ������. Ǧ�������е绯ѧ���������߿���[J]. ���Ϲ�ҵ��ѧѧ��, 1997, 28(4): 351-354.
LI Shi-xiong, LIU Ai-xin. On-line control of electrochemical parameters in in lead electrolysis[J]. Journal of Central South University of Technology, 1997, 28(4): 351-354.
[15]������, ������. ���������������л����Ӽ����߿��Ƶķ�����װ��[P]. �й�ר�� ZL 96184930A, 1998-07-08.
LI Shi-xiong, LIU Ai-xin. Method and Installation of Control on-line by Organic Additive During Metal Deposit Process[P]. CN ZL 96184930A, 1998-07-08.
(�༭�°���)
�ո�����: 2006-03-02; ������: 2006-06-13
ͨѶ����: ������, ����; �绰: 0731-8837505; E-mail: lsxyjs@tom.com