������ʱ��: 2015-08-13 08:35
ϡ�н��� 2015,39(12),1123-1129 DOI:10.13373/j.cnki.cjrm.2015.12.010
������ͭ����ϸ������ʵ���о�
������ ���� ������
�й���ѧԺ���л����о������л����뽡���ص�ʵ����
��Ʒλ�Ѵ����ƽ���Դ�ۺ����ù����ص�ʵ�����Ͻ��ҵ���Źɷ�����˾
������ϡ����������˾
ժ Ҫ��
��Ժ�����ͭ��ĸ���ͭ�������ϸ������ʵ���о�,���鲻ͬ��Ũ�ȡ���ͬ��ʼFe2+Ũ�Ⱥ��¶ȶ�ͭ����ϸ��������Ӱ�졣ϸ���������Դٽ�ͭ������ܽ�,�����Ǵٽ�����ͭ��������ֽ⡣�ڿ�Ũ��4.0%,��ʼFe2+Ũ��2.5 g��L-1,�����¶�45��,�������½���85 d,ͭ������ͭ����Ľ����ʷֱ�Ϊ26.4%,1.26%��ͬ��������,ϸ������ͭ������ͭ����Ľ����ʷֱ��62%,14%,�ֱ�Ϊ�����յ�2.35����11.00������Ũ�Ⱥͳ�ʼFe2+Ũ�ȶ�ͭ����Ľ�����������Ӱ��:�߿�Ũ������Ľ����ܵ���������;���ߺ��͵�Fe2+Ũ�Ȳ�������Ľ���,��ʼFe2+Ũ����10.0 g��L-1ʱ,ͭ����Ľ�������߷ֱ�ɴ�77.9%,11.9%,��ʱ��ϵ��Ũ��ά���ڽϵ�ˮƽ������ͭ����ϸ������ʵ��������,ͭ���������Ϊ���ڲ���:��������ͭ������ܽ�,����60 dʱͭ���ٽ���,�����������½���ϸ������������,��������������ʵ���2%,�����ʱ����ӳ��������������,˵������ͭ���������ͭ��ͭ������������¶ȶ�����ͭ��Ľ����������Ĵٽ����á�
�ؼ��ʣ�
����ͭ����;����ͭ��;ϸ������;������Ϊ;
��ͼ����ţ� TF18
����飺������(1978-),Ů,�����Ϻ���,˶ʿ,�о�����:����ұ�𡢻ƽ���ȡ��������ѧ;E-mail:zlwu@iue.ac.cn;;������,�о�Ա;�绰:0592-6190997;E-mail:ygzhu@iue.ac.cn;
�ո����ڣ�2015-05-22
����������Ȼ��ѧ������Ŀ(51504071,51474075);����ʡ�����ش���Ŀ(����ʡ�Ƽ���)(2013H4020)����;
Bioleaching of High-Arsenic Copper Concentrate
Wu Zengling Kong Weizhang Zhu Yongguan
Key Laboratory of Urban Environment and Health,Institute of Urban Environment,Chinese Academy of Sciences
State Key Laboratory of Comprehensive Utilization of Low-Grade Refractory Gold Ores,Zijin Mining Group Co.,Ltd.
Sanming Rare Earth Development Co.,Ltd.
Abstract��
Bioleaching experiments of high-arsenic copper concentrate bearing enargite were performed. The effect of pulp density,initial concentration of ferrous iron and leaching temperature on copper concentrate bioleaching was investigated. Only 26. 4% and1. 26% of copper and arsenic were extracted respectively after leaching at 45 �� for 85 d under the condition of 4. 0% pulp density and2. 5 g��L-1 ferrous iron without bacteria. The dissolution of copper sulfides was obviously improved by bioleaching,especially the oxidation of enargite decomposition. Under the same experimental condition,the extractions of copper and arsenic reached 62% and 14%,2. 35 and 11. 00 times those of sterile control,respectively. The results showed that both pulp density and initial concentration of ferrous iron had a significant impact on the dissolution of arsenic copper concentrate. The leaching of arsenic was obviously inhibited under too high pulp density,too high and not enough ferrous iron concentration. Under the condition of 10. 0 g��L-1 ferrous iron,the extractions of copper and arsenic reached 77. 9% and 11. 9%,respectively,and the concentration of total iron kept lower level. Bioleaching of high-arsenic copper concentrates showed clear difference between copper and arsenic: copper was extracted rapidly in the first 60 d due to rapid conversion of digenite to secondary covellite,which was followed by a period of lower copper leaching rate. Arsenic extraction was less than 2% in the first stage of leaching and then increased with the leaching time,suggesting that enargite was extracted after digenite and covellite. The results showed that increasing temperature had a notable promotion on the leaching of enargite.
Keyword��
high-arsenic copper concentrate; enargite; bacteria leaching; leaching behavior;
Received�� 2015-05-22
ͭ�ڹ��÷�չ�о�����Ҫ��ս�Լ�ֵ, ���ҹ�ͭ����Դ��ȱ������Ӧ��,��������ȸߴ�65% ��������Ʒλ���Ѵ���ͭ����Դ���ܻ����ҹ�ͭ����Դ��ȱ֮��,Ҳ˳Ӧ����ͭ����Դ��������������ͭ��ֲ��㷺,��һ����Ҫ�Ŀ����Դ�� ����ͭ������Ҫ������ͭ��Ϊ��[1,2],Ҳ��һ����������ͭ����ʽ����[3]������ͭ������Ҫָ�����2% ��ͭ����ϸ������������������ܹ����������Դ��Ͷ��С���ɱ��͡����ܺġ��Ի����Ѻõ��ŵ㳣�����ڵ�Ʒλ���Ѵ������������ͭ����Դ�Ŀ���������[4]������ϸ������ʵ���о������ں�����ͭ���ͭ����[1,2,5]��
����ͭ���Ǻ�����ͭ��ĵ��Ϳ���֮һ, �Ⱥ��м۽���ͭ,�ֺ��к�Ԫ����,�о������ﴦ��������Ҫ�����������ʵ��Ӧ�ü�ֵ��������, �ܶ��ѧ���о�����ͭ����е����Ⱦ�[6,7,8,9,10]�����Ⱦ�����[11,12,13,14],��Щ�о����ص��������ڻ����ʺͻ���Ч����,���ھ���Ľ�������ѧ�����������о����١�Fantuazzi��[6]����A. ferrooxidans�ܽ�����ͭ��,֤ʵ��ϸ��ͨ������ۺ���������ͭ���ֱ�����û��Ƽ�˵,�����ϸ����������ͭ��Ķ������ܽ���ơ�Corkhill��[8]������������������������������ͭ��,�������ϸ���ӿ���ͭ���ܽ�,����ͭ��ı���仯����,��������Ч�������ĸߡ����Ⱦ���������Ч���ͭ������,���ʺ������¿ɴٽ��������������߾��γ���ʯ��ʽ�̶��ڽ������С�Escobar��[11]�о����»�������Ҷ��ҡƿ��������ͭ��,�������: ��70 ��,��Fe3 +1 g��L- 1��������,����550 h,ͭ�Ľ����ʴ�52% ; ϸ��ֱ�������ڿ������,ͨ��ֱ�����û��ƴ�����ͭ��Ľ����������ʼ����ں�����ͭ��ĸ���ͭ����ϸ���������о�������л����[12]������������˾����е����Ⱦ��ֱ����������ͭ���ͭ����,�е����Ⱦ�����35 d,Cu,As�����ʴ�90% ����,��������������˾�������,Fe3 +���ӽ�������,��Ũ��Fe3 +�ٽ�ͭ����Ľ�����������δ��ͭ�����в�ͬ��ͭ���ϸ��������ͭ���������Ϊ���бȽϡ���������,��������������Ƶ���( ������ͭ��ͭ������ͭ��ͭ�������) ����ʱ[15],��ͬ�����ϸ���������ʡ������������������Լ�����ͭ���ϸ����������ѧ�д������о���
���о��Ժ�����ͭ��ĸ���ͭ����Ϊ�о�����,�ֱ�������������ѧ�ȷ��濼����ϸ����������ͭ�������ҪӰ������,�о��˸���ͭ�����в�ͬ�����ܳ�˳���ͭ���顢���Ľ�����Ϊ,Ϊ����������Դ�Ĺ��տ����ṩ����֧�š�
1ʵ��
1. 1����
ʵ���þ���Ϊ��Ʒλ�Ѵ����ƽ���Դ�ۺ�����ʵ����������ѱ����Acidithiobacillus ferrooxidans, Leptospirillum ferrooxidans,Sulfobacillus��Ͼ���������Ϊ����0 K������,121 �� �¸����������20 min�����������Ϊ: 3. 0 g��L- 1( NH4)2SO4,0. 1 g ��L- 1KCl,0. 5 g��L- 1K2HPO4,0. 5 g��L- 1Mg SO4�� 7H2O��0. 01 g��L- 1Ca( NO3)2��4H2O��
1. 2����
ʵ���ø���ͭ������Ը���ijͭ��,��Ʒ������0. 048 ~ 0. 075 mm֮��,��ҪԪ�غ���( ��������) ΪCu 46. 48% ,As 3. 56% ,Fe 13. 58% ,S 33. 12% ����Ҫ����Ϊ18. 7% ����ͭ��35. 32% ����ͭ��15. 33% ͭ����29. 96% ������,��ʯ������Ҫ��ʯӢ������ʯ���ؿ�ʯ�ȡ�
1. 3����
ϸ������ʵ����500 ml��ƿ�н���,�����趨��ʵ����������һ������������ѱ���ľ���( ������10% ) ,���趨�¶�����������ʵ�������ÿ��ⶨ������ϵ��p H,������ԭ��λ( Eh) ,Fe2 +Ũ����ϸ��Ũ��,��ϵ���ز�������Ӧ������������ˮ��ÿ��6 dȡ4 ml����Һ����,�ⶨ����Һ��ͭ���顢����Ũ��,��������Ӧ�����0 K�������������趨��ʵ����������������ʵ��,������ϵΪ��ˮ,����0. 075 g��L- 1Na F��Ϊ�־���,����ʵ�鷽����ϸ������ʵ����ͬ��
ϸ������ʵ�������ͼ���豸��Ҫ��: ������ԡ��������������ո����䡢����ʽ�����ޡ���ȼ�( METTLER TOLEDO In lab Routine pro) ����λ��( HANNA HI3131B) ��
������������Ʊ���Һ�ζ����ⶨ����Һ��ͭ����Ũ��; �����ظ���صζ����ⶨ����Һ������Ũ��; ����ԭ��ӫ������ⶨ����Һ����Ũ�ȡ�
2���������
2. 1��ͬ��Ũ�ȶԽ�����Ӱ��
ʵ������: Fe2 +��ʼŨ��2. 5 g��L- 1�������¶�45 �桢�����ٶ�Ϊ300 r��min- 1,�����ڲ�ͬ��Ũ��( 1. 0% ,2. 5% ,4. 0% ,5. 5% ,8. 0% ) �Ը���ͭ���������Ӱ�졣ͬʱ����4. 0% ��Ũ�������µ�������ʵ�顣ʵ�������p H��������ԭ��λ( Eh) ��ͭ���������ʱ��仯������ͼ1��ʾ��
��ͼ1( a) ��֪,����ǰ��( 20 d��) ,������Ʒ�к�������ʯ����,ϸ������ʵ����ϵp H��������,��Ũ��Խ��,������ϵp H�IJ�����ΧԽ��,p H���ڵ�ʱ��Խ������Ũ��8. 0% ʱ,30 d��p H������ڡ����Ž���ʱ����ӳ�,ϸ������ʵ����ϵp H���½�����Ũ��Խ��,��ϵp H���ͷ���Խ��,8. 0% �Ŀ�Ũ����,��������ʱp H���,����0. 74����ͼ1( b) ��֪,��Ũ������,������ϵ������ԭ��λ����������ʱ��Խ���� ��Ũ��1. 0%~ 5. 5% ������,����20 ~ 30 dʱ������ԭ��λ����������830 m V; ��Ũ��8. 0% ʱ,��λ�����ٶȽ���,����40 dʱ��ϵ��λ������800 m V����������ϵ��p H�͵�λ�ڽ���������û�������仯: p H�����ȶ���2. 0����( ͼ1( a) ) ; ������ԭ��λ��������,ʼ��ά����570 m V����( ͼ1( b) ) ��
��Ũ�ȶԺ�����ͭ��ͭ�����ϸ����������������Ӱ�졣���ſ�Ũ�ȵ�����,������ϵϸ�����ܵļ�����������,��ϸ��������ͭ�����Ч����ɲ���Ӱ��,ͭ����Ľ�������֮����( ͼ1( c) ��( d) ) ����Ũ��8. 0% ������,����40 dʱͭ�Ľ����ʲ�������59% ,��������ʱͭ�Ľ����ʽ�Ϊ61. 5% ; ��Ľ��������,��Ϊ7. 72% �� ʵ������ͭ����Ϊ����ͭ��������ͭ��ͭ���Ȼ�Ͽ���,�����ܽ������ͭ���ͭ���ȿ�����ϸ�������¿��ٽ���,ͭ�������ڽ���ǰ��( 20 d) ��������,֮��ͭ������������,���������½�������ͭ��ѧ�����ȶ�,���ѽ���,�ҿ�Ũ�ȶ�����ͭ��Ľ���Ӱ����������ͼ1( d) ����ܽ����߿��Կ���,��Ũ��8. 0% ʱ,ǰ35 d����ͭ�����δ������,40 d������ͭ��ſ�ʼ�н����ԵĽ���; �Ϳ�Ũ������Ľ����ʸ�,��Ũ��1. 0% ʱ��Ľ�����Ϊ17% ��ϸ���������Դٽ�ͭ����,����������ͭ��������ֽ⡣ϸ������ͭ����Ľ�����ԶԶ����������,��Ũ��4. 0% ʱͭ��������ʷֱ�Ϊ62% ,14% ,�ֱ�Ϊ������( 26. 4% ,1. 26% ) ��2. 35����11. 00����
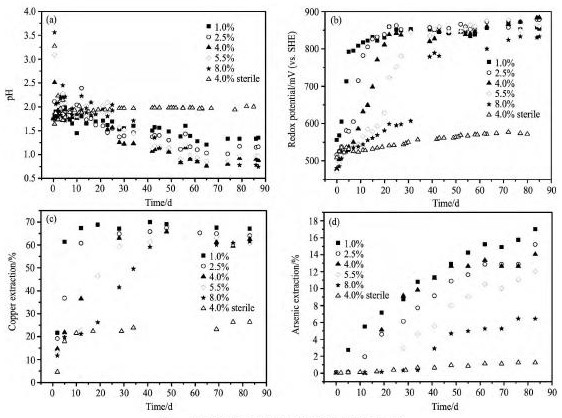
ͼ1��ͬ��Ũ�ȶԸ���ͭ���������Ӱ������Fig. 1 Effect of pulp density on dissolution of copper concentrate ( a) p H; ( b) Eh; ( c) Copper extraction; ( d) Arsenic extraction
2. 2��ͬ��ʼFe2 +Ũ�ȶԽ�����Ӱ��
ʵ������: ��Ũ��4% �������¶�45 �桢�����ٶ�Ϊ300 r��min- 1,���鲻ͬ��ʼFe2 +Ũ��( 0. 5,2. 5,4. 5,5. 0,10. 0,17. 5 g��L- 1) �Ը���ͭ���������Ӱ�졣����Fe2 +Ũ����2. 5 g��L- 1�����µ�������ʵ�顣ʵ�����p H����λ����Һ��ϸ��Ũ�ȱ仯���ߺ�ͭ���顢������������ͼ2��ʾ��
��ʼFe2 +Ũ����0. 5 ~ 17. 5 g��L- 1��Χ��,��ͬ������Ũ�Ƚ�����ϵ��p H�͵�λ�仯����û����������( ͼ2( a,b) ) �����Ũ��ʵ����ͬ,������ϵ��p H����ʱ����ӳ����½�,20 d��p H���ٽ���; ��λ���Ž���ʱ����ӳ�������,0 ~ 20 d���߷��Ƚ�С,25 d�����������860 m V������Fe2 +Ũ��10. 0 g��L- 1ʱ,������ϵp H���½����Ƚ���,��������ʱp HΪ1. 53,����������Ũ�Ƚ�����ϵ��p H; 20 dʱ��λ������800 m V, ά���ȶ�40 d,����60 dʱ��λ������870 m V��ά���ȶ��������������p Hʼ��ά����2. 0����( ͼ2( a) ) ,������ԭ��λ��������,����ά����600 m V����( ͼ2( b) ) ������Һ��ϸ��Ũ�ȱ仯����( ͼ2( c) ) ���Կ���,ϸ������15 d���ҵ���Ӧ��,Ũ�ȿ�ʼ���ֶ�������,ϸ��������������,���Ӧ��p H�½��͵�λ�����ı仯����һ�¡� ϸ��Ũ�ȴﵽһ����ֵ��ʼ�����½�����,��ʱ��λ����������Ҳ��û�����������Ũ�ȹ����߹��;������ڽ����������,10. 0 g��L- 1ʱ������������,ϸ��Ũ��ʼ�ձ��������ˮƽ��
��ͼ2( d ~ f) ��֪,������ͭ���ͭ����ϸ��������Ϊ3����,ͭ����Ľ�����Ϊ�������Բ��졣��һ��( 0 ~ 20 d) : ͭ������Լ30% ,��ʱ�����ܽ������ͭ��ϸ����������ʱ��Ľ����ʺܵ�( 0. 1% ~ 1. 6% ) ,����ͭ����ܳ�������( ͼ2( e) ) ����ʼFe2 +Ũ����0. 5 ~ 5. 0 g��L- 1��Χʱ����Ũ�ȱ仯����,10. 0 ~ 17. 5 g��L- 1��Χʱ����Ũ�ȿ����½�( ͼ2( f) ) �������ڸ���( 45 ��) �� p H1. 8������,��Ũ�ȵ�Fe2 +����ˮ���������, ����Ũ�ȿ����½������ͼ2( e) ��( f) ���߷���,�ý��в�������ͭ�������,��Һ�е��������������������,����������ʵ͡�����Ũ���½����˹�����Ҫ�������ϸ����ֱ������ʵ�ֺ�ͭ����Ľ���,���ܷ������·�Ӧ( 1) ~ ( 3) :
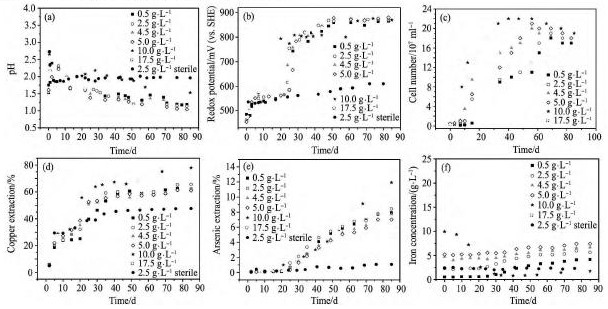
ͼ2��ͬ��ʼFe2 +Ũ�ȶԸ���ͭ���������Ӱ������Fig. 2 Effect of ferrous iron concentration on dissolution of copper concentrate
(a)pH;(b)Eh;(c)Cell number;(d)Copper extraction;(e)Arsenic extraction;(f)Iron concentration
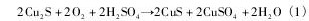

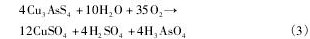
�ڶ���( 20 ~ 60 d) : ϸ�������ʶ�������,������ԭ��λ��������,ͭ����Ľ����ʲ�������,ͭ�����ʴﵽ57%~ 59% ,�������������5. 3%~ 6. 7% ,����Ũ����������( ��Fe2 +Ũ����10. 0 g��L- 1ʱ����Ũ�Ȳ����½���ά����1. 0 g��L- 1��Χ��) ���˽γ�����ͭ���ܽ���,ͭ��������ͭ����ϸ�����������Ҳ��������������������һ�η�Ӧ��,�����ܷ�����Ӧ( 4) ~ ( 5) :
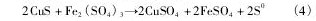
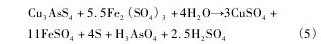
������( 60 ~ 83 d) ,��ʼFe2 +Ũ����0. 5 ~ 5 g��L- 1��Χʱ,ͭ����Ľ����ʵ�������������ƽ��,ͭ�����ʴﵽ61%~ 65% ,���������7. 0%~ 8. 4% ��Χ( ͼ2 ( d,e) ) ; ��ʼFe2 +Ũ����10. 0 g��L- 1����ʱ,ͭ����Ľ������Գ�����������; ��ʼFe2 +Ũ��10. 0 g��L- 1ʱ,ͭ����Ľ�������߷ֱ�ﵽ77. 9% ,11. 9% ������Ũ�����ƺ͵ڶ��λ���һ�¡�
ʵ������һ��˵��,ϸ�������������ͭ�� ��Ľ�����,�ٽ�����ͭ��������ֽ⡣��ʼFe2 +Ũ����2. 5 g��L- 1ʱ,ͭ����Ľ����ʷֱ�Ϊ65. 52% ,8. 43% ,Զ��������������( 47. 56% , 1. 05% ) ,�ֱ�Ϊ�����յ�1. 4����8. 0����
2. 3��ͬ�¶ȶԽ�����Ӱ��
ʵ������: ��Ũ��4% �������ٶ�Ϊ300 r��min- 1,�ڳ�ʼFe2 +Ũ�ȷֱ�Ϊ0. 5,2. 5,5. 0 g��L- 1ʱ���в�ͬ�����¶�( 30,45 ��) �Ը���ͭ���������Ӱ�졣ʵ�������p H����λ��ͭ�������������ͼ3��ʾ��
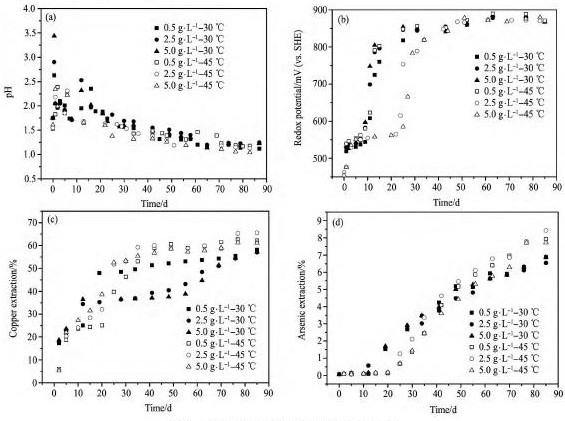
ͼ3��ͬ�¶ȶԸ���ͭ���������Ӱ������Fig.3 Effect of temperature on dissolution of copper concentrate
(a)pH;(b)Eh;(c)Copper extraction;(d)Arsenic extraction
��ͬ��ʼFe2 +Ũ��,��ͬ�¶���ϸ��������ϵ��p H�仯������һ��,����ʱ����ӳ�������( ͼ3( a) ) ��Fe2 +Ũ����2. 5 ~ 5. 0 g��L- 1ʱ,����10 ~ 40 dʱ45 ����ϵ��������ԭ��λ����ͬһ������30 ��ʱ�ĵ�λ,40 d��ͬ�¶��µ�λ���ڽӽ�,��870 ~ 880 m V��Χ( ͼ3( b) ) ��
��ͬ��ʼFe2 +Ũ��,��ͬ�¶���ϸ������ͭ�� ��Ľ����ʴ�����������: ����ǰ��( 0 ~ 30 d) ͭ�Ľ����ʽ�Ϊ�ӽ�,35 d��45 �� ��ϵͭ�Ľ��������Ը���ͬһ������30 �� ʱͭ�Ľ����ʡ�����ǰ��( 0 ~ 40 d) 30 ����ϵ��Ľ��������Ը���ͬһ������45 �� ʱ��Ľ�����; 40 d�������¶ȵ�����,45 ����ϵ��Ľ����ʿ�������,����ͬһ������30 �� ʱ��Ľ����ʡ���ͬ����������,����ǰ��ͭ�Ľ����������ٶȿ�,����Ľ����ʵ�,�к���ͭ����Ľ����ʾ�������,˵������ͭ�� ͭ���Ȳ�������ͭ����������ͭ���������ͬ�¶�ϸ����������������,ϸ������������ͭ���ͭ��������и������Դٽ�����ͭ����ܽ�,������ͭ��Ļ�ѧ��������ѧʵ����һ�¡��������[16]�о�������ͭ������������Ի�ѧ����,ʵ��������,��������ԭ��λ800 m V,�����¶�30 ~ 75 �� ʱ,���ۻ��Ea= 57. 87 k J��mo L- 1���¶�ÿ����15 K,����ͭ������Ľ�����������2. 48 ~ 2. 86��,����¶ȴٽ�����ͭ����ܽ⡣
3����
1. ϸ������������ͭ��ĸ���ͭ������Դٽ�ͭ������ܽ�,�����Ǵٽ�����ͭ��������ֽ⡣�ڿ�Ũ��4. 0% ����ʼFe2 +Ũ��2. 5 g��L- 1�� �����¶�45 ��,�������½���85 d,ͭ������ͭ����Ľ����ʷֱ�Ϊ26. 4% ,1. 26% ��ͬ��������,ϸ������ͭ������ͭ����Ľ����ʷֱ��62% ,14% , �ֱ�Ϊ�����յ�2. 35����11. 00����
2. ��Ũ�Ⱥͳ�ʼFe2 +Ũ�ȶ�ͭ�����ϸ��������������Ӱ��: �߿�Ũ������Ľ����ܵ���������; ���ߺ���Fe2 +Ũ�ȶ���������Ľ���,��ʼFe2 +Ũ����10. 0 g��L- 1ʱ,ͭ����Ľ�������߷ֱ�ɴ�77. 9% ,11. 9% ,��ʱ��ϵ��Ũ��ά���ڽϵ�ˮƽ��
3. ������ͭ���ͭ����ϸ������������ͭ�� ��Ľ�����Ϊ���ڲ���: ����ǰ��,ͭ�����ʿ�������,��ʱ�����ܽ������ͭ��ϸ������,ͭ���ڼ��������Ҳ���������ܽ�,������ͭ���ʱ����δ������,��Ľ����ʵ���2% �������ʱ����ӳ�,�������������,����ͭ����ϸ����������·�����������������ͭ�Ľ�����������������ƽ����
4. ��ͬ�¶ȶԺ�����ͭ��ĸ���ͭ����ϸ��������Ӱ��������,����¶ȶ�����ͭ��Ľ����������Ĵٽ����á�
�����
[1] Zou P,Zhang W B,Wang J K,Wen S M,Zhou X L.Study on bioleaching of high arsenic-bearing copper concentrateby joint use of arsenic-tolerant mutant of thiobacillus ferrooxidans and high temperature-tolerating thermoacidophilic archae[J].Mining and Metallurgical Engineering,2006,26(3):57.(��ƽ,���ı�,������,������,������.�и��½������϶Ը���ͭ����Ľ����о�[J].��ұ����,2006,26(3):57.
[2] Lu G N,Mo Z H,Luo H J,Ke L.Study on leaching mechanism of high arsenic-bearing copper concentrate by mesophilic bioleaching bacteria[J].Mining and Metallurgical Engineering,2012,32(3):82.(¬����,Ī��,����,����.���½�����Ը���ͭ��������������о�[J].��ұ����,2012,32(3):82.)
[3] Kong W Z,Wu Z L,Liu J Y.Technical progress of enargite leaching technology[J].Nonferrous Metals(Extractive Metallurgy),2014,8:14.(��ά��,������,������.����ͭ�����������չ[J].��ɫ����(ұ������),2014,8:14.)
[4] Liu X,Song Y S,Wen J K.Dissolution behavior of arsenic-bearing complex nickel sulfide ores at low-temperature by bacteria leaching[J].Chinese Journal of Rare Metals,2014,38(6):1127.(��ѧ,����ʤ,�½���.���鸴��������������������Ϊ�о�[J].ϡ�н���,2014,38(6):1127.)
[5] Fornasiero D,Fullston D,Li C,Ralston J.Separation of enargite and tennantite from non-arsenic copper sulfide minerals by selective oxidation or dissolution[J].Int.J.Miner.Process,2001,61:109.
[6] Fantauzzi M,Elsener B,Atzei D,Lattanzi P,Rossi A.The surface of enargite after exposure to acidic ferric solutions:an XPS/XAES study[J].Surface and Interface Analysis,2007,39(12-13):908.
[7] Fantauzzi M,Rossi G,Elsener B,Loi G,Atzei D,Rossi A.An XPS analytical approach for elucidating the microbially mediated enargite oxidative dissolution[J].Analytical and Bioanalytical Chemistry,2009,393:1931.
[8] Corkhill C L,Wincott P L,Lloyd J R,Vaughan D J.The oxidative dissolution of arsenopyrite and enargite by Leptospirillum ferooxidans[J].Geochim.Cosmochim.Acta,2008,72:5616.
[9] Sasaki K,Takatasugi K,Ishikura K,Hirajima T.Spectroscopic study on oxidative dissolution of chalcopyritie,enargite and tennantite at differnt p H values[J].Hydrometallurgy,2010,100(3-4):144.
[10] Xie H Y,Lu J S,Lan Z Y,Tong X,Zhuang G Z.Study on bioleaching of high arsenic-bearing copper concentrate by moderate thermophile[J].Journal of Kunming University of Science and Technology(Science and Technology),2010,35(1):24.(л����,½����,��Խ,ͯ��,ׯ����.�е����Ⱦ���������ͭ�����о�[J].����������ѧѧ��(������),2010,35(1):24.)
[11] Escobar B,Huenupi E,Godoy I,Wiertz J V.Asenic precitation in the bioleaching of enargite by sulfolous BC at 70��[J].Biotechnology Letters,2000,22:205.
[12] Xie H Y.The Technology and Mechanism of Bacterial Leaching High-Arsenic Copper Sulfide Concentrate and Comprehensive Utilization of Arsenic[D].Kunming:Kunming University of Science and Technology,2007.43.(л����.������ͭ����ϸ������������ۺ����ù��ռ������о�[D].����:����������ѧ,2007.43.)
[13] Sasaki K,Takatsugi K,Hirajima T.Effects of initial Fe2+concentration and pulp density on the bioleaching of Cu from enargite by Acidianus brierleyi[J].Hydrometallurgy,2011,109:153.
[14] Takatsugi K,Sasaki K,Hirajima T.Mechanism of the bioleaching of copper from enargite by thermophile ironoxidizing archaea with the concomitant precipitation of arsenic[J].Hydrometallurgy,2011,109:90.
[15] Lattanzi P S D,Musu E,Atzei D B,Rossi A.Enargite oxidation:a review[J].Earth Science Reviews,2008,86:62.
[16] Wu Z L,Wu Z,Zhu Y G.Kinetics of enargite chemical leaching[J].Chinese Journal of Rare Metals,2015,39(8):735.(������,����,������.����ͭ��ѧ��������ѧ�о�[J].ϡ�н���,2015,39(8):735.)