DOI��10.19476/j.ysxb.1004.0609.2019.10.08
����������Ti-15Zr�Ͻ���ĥ���ܵ�Ӱ��
���մ�1���� ӽ1���Դ���2�����ľ�1
(1. ���ϴ�ѧ ��ĩұ������ص�ʵ���ң���ɳ 410083��
2. ���ϴ�ѧ ����ѧԺ����ɳ 410082)
ժ Ҫ��Ŀǰ���������ٴ�Ӧ�õ�Ti-Zr�Ͻ���Ȼ������ĥ�Բ������ѧ�������⣬��Լ��������������Ľ�һ����չ����ʵ����÷�ĩұ��ķ������Ʊ����������ϸߵ�Ti-15Zr-0.72O(����������%)��Ti-15Zr-0.86O�Ͻ�ͨ���봫ͳ����ұ���Ʊ���Ti-15Zr�Ͻ�Աȣ��о��������Բ�����ѧ���ܵ�Ӱ�졣Ti-15Zr-0.86O�Ͻ����ά��Ӳ�ȴﵽ449.9HV����Ti-15Zr-0.72O�ĸ�8%�����Ti-15Zr�ĸ߳�76%����ģ����Һ�н��е�Ħ��ĥ��ʵ����ʾ��Ti-15Zr-0.86O�����Ti-15Zr-0.72Oĥ���������٣��������������٣�������ĥ����ԶС��Ti-15Zr��ʵ��������ͨ��������Ԫ�أ�Ti-15Zrϵ�кϽ��Ӳ�Ⱥ���ĥ���ܵõ������������
�ؼ��ʣ�Ti-Zr�Ͻ𣻷�ĩұ�𣻹�������ά��Ӳ�ȣ�Ħ��ĥ������
���±�ţ�1004-0609(2019)-10-2285-07�� ��ͼ����ţ�TG166.5��TH117.1���� ���ױ�־�룺A
���ھ��и߱�ǿ�ȡ��������ʴ�������������ԣ��Ѽ��ѺϽ��ڳݿƵ�����õ��˹㷺�Ĺ�ע[1]��Ŀǰ����õ��Ǵ��Ѻ�Ti-6Al-4V�Ͻ�[2-3]��Ȼ����ͨ��ģ����Һ�е���ʴ���о���������Ti-6Al-4V����һ������ĥ���ܣ�������ĥ���ܲ����ߣ��������ڳݿƲ��������Ӧ��[4-5]�����⣬Ti-6Al-4V�е����ͷ�Ҳ��DZ�ڵ�ϸ�����Ժ����ԣ�����Լ������ҽ������İ�ȫʹ��[6]��������ѺϽ��У����һ�����ĺϽ�Ԫ��[7-8]����ʹTi-Zr�Ͻ����ĥ�Ե��ۺ���ѧ������ߣ����ʺ���Ϊ����ҽ�ò���[9]������ﯡ����������ǻ���ʯ���մɻ��ݿƲ�����Ŀǰ�����õijݿ�ҽ�ò��ϡ������ǻ���ʯͿ������Ӧ��ʮ�ֹ㷺������ĥ���ܽϺã������������Ըߣ�������ģ����Һ���е��ȶ��Ի��д����[10-11]��Ti-Zr�Ͻ���������ܺͿ�ƣ������������������ﯡ����������ǻ���ʯͿ����մɲ��ϵ��������ܺͿ�ƣ�����ܣ��ھ����������������Ե�ͬʱ������ģ����Һ�����µı���Ҳ�൱�ȶ�������Ӳ�ȵ͡���ĥ���ܲ�����������ʵ��Ӧ�á�
���ѻ������У�����Ԫ�ص���������ǿ�Ͻ���ѧ���ܵ�һ����Ҫ;��[12]��������Ҫ������Ԫ�أ�ͨ������ǿ���Ϳ���ǿ���Ȼ����ܹ��Բ��ϵ�Ӳ�ȡ�ǿ�Ⱥ���ĥ�Ե���ѧ����������ߡ�LIM��[13]������Ti-8Al�Ͻ��в������������ڦ���ͦ�+�������������ǿ�����á�OH��[14]�о���������Ϊ1000��10-6~4000��10-6֮���Ti-6Al-4V�Ͻ����ѧ���ܣ�������������������ߣ��Ͻ��Ӳ�Ⱥ�ǿ�ȶ����������������Ͻ��Ӳ����������ĥ����������أ�ͨ����������Ԫ��Ҳ�����Ti�Ͻ���ĥ�Ե���Ҫ;��[15]��
���IJ��÷�ĩұ����ͨ�����ƺ�������ͬ��ԭ�Ϸ�ĩ�������Ʊ���������ͬ��Ti-15Zrϵ�кϽ�ͨ������̬����Ti-15Zr�Ͻ���жԱȣ��о����������ԺϽ�����֯��Ӳ�Ⱥ���ĥ���ܵ�Ӱ�죬Ϊ���ͳݿ�Ti-Zr�Ͻ���о���Ӧ���ṩ����;����
1 ʵ��
ʵ���Ըߴ��⻯����(HDH) �ѷ�(���ȣ�99.9%��������45 ��m��w(O)=0.15%)��������е�����ĸߺ�����HDH �ѷ�(���ȣ�99.9%��������45 ��m��w(O)= 0.43%)���ߴ�HDH ﯷ�(���ȣ�99.9%��������75 ��m)Ϊԭ�Ϸ�ĩ�����ߴ��⻯����(HDH) �ѷۡ��ߺ�����HDH�ѷۺߴ�HDHﯷ۷ֱ���34:51:15��51:34:15�ijɷ��������������зֱ��ֻ��6 h����Ϻ�����ַ�ĩ���ֱ����װ����Բ���ε�ģѹģ��(~d 26 mm)�У���188 MPa��ѹ���±�ѹ10 s������ģѹ���͡����ѹ����������ս�¯�н����սᣬ��ն�Ϊ1��10-3 Pa����1300 ���±���4 h���ս�����Ʒ��750 ���½������������Ʊ�����Ϊ70%�����յõ���������ͬ������Ti-15Zr-xO(����������%)�Ͻ���DHL-400����յ绡����¯�Ʊ���̬Ti-15Zr�Ͻ���Ϊ�Աȡ�
ʹ��Leco TCH600���������DzⶨTi-15Zrϵ�кϽ����������������1��ʾ��
��1 Ti-15Zrϵ�кϽ��������
Table 1 Oxygen contents of Ti -15Zr alloys

���ֺϽ��������Rigaku D/max 2550 X���߷����ǽ��з�������������Ti-15Zr-0.72O�Ͻ�10 min��ʴ�Ƴɵ羵��Ʒ������ESCALAB250Xi��X���߹����������(XPS)�����������γɡ�����FEI Quanta FEG 250ɨ��羵������ò������BUEHLER5104��ѹ��Ӳ����������Բ�����ά��Ӳ�ȡ�
Ħ��ĥ��ʵ�����HT-1000����Ħ��ĥ��������������������˹���Һ�н���37 ���µ�Ħ��ĥ�����顣����ISO/TRl0271�������˹���Һ���˹���Һ�ijɷ����2��ʾ�����ð뾶Ϊ2 mm��Si3N4����ѹͷ������ת����ת��Ϊ0.1 m/s�����ϵ�Ħ�����ܲ����ǹ��в�������ԣ���������ֻ���������ص����ܣ����غɡ��¶ȡ�Ħ���ٶȺ�Һ�廷���ȵ�Ӱ�졣HEINTZE��[16]�о�ָ����ǻ������������ʱ���ܵ�ҧ������3~36 N֮�䡣Ϊ��ģ���ǻ����ѧ�������������20 NΪ��ѹ�غɣ�Ħ��ʱ��Ϊ60 min������������Ħ��ĥ��ǰ���������ʧ������FEI Quanta FEG 250ɨ��羵�۲�Ħ���������ı�����ò����Ħ��ĥ�����ĥ�۵����������˹�����ϸ��(MG-63)������24 h������FEI Quanta FEG 250ɨ��羵�۲�ϸ����������̬�����������
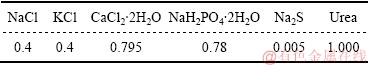
��2 �˹���Һ�ijɷֱ�
Table 2 Ingredient concentrations of artificial saliva (g��L-1)
2 ���������
ͼ1��ʾΪTi-15Zrϵ�кϽ��XRD�ס���ͼ1���Կ����� Ti�C15Zr-0.72O��Ti�C15Zr-0.86O��Ti-15Zr���ֺϽ���������ֻ�е�һ�Ħ��ࡣͨ���Ա����ֲ�ͬ��������Ti-15Zr�Ͻ𣬿ɷ���������������ᵼ���������ƣ�����Ҫ��������ԭ���ڰ������϶��������һ���̶ȵľ�����䣬ʹ�������ơ�
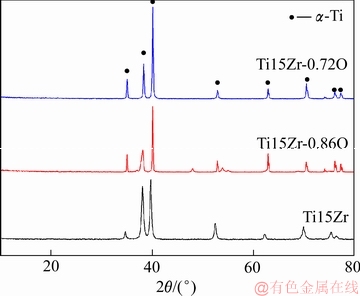
ͼ1 Ti-15Zrϵ�кϽ��XRD��
Fig. 1 XRD patterns of Ti-15Zr alloys
ͼ2��ʾΪTi-15Zrϵ�кϽ��XPS������Zr3d����ͼ�������ϵ������ͨ������õ���Zr���ZrO2�塣Ti-15Zr-0.72O��Ti-15Zr-0.86O�ķ������ƣ�����ZrO2��ǿ��Զ����Ti-15Zr�ġ�˵��Ti-15Zr-0.72O��Ti-15Zr-0.86O�Ͻ�����������Ĵ��ڡ���Ti-15Zr�Ͻ�����Ԫ�ط�������ʱ���������ܵͣ�XPS����Ȼ���ֽϵ͵���������DZ���Ӵ��������������Ȼ�����˿�ʴ������������������������������ĺ�������XRD�ɼ��ֵ������XRD��ֻ���õ���һ�Ħ�����塣
���3��ʾ����Ԫ�ص��������������Ti-15Zr�Ͻ��Ӳ�ȡ�ͨ����ĩұ��������Ti-15Zr-0.72O��Ti-15Zr-0.86Os�Ͻ���������ά��Ӳ��Զ������̬Ti-15Zr�Ͻ���������ά��Ӳ�ȣ��ӽ�Ti-15ZrӲ��ֵ����������Ti-15Zr-0.86O������������Ti-15Zr-0.72O�ĸ߳�1400 ��10-6��ȴʹӲ��ֵ�����Ե�������
ͼ3��ʾΪTi-15Zr��Ti-15Zr-0.72O��Ti-15Zr-0.86O�Ͻ�������SEM�����ֲ�ͬ��������������֯��ò��ΪƬ��״���࣬����XRD��������ͨ����ĩұ�����ֹ�̬�ս᷽���Ʊ���Ti-15Zr-0.72O��Ti-15Zr-0.86O�Ͻ����ڴ���һ���̶��ϵ���ɢ����֣���Ti-15Zr �Ͻ���ȣ�ǰ���ߵ�Ƭ�������
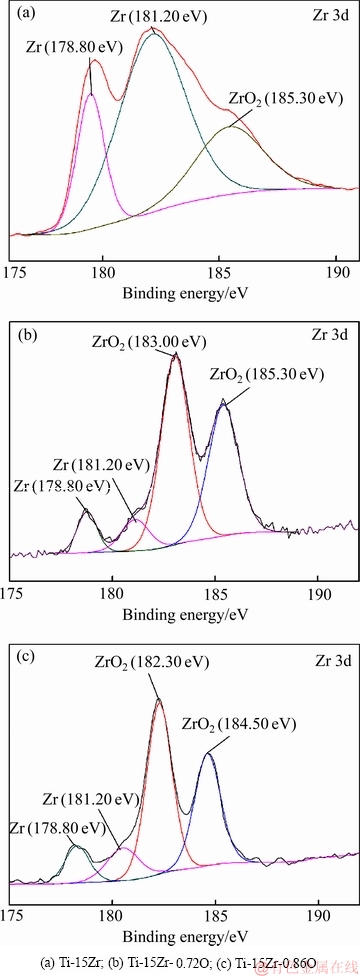
ͼ2 Ti-15Zrϵ�кϽ��XPS������
Fig. 2 XPS patterns of Ti-15Zr alloys
��ʵ���÷�ĩұ�������÷�ĩ���������������ú������ߵ��ѷ۽����˵��أ����������ZrO2��ĩ�ܸ��Ӿ��ȵز�����Ԫ�أ��������γɽϴ��������ɢ�����������������ѻ������У�������Ҫ������Ԫ�أ�ͨ���Լ�϶ԭ�ӵ���ʽ�����ڰ������϶��[17]����Ԫ��ͨ���Թ�����ԭ����ʽ���ڣ�������һ���̶ȵľ�����䡣������ԭ���谭��λ�����˶������²���Ӳ�����Ӷ�������ѻ����ϵ�Ӳ��[16-17]�������ڦ�-Ti�Ͻ��У��ߵĹ�����������ʹλ�������Ƶķ���������ѣ��Ӷ�ʹλ���Ļ���ģʽ�Ӳ�״������ƽ�滬��ת�䣬�谭λ���˶��Ӷ������������ѧ����[18]������Ti-15Zrϵ�кϽ�Ϊ���͵Ħ�-Ti�Ͻ���ԭ����Ҫ��Ϊ��϶����ԭ�Ӵ����ڦ�-Ti�Ͻ��У�����ԭ���谭λ���˶�������λ������ЧӦ���������ǿ�������ң�������ͨ���γ�������С�����ķ�ʽ�������ѻ������У���������ǿ�����ã���Ӳ��Ҳ���������[19]��XPS�������֤����ԭ������γ���С��ZrO2��������С��������������谭λ���˶����ṩ����ǿ�����ã��Ӷ�����˲��ϵ���ĥ�ԡ�
��3 Ti-Zrϵ�кϽ��ά��Ӳ��
Table 3 Microhardness of Ti-Zr alloys


ͼ3 Ti-Zrϵ�кϽ��SEM��
Fig. 3 SEM images of Ti-15Zr alloys
��4��ʾΪTi-15Zrϵ�кϽ��ĥ��������ʧ��Ħ���������ɱ�4�ɼ���Ti-15Zr-0.86O�Ͻ���Ħ��ĥ��ʵ���е�������ʧ�����Ե���Ti-15Zr-0.72O�Ͻ�ģ�Ti-15Zr�Ͻ��������ʧ����ǰ���ߵ�3������˵������������߿��������������ϵ���ĥ���ܡ�������ֺϽ�Ӳ��������Ħ��ĥ���������������ڱ�ʵ��������Χ�ڣ�Ti-15Zr�Ͻ��Ӳ����ĥ��������ʧ�ʸ���أ�������Խ�ߣ�Ti-15Zrϵ�кϽ��Ӳ��Խ�ߣ���ĥ��Խ�á����⣬Ti-15Zr�Ͻ��Ħ�������߳��ܶ࣬��ͨ����Ϊ��Ħ�������ߵ�����������ĥ��һ�¡�ֵ��ע����ǣ�Ti-15Zr-0.72O�Ͻ��Ħ��������Ti-15Zr- 0.86O�Ͻ���Ըߣ�ԭ������Ħ��ĥ�������У���ż��Ͻ����֮���Ħ�������������£�ʹ��Ti-15Zr-0.86O�Ͻ�����γ�Ħ�������ϸߵ�������Ĥ��������Ĥ����ĥ�����ڻ���ģ����Ҳ����װ��䣬ʹ�������İ������ʸ�������
��4 Ti-15Zr�Ͻ�ĥ������Ħ������
Table 4 Weight loss and coefficient of wear of Ti-15Zr alloys

ͨ���ݿƲ�����������ĥ������У�ĥ��ĥ��ճ��ĥ��ƣ��ĥ�𡢸�ʴĥ��[20-21]��CORREA��[22]��ΪTi-15Zrϵ�кϽ���Ħ��ĥ��ʵ���У���Ҫ�Ƿ�����ĥ��ĥ���ճ��ĥ����ĥ�������ĥ����Ũ�Ȼ����ۻ������ڵ�λ�����ĥ���������������Ͻ��������������ӣ��Ͻ�������ڲ���Ӧ������������Ħ�����治�ϲ������Ա��Σ����Ͻ�����������ʧ������ģ����Һ�����£���ĥ��ĥ��Ϊ����������һ���̶ȵĸ�ʴĥ�����������ܵ���ʴ��������ʴ�����¹��۱��ضѻ������IJ��ϱ�����ɶ��ױ�ĥ������ĥ���븯ʴ����������£��Ӷ��Ӿ������ʧ[23]��ͼ4(a)��ʾΪ��̬Ti-15Zr�Ͻ�Ħ��ĥ����������ò�������д������繵�Ͱ��ӣ������˾��ҵ����Ա��Σ��д�����ĥ�������������������Ҫ��ճ��ĥ���ĥ��ĥ��ͼ4(b)��ʾΪTi-15Zr-0.72O�Ͻ������ò�����������Ե��繵�����Ա��Ρ����Ա�����ճ��ĥ��ĵ���������������Ħ����������������ܵ���ѹ������������ŵ��ܵ��˼���Ӧ�����ӱ����ܵ�˺�����γɴ�Ƭ���䡣��ͼ4(b)�п��Կ����������Ա��β������繵�Ͱ����γɵİ��ӣ�Ti-15Zr-0.72O�Ͻ���ճ��ĥ���ĥ��ĥ��Ϊ����

ͼ4 Ħ��ĥ��Ʒ������ò
Fig. 4 SEM micrograph of Ti-15Zrwear track
ͼ4(c)��ʾΪTi-15Zr-0.86O�Ͻ������ò����Ʒ������Ҫ���Կ���һЩ����Ĺ���״���ۺ������İ���ĥ��������ij̶Ȳ����ԣ���Ϊ�⻬��˵�����Ա��γ̶Ƚϵ͡�Ti-15Zr-0.86O�Ͻ��ĥ��ʽ��ĥ��ĥ��Ϊ����Ti-15Zr-0.72O��Ti-15Zr-0.86O�Ͻ���ĥ��ĥ����̲�����ĥ�������ڱ����ܵ�ѹ��ʱ�����ӹ�Ӳ�����γ�Ӳ�ʲ㡣���������ߵĺϽ����Ӳ�ȸ��ߣ�ĥм���Դӱ�����䣬ĥм����֮��������繵Ҳ��Ƚ�dz�����Ҽ��������Ա��εķ��������Ի���Ч����ճ��ĥ��ķ�����������Ħ��ĥ���������ʧ��
ͼ5��ʾΪ��Ħ��ĥ����������������������ʵ��Ľ����������������ĥ�۱�������˹�����ϸ��(MG-63)��������������ʱ��Ϊ24 h����ͼ5�ɼ�������������ĥ�۱��涼�����д������˹�����ϸ����ϸ������״�����ã��Ҿ��кܺõĻ��ԣ�����ϸ������˿״α�㡣 ����ڱ���ֶ�����Բ��ϸ����Ti-15Zr�Ͻ���˵��Ti-15Zr-0.72O�� Ti-15Zr-0.86O�Ͻ�����ϸ����Ϊ���ͣ��ҳ���˿״α���ϸ�������϶ࡣ���͵�ϸ�������Բ�κ���Բ��ϸ�����ԣ������������ǿ�������dz�����α��������ϸ���˶���˵��ϸ�����״�����á��Ͻ�����������ĥм��������ϸ�����ԣ��ұ��������������������ԣ���������Ϊ����ҽ�ò��ϡ�

ͼ5 Ħ��ĥ�����MG-63ϸ��������ò��SEM��
Fig. 5 SEM micrograph of MG-63 cells on wear tracks
3 ����
1) ͨ������ԭ�Ϸ�ĩ�ı������÷�ĩұ��ķ����õ�Ti-15Zr-0.72O��Ti-15Zr-0.86O�Ͻ𣻲�����յ绡�����Ʊ�����������Ti-15Zr�Ͻ���Ϊ�Աȡ�
2) �������̬����������Ti-15Zr�Ͻ���������Ti-15Zr-0.72O��Ti-15Zr-0.86O�Ͻ��ά��Ӳ���д������ߡ���������Ԫ����Ϊ��϶����ԭ���ܲ�����ǿ�Ĺ���ǿ�����ã��γɵ�������С�������п���ǿ�����ã������Ti-Zr�Ͻ��Ӳ�ȡ�
3) ����������ܹ�����Ti-15Zr�Ͻ��Ħ��ĥ��������ʧ��Ti-15Zr-0.86O��Ti-15Zr-0.72O�Ͻ��������ʧԶԶ����Ti-15Zr�Ͻ�ġ���˵�������������Ti-15Zr�Ͻ�ı���Ӳ�ȣ�ʹ�ò�����ĥ��������������
4) ͨ��ϸ��ʵ�飬��֤��Ti-15Zr��Ti-15Zr-0.72O��Ti-15Zr-0.86O�Ͻ���ĥм��������ϸ�����ԣ�����������ҽ�ò��ϡ�
REFERENCES
[1] GEETHA M, SINGH A K, ASOKAMANI R, GOGIA A K. Ti based biomaterials, the ultimate choice for orthopaedic implants��A review[J]. Progress in Materials Science, 2009, 54(3): 397-425.
[2] PARR G R, GARDER L K, TOTH R W. Titanium: The mystery metal of implant dentistry. Dental materials aspects[J]. Journal of Prosthetic Dentistry, 1985, 54(3): 410-414.
[3] �� ��, ������, �� ��, ���к�, �ָ���. 3D��ӡTi6Al4V�ѺϽ�֧�ܵ���ѧ���ܼ�����������[J]. �й���ɫ����ѧ��, 2018, 28(4): 120-127.
LIU Chang, WANG Chen-yu, LIU He, WANG Zhong-han, LIN Gao-yong. Mechanical properties and biocompatibility of 3D printed Ti6Al4V titanium alloy stent[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(4): 120-127.
[4] BASSEVILLE S, CAILLETAUD G. An evaluation of the competition between wear and crack initiation in fretting conditions for Ti-6Al-4V alloy[J]. Wear, 2015, 328/329: 443-455.
[5] �� ��, �� ��, �����, ������. CP-Ti��Ti-0.2Pd�Ͻ������֯������ʴ�Ե�Ӱ��[J]. �й���ɫ����ѧ��, 2015, 25(4): 959-966.
LIU Bing, ZHOU Qing, QU Rui-feng, CHANG Wang-tao. Effect of microstructure on corrosion resistance of CP-Ti and Ti-0.2Pd alloy[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(4): 959-966.
[6] SCHIFF L J, GRAHAM J A. Cytotoxic effect of vanadium and oil-fired fly ash on hamster tracheal epithelium[J]. Environmental Research 1984, 34(2): 390-402.
[7] ALTUNA P, LUCAS-TAULE E, GARGALLO-ALBIOL J, FIGUERAS-ALVAREZ O, HERNANDEZ-ALFARO F, NART J. Clinical evidence on titanium-zirconium dental implants: A systematic review and meta-analysis[J]. International Journal of Oral and Maxillofacial Surgery, 2016, 45(7): 842-850.
[8] ITO A, OKAZAKI Y, TATEISHI T, ITO Y. In vitro biocompatibility, mechanical properties, and corrosion resistance of Ti-Zr-Nb-Ta-Pd and Ti-Sn-Nb-Ta-Pd alloys[J]. Journal of Biomedical Materials Research, 1995, 29(7): 893-899.
[9] IKARASHI Y, TOYODA K, KOBAYASHI E, DOI H, YONEYAMA T, HAMANAKA H, TSUCHIYA T. Improved biocompatibility of titanium-zirconium (Ti-Zr) alloy: Tissue reaction and sensitization to Ti-Zr alloy compared with pure Ti and Zr in rat implantation study[J]. Materials Transactions, 2005, 46(10): 2260-2267.
[10] GU Y W, KHOR K A, CHEANG P. In vitro studies of plasma-sprayed hydroxyapatite/Ti-6Al-4V composite coatings in simulated body fluid (SBF)[J]. Biomaterials, 2003, 24(9): 1603-1611.
[11] FU Y, BATCHELOR A W, YING W, KHOR K A. Fretting wear behaviors of thermal sprayed hydroxyapatite (HA) coating under unlubricated conditions[J]. Wear, 1998, 217(1): 132-139.
[12] ������, �����, ������. Mn������ҽ��Ti-Mo�Ͻ���֯����ѧ���ܵ�Ӱ��[J]. �й���ɫ����ѧ��, 2017, 27(9): 1902-1908.
WU Xiao-feng, YANG Hui-qi, WANG Chun-yu. Effect of manganese addition on microstructure and mechanical properties of Ti-Mo biomedical alloys[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(9): 1902-1908.
[13] LIM J Y, MCMAHON C J, POPE D P, WILLIAMS J C. The effect of oxygen on the structure and mechanical behavior of aged Ti-8 wt pct Al[J]. Metallurgical Transactions A, 1976, 7(1): 139-144.
[14] OH J M, LEE B G, CHO S W, LEE S W, CHOI G S, LIM J W. Oxygen effects on the mechanical properties and lattice strain of Ti and Ti-6Al-4V[J]. Metals and Materials International, 2011, 17(5): 733-736.
[15] ����Ӱ, ����ɽ, Ǽ����. ������ٳ���Ti64.52Fe29.32Zr5.86Y0.30ҽ�úϽ���֯������[J]. �й���ɫ����ѧ��, 2018, 28(3): 474-482.
HAN Li-ying, WANG Cun-shan, QIANG Jian-bing. Microstructure and properties of Ti64.52Fe29.32Zr5.86Y0.30 biomedical alloy produced by laser rapid prototyping[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(3): 474-482.
[16] HEINTZE S D, ROUSSON V. Survival of zirconia- and metal-supported fixed dental prostheses: A systematic review[J]. International Journal of Prosthodontics 2010, 23(6): 493-502.
[17] OBERSON P G, WYATT Z W, ANKEM S. Modeling interstitial diffusion controlled twinning in alpha titanium during low-temperature creep[J]. Scripta Materialia 2011, 65(7): 638-641.
[18] WILLIAMS J C, SOMMER A W, TUNG P P. The influence of oxygen concentration on the internal stress and dislocation arrangements in ��-titanium[J]. Metallurgical Transactions 1972, 3(11): 2979-2984.
[19] YU Q, QI L, TSURU T, TRAYLOR R, RUGG D, MORRIS J W JR, ASTA M, CHRZAN D C, MINOR A M. Origin of dramatic oxygen solute strengthening effect in titanium[J]. Science, 2015, 347(622): 635-639.
[20] K��BARSEPP J, KLAASEN H, PIRSO J. Behaviour of TiC-base cermets in different wear conditions[J]. Wear, 2001, 249(3): 229-234.
[21] ZHOU Y, ZHANG Q Y, LIU J Q, CUI X H, MO J G, WANG S Q. Wear characteristics of a thermally oxidized and vacuum diffusion heat treated coating on Ti-6Al-4V alloy[J]. Wear 2015, 344: 9-21.
[22] CORREA D R N, KURODA P A B, GRANDINI C R, ROCHA L A, OLIVEIRA F G M, ALVES A C, TOPTAN F. Tribocorrosion behaviorof ��-type Ti-15Zr-based alloys[J]. Materials Letters, 2016, 179: 118-121.
[23] ֣����, �����, ��ΰ��. Hank��sģ����Һ��Ti-25Nb-3Mo-3Zr-2Sn��Ti-2.5Al-3Mo-2.5Zr�Ͻ��ĥ����Ϊ[J]. �й���ɫ����ѧ��, 2016, 26(6): 1222-1227.
ZHENG Zi-qin, WANG Zhen-guo, HUANG Wei-jiu. Micro-scale wear behavior of biomedical material Ti-3Zr-2Sn-3Mo-25Nb and Ti-2.5Al-3Mo-2.5Zr alloy in Hank��s solution[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(6): 1222-1227.
Influence of oxygen on grindability of Ti-15Zr-based alloy as dental material
TANG Han-chun1, LIU Yong1, ZHAO Da-peng2, CHENG Wen-juan1
(1. State Key Laboratory for Powder Metallurgy, Central South University, Changsha 410083, China
2. College of Biology, Hunan University, Changsha 410082, China)
Abstract: Clinical Ti-Zr alloys still have the problem of insufficient wear resistance, which limits its further development in the dental field. Therefore, the wear resistance can be improved by introducing oxygen into the Ti-Zr alloy. In this work, Ti-15Zr-0.72O (mass fraction, %) and Ti-15Zr-0.86O alloys were prepared with the method of powder metallurgy. Ti-15Zr was prepared by arc-melting. The effect of oxygen content on the mechanical properties of Ti-15Zr alloys was studied. The Vickers hardness of Ti-15Zr-0.8O reaches 449.9 MPa, which is 8% higher than Ti-15Zr-0.7O, and 76%higher than Ti-15Zr. The tribological behavior of sintered composites was studied in artificial saliva solution. Ti-15Zr-0.86O hardness weight loss and surface peeling than Ti-15Zr-0.72O. Both of their weight losses are less than that of Ti-15Zr. The results show that the hardness and wear resistance of Ti-15Zr alloys are significantly improved by adding oxygen.
Key words: Ti-Zr alloy; powder metallurgy; oxygen solute; Vickers hardness; wear resistance
Foundation item: Projects(5162500387, 51604104) supported by the National Natural Science Foundation of China
Received date: 2018-08-26; Accepted date: 2019-05-08
Corresponding author: LIU Yong; Tel: +86-731-88876630; E-mail: yonliu@csu.edu.cn
(�༭ ��ѧ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(5162500387��51604104)
�ո����ڣ�2018-08-26�������ڣ�2019-05-08
ͨ�����ߣ��� ӽ�����ڣ���ʿ���绰��0731-88876630��E-mail��yonliu@csu.edu.cn