DOI: 10.11817/j.ysxb.1004.0609.2021-36603
�ܶ������ȡ���Ķ������������о���չ
�˾��1, 2, 3, 4���� ��1, 2, 3, 4���� ��1, 2, 4���½���1, 2, 3, 4���� ѧ1, 2, 4
(1. ���пƼ���������˾ ����ұ����ҹ���ʵ���ң����� 101407��
2. ������Դ���������о�Ժ(����)����˾������ 101407��
3. ������ɫ�����о���Ժ������ 100088��
4. ���й��̼����о�Ժ����˾������ 101407)
ժ Ҫ������ȡʵ���з��֣��ܻ�������ȡ������������������Լ����ȡұ���Ӧ�úͷ�չ�������������ȡ��ϵ������ȡ�ķ�չ��״����ϸ�����������ȡ��ϵ���ܵ������Ͷ�����Ϊ���������ͨ���Աȷ��������ڰ��Խ�����Һ��ϵ�������ȡ��ϵ�µĻ�ѧ���ʼ���Ϊ�������ܶ������ȡ������������ԭ���ڴ˻����ϣ��ص������л�������л�����������ȡ��ϵ���ܵĶ�����������Ϊ���������������л�����/���Э����ϵ�¶��������Ƶ�ԭ��ָ����ǰ���ܶ������ȡ���������������о�������ڵ������벻�㣬չ��δ���������д������о��ķ����뷽����Ϊ�ܶ������ȡ����������Ľ���ṩ���������ݺ�ָ������
�ؼ��ʣ������ȡ�����ܵ���ȡ���������л�����ƻ���
���±�ţ�1004-0609(2021)-07-1922-11���� ��ͼ����ţ�TF111���� ���ױ�־�룺A
���ĸ�ʽ���˾��, �� ��, �� ��, ��. �ܶ������ȡ���Ķ������������о���չ[J]. �й���ɫ����ѧ��, 2021, 31(7): 1922-1932. DOI: 10.11817/j.ysxb.1004.0609.2021-36603
DENG Jing-xian, WU Biao, SUN Qi. Research progress of poisoning and inhibition of cobalt to hydroxyoxime extractant and its inhibition[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(7): 1922-1932. DOI: 10.11817/j.ysxb.1004.0609.2021-36603
����һ��ս���Կ����Դ�����Ʊ����ºϽ�Ӳ�ʺϽ𡢷����Ͻ𡢴��ԺϽ��Լ��������ε���Ҫԭ��[1]���㷺Ӧ������Ϣ���������պ��졢����ҽҩ������Դ����������[2-3]������Ȼ���У�����Ҫ��ͭ�����İ�����Դ��ʽ���ڣ���ͭ�ܰ��������ܰ�����ȣ������ܿ��K��[4]������������������Դ��ء�������Ϣ��ҵ������Ŀ��ٷ�չ���������������������˴������ܷ��ϣ�����Ŀǰ��һ��Ҫ����Դ���������⸳��״̬����ͨ����Ϊͭ�����Ƚ�����ұ������Ʒ����ȡ�����Ի�-ʪ����ϡ�ȫʪ����������Ϊ�����ܼ���ȡ���������е���Ҫ���ڡ��ܼ���ȡ��ͨ�����ý���������ͬһ���еķ���ϵ����ͬ�����ﵽ����Ŀ��һ�ַ��뼼��[5]����Ŀǰ��ҵ����õ���ȡ�ͷ��뷽��֮һ������ѡ���Ըߡ���ɫ��Ч���豸�����ڹ�ҵ���������ص�[6]���㷺Ӧ���ڽ����ķ���ͻ��ա�������ұ���У������仯ѧ�������ƣ��ڿ��й��������̶Ⱥܸߣ������Ѷȴ��ִ���ҵ��չ����������ұ���Ҫ��Ƚϸߣ�����ܼ���ȡ���õ��㷺��Ӧ�á�
�������ܵ���ȡ����Ҫ��������ȡ����������ȡ������������ȡ���ȡ����У������ȡ��������ȡЧ�ʸߡ�ѡ���������졢�ṹ�ȶ�����Ŀǰͭ����ұ�������Ӧ����㷺����ȡ��֮һ[7-8]�������ȡ��������ͬʱ�����ǻ�(��OH)��뿻� (��C=NOH)���������š�����뿻���̼ԭ���ϵ�λ�ò�ͬ���ɷ�Ϊ��-��뿺ͦ�-��뿣���뿻��ֱ��������ǻ����ڵĦ��ͦ�̼ԭ���ϣ�����LIX63(5,8-���һ�-7-�ǻ�-6-ʮ������)��LIX84(2-�ǻ�-5-�ɱ�����ͪ�)������ȡ�������������������λ�ֱ��γ���Ԫ������Ԫ��������ڦ�-��뿣���-��뿺ͽ���������λʱ�ռ�λ���С���γ����ϻ��Ļ�������Ҳ��С������ͺ�����ȶ����Խ������ӵ���ȡ������ǿ��Ӧ�����Ƹ����ԡ���-�����Ҫ��Ϊ��ͪ�(��LIX84)����ȩ�(��LIX860��2-�ǻ�-5-ʮ����ˮ��ȩ�)������ȡ�������У���ͪ���ȡ������������Լ��ѡ������γɵ����൫��ȡ���������ص㣻��ȩ���ȡ��������ȡ�������졢��ȡ�ٶȽϿ졢��ȡ�����ʽϸߵ����ͽ��ѵ��ص�[9-10]��
��ҵ�ϣ�ͨ������ͪ뿺���ȩ���һ��������ϣ��Ӷ��ﵽ��ѵ���ȡЧ����Ȼ���������������ȡ����ȡ��Co2+��Һʱ��Co2+����ȡ�����л�����������ȡ���γ�һ�ַdz��ȶ��������ͺ����ʹ���ü�Ϊ���̵�������Ҳ���ѽ�����ȫ���ͳ��������ܶ������ȡ�������˶���[11]��������ȡ����ѭ��ʹ�ã������л��������ۻ���������ȡ������ȡ�������ؽ��ͣ��谭��ȡ�������С���ˣ���ξ�����Ч����ܶ������ȡ���Ķ����ǵ�ǰؽ���о��Ĺؼ����⡣
1 �����ȡ��ϵ���ܵ���ȡ�������о���״
1.1 �����ȡ����ȡ�ܵ��о���״
�����ȡ����ͭ��������ȡ�������������ȡ�����з����Ľ����乤ҵ��Ӧ�ã�ѧ���dz��Խ��������ܵ���ȡ�ͷ��룬������Һ���ʺ���ȡ�����������濪չ����о���һ���棬��Һ������ϵֱ��Ӱ���ܵ����״̬������Ӱ������ȡ��Ϊ����ͬ��Һ��ϵ���ܵ����״̬��ͬ����ȡ��Ӧ���̺ͻ���Ҳ������ͬ[12]��Ŀǰ����ҵ�ϳ���������Һ������ϵ��Ҫ��������ϵ����(�)����ϵ��������ϵ�ȣ����о���༯����������ϵ����һ���棬�����ȡ���Ľṹ���ﻯ���ʵ����ؾ���������ܵ����������ϴ�Ӱ�죬Ŀǰ�������ȡ�����ɦ�-������-��뿹��ɡ�
��20����70�����ѧ�����ձ���æ�-�����ȡ��(��LIX63)��ȡ����������Һ�е��ܡ�RENNINGER��[13]����LIX63��������Һ����ȡ�ܣ���������ȡ�¶�Ϊ25 �桢���O/A(�л�����ˮ�����֮��)Ϊ1:1��pHֵΪ5.5�������£��ܵ���ȡ�ܿ�ﵽƽ�⡣CHENG��[14]����LIX63�Ӻ�ͭ���ܡ�п������Һ�з�����ʱ���֣���40 �桢���O/AΪ1:1�������£�������ȡƽ��pHֵ�����ߣ���ȡ�ʳ��������ƣ���ƽ��pHֵΪ7.0ʱ���ܵ���ȡ�ʿɴﵽ98%��BARNARD��[15-16]�ڲ���LIX63��ȡ��ʱ���֣�����ȡ�����ȶ��Խϲ��ϵ�¶Ƚϸ�ʱ���ڽ��⣬��LIX63��Co2+��ѡ�����ܽ�ǿ������ij��˾��LIX64N(LIX63��LIX64�Ļ�ϣ�LIX64��2-�ǻ�-5-ʮ�����������ͪ�)��ȡ�������ܽ������о���������10% LIX64N�������£�������ȿ�������ܵ���ȡЧ��[12]��ͨ�������о����֣���Ȼ��-�����ȡ�����ܾ��н�ǿ����ȡ�ͷ������ܣ������ȶ��Խϲ������ǿ���¶Ƚϸߵ����������ڷֽ⡣���LIX84��LIX860�Ȧ�-�����ȡ���ܵ��㷺��ע��ZHANG��[17]�о���LIX860��ȡ��ϵ����������ȡ�������ܣ�ͨ����ȡƽ�����߷��֣�����ȡ�����ܾ���һ����ѡ���ԣ���20% LIX860(�������)���¶�Ϊ25 �桢���O/AΪ1:1��ƽ��pHΪ5�������£��ܵ���ȡ�ʴﵽ90%���ϡ�HUTTON-ASHKENNY��[18]����LIX860��ȡ��ʱ���֣����¶�Ϊ40 �桢pHΪ6.1ʱ���ܵ���ȡ�ʿɴ�90%���ϡ��װ��ɵ�[19]����LIX84��ȡ�Ͼ�﮵���������Բ��ϵ��������Һʱ���֣��ܵ���ȡ����LIX84������������ӳ��������ơ������б��������-�����ȡ����ȣ���-�����ȡ�������ṹ���ȶ����Ҷ��ܵ�ѡ���Ը�ǿ�����⣬ѧ���ǻ������о��������ȡ��ϵ���ܵ���ȡ��Ӧ���Ƽ��ͺ�����λ״̬��һ����Ϊ1��Co2+��2�������ȡ�����ӷ�����λ��Ӧ����Co(HL)2�������ȡ���з��ǻ��е���ԭ�Ӻ�뿻��еĵ�ԭ�Ӳ���Co2+��λ���γ�ƽ������λ�ṹ(��ͼ1)����ȡ��Ӧ��ʽ(1)��ʾ������HL��ʾ�����ȡ��[20-21]��
Co2++2HL(o)=CoL2(o)+2H+ (1)
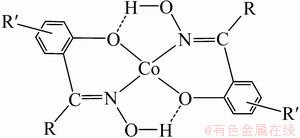
ͼ1 ���������ȡ����λ�ṹͼ[20-21]
Fig. 1 Coordination structures of cobalt with hydroxyoxime[20-21]
���������ȡ����ȡ�����ܵ��о����в��ٱ������ڶ��о�������������ȡ�����ܾ��нϺõ�ѡ�����ܣ��������ܵ���ȡ���롣Ȼ���������о������ڶ������ȡ��ϵ���ܵ���ȡ���ʵ�̽����ȱ������ȡ����ȫ����ϵͳ�о����ܶ������ȡ������������δ�������㹻�����ӡ������������������ȡ����ͭ������ȡұ��ҵ�еĴ��ģӦ�ã�������������ͻ����
1.2 �ܶ������ȡ��������������о���״
ΪŪ���ܶ������ȡ������������ԭ������ѧ�߽����ڵ绯ѧ���ۺ���λ��ѧ���۵ȣ�Χ��Co2+�������ȡ���еĻ�ѧ��Ϊ�仯�Ϳռ���λ�ṹ�������濪չ�����о���ȡ����һЩ���Գɹ����������ܶ������ȡ������������ԭ��ѧ���Ƿ��ְ����ӻ������ȡ����Co2+��λ���߱��ֳ����ƵĻ�ѧ��Ϊ����ˣ����������������Բ��ջ�Աȷ�����
1.2.1 ���������ȡ���еĻ�ѧ��Ϊ
����1981�꣬GUESNET��[22]������LIX65N (2-�ǻ�-5-�ɻ�������ͪ�)��ȡCo2+ʱ�ͷ��֣�Co2+��Ը������ȡ�����������������������Dz������������Աȷ��ͻ�ԭ���ȶ�Co2+�������ȡ���л�ѧ״̬����Ϊ�����о������֤ʵ��Co2+�������ȡ���з����������Ҹ���������������е�O2�йء���ʤ����[23]��ʹ��LIX84�Ӱ�����Һ����ȡͭ����ʱ���֣���ͬʱҲ�ܱ���ȡ����Co2+��LIX84�γɵ��ͺ��ﲻ�ȶ����ܱ�Ѹ���������γɷdz��ȶ���Co3+�ͺ�������Է��ͣ�Ӱ����ȡ���ļ���ʹ�á�Ϊ��ֱ���������ʶCo2+�������ȡ���е��������̣�NISHIHAMA��[24]���õ��ӹ������о���Co2+��LIX84�е�������Ϊ���Ա�����Ϳ��������������ͺ���ĵ��ӹ������֣���������µ��ͺ�����Co2+���������塣ͨ�������������������ʧ��ת������Co3+�ļ�壬֤����Co2+���л����б�O2����ΪCo3+����Co2+����������������ϣ�����������Co3+�γɳ��������(��ʽ(2)��ʾ)�����ֳ�������������һ��Co2+��ϣ��γɦ�-���������(��ʽ(3)��ʾ)��
Co2++O2��Co3+��O��O�� (2)
Co3+��O��O��+Co2+��Co3+��O��O��Co3+ (3)
Ϊ�˽�һ���о�Co2+�������ȡ���е��������̣��ӵ绯ѧ�ǶȽ�һ����֤��������Ӧ�����Ŀ����ԣ�ѧ���Ǵ�Co2+�ľ�����Һ��ѧ�������֣��������л���ϵ���ɡ��ӵ绯ѧ�Ƕȶ��ԣ�Co2+�������ȡ����λ�������Ĺ��̱��������ڵ绯ѧ��Ӧ���������ṹ��Ӧ��������λԽ�ͣ�Խ���ױ���������ˮ��Һ�У�Co2+��������λ����Һ���������й�ϵ����ˮ��Һ��Co2+��������λΪ 1.8 V������Һ��������ν��ʺ�Co2+��������λ����0.17 V�����Co2+�ڰ��Խ�����Һ����������ΪCo3+��������һ���ʣ�������[25-26]����ѭ���������о���Mextral 84H(��2-�ǻ�-5-�ɱ�����ͪ�Ϊ��Ч�ɷ�)��ϵ��Co2+�ͺ����ѭ���������ԣ�������ܵ�������ԭ��λ��ͨ���ԱȲ�ͬ������ϵ��Co2+��������λ��֤����������Ӧ���Է����̡���ͬ������ϵ��Co2+��������ԭ��λ���1��ʾ��
��1 ��ͬ������ϵ��Co2+��������λ
Table 1 Oxidation potential of Co2+ in different media

ͨ���о�Co2+�������ȡ���еĻ�ѧ��Ϊ�����ǶԶ����������˽�Ϊ��������ʶ����Co2+�����л�����������ȡ���γ�ƽ������λ�ṹ�����������е�O2Ѹ������ΪCo3+���������ȡ�������γ��˷dz��ȶ����ͺ����ʹ���ü�������Ҳ���ѽ�����л����з��ͳ�������ˣ�����ǰ���ͺ������ʺ���λ״̬��Ϊ̽������ԭ��Ĺؼ���
1.2.2 �����ȡ��ϵ�����ͺ�������ʼ���λ�ṹ
Ϊ�˽�һ�����۽Ƕ�ȫ����ʶ�ܶ������ȡ������������ԭ���üۼ����ۺ��ӻ����۴��۷��Ӳ���������ȡ��ϵ���ܵ�������λ����λ״̬���ռ�ṹ���ӻ���ʽ�����о��Ե���Ϊ��Ҫ��

ͼ2 ��ͬ�ӻ���ʽ��Co2+�����������Ų�
Fig. 2 Outermost electron arrangement of Co2+ under different hybridization methods
Co2+�����������Ų�Ϊ3d7���䳣�����ӻ���ʽΪ����λ��sp3�ӻ�������λ���ڹ���d2sp3�ӻ�������λ�������sp3d2�ӻ��������ӻ���ʽ��Co2+���������Ų���ͼ2��ʾ[25]��Co2+����Һ�е���λ���ӻ���ʽ����λ����������ʴ��ڽ��ܵĹ������ۼ�������Ϊ����λԭ�ӵĵ�ɶ�Co2+����λ������ṹ�нϴ��Ӱ�죺һ���棬������������λԭ�ӵĵ縺�����ϴ�ʱ����������������λ�������sp3d2�ӻ��������ӣ�������������λԭ�ӵĵ縺������Сʱ������������������λ���ڹ���d2sp3�ӻ���������ӡ���һ���棬����λ���ĸ�����������±�����ӵȲ�����λʱ���ر���������������λ��sp3�ӻ���������[27]������λ��sp3�ӻ�������λ���ڹ���d2sp3�ӻ�����Ϊ�ȶ�����һ�������������ת����
���ݾ�����Һ��ѧ���ۣ����Ƿֱ�õ�Co2+��Co3+�ڴ�ˮ�Ͱ��Խ�����Һ�е���ϲ�����״̬���ӻ���ʽ���ڴ�ˮ��Co2+����λ��ʽΪ[Co(H2O)6]2+���������λ����ԭ�ӵĵ縺�Խϴ����ӻ���ʽΪ�����sp3d2�ӻ��������ӻ���ʽ������Co2+��4d��������ԳɶԵ��ӣ����������幹������ȶ����ܵ�������λΪ1.8 V���ڰ��Խ����У�����ҺpH��7ʱ����Һ����NH4+Ϊ�������Ѳ�����λ��Co2+�����״̬��ˮ��Һ�����ƣ���pH��8ʱ������̬��NH3Ũ�ȼ������ߣ�Co2+��������NH3�γ������[Co(NH3)6]2+���ýṹ���ȶ�����Ϊ1.3��105���ڿ����м��ױ�����������[Co(NH3)6]3+�����������ɵ��������ȶ�����Ϊ4.5��1033 [28-29]���������������ԭ����Ҫ�ǣ�����Һ����NH3����ʱ��Co2+����λ��ʽΪ [Co(NH3)6]2+��������λ�ĵ�ԭ�ӵĵ縺�Խ�С�����ӻ���ʽΪ�ڹ��͵�d2sp3�ӻ��������ӻ���ʽ��Co2+��4d���ֻ��һ�����õŵ��ӣ����ױ�������ʧȥ����ʱCo2+��������λΪ0.17 V[30]����ˣ��ӻ���ʽ�������ͺ�����Co2+��������λ�������л�����������Ϊ����λ״̬���ӻ���ʽ֮��Ҳ�������ƵĹ�������ͬ������Һ��ϵ��Co2+��������λ���ӻ���ʽ���2��ʾ[31]��
��2��ͬ������ϵ��Co2+��������λ���ӻ���ʽ
Table 2 Oxidation potential of Co2+ and coordination and hybridization mode of complex under different coordinations

���������ۺ��о������ϣ�HUTTON- ASHKENNY��[18]�о���Co2+��LIX860�Ķ�����Ϊ��ͨ��ʵ�������Ʋ⣬Co2+���л������γ���Co+LIX8602�ͺ�����ͺ���Ϊ����λ��ƽ���ı��νṹ��O2��������������λʹ��Co2+�����������ý���ȱ����Ӧ������֧�š�NOMBONA��[32]����ܵ�������λ��С������λ�ṹ���ӻ���ʽ�йء�������[26]ͨ����Mextral 84H���ܵ��ͺ������ѭ������ɨ�衢����-�ɼ����������������������л�����Co2+��������λΪ0.29 V�����Mextral 84H���ܵ��ͺ�����ɺ���λ�ṹ�о����Ʋ�Mextral84H��Co2+�γ�������λ�İ�����ṹ�����ӻ���ʽΪ�ڹ���d2sp3�ӻ�����λ���ͺ����е�Co2+�����ױ�����ΪCo3+���ͺ������ܵ�4d����ĵ���������ʧȥ���ͺ�����Co3+��3d��4s��4p���������ȫ��״̬�����ȶ��������sp3d2�ӻ���������ǿ��������Խ�Co3+��Mextral 84H�з��ͳ��������¶����IJ�����
Ŀǰ��ѧ����ͨ���������ȡ��ϵ��Co2+������Ϊ��һϵ��ʵ���о�����Co2+���л����е����������ѳ�����ɹ�ʶ������Co2+�������ȡ�������������Լ��������γɷdz��ȶ��ͺ����ԭ����Ȼ��ѧ�߸�����λ��ѧ�ͽṹ��ѧ��������˿��ܵĻ��ƣ������ѧ����Ҫ�����ڶ��������������о�����δ��ѧ�߶�����ǰ�����ͺ�����ﻯ���ʼ��ȶ��Բ������ϵͳ�о������������ȡ���γ��ͺ������λ״̬���ռ�ṹ�ͼ���״̬����Ҫ��һ����ȷ��
2 �л���������ϵ������ȡ������Ӱ����о���״
Ϊ����Ч����ܶ������ȡ���Ķ������⣬������ѧ�ߴӺ�����Һ�������ϵ�����������֣��Զ�������չ��������о���һ���棬ͨ��������Һ�м���縺�Խ�ǿ�����壬ʹ���γɽ�Ϊ�ȶ��������������Ա����������ȡ���У��Ӷ����ⶾ���IJ�����MACKENZIE��[33]����LIX84�Ӱ��Ժ����������Һ����ȡ��ʱ�����ð�������Co2+���������γ��ȶ����������ԣ����ڽ���ܶ�LIX84���������⡣Ȼ��������ȡ�������й����з��֣���������Һ����Ȼ��������Co2+����������һͬ����ȡ�����л��࣬������������������Ҫ�Զ������л�����к������������ԴӸ����Ͻ�����⡣��һ���棬ͨ���������ȡ��ϵ���������Ƽ����Ӷ������ܶ������ȡ���Ķ������÷�����Ŀǰ������ѧ���о�����Ҫ�����γ�һЩ�����о��ɹ������о����֣��л�������벻���ܹ���Ч�����ܶ������ȡ���Ķ�������ɵĶ�Ԫ��ȡ��ϵ�����ܲ���Э��ЧӦ����������ȡ�����ܵķ������ܺ���ȡЧ��[34]��
���������л���/���Эͬ��ȡ��ϵ���ܷ��������Ӧ�õõ��˹㷺�Ĺ�ע��һ����Ϊ���ܱ������ȡ�������л�����������ȡ����λ�γ�ƽ������λ�ṹ����ʱ������Co2+����λ����δ�ﵽ���ͣ�ˮ����Ҳ�п��ܲ�����λ���γ��˺�ˮ���ͺ���Co(HL)2��2H2O�����ͺ��������Խϲ����ȡ��ϵ�������л�����л���ȡ�����ͺ����е�ˮ���ӣ��Ӷ�������ͺ������ˮ�ԣ�������Э��ЧӦ�����ܵ�ѡ������ǿ[35]�������л���IJ��죬Э����ϵ�ɷ�Ϊ�л�����/���Э����ϵ���л����/���Э����ϵ������Э����ϵ��ͬ�����ܵ���ȡ������ ͬ���л���������ȡ���ܵĶ������ƻ���Ҳ����ͬ[36]��
2.1 �л�����/���Э����ϵ
�л�����/���Э����ϵ��Ҫ��Ϊ�л�����/��-�����ϵ���л�����/��-�����ϵ�����ڦ�-������-���֮����ڽϴ�Ļ�ѧ���ʲ��죬ʹ��������ϵ��Co2+����ȡ�����Ͷ������ƻ�����ͬ��
2.1.1 �л�����/��-���Э����ϵ
19����70�����FLETT��[37-38]��Versatic 10/LIX63��P507/LIX63��������/LIX63��ʮ������/ LIX63��Э����ϵ�н���ϵͳ�о����������������Э����ϵ�Զ��۽��������ܲ���������ЭͬЧӦ��ʹ������ܵ�ѡ���Դ����ߣ���ͨ�����������֣����ͺ���Ϊ�������������LIX63뿻������ŵ�ԭ�����ӻ�ʹ���ܷ��ͱ�����ѡ�JONES ��[39]����Versatic 10/LIX63��ϵ��ȡ�ܣ���һ����ȡ���ܵ���ȡ�ʱ�ɴﵽ96%���ϡ���ϼ��[40]����б�ʷ���Versatic 10/LIX63Э����ϵ��Co2+����ȡ��Ϊ�����о����õ��ͺ����н������Ӻ���ȡ���Ļ�ѧ������Ϊ1:2:2���ͺ���Ľṹ����ΪCo(HL)2(HA2)2 (HA��ʾVersatic 10)��ZHU��[41]�о���Versatic 10/LIX63��ϵ���ܵ���λ�ṹ���Ʊ����ͺ��ᄃ�壬������XRD�Ծ�����б�����֤ʵ���ͺ���ΪCo(HL)2(HA2)2�İ�����ṹ��BARNARD��[42]����Versatic 10���ºϳɵ������ȡ��(1-�ǻ�������)-����ͪ���ɵ�Э����ϵ��ȡ�ܣ�ͨ������������㣬�ó���ȡ���ͽ��������γɵ��ͺ���Ļ�ѧ������ͬ��Ϊ1:2:2���˺�D��ALESSIO��[43]���ø������ȡ�����춡����ɵ�Э����ϵ��ȡ�ܣ��ɹ��Ʊ����ܵ��ͺ��ᄃ�壬��ͨ��X��������������ͺ���Ľṹ�������ڸ���ϵ���ͺ������ʽΪCo3(L-H)4(O2CC3H7)2���ڸ��ͺ����У�����Co2+Ϊ��������λ�ṹ��������λ����N2O4����������Co2+��λ��λΪ5��������λ����NO4���������ͺ���Ľṹ���ӣ�������ȷ��������ȡ���ǻ������ӵ�ȥ������Co2+������λ��ʽ���ͺ����бȽϳ�������������λ��ʽ�У�������λ������Ϊ�����ӵ�ȩ뿺�һ���ӵ���������������ȩ��ϵ�N2O2���棬������������λ��ƽ�涥�ˣ��γ������Ŀռ�ṹ��
��������ȡ��Ϊ�ͻ����о������ϣ�CHENG[44]������Versatic 10/LIX63��ȡ��ϵ�������������Һ����ȡ����ʱ���֣�Versatic 10�ļ����ܹ������ܶ�LIX63�Ķ��������л������ܵĸ���ʱ��Ϊ 76 hʱ����һLIX63��ϵ���ܵķ����ʽ�Ϊ29%����Э����ϵ���ܵķ����ʴﵽ99%���ϡ�ͨ����ȡ������ʵ���ƶϣ���Versatic 10/LIX63Эͬ��ϵ�У�������ȡ���γ���Co2+-Versatic 10-LIX63���ͺ������Versatic 10��Ϊ��ȡ��ʱ��LIX63ΪЭ�ͼ�������Ӳ���Co2+����λ�����û�в�������������[13, 15]�з��֣���ȻVersatic 10��LIX63����ʱ�Ķ������нϺõ��������ã�������LIX63�ṹ�ȶ��Խϲ��ҵӦ�ý��٣������Զ������о����٣���δ�����Ϊϵͳ�Ķ������ƻ��ơ�
2.1.2 �л�����/��-���Э����ϵ
�л�����/��-���Э����ϵ���ܼ���������Э��ЧӦ��JOO��[45]��Versatic 10/LIX84-I��ϵ��Э�����ܽ������о���������ͬ���������뵥һ��ϵ��ȣ���LIX84-I�м���Versatic 10������߸���ϵ���ܵ���ȡ������HUTTON-ASHKENNY��[18]�Ե�һLIX860�͵��͵��л���/LIX860��ϵ��ȡ�ܽ����о����֣��뵥һLIX860��ϵ��ȣ�Versatic 10�ļ��벢û����������ܵ���ȡ�ʣ��Զ����������������ޡ�����[25]���õ����л���/ Mextral84H��ϵ�о����ܵ���ȡ����������ȡ���������ƣ����������Versatic 10/Mextral84HЭ����ϵ���ܼ���û��Э��ЧӦ��Versatic 10û�в���Mextral84H��Co2+����λ�����δ�����ƶ������ͺ���Ŀռ�ṹ���ӻ���ʽ�뵥һMextral84H��ϵ����λ�����ͬ�������ķ���ʽΪCo(HL)2��2H2O (��ͼ3)��
�����л�����/��-���Э����ϵ��ȡ��ʱ���л����Ტ�������ܵ���ȡ������ȡ��Ӧ���̺ͻ����뵥һ�����ȡ����ϵ���ƣ����������ܶ������ȡ���Ķ������⡣
2.2 �л����/���Э����ϵ
�л����/���Э����ϵ���ܱ��ֳ���ǿ��ЭͬЧӦ��Ŀǰ����Ը���ϵ���о�������л����/ LIX84���л����/LIX860Ϊ����ZHANG��[17]����P204/LIX860��ϵ��������Һ�е�����������ȡ�о�������������뵥һ�����ϵ��ȣ�Э����ϵ���ܵ�pH50(ָ������ȡ��Ϊ50%ʱ��Ӧ��ƽ����ȵĴ�С)������ЭͬЧӦ�����ƶ���0.89��pH��λ�����ܵ���ȡ�ͷ������ʺܿ죬3 min�ڼ����Դﵽƽ�⡣WANG��[46]����Cyanex 301/LIX63��ϵ��ȡ�������֣�����ϵ�ܺõ���ǿ���ܵ���ȡ��
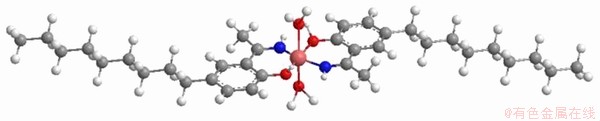
ͼ3 Versatic 10/Mextral 84H��ϵ�����ͺ�����ܵĿռ�ṹ
Fig. 3 Possible spatial structure of cobalt extract with Versatic 10/Mextral 84H
HUTTON-ASHKENNY��[18]�о���LIX860��P204/LIX860��P507/LIX860��Cyanex 272/LIX860��Versatic 10/LIX860��ϵ���ܶ�LIX860�Ķ����������������������л����ܹ�����Co2+�������ȡ���Ķ��������Խ�ǿ���л���Զ���������Ч�����ã�����Ч���ɴ�С����ΪP204��Cyanex 272=P507��Versatic10��ͨ��ʵ�����Ʋ⣬��һLIX860��ȡCo2+ʱ���γ�������λ��ƽ���ı��νṹ���ͺ����P204�������ȡ��ϵ������P204���м�ǿ����λ�����ڸ��ͺ����������λ���γ��˸��ȶ����ͺ������[25]�о��˵����л�����������Զ�����Ӱ�죬�������Ÿ���Co2+�л��ྲ��ʱ����ӳ�����һMextral84H��ϵ���ܵķ��������Խ��ͣ���P204/Mextral84H��P507/Mextral84H��Cyanex 272/Mextral84H��ϵ���ܵķ����ʽ������͡�������ܶԵ�һMextral84H��ϵ���Բ����˶�������P204��P507��Cyanex 272�������ܹ���Ч���ƶ������������Ũ�ȵ����ߣ��Զ���������Ч������ǿ�����SUN��[26]ͨ���绯ѧ�����ȷ����Ե�һMextral84H��P204/Mextral84H��Versatic 10/Mextral84H��Cyanex 272/Mextral84H��Э����ϵ��Co2+����ȡ�������о���������P204/Mextral 84H��ϵ�У�����P204Ҳ����Co2+����λ��ȡ����ԭ�������H2O��λ�ã����ӻ���ʽ��d2sp3�ӻ���������λ���ߵ�sp3d2�ӻ�ת������������˶����������ķ���ʽΪCo(H2B2L2)(��ͼ4[26]������ʽ��HB��ʾP204)��P204�����ܶ�Mextral84�����Ĺ�����ͼ5��ʾ[26]��
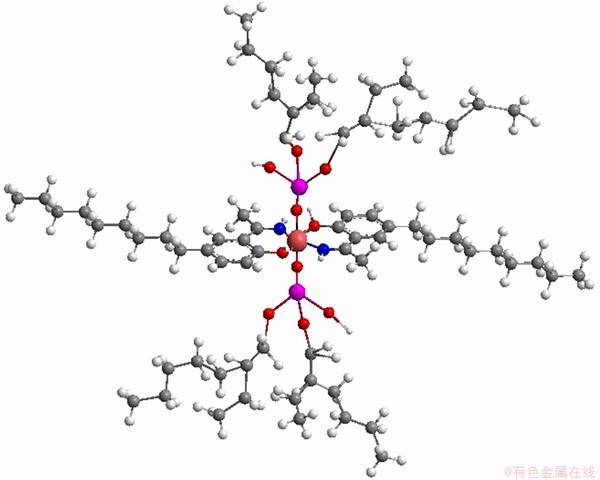
ͼ4 P204/Mextral 84H��ϵ�����ͺ�����ܵĿռ�ṹ[26]
Fig. 4 Possible spatial structure of cobalt extract with P204/Mextral 84H[26]
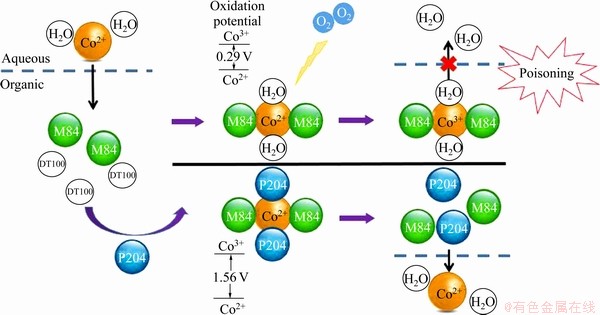
ͼ5 P204�����ܶ�Mextral 84H����ʾ��ͼ[26]
Fig. 5 Schematic diagram of P204 inhibiting cobalt poisoning on Mextral 84H[26]
����������ͨ�������л��������ƶ���ʱ���л���Ҫ�н�ǿ�����Ժ���λ���������Բ����ܵ���λ��ʹ���ͺ�������ȶ�����λ���ӻ���ʽת�䣬�������Co2+��������λ���Ӷ����ƶ�����
���忴�����л��������Զ�������һ�����������ã��������������л������Ժ���λ��������ǿ����ǿ��ͬʱ�л���ļ��뻹�ܹ��Ϻõ�ʵ�ֽ������ӵķ��롣�����л������ƶ����Ļ��ƣ�Ŀǰ��ʵ�����ͽṹ�����ĽǶȿ�����һ�����о���չ���������߽��������Э�ͼ��������ƻ������е�ϵͳ�о����٣��Զ����������Ƶ��ۻ���ȱ���㹻����ʶ����δ�Ӹ����Ͻ���ܶ������ȡ�����������⣬���һ�����۽ṹ��̽���л���Զ��������ƣ��Ӷ����õ�ָ������������⡣
3 ���Pչ��
�ܶ������ȡ���Ķ����������谭�����ȡ��Ӧ�õ�ԭ��֮һ����ǰ���о����ܶ������ȡ���Ķ�����������ԭ�������˳�������ʶ��Ҳ̽�����Զ������Ƶķ������ܶ������ȡ���Ķ�����Ҫȡ�����ͺ������λ��ʽ�Ϳռ�ṹ�����л��������ı������������ȡ��֮�����λ״̬���Ӷ������˶��������������ƶ����ķ�����ȣ��л���/���Э����ϵ�����Զ�����һ�����������ã������ܽϺõ�ʵ�ֽ������ӵķ��룬��δ�������������ķ�չ����
��ǰ�����ܶ������ȡ�������������Ƶ��о�������һ���ijɹ��������ڶ���������ԭ���Լ����ƶ������ۻ��ƻ�ȱ��ϵͳ�о������轫ʵ��̽����ƽ����㡢�����ֶ����ϣ���һ���Զ���ǰ�����ͺ�����ﻯ���ʼ��ȶ��Բ�������о��������������ӻ�ѧ�����X�������չ��ȷ���Խ��Խ���Ӧ������ȡ�����Ӻͽ����ͺ���Ľṹ�������о��У�δ��Ҳ�ɽ�����ʵ��̽�����ϣ��Ա��ȫ��ؽ�ʾ�ܶ������ȡ�����������ƻ�����
REFERENCES
[1] �� ��. ����������ʱЧӲ������ֵĵ绯ѧ������ ��[D]. ����: ���������Ƽ���ѧ, 2019.
ZHANG Xin. Study on electrochemical properties of Co-containing martensitic age-hardened stainless steels[D]. Xi��an: Xi��an University of Architecture and Technology, 2019.
[2] �� ��, �����, ������. ȫ���ܿ���Դ�����������о���չ[J]. ����, 2019, 38(4): 739-750.
WANG Hui, FENG Cheng-you, ZHANG Ming-yu. Characteristics and exploration and research progress of global cobalt deposits[J]. Mineral Deposits, 2019, 38(4): 739-750.
[3] �� ��, ʯ�㽭, ���ٳ�, ��. δ���й�����Դ����Ԥ ��[J]. �й���Դ����, 2019(10): 28-33.
WANG Jing, SHI Xiang-jiang, WANG Shou-cheng, et al. Demand forecast of China��s cobalt resource in the future[J]. Natural Resource Economis of China, 2019(10): 28-33.
[4] ����M, �� ��. ȫ���ܿ���Դ��״��������������[J]. �������������, 2019, 39(5): 41-49, 55.
YANG Hui-fan, WANG Wei. Global cobalt resources status and exploitation trends[J]. Conservation and Utilization of Mineral Resources, 2019, 39(5): 41-49, 55.
[5] �Ž���, ��Ϊ��, ���ո�. �������л����ܵ��о���չ[J]. ����ۺ�����, 2017(4): 11-15.
ZHANG Jian-jun, CHEN Wei-liang, LI Zhao-gang. Research progress of recovering cobalt from cobalt residues[J]. Multipurpose Utilization of Mineral Resources, 2017(4): 11-15.
[6] ����ɭ, �� ��, ������, ��. �����ӻ����������л���Эͬ��ϵ����,����ȡ�����е�Ӧ��[J]. ���̹���ѧ��, 2020, 20(4): 19-26.
LIU Wen-sen, LEI Ze, ZHU Zhao-wu, et al. Application of synergistic system of nitrogenous heterocyclic compounds and organic acids in extraction and separation of nickel and cobalt[J]. The Chinese Journal of Process Engineering, 2020, 20(4): 19-26.
[7] �����, ������, �� ��, ��. ͭ������ȡ�����о��� չ[J]. �����Ϳ��, 2020, 39(9): 60-68.
YANG Jia-qi, LI Li-qing, FENG Luo, et al. Research progress of copper extractants[J]. Electroplating & Finishing, 2020, 39(9): 60-68.
[8] HEALY M R, ROEBUCK J W, DOIDGE E D, et al. Contributions of inner and outer coordination sphere bonding in determining the strength of substituted phenolic pyrazoles as copper extractants[J]. Dalton Transactions, 2016, 45(7): 3055-3062.
[9] �� �h. Mextralϵ�н�����ȡ�������ܺ�Ӧ��[J]. ӡ�Ƶ�·��Ϣ, 2010(4): 52-54.
LIU Yue. Performance and application of Mextral series metal extractants[J]. Printed Circuit Information, 2010(4): 52-54.
[10] ������, �����, ������, ��. �����ȡ��LIX984N����ͭ��ȡ��������[J]. �й���ɫ����ѧ��, 2017, 27(4): 818-824.
LIU Xiao-rong, SHEN Jun-hui, LIU Yan-jun, et al. Degradation of oxime extractants LIX984N under impact of acid solution and phase disengagement of copper solvent extraction[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(4): 818-824.
[11] HUTTON-ASHKENNY M, BARNARD K R, IBANA D. Reagent degradation in the synergistic solvent extraction system LIX63/Versatic10/Nonyl-4PC[J]. Solvent Extraction and Ion Exchange, 2016, 7(34): 603-621.
[12] ���ٿ�. ��ȡұ��[M]. ����: ұ��ҵ������, 2009: 489-563.
MA Rong-jun. Extraction metallurgy[M]. Beijing: Metallurgical Industry Press, 2009: 489-563.
[13] RENNINGER D R, OSSEO-ASARE K. Stoichiometry of liquid-liquid extraction of nickel and cobalt by LIX63[J]. Metallurgical & Materials Transactions B, 1983, 14(1): 41-47.
[14] CHENG C Y, BARNARD K R, ZHANG W S, et al. Recovery of nickel, cobalt, copper and zinc in sulphate and chloride solutions using synergistic solvent extraction[J]. Chinese Journal of Chemical Engineering, 2016, 24(2): 237-248.
[15] BARNARD K R, TURNER N L. The effect of temperature on hydroxyoxime stability in the LIX63-Versatic 10-tributyl phosphate synergistic solvent extraction system under synthetic nickel laterite conditions[J]. Hydrometallurgy, 2011, 109(3/4): 245-251.
[16] BARNARD K R, TURNER N L, SHIERS D W. LIX63 stability in the presence of Versatic 10 under proposed commercial extract and strip conditions, part ��: Effect of manganese and cobalt loading on oxime stability at 30 ��[J]. Hydrometallurgy, 2010, 104(2): 268-277.
[17] ZHANG P W, YOKOYAMA T, SUZUKI T M, et al. The synergistic extraction of nickel and cobalt with a mixture of di(2-ethylhexyl)phosphoric acid and 5-dodecylsalicylaldoxime[J]. Hydrometallurgy, 2001, 61: 223-227.
[18] HUTTON-ASHKENNY M, BARNARD K R, IBANA D. Partial inhibition of LIX860-cobalt(��) formation by organic acids[C]// International Solvent Extraction Conference. W��rzburg: International Solvent Extraction Conference, 2014.
[19] �װ���, �� ��, ������, ��. �Ͼ�﮵���������Բ����������Һ��ȡ����[J]. ������ѧѧ��(��Ȼ��ѧ��), 2019, 40(10): 64-70.
YI Ai-fei, ZHANG Jian, ZHU Zhao-wu, et al. Extraction of impurities from leaching solution of cathode active material of spent lithium ion batteries by sulfuric acid [J]. Journal of Northeastern University(Natural Science), 2019, 40(10): 64-70.
[20] ELIZALDE M, OCIO A, ANDRADE F, et al. Synergistic extraction of cobalt(��) by mixtures of Bis(2-Ethylhexyl) Phosphoric acid and LIX 860[J]. Solvent Extraction and Ion Exchange, 2013, 31(3): 269-280.
[21] KAKOI T, URA T, KASAINI H, et al. Separation of cobalt and nickel by liquid surfactant membranes containing a synthesized cationic surfactant[J]. Separation Science and Technology, 1998, 33(8): 1163-1180.
[22] GUESNET P, BAUER D. Solvent-extraction of cobalt by LIX-65-N-oxidation of cobalt(��) chelates in organic- phase[J]. Analusis, 1981, 9(4): 129-134.
[23] ��ʤ��, ���ų~, ����ϲ, ��. �������˰���Һ������ͭ����ȡ����[J]. ��ɫ����(ұ������), 2002(6): 7-9.
WANG Sheng-dong, YIN Cai-qiao, JIANG Kai-xi, et al. Solvent extraction separation of Ni, Co and Cu from ammonia leaching solution of ocean polymetallic nodules[J]. Nonferrous Metals(Extractive Metallurgy), 2002(6): 7-9.
[24] NISHIHAMA S, SAKAGUCHI N, HARAI T, et al. Photoreductive stripping of cobalt loaded on hydroxyoxime extractant in a liquid-liquid extraction system[J]. Industrial & Engineering Chemistry Research, 2000, 39(12): 4986-4990.
[25] �� ��. �л���/���Эͬ��ȡ������ϵ��ͭ����п�Ӽ������о�[D]. ����: ������ɫ�����о���Ժ, 2017.
SUN Qi. Study on synergistic solvent extraction and mechanism of copper, nickel, cobalt, zinc and cadmium in complex solution with organic acids and hydroxyoximes[D]. Beijing: Beijing General Research Institute for Nonferrous Metals, 2017.
[26] SUN Q, YANG L M, HUANG S T. Mechanism of poisoning hydroxyoximes by cobalt in different organic systems[J]. Hydrometallurgy, 2018, 181: 64-73.
[27] Ф ��, Ф����. �ܡ�����ȡ����ԭ���뷽��[J]. ʪ��ұ��, 2010, 29(4): 225-228.
XIAO Chao, XIAO Lian-sheng. Theory of solvent extraction separation of cobalt and nickel[J]. Hydrometallurgy of China, 2010, 29(4): 225-228.
[28] �糣��. �ܼ���ȡ���백����Һ�е�ͭ���ܼ������� ��[D]. ����: ���ϴ�ѧ, 2019.
MIAO Chang-lin. Separation of copper, nick and cobalt from ammonia solution by solvent extraction and its mechanism[D]. Kunming: Yunnan University, 2019.
[29] ������. ��������������������ȡ���ķ�ЭͬЧӦ���백/�Ȼ����ϵ�е�ͭ����[D]. ����: ���ϴ�ѧ, 2016.
YANG Rui-si. Separation of copper, cobalt and nickel in ammonia/ammonium chloride solutions based on the antisynergism effect of phosphorous oxide compounds on hydroxamic extractants[D]. Kunming: Yunnan University, 2016.
[30] �� ��, ����÷, ������, ��. ������ȡ�������ͺ�����λ�ṹ���о���չ[J]. ϡ�н���, 2017, 41(7): 816-825.
SUN Qi, YANG Li-mei, HUANG Song-tao, et al. Research and prospect on coordination structures of cobalt and nickel extracted complexes during solvent extraction: A review[J]. Chinese Journal of Rare Metals, 2017, 41(7): 816-825.
[31] MACKENZIE M, VIRNIG M, FEATHER A. The recovery of nickel from high-pressure acid leach solutions using mixed hydroxide product LIX 84-INS technology[J]. Minerals Engineering, 2006, 19(12): 1220-1233.
84-INS technology[J]. Minerals Engineering, 2006, 19(12): 1220-1233.
[32] NOMBONA N, NYOKONG T. The synthesis cyclic voltammetry and spectro-electrochemical studies of Co2+ phthalocyanines tetra-substituted at the �� and �� positions with phenylthio groups[J]. Dyes and Pigments, 2009, 80(1): 130-135.
[33] MACKENZIE M, VIRNIG M, FEATHER A. The recovery of nickel from high-pressure acid leach solutions using mixed hydroxide product-LIX84-INS technology[J]. Minerals Engineering, 2006, 19(12): 1220-1233.
[34] ��־��, ���о�, ������, ��. ��Һ��������ȡ���뼼���о�״��[J]. ʪ��ұ��, 2018, 37(5): 342-348.
XU Zhi-gang, JI Shang-jun, WANG Chao-hua, et al. Review on separation of nickel and cobalt in solution by solvent extraction technology[J]. Hydrometallurgy of China, 2018, 37(5): 342-348.
[35] �� ��, ����÷, ������, ��. Эͬ��ȡ���Ƶ��о���״��չ��[J]. ϡ�н���, 2016, 40(11): 1177-1187.
SUN Qi, YANG Li-mei, HUANG Song-tao, et al. Research and prospect on synergistic solvent extraction mechanism[J]. Chinese Journal of Rare Metals, 2016, 40(11): 1177-1187.
[36] ������, ������, �½���, ��. �ܺ���Эͬ��ȡ�����о���չ[J]. �й���ɫ����ѧ��, 2013, 23(7): 2026-2032.
LI Xiao-hui, HUANG Song-tao, WEN Jian-kang, et al. Research progress of synergistic solvent extraction of cobalt and nickel[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(7): 2026-2032.
[37] FLETT D S, WEST D W. Extraction of metal ions by LIX63/ carboxylic acid mixtures[C]// Proceedings International Solvent Extraction Conference. London: Society of Chemical Industry, 1971: 214-223.
[38] FLETT D S, TITMUSS S. Synergistic effect of LIX63 on the extraction of copper and cobalt by naphthenic acid[J]. J Inorg Nucl Chem, 1968, 31(8): 2162-2163.
[39] JONES D, MAYHEW K, MCCOY T, et al. A process to separate cobalt from nickel[C]// Proceedings of ALTA 2010 Nickel/Cobalt/Copper. Melbourne: ALTA Metallurgical Services, 2010: 1-9.
[40] �� ϼ, �� ɽ, �� ��. LIX63��Versatic 10��ȡ��ϵ�������̵�Э�ͻ����о�[J]. ʪ��ұ��, 2020, 39(1): 34-40.
WU Xia, ZHU Shan, LI Song. Synergistic extraction mechanism of Versatic 10 and LIX63 for Ni2+, Co2+, Mn2+[J]. Hydrometallurgy of China, 2020, 39(1): 34-40.
[41] ZHU S, HU H P, LI J Y, et al. The coordination structure of the extracted cobalt(��) complex with a synergistic mixture containing Lix63 and Versatic10[J]. Journal of the Chinese Chemical Society, 2017, 64(7): 833-842.
[42] BARNARD K R, SHIERS D, KELLY N J, et al. Synthesis of at-��-hydroxy oxime and its synergistic behavior with Versatic 10[J]. Solvent Extraction and Ion Exchange, 2015, 33(2): 166-182.
[43] D��ALESSIO D, LOMBARDO D M, VAUGHAN J G, et al. Structural variations in metal complexes of a tertiary ��-hydroxyoxime[J]. Dalton Transactions, 2015, 44(16): 7163-7168.
[44] CHENG C Y. Solvent extraction of nickel and cobalt with synergistic systems consisting of carboxylic acid and aliphatic hydroxyoxime[J]. Hydrometallurgy, 2006, 84(1): 109-117.
[45] JOO S H, SHIN D J, OH C H, et al. Selective extraction and separation of nickel from cobalt, manganese and lithium in pre-treated leach liquors of ternary cathode material of spent lithium-ion batteries using synergism caused by Versatic 10 acid and LIX84-I[J]. Hydrometallurgy, 2016, 159: 65-74.
[46] WANG L Y, LEE M S. Synergistic extraction of Co(��) over Ni(��) from chloride solutions by a mixture of Cyanex 301 and LIX 63[J]. Geosystem Engineering, 2017, 6(20): 311-317.
Research progress of poisoning and inhibition of cobalt to hydroxyoxime extractant and its inhibition
DENG Jing-xian1, 2, 3, 4, WU Biao1, 2, 3, 4, SUN Qi1, 2, 4, WEN Jian-kang1, 2, 3, 4, LIU Xue1, 2, 4
(1. National Engineering Laboratory of Biometallurgy, GRINM Group Co., Ltd., Beijing 101407, China;
2. GRINMAT Resources and Environment Technology Institute Co., Ltd, Beijing 101407, China;
3. General Research Institute for Nonferrous Metals, Beijing 100088, China;
4. GRIMAT Engineering Institute Co., Ltd., Beijing 101407, China)
Abstract: The poisoning of the extractant caused by cobalt was observed during cobalt extraction process, which severely restrict the application of hydroxyoxime extractant and the further growth of cobalt extraction. This article introduces the development status of cobalt extraction with hydroxyoxime extractants. The oxidation and poisoning behaviors and mechanisms of cobalt under hydroxyoxime extraction system in detail were reviewed. Comparative analyses of the chemical properties and behavior of cobalt in ammonia and hydroxyoxime organic solution were conducted, and the cause of poisoning of hydroxyoxime extractants by cobalt was clarified. On this basis, the inhibition behaviors and mechanisms of the poisoning organic carboxylic acid and phosphoric acid with the hydroxyoxime extraction system were reviewed emphatically, the reasons why the poisoning inhibited with phosphoric acid/hydroxyoxime synergistic extraction systems were analyzed. The current problems and deficiencies of poisoning of hydroxyoxime extractants caused by cobalt and its inhibitions are pointed out. Finally, the paper looks forward to the future directions and methods for in-depth research in this field, which provides a theoretical basis and guidance for solving the problem of poisoning of hydroxyoxime extractants caused by cobalt.
Key words: hydroxyoxime extractant; cobalt extraction; poisoning; organic acid; inhibition mechanism
Foundation item: Project(51904271) supported by the National Natural Science Foundation of China
Received date: 2020-07-01; Accepted date: 2021-01-26
Corresponding author: SUN Qi; Tel: +86-17813216287; E-mail: sunqi@grinm.com
(�༭ ����)
������Ŀ��������Ȼ��ѧ����������Ŀ(51904271)
�ո����ڣ�2020-07-01�������ڣ�2021-01-26
ͨ�����ߣ��� ����������ʦ����ʿ���绰��17813216287��E-mail:sunqi_je@163.com