文章编号:1004-0609(2008)S1-0148-07
橘子皮化学改性及其对Cu(Ⅱ) 离子的吸附性能
冯宁川1, 2,郭学益1,梁 莎1,田庆华1
(1. 中南大学 冶金科学与工程学院,长沙 410083;2. 宁夏医学院 基础学院,银川 750004)
摘 要:以橘子皮为基体,经环氧氯丙烷交联后,以Ce4+为引发剂将丙烯酸甲酯单体接枝到橘子皮上,再经过皂化制备改性橘子皮生物吸附剂。研究溶液pH、吸附时间和Cu2+初始浓度对生物吸附剂吸附性能的影响。结果表明,在pH值为5.5,Cu2+初始质量浓度为50 mg/L,吸附时间为3 h的条件下,该生物吸附剂对Cu2+去除率为94.6%,吸附容量为24.41 mg/g。Cu2+在该生物吸附剂上的吸附过程可以用准二级动力学方程很好地描述。吸附等温线结果表明,该生物吸附剂对Cu2+的吸附用Freundlich方程拟合效果优于用Langmuir方程拟合效果。将该生物吸附剂用于含Cu2+ 5.8 mg/L的电镀废水,Cu2+去除率可达97%。通过红外光谱表征该生物吸附剂的结构,说明羧基和羟基与金属离子的结合引起该生物吸附剂对Cu2+的吸附。该生物吸附剂可以再生重复使用4次以上。
关键词:橘子皮;化学改性;Cu(Ⅱ)离子;生物吸附
中图分类号:X 703.1 文献标识码:A
Biosorption of Cu(Ⅱ) ion on modified orange peel
FENG Ning-chuan1, 2, GUO Xue-yi1, LIANG Sha1, TIAN Qing-hua1
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. School of Basic Medical Science, Ningxia Medical College, Yinchuan 750004, China)
Abstract: The chemically modified orange peel was prepared from hydrolysis of the grafted copolymer, which was synthesized by interacting methyl acrylate with cross-linking orange peel. Various factors were investigated by batch experiments, including pH value, adsorption time and initial concentration of Cu2+, to study their effects on adsorption characteristics of the biosorbent on Cu2+. The results show that when pH value is 5.5 and the initial concentration of Cu2+ is 50 mg/L, the removal rate achieves 94.6% after 3 h adsorption, and the adsorption capacity is 24.41mg/g. The kinetic characteristics of Cu2+ biosorption were investigated and the adsorption processes were found to follow pseudo-second order type adsorption kinetics. The adsorption isotherms results indicate that Freundlich model fits the adsorption process much better than the Langmuir model. The removal rate of 5.8 mg/L Cu2+ in 50 mL of electroplating wastewater is 97% when 1 g of the biosorbent is used at pH value of 5.5. The biosorbent was characterized by using infrared spectroscopy. The analysis of IR spectrum indicates that the adsorption of Cu2+ by the biosorbent caused the combination of carboxyl and hydroxyl groups with heavy metal. The biosorbent is suitable for repeated use more than four cycles.
Key words: orange peel; chemical modification; Cu(Ⅱ) ion; biosorption
随着有色金属工业的发展,重金属污染日趋严重。环境中的重金属离子通过各种途径而进入水体,经过水体中的各种生物链的富集,最终由水体进入人体,并对人的健康产生危害。除去水中重金属离子的方法很多,常用的有氢氧化物沉淀法、离子交换法和活性炭吸附法等。近十几年来,许多研究者在探索利用廉价高效的生物吸附剂如菌类、藻类、工农业副产物等治理重金属废水污染[1-2]。生物吸附法是一种新兴的重金属废水处理技术,它利用廉价的生物材料对重金属进行吸附,尤其适宜低浓度重金属废水的处理[3],并且具有吸附量高、吸附速度快等优点。柑橘渣是生物吸附剂的一种,它含有丰富的果胶、纤维素、半纤维素等多糖类高分子化合物和木质素。由于这些分子表面含有大量羟基、羧基等活性官能团,可以同重金属离子通过离子交换、螯合等方式结合,从而可用于溶液中重金属离子的净化。为了开发利用柑橘渣类废弃物质,国内外学者做了许多研究[4-7],P?REZ-MA?IN等[5]用柑橘渣从水溶液中除去镉,AJMAL M等[7]用橘子皮除去废水中的Ni(Ⅱ)。但直接采用柑橘渣做吸附剂存在着吸附能力较低、由于可溶性有机物质的溶解而导致水中化学耗氧量增加等问题[8-9]。
近年来,有学者通过皂化、磷酸化、交联等方 法[10-12],对柑橘渣进行改性处理,使其活性官能团的数目提高,去除金属离子的能力增强。研究表明,对柑橘渣等废弃物质进行化学改性,可以改善它们的物理化学性能,提高对重金属的吸附能力。但目前对果渣类生物吸附剂的改性主要是对果胶分子上甲酯化的羧基的皂化、纤维素分子中羟基的磷酸酯化和交联,而通过羟基的醚化反应和亲核取代反应以及接枝共聚反应在其所含的纤维素、果胶等高分子骨架上引入活性官能团以提高吸附性能的改性尚未见报道。本文作者以橘子皮为基体,经环氧氯丙烷交联后,以Ce4+为引发剂将丙烯酸甲酯单体接枝到橘子皮上,再经过皂化制备了改性橘子皮生物吸附剂,并由此研究Cu2+在该吸附剂上的吸附,包括吸附平衡时间、初始浓度等对生物吸附的影响,分析生物吸附动力学及等温方程。
1 材料与方法
1.1 仪器与试剂
仪器:3510原子吸收分光光度计(安捷伦公司), PHS-3C酸度计(上海雷磁), SHA-C水浴恒温振荡器(江苏荣华),Nicolet 380傅立叶变换红外光谱仪。
试剂:CuSO4×5H2O,HCl,NaOH,环氧氯丙烷和丙烯酸甲酯等均为分析纯。
1.2 改性橘子皮生物吸附剂的制备
橘子皮(OP)经自来水和蒸馏水洗净后于在80 ℃烘箱中烘干24 h,粉碎,取1.5 mm以下颗粒5 g,放入三口瓶中,加入乙醇50 mL和2.5 mol/L NaOH溶液50 mL,搅拌15 min后,加入12 mL环氧氯丙烷,在45 ℃下搅拌回流1 h。冷却至室温后用2%的盐酸调节pH值至5左右,过滤,以60%乙醇洗涤,干燥,得到的交联橘子皮,简写为COP。
在三口瓶中加入2.8 g COP和100 mL的2.5×10-2 mol/L HNO3,搅拌并通入氮气,30 min后,加入5.0×10-3 mol/L硝酸铈铵溶液和15 mL丙烯酸甲酯,搅拌,1 h后,加入2 mL 5%对苯二酚溶液中止反应。接枝产物过滤,用蒸馏水洗涤多次,在60 ℃下干燥至质量不变,在索氏提取器中用丙酮洗去均聚物。干燥后的接枝产物(OPMA)在0.5 mol/L NaOH溶液中于60 ℃下皂化10 h;冷却后,用盐酸溶液调节pH值至6.5左右,将产物OPAA过滤,用丙酮洗涤,在60 ℃下真空干燥, 研成粉末, 取粒径在1.5 mm以下的颗粒备用。
1.3 实验方法
静态吸附实验方法:在100 mL锥形瓶中加入生物吸附剂0.05 g及Cu2+溶液25 mL,用0.1 mol/L的HCl和0.1 mol/L的NaOH调节溶液pH值,密闭瓶口以防实验过程中体积变化。将其放入水浴恒温振荡器振荡,控制温度30 ℃,离心分离并过滤,用原子吸收分光光度计测定滤液中Cu2+平衡浓度。用下式计算吸附量:

解吸附实验方法:将达到吸附平衡的生物吸附剂与溶液离心分离,向吸附剂中加入25 mL的0.1 mol/L HCl,恒温振荡3 h,过滤,测定滤液中Cu2+浓度。吸附剂用蒸馏水洗至中性,烘干。再生后的吸附剂被反复使用。
2 结果与讨论
2.1 橘子皮改性处理对吸附性能的影响
测试OP和OPAA对Cu2+吸附的效果,结果如表1所列。由表1可见,橘子皮改性后对Cu2+的去除率提高,这是由于聚丙烯酸分子被接枝到OP表面上,吸附剂表面羧基官能团的数目增加,对Cu2+吸附的能力增强。橘子皮的改性处理不仅提高了它对Cu2+吸附能力,而且使吸附剂的化学稳定性也得以提高,化学需氧量明显降低。
表1 橘子皮的预处理对吸附Cu 2+的影响
Table 1 Effect of orange peel pretreatment on Cu2+ adsorption

2.2 pH值的影响
图1所示为溶液pH值对吸附的影响。由图1可以看出,pH值对OPAA的吸附容量影响很大。吸附容量在pH值为2.0时达到最低,且随着pH值的增加而增加。最大的吸附率(94.6%)出现在pH值为5.5时,以后随着pH值的继续增大,吸附容量降低。最低的吸附率出现在pH值为2.0。这可能是因为较低pH值下H+的浓度和活动性较高,与其它的阳离子形成了竞争吸附,从而吸附率较低[7]。随着pH值的增大,H+的浓度降低,带负电荷的配体比例增大,吸附率升高。羧基(―COOH)是生物吸附剂对离子的吸附有重要影响的官能团。当pH值增大到3~4时,羧基去质子化带负电荷,因此易于吸引带正电荷的金属阳离子。
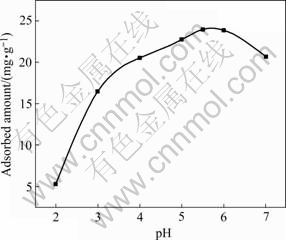
图1 pH值对吸附的影响
Fig.1 Effect of pH value on adsorption (Adsorbent dose: 2 g/L; Temperature: 30 ℃; Agitation time: 3 h; c0: 50 mg/L)
2.3 吸附动力学
在30 ℃的溶液中,当Cu2+初始浓度分别为50和100 mg/L时,吸附量随吸附时间的变化如图2所示。从图中可以看出,在初始阶段(0~30 min),吸附量随着时间的增加迅速增大,即吸附速度较快;随后是一个速度较慢的吸附过程,最终达到吸附平衡(约120 min)。从图中还可以看出,尽管Cu2+初始浓度不同,但吸附速度的变化趋势相同,达到吸附平衡所需时间基本相同。根据实验的结果,选择实验时间为3h,以确保达到吸附平衡。
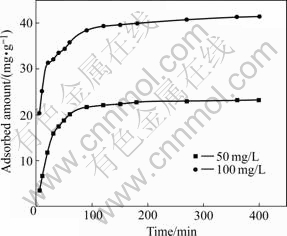
图2 吸附时间对吸附的影响
Fig.2 Effect of contact time on adsorption (pH: 5.5; Tempera- ture 30 ℃; Adsorbent dose: 2 g/L)
在生物吸附动力学的研究中,通常用一级和二级动力学方程对实验数据进行模拟,以分析金属离子浓度随吸附时间的变化关系[13]。准二级动力学方程[14]的线性表达式为

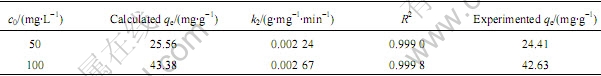
利用上述方程对实验数据进行模拟,以t/q对t作图,可得到准二级动力学方程,如图3 所示。表2中列出了准二级动力学方程的模拟结果。从图3和表2可以看出,实验结果可以很好地用准二级动力学方程进行模拟,两种金属离子浓度下的相关系数均达0.999,且qe的实验值与理论值相差很小。这表示吸附过程遵循准二级反应机理,吸附速率被化学吸附所控制[15]。

图3 准二级吸附动力学方程模拟结果
Fig.3 Simulated result of pseudo second-order kinetics
表2 Cu 2+吸附的准二级动力学方程的动力学参数
Table 2 Kinetic parameters of pseudo-second-order equation for Cu2+adsorption
2.4 等温吸附
图4所示为30 ℃下Cu2+初始浓度在10~250 mg/L范围内的吸附等温线。由图4可以看出,吸附量随溶液中Cu2+浓度的增加而增加。采用Langmuir和Freundlich吸附等温模型对图4 数据进行模拟。Langmuir方程为

图4 Cu2+的吸附等温线
Fig.4 Adsorption isotherm of Cu2+ (pH: 5.5; Adsorbent dose: 2 g/L; Temperature: 30 ℃; Agitation time: 3 h)

Q0和b可由ce/qe对ce作直线方程的斜率为1/Q0,截距为1/(Q0b)求出。
Freundlich方程为

Langmuir和 Freundlich方程的模拟结果如图5和6所示。Langmuir方程和Freundlich方程的相关系数分别为0.937和0.986。可以看出,实验结果用Freundlich方程模拟的结果较好。根据图5和6计算出Q0和b的值分别为180.8 mg/g和0.023 L/mg,KF和1/n的值分别为5.44和0.75。
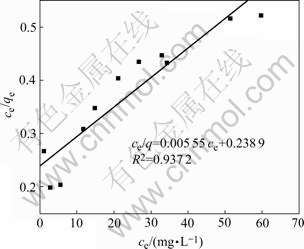
图5 Langmuir方程模拟结果
Fig. 5 Simulated result of Langmuir isotherm equation

图6 Freundlich方程模拟结果
Fig.6 Simulated result of Freundlich isotherm equation
2.5 对电镀废水的吸附应用
将生物吸附剂用于长沙某电镀厂电镀废水的处理,表3所列为长沙某电镀厂废水成分,图7所示为生物吸附剂用量对电镀废水中Cu2+去除率的影响。从图中可以明显看出,在50 mL含Cu2+为5.8 mg/L的废水中,当生物吸附剂量为500 mg时,Cu2+去除率可达到80%;当生物吸附剂量达到1 500 mg时,Cu2+去除率可达到97%。实验结果表明,这种方法可以有效地去除废水中低浓度的Cu2+。
表3 电镀废水的成分
Table 3 Component of electroplating wastewater(pH=2.4)
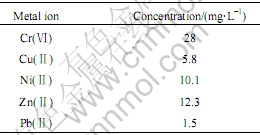
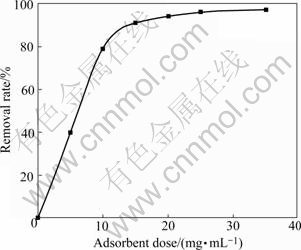
图7 吸附剂量对电镀废水中Cu2+去除率的影响
Fig.7 Effect of adsorbent dose on removal rate of Cu2+ from electroplating wastewater
2.6 再生
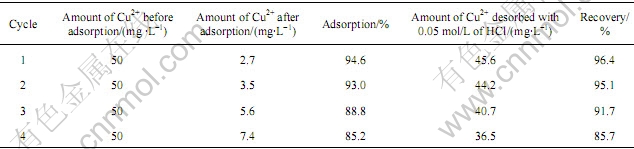
本文作者研究了已吸附Cu2+的OPAA生物吸附剂的再生方法。将已经吸附了Cu2+的生物吸附剂放入0.1 mol/L的HCl溶液中,浸泡3 h,过滤,解吸后的吸附剂再用去离子水洗至中性,烘干,反复使用。表4所列数据说明,用再生后的生物吸附剂进行吸附实验,吸附能力降低的程度很小。
表4 Cu2+吸附-解吸实验结果
Table 4 Results of Cu2+ adsorption-desorption experiment
2.7 红外光谱
OP、OPAA 和OPAA吸附Cu2+后的红外光谱如图8所示。OP主要成分有果胶、纤维素、半纤维素和木质素等。3 430 cm-1处的吸收峰较强且宽,说明OP表面存在大量存在―OH, 2 920~2 800 cm-1之间的吸收峰为―CH3、―CH2 中C―H键的伸缩振动,出现在1 744 cm-1的峰来自羧基中C=O特征伸缩振动, 在1 638 cm-1出现吸收是木质素中芳香环的环伸缩振动。而1 434 cm-1处的吸收峰为―CH3和―CH2中C―H的不对称弯曲振动峰。1 226 cm-1处的吸收是木质素中苯羟基中C―O键的伸缩振动引起的。1 066 cm-1处的吸收,主要产生于O―H的弯曲振动和C―O―C(纤维素等中存在)的伸缩振动[5]。将OPAA的红外光谱与OP比较, 可以发现在1 410 cm-1和1 575 cm-1处存在两个特征峰, 这是OP经交联、接枝、皂化水解后, 由接枝侧链上的―COOCH3转变为 ―COONa的结果。比较OPAA吸附Cu2+前后的红外光谱图,可以发现生物吸附剂吸附Cu2+后,在3 430 cm-1和1 730 cm-1的吸收峰都增强和变宽了,说明生物吸附剂表面的羟基和羧基是与Cu2+发生反应的结合点[16]。
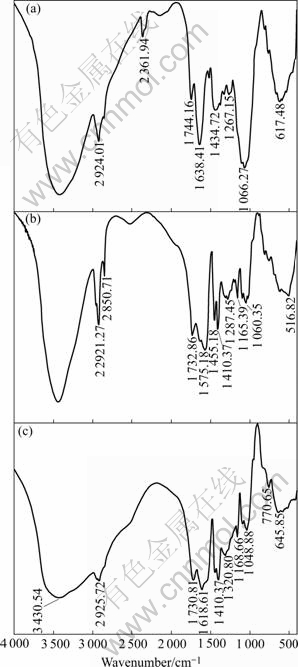
图8 OP, COP和OPAA红外光谱
Fig.8 FT-IR spectrum of OP, COP and OPAA: (a) OP; (b) OPAA; (c) OPAA-Cu2+
3 结论
1) 以废弃物质橘子皮为基体,经环氧氯丙烷交联后,以Ce4+为引发剂将丙烯酸甲酯单体接枝到橘子皮上,再经过皂化制备了改性橘子皮生物吸附剂。用该生物吸附剂处理低浓度含铜废水,去除效率高, 且该生物吸附剂可以再生重复使用,是一种性能良好的吸附剂。
2) 溶液pH值是影响生物吸附剂对Cu2+吸附效果的重要因素,在pH值为5.5时,吸附量最大。Cu2+在生物吸附剂上的吸附在初始30 min内进行很快,随时间推移,吸附量增加缓慢,约120 min时达到吸附平衡。吸附动力学可以用准二级动力学方程很好的描述(R2=0.999)。吸附等温线结果表明,用Freundlich方程拟合效果优于用Langmuir方程拟合效果。
3) 通过红外光谱,表征了生物吸附剂的结构,说明了羧基和羟基与金属离子的结合引起生物吸附剂对Cu2+的吸附。
REFERENCES
[1] OZSOY H D, KUMBUR H. Adsorption of Cu(Ⅱ) ions on cotton boll [J]. Journal of Hazardous Materials, 2006, B136: 911-916.
[2] MA W, TOBIN J M. Determination and modelling of effects of pH on peat biosorption of chromium, copper and cadmium [J]. Journal of Biochemistry Engineering, 2004, 18: 33-40.
[3] WANG X S, QIN Y. Equilibrium sorption isotherms for Cu2+ on rice bran [J]. Process Biochem, 2005, 40(2): 677-680.
[4] BISWAS B K, INOUE K, GHIMIRE K N, OHTA S, HARADA H, OHTO K, KAWAKITA H. The adsorption of phosphate from an aquatic environment using metal-loaded orange waste [J]. Journal of Colloid and Interface Science, 2007, 312(2): 214-223.
[5] P?REZ-MAR?N A B, ZAPATA V M, ORTU?O J F, AGUILAR M, S?EZ J, LLOR?NS M. Removal of cadmium from aqueous solutions by adsorption onto orange waste [J]. Journal of Hazardous Materials, 2007, B139: 122-131.
[6] ANNADURAI G, JUANG R S, LEE D J. Adsorption of heavy metals from water using banana and orange peels [J]. Water Science and Technology, 2003, 47(1): 185-190.
[7] AJMAL M, RAO R A K, AHMAD R, AHMAD J. Adsorption studies on Citrus reticulata (fruit peel of orange): removal and recovery of Ni(Ⅱ) from electroplating wastewater [J]. Journal of Hazardous Materials, 2000, B79: 117-131.
[8] NOELINE B F, MANOHAR D M, ANIRUDHAN T S. Kinetic and equilibrium modelling of lead(Ⅱ) sorption from water and wastewater by polymerized banana stem in a batch reactor [J] . Separation Purification Technology, 2005, 45: 131-140.
[9] GABALLAH I, GOY D, ALLAIN E, KILBERTUS G, THAURONT J. Recovery of copper through decontamination of synthetic solutions using modified barks [J]. Metallurgical and Materials Transactions, 1997, B28: 13-23.
[10] DHAKAL R P, GHIMIRE K N, INOUE K. Adsorptive separation of heavy metals from an aquatic environment using orange waste [J]. Hydrometallurgy, 2005, 79(3/4): 182-190.
[11] GHIMIRE K N, INOUE K, YAMAGUCHI H, MAKINO K, MIYAJIMA T. Adsorptive separation of arsenate and arsenite anions from aqueous medium by using orange waste [J]. Water Research, 2003, 37(20): 4945-4953.
[12] LI X, TANG Y, XUAN Z, LIU Y, LUO F. Study on the preparation of orange peel cellulose adsorbents and biosorption of Cd2+ from aqueous solution [J]. Separation and Purification Technology, 2007, 55: 69-75.
[13] YAN G Y, VIRARAGHAVAN T. Heavy-metal removal from aqueous solution by fungus Mucor rouxii [J]. Water Research, 2003, 37: 4486-4496.
[14] HO Y S, MCKAY G. Pseudo-second order model for sorption processes [J]. Process Biochem, 1999, 34: 451-465.
[15] ?ZACAR M, ?ENGIL ? A. Adsorption of reactive dyes on calcined alunite from aqueous solutions [J]. Journal of Hazardous Material, 2003, B98: 211-224.
[16] 李克斌, 刘维屏, 邵 颖. 重金属离子在腐殖酸上吸附的研究[J]. 环境污染与防治, 1997, 19(1): 9-11.
LI Ke-bin, LIU Wei-ping, SHAO Yin. Adsorption of heavy metal ions on humic acid [J]. Environmental Pollution & Control, 1997, 19(1): 9-11.
基金项目:国家自然科学基金资助项目(50774100)
通讯作者:郭学益,教授, 博士;电话:0731-8836207; E-mail: xyguo@mail.csu.edu.cn
(编辑 何学锋)