稀土Ce改性TiO2的制备及光催化降解苯甲羟肟酸的研究
来源期刊:稀有金属2018年第4期
论文作者:王俊蔚 王春英 祝思频 罗仙平 李智慧 徐亮亮
文章页码:393 - 401
关键词:稀土掺杂;Ce/TiO2;光催化降解;苯甲羟肟酸;
摘 要:通过溶胶-凝胶法制备Ce改性TiO2(Ce/TiO2)复合材料,并以选矿废水中残余的浮选捕收剂苯甲羟肟酸为对象来考察Ce/TiO2的光催化降解活性;通过多种分析检测手段(X射线衍射(XRD)、X射线光电子能谱(XPS)、扫描电镜(SEM)、紫外-可见漫反射(UV-Vis DRS)等)对所合成催化剂的结构、形貌、光吸收等物理化学性能进行一系列表征。表征结果表明:相较于纯TiO2,Ce的掺杂可以有效抑制TiO2晶粒的生长,增大改性后Ce/TiO2的比表面积,从而提高其光催化活性;当掺杂量为0.20%时,其结晶度好、颗粒较均匀、具有较强的光吸收性能。苯甲羟肟酸的降解试验结果表明:当Ce的掺杂比为0.20%、煅烧温度为500℃,光催化活性最强,120 min后,苯甲羟肟酸降解率达90.98%(0.3 g・L-1的Ce/TiO2),矿化率达82.8%。此外,Ce/TiO2重复使用4次后,苯甲羟肟酸的光催化降解率无明显降低,表明Ce/TiO2是一种有效稳定的光催化剂。
网络首发时间: 2017-11-07 17:25
稀有金属 2018,42(04),393-401 DOI:10.13373/j.cnki.cjrm.xy16080006
王俊蔚 王春英 祝思频 罗仙平 李智慧 徐亮亮
江西理工大学资源与环境工程学院江西省矿冶环境污染控制重点实验室
西部矿业股份有限公司博士后科研工作站
通过溶胶-凝胶法制备Ce改性TiO2 (Ce/TiO2) 复合材料, 并以选矿废水中残余的浮选捕收剂苯甲羟肟酸为对象来考察Ce/TiO2的光催化降解活性;通过多种分析检测手段 (X射线衍射 (XRD) 、X射线光电子能谱 (XPS) 、扫描电镜 (SEM) 、紫外-可见漫反射 (UV-Vis DRS) 等) 对所合成催化剂的结构、形貌、光吸收等物理化学性能进行一系列表征。表征结果表明:相较于纯TiO2, Ce的掺杂可以有效抑制TiO2晶粒的生长, 增大改性后Ce/TiO2的比表面积, 从而提高其光催化活性;当掺杂量为0.20%时, 其结晶度好、颗粒较均匀、具有较强的光吸收性能。苯甲羟肟酸的降解试验结果表明:当Ce的掺杂比为0.20%、煅烧温度为500℃, 光催化活性最强, 120 min后, 苯甲羟肟酸降解率达90.98% (0.3 g・L-1的Ce/TiO2) , 矿化率达82.8%。此外, Ce/TiO2重复使用4次后, 苯甲羟肟酸的光催化降解率无明显降低, 表明Ce/TiO2是一种有效稳定的光催化剂。
中图分类号: O643.36;O644.1
作者简介:王俊蔚 (1992-) , 女, 江西九江人, 硕士, 研究方向:矿山环境污染控制与生态修复;E-mail:Wangjunyu1025@163.com;;罗仙平, 教授;电话:13507979491;E-mail:lxp9491@163.com;
收稿日期:2016-08-04
基金:国家科技部“十二五”国家科技支撑计划项目 (2012BAC11B07);教育部新世纪优秀人才支持计划项目 (NCET-10-0183);国家自然科学基金项目 (51408277);江西省主要学科与技术带头人培养对象计划项目 (2010DD01200);“赣鄱英才555工程”领军人才培养计划项目;中国博士后科学基金项目 (2015M582776XE, 2016T90967) 资助;
Wang Junyu Wang Chunying Zhu Sipin Luo Xianping Li Zhihui Xu Liangliang
Jiangxi Key Laboratory of Mining & Metallurgy Environmental Pollution Control, Faculty of Resource and Environmental Engineering, Jiangxi University of Science and Technology
Post-Doctoral Scientific Research Workstation of Western Mining Co., Ltd.
Abstract:
Rare earth element Ce doped TiO2 (Ce/TiO2) was synthesized by sol-gel method.Benzohydroxamic acid was used as the objective pollutant to investigate the photocatalytic activity of Ce/TiO2.The structure and physicochemical properties of prepared materials were characterized by X-ray diffraction (XRD) , X-ray photoelectron spectroscopy (XPS) , scanning electron microscopy (SEM) , ultraviolet-visible diffuse reflectance spectroscopy (UV-Vis DRS) , and so on.As a result, the doping of Ce could inhibit the crystal growth of TiO2, retain a smaller grain size, increase its specific surface area, and improve the photocatalytic activity of Ce/TiO2.The crystallinity was good when the doping ratio of Ce to TiO2 was 0.20%.The prepared Ce/TiO2 particles were more uniform, and of stronger optical absorption properties.Ce/TiO2 with the doping ratio of 0.20% calcined at 500 ℃ showed the highest photocatalytic activity to degrade benzohydroxamic acid.After 120 min, the removal rate of benzohydroxamic acid reached 90.98% (0.3 g・L-1 of Ce/TiO2) , and 82.8% of the total organic carbon was eliminated.In addition, after four recycling runs, Ce/TiO2 (0.20%) still kept high photocatalytic activity on the photodegradation of benzohydroxamic acid.
Keyword:
rare earth doped; Ce/TiO2; photocatalytic degradation; benzohydroxamic acid;
Received: 2016-08-04
Ti O2作为一种常见的半导体光催化材料, 由于它安全无毒、成本低、对环境友好、高的化学稳定性和氧化还原能力强等优点, 在环境治理领域研究应用比较广泛。但是, Ti O2光催化剂自身也存在一定的缺陷:带隙较宽 (3.2 e V) 、只能利用太阳能的5%左右、光生电子-空穴容易复合、光催化效率低等[1,2]。因此, 为了有效提高Ti O2的光催化效率, 抑制光生载流子的复合, 可以通过各种手段对Ti O2进行掺杂改性。稀土元素由于具有4f电子层, 能级结构丰富, 而且容易产生多电子组态, 其氧化物晶型也比较多, 被广泛用于掺杂改性Ti O2的研究中[3,4,5,6,7,8]。稀土元素Ce具有可变的离子对Ce3+/Ce4+, 而且具有Ce3+ (4f15d0) 和Ce4+ (4f05d0) 特殊的氧化态电子结构[9]。Ce3+失去电子后转变成Ce4+, 在4f层上产生电子陷阱, 结合电子后再次被还原成Ce3+, Ce3+与Ce4+之间的氧化还原转化能够提高储存或者释放氧气的容量[10], 其中储存的氧气对电子转移过程和可见光的响应起着非常重要的作用。Xiao等[11]研究了Ce掺杂Ti O2光催化降解Rh B的实验, 结果表明相比于纯Ti O2和P25, Ce/Ti O2具有更高的光催化效率, 经80 min光反应后Rh B降解率达到99.59%, 其矿化率也达到了77.59%。
光催化技术在污水处理方面的应用比较多, 但对于选矿废水中残留选矿药剂的处理研究尚少。在中国赣南地区, 离子型稀土矿分布较广[12]。苯甲羟肟酸作为一种高效的螯合型氧化矿捕收剂, 广泛用于稀土矿等的浮选[13]。由于苯甲羟肟酸含有苯环结构及元素N, 当其在环境中累积后, 将导致水体中COD浓度增加和水体富营养化, 进而产生一定的生理毒性, 给环境造成严重的影响及危害[14,15]。所以, 利用Ce改性Ti O2光催化降解苯甲羟肟酸对于赣南选矿废水的治理具有重要的现实意义。
本实验通过溶胶凝胶法成功制备出具有介孔结构的Ce/Ti O2光催化剂, 通过多种手段对其物理化学性质进行表征, 并以选矿废水中选矿药剂苯甲羟肟酸为处理对象, 考察其光催化活性及重复使用性。
1实验
1.1主要试剂与仪器
试剂:硝酸铈 (Ce (NO3) 3・6H2O, AR) , 钛酸四丁酯 (TBT, AR) , 无水乙醇 (Et OH, AR) , 冰醋酸 (HAc, AR) , 苯甲羟肟酸 (C7H7NO2, AR) , 实验用水为去离子水。
仪器:p H计 (上海三信MP551型) ;电子天平 (OHAUS AR224CN型) ;台式高速离心机 (湖南CENCE湘仪TG16-WS型) ;六联恒温搅拌器 (常州郎越HJ-6A型) ;电热鼓风干燥箱 (天津市泰斯特101-1AB型) ;马弗炉 (上海西格马SHF.M25/10型) ;XPA系列光化学反应仪 (南京胥江机电厂XPA-7型) ;紫外-可见分光光度计 (上海仪电分析仪器L5型) ;TOC分析仪 (德国Ellementar公司vario TOC) 。
1.2 Ce/Ti O2光催化剂的制备与表征
称取一定量的硝酸铈, 加入10 ml无水乙醇、2 ml冰醋酸及2 ml去离子水, 充分搅拌配成均匀、透明的溶液A, 待用;在室温条件下, 移取10 ml钛酸四丁酯并缓慢滴加到15 ml无水乙醇中, 搅拌0.5 h后, 获得透亮溶液B;再将溶液A缓慢滴入溶液B中, 继续搅拌得到Ce/Ti O2湿凝胶, 将所得湿凝胶置于空气中陈化2 d得到干凝胶, 然后置于干燥箱中于90℃下干燥, 经充分研磨后置于马弗炉在不同的高温 (400, 450, 500, 550和600℃) 煅烧6 h, 最终得到Ce/Ti O2纳米光催化剂。稀土Ce掺杂比按照Ce相对于Ti O2的质量分数设置为0%, 0.10%, 0.20%, 0.30%, 0.40%和0.50%。
晶型结构通过X射线衍射仪 (XRD, 日本理学Miniflex型) 测量, 衍射靶为Cu Kα (波长λ为0.1541 nm) , 扫描角度范围2θ从20°~80°, 扫描步长为0.02°, 扫描电压为40 k V;表面元素分析采用多功能成像电子能谱仪 (XPS, 美国Thermo ESCACEB 250XI型) , 单色Al Kα (hv=1486.6e V) , 功率150 W, 500μm束斑;Ce/Ti O2紫外可见吸收光谱采用紫外-可见分光光度计 (日本岛津UV-2550型) , 利用小球积分法, 参比为Ba SO4, 扫描范围为200~700 nm;Ce/Ti O2比表面积和孔径分布利用低温N2物理吸附比表面仪 (美国Micromeritics ASAP 2460型) 测得;Ce/Ti O2表面形貌采用扫描电子显微镜 (SEM, 美国FEI MCE650F型) 和透射电子显微镜 (HRTEM, 美国Tecnai G2-20型, 工作电压为220 k V, 频率为50 Hz) 观测;采用ULTIMA型单道扫描电感耦合等离子体发射光谱仪 (Prodigy xp, 美国Lee labs公司) 测Ce/Ti O2中Ce的质量分数。
1.3催化剂活性评价
将一定量的Ce/Ti O2光催化剂分散到50 ml苯甲羟肟酸溶液 (30 mg・L-1) 中并置于光化学反应仪中。经过30 min避光搅拌后, 开启300 W汞灯照射, 分别在开灯光照后的0, 20, 40, 60, 80, 100, 120min取反应溶液5 ml, 用离心机 (14000 r・min-1) 离心5 min后, 在229 nm波长下用紫外-可见分光光度计测上清液的吸光度, 根据标准曲线得到溶液相应的浓度Ct。苯甲羟肟酸的降解率R根据公式 (1) 计算得到, 并以此来评价Ce/Ti O2的光催化活性。

式中:R为浮选捕收剂苯甲羟肟降解率, C0为光照前苯甲羟肟酸溶液初始浓度, mg・L-1;Ct为光照反应t min后苯甲羟肟酸溶液浓度, mg・L-1。
2结果与讨论
2.1 XRD分析
由图1可见, 所有Ce/Ti O2的衍射峰相似, 衍射峰的位置在2θ=25.21°, 36.75°, 37.53°, 38.40°, 47.87°, 53.53°, 54.86°, 62.37°, 68.30°, 70.03°, 74.63°附近, 与XRD标准卡中锐钛矿Ti O2 (JCPDS Card No.21-1272) 衍射峰相似[16,17]。由图1 (a) 可知, 所有Ce掺杂样品的衍射峰均变宽, 而且峰强度弱于纯Ti O2的相关衍射峰。可能是由于随着Ce的掺杂导致Ti O2的结晶度产生一定的下降, 使得Ce/Ti O2晶粒尺寸变小。催化剂的晶粒尺寸可根据Scherrer公式 (公式 (2) ) 来计算得到:

式中:D为晶粒大小;λ为X射线的波长, θ为0.154056 nm;β为衍射角;k为特征衍射峰半峰宽;k为谢乐常数, k=0.89。
由Scherrer公式计算得, 500℃下焙烧的纯Ti O2, 0.10%Ce/Ti O2, 0.20%Ce/Ti O2, 0.30%Ce/Ti O2, 0.40%Ce/Ti O2, 0.50%Ce/Ti O2的平均粒径分别为19.0, 16.5, 13.3, 13.1, 12.5, 12.4 nm。这可能是因为Ce3+的离子半径 (0.103 nm) 大于Ti4+的离子半径 (0.068 nm) , 导致大部分Ce3+难以进入Ti O2晶格中去取代Ti4+, 而是以氧化物Ce2O3的形式分散于Ti O2表面[18], 从而阻碍Ti O2晶粒的生长, 而这种氧化物易成为光生截留子捕获中心, 最终影响光催化活性。
图1 500℃煅烧的不同Ce/Ti O2的XRD图谱和不同温度煅烧的0.20%Ce/Ti O2的XRD图谱Fig.1 XRD patterns of samples
(a) Ce/Ti O2with different dopant amounts of Ce calcined at500℃; (b) 0.20%Ce/Ti O2at different calcined temperatures
2.2 XPS分析
图2 (a) 是经500℃煅烧处理的纯Ti O2和0.20%Ce/Ti O2的XPS全扫描图谱。由图2可见样品中含有元素Ti, O, C, 其中C可能是由外源性污染引起的[19]。图2 (b) 显示掺杂前后的全扫描图谱大致相似, 但掺杂后的XPS图谱中未检测出Ce在882 e V附近的特征峰, 说明在样品表面Ce的含量极低, 而经电感耦合等离子体发射光谱仪分析测得0.20%Ce/Ti O2中Ce的含量为0.016%, 证明了Ce的成功掺杂。
图2 (c) 和 (d) 是经500℃煅烧处理的纯Ti O2和0.20%Ce/Ti O2样品的Ti 2p窄扫描图谱。由图2可知, 经过拟合后两个样品中的Ti 2p的峰均是由Ti 2p1/2和Ti 2p3/2两个峰所组成的。其中纯Ti O2的Ti 2p1/2, Ti 2p3/2结合能在464.43, 458.73 e V处, 而经Ce掺杂样品的Ti 2p1/2, Ti 2p3/2结合能在464.38, 458.63 e V处, 这两个峰均为Ti4+的特征峰[20]。图2 (e) 和 (f) 是经500℃煅烧处理的纯Ti O2和0.20%Ce/Ti O2样品的O 1s窄扫描图谱。由图2 (e) 可以看出, O 1s特征峰经过拟合后, 样品的O 1s窄扫描XPS图谱出现了不同的分峰, 表明样品中的氧是以不同的形式存在的。其中纯Ti O2的O 1s结合能在529.88 e V处的强峰, 对应于Ti O2中的Ti-O键, 即Ti O2晶格中的晶格氧;位于531.41 e V处的弱峰则对应于Ti O2表面吸附氧的峰。而图2 (f) 则显示, 掺杂Ce后Ti O2样品中O 1s结合能在529.97, 531.46 e V处。因而, Ce掺杂后Ti 2p和O 1s的轨道峰位均有微弱的偏移。分析其原因可能由于Ti O2中掺杂的Ce原子与体相Ti O2之间产生了交互作用[21]。众所周知, 吸附氧可以抑制电子空穴的复合[22,23,24]。因此, 掺杂的催化剂相比未掺杂的催化剂具有更高的活性。
图2 Ti O2和0.20%Ce/Ti O2的XPS谱图Fig.2 XPS spectra of Ti O2and 0.20%Ce/Ti O2
(a) Survey spectra; (b) Ce 3d; (c, e) Ti 2p and O 1s of pure Ti O2; (d, f) Ti 2p and O 1s of 0.20Ce/Ti O2
2.3 UV-Vis DRS分析
图3为不同Ce掺杂比的Ce/Ti O2 (500℃) 的UV-Vis DRS光谱图。由图3可见, Ce掺杂后的光响应强度较纯Ti O2的光响应强度增强, 吸收边带发生一定程度的红移现象, 其中Ce掺杂比为0.20%时红移量最大。这可能与粒子丰富的表面态有关, 光响应范围向可见光区延伸, 光吸收能力的增强, 可激发产生更多的光生电子-空穴对, 从而有效提高光催化效率。通过带隙能公式[25]:

式中:α为吸收系数;h为普朗克常量, 为4.14×10-15e V・s;v为光的频率;Eg为带隙能;n的值由半导体的类型决定。由公式可计算Ti O2 (500℃) 和0.20%Ce/Ti O2 (500℃) 的禁带宽度Eg分别为3.18和2.93 e V。掺杂Ce后, Ti O2带隙间发生相应跃迁, 带隙能降低, 从而加快了光生载流子分离效率。
2.4比表面积及孔径分析
由图4 (a) 和 (b) 可见, 纯Ti O2和0.20%Ce/Ti O2的吸脱附曲线类型均显示为Ⅳ型等温曲线, 说明所制备的催化材料具有介孔结构[26,27]。吸脱附曲线不重合且会出现明显滞后环, 图4 (a) 为H4型, 图4 (b) 为H2型。由图中内插的孔径分布图可知, 催化剂的孔径分布范围均较窄, 基本分布在2~10 nm之间, 表明颗粒孔径大小处于介孔孔径的范围。纯Ti O2的最可几孔径为7.95 nm, BET测得比表面积为5.6998 m2・g-1。0.20%Ce/Ti O2的最可几孔径为7.76 nm, BET测得比表面积为40.4227m2・g-1。0.20%Ce/Ti O2的比表面积明显大于纯Ti O2。因而, 孔结构的构建有利于增大Ti O2比表面积。一般相对于催化材料, 比表面积越大, 表面起重要作用的反应活性位点也就随之越多, 从而越有利于光催化活性的提高[28]。
图3 不同Ce掺杂比的Ce/Ti O2的UV-Vis DRS图谱Fig.3 UV-Vis DRS patterns of Ce/Ti O2with different Ce do-ping ratios
图4 Ti O2和0.20%Ce/Ti O2N2吸脱附等温曲线及孔径分布曲线图Fig.4N2adsorption-desorption isotherms and BJH pore size distribution of Ce/Ti O2
(a) Undoped; (b) 0.20%Ce/Ti O2
2.5微观结构分析
由图5 (a) 和 (b) 可见, 纯Ti O2和0.20%Ce/Ti O2呈不规则形状, 颗粒大小不均。0.20%Ce/Ti O2的粒径明显小于纯Ti O2, 分散性也优于纯Ti O2, 说明Ce掺杂后可能导致Ti O2的粒径减小, 比表面积相应地增加, 催化剂颗粒没有掺杂前的团聚, 相对更加分散, 与上述XRD和BET的表征结果相一致。
图5 样品的SEM和HRTEM图Fig.5 SEM and HRTEM images of samples
(a, c) Ti O2; (b, d) 0.20%Ce/Ti O2
图5 (c) 和 (d) 为纯Ti O2和0.20%Ce/Ti O2的HRTEM图和相应的傅里叶变换衍射图。由图5可见, 纯Ti O2的晶格条纹间距主要为0.351和0.180nm, 0.20%Ce/Ti O2的晶格条纹间距主要为0.357和0.189 nm, 它们均分别对应于锐钛矿相Ti O2标准卡中 (101) 晶面和 (200) 晶面, 与XRD表征结果相符合。清晰的晶格条纹说明催化材料具有很好的结晶性, 其相应的傅里叶变换衍射图, 也显示出材料具有非常明显的单晶衍射点[29,30]。
2.6光催化活性评价
2.6.1不同Ce掺杂比的影响
室温下, 控制Ce/Ti O2 (500℃) 用量为0.3 g・L-1, 300 W汞灯照射, Ce的不同掺杂比对Ce/Ti O2光催化降解苯甲羟肟酸的效果见图6。
由图6可见, 掺杂Ce后光催化降解苯甲羟肟酸的效率均高于纯Ti O2的光催化效率。随着Ce掺杂比提高, 苯甲羟肟酸的降解率先增加后降低, 降解效果最佳的Ce掺杂比为0.20%。这可能是因为随着Ce量的增加, 影响了Ti O2的晶体结构, 使得Ti O2晶体产生一定的缺陷, 相应地, 晶体结构就会发生一定程度的畸变, 改变了能带结构而且降低了电子-空穴对复合的几率, 从而提高了Ce/Ti O2的光催化性能。当Ce掺杂比较小时, 在Ce/Ti O2晶格表层未产生足够的光生载流子捕获中心, 从而导致光催化活性较低;当Ce的掺杂比较大时, 晶格畸变导致晶体出现大量缺陷, 产生过多的氧空位引起空穴和电子的重新复合, 也会降低二氧化钛的光催化活性[31];当Ce掺杂比达到一个合适值时, 光催化活性才能达到最大, 结果表明Ce的最佳掺杂比为0.20%。上述实验结果与UV-Vis DRS表征结果相符。
图6 Ce掺杂比对Ce/Ti O2光催化降解苯甲羟肟酸的影响Fig.6 Effect of different doping ratios of Ce on photodegrada-tion of benzohydroxamic acid by Ce/Ti O2
2.6.2煅烧温度的影响
室温下, 控制0.20%Ce/Ti O2用量为0.3 g・L-1, 300 W汞灯照射, 考察不同的煅烧温度对Ce/Ti O2光催化降解苯甲羟肟酸的效果, 结果见图7。
由图7可见, 当Ce/Ti O2的煅烧温度为500℃, 光催化降解苯甲羟肟酸的效率比其他温度下的Ce/Ti O2要好。分析其原因:煅烧温度过低, Ce/Ti O2煅烧不完全, 结晶化程度不高, 有无定型态的Ti O2存在, 表面存在大量的光生电子与空穴复合中心;随着温度的适当升高达到一定值时, Ce/Ti O2的晶型由无定型态慢慢转变为锐钛矿相, 结晶化程度更完全, 使得光生电子-空穴复合几率减少, 从而光催化活性也相应地增强;当催化剂的温度过高时, Ce/Ti O2晶相会由锐钛矿相向金红石相转变, 晶相的转变可能会导致光催化降解活性降低。
图7 煅烧温度对Ce/Ti O2光催化降解苯甲羟肟酸的影响Fig.7Effect of calcination temperatures on photodegradation of benzohydroxamic acid by Ce/Ti O2
2.6.3苯甲羟肟酸的矿化率
矿化率更能直接的反应有机污染物质向CO2和H2O等简单的无机物质转化的程度。在室温下, 控制0.20%Ce/Ti O2用量为0.3 g・L-1, 300 W汞灯照射, 降解后的溶液经0.22μm滤膜过滤后, 通过TOC分析仪测定, 结果见图8。
由图8可见, 加入0.20%Ce/Ti O2后, 苯甲羟肟酸的矿化率可达到82.8%, 说明苯甲羟肟酸经降解后可能转变成小分子的物质CO2和H2O等。
2.6.4催化剂稳定性研究
在实际的生产应用当中, 半导体催化剂的稳定性能对于其能否长期使用是十分重要的。因此, 考察Ce/Ti O2光催化降解苯甲羟肟酸的重复利用效率是十分必要的。室温下, 选择0.20%Ce/Ti O2 (500℃) 用量为0.5 g・L-1, 300W汞灯照射120 min, Ce/Ti O2重复使用对光催化降解苯甲羟肟酸的影响结果如图9。
由图9可知, 随着Ce/Ti O2光催化降解重复使用次数的增多, 苯甲羟肟酸的降解率并无明显降低, 重复使用4次的降解实验中的最大和最小降解率仅相差3.4%, 说明所合成的Ce/Ti O2催化材料在长时间的使用下仍保持较高的稳定性和活性, 可以被多次重复使用, 从而为其在实际的工程应用中提供了可能。
图8 苯甲羟肟酸的矿化率Fig.8TOC mineralization rates of benzohydroxamic acid by0.20%Ce/Ti O2, pure Ti O2and blank
图9 Ce/Ti O2重复使用次数对光催化降解苯甲羟肟酸的影响Fig.9 Recycling test of Ce/Ti O2for photocatalytic degradation of benzohydroxamic acid
2.7机制探讨
根据实验结果和相关文献[8, 32-33], Ce/Ti O2光催化的机制可能主要与稀土元素Ce具有特殊的4f电子层和可变的离子对Ce3+/Ce4+相关, 其过程为:
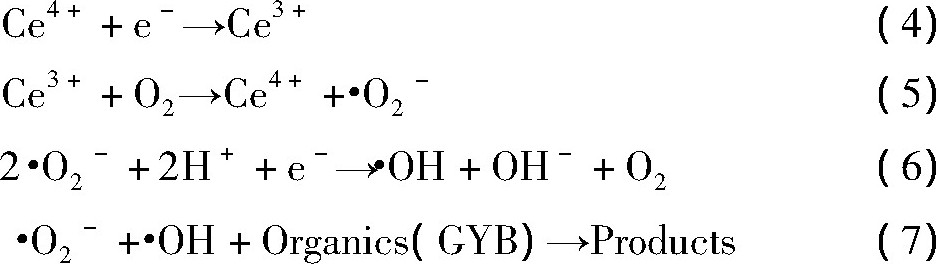
Ce3+和Ce4+共存于Ce/Ti O2的表面, 两者之间的相互转换改变了光催化反应中电子空穴对的复合速率。反应 (4) 显示Ce4+会形成电子捕获陷阱, 捕获电子后形成Ce3+, 反应 (5) 显示了化学吸附氧能够与产生的Ce3+作用产生超氧离子自由基。反应 (6) 显示了超氧离子自由基在酸性条件下可以更加容易得到电子而生成羟基自由基 (经测定, 30mg・L-1的苯甲羟肟酸溶液为弱酸性, p H约为4.4) , 由于羟基自由基和超氧离子自由基属于强氧化性物质, 因此能够将有机污染物氧化分解生成小分子的产物, 即发生反应 (7) 。在纯Ti O2的表面, 吸附氧转换生成超氧离子自由基受到很大程度的限制, 从而导致光催化效率较低。当Ce掺杂后, 能够激发受束缚的电子, 增加了Ti O2对O2的吸附, 从而加速反应 (5) 的进行, 从而提高光催化效率。
图1 0 Ce/Ti O2光催化降解苯甲羟肟酸过程中可能的电荷转移机制Fig.10 Proposed mechanism of charge carrier transition of Ce/Ti O2
3结论
1.通过溶胶-凝胶法成功制备出了锐钛矿型Ce/Ti O2纳米光催化剂, 其结晶度好, 颗粒分散性较均匀。
2.表征结果表明Ce的掺杂抑制了锐钛矿相Ti O2晶粒生长, 使催化剂晶粒尺寸减小, 从而比表面积增大, 0.20%Ce/Ti O2 (500℃) 比纯Ti O2 (500℃) 的比表面积有显著提高 (7倍多) ;另外, Ce的掺杂增强了光响应强度, 吸收边带发生红移, 为利用可见光降解苯甲羟肟酸提供了可能。
3.苯甲羟肟酸降解实验数据表明当Ce的掺杂比为0.20%, 煅烧温度为500℃时, Ce/Ti O2光催化降解苯甲羟肟酸效果为最佳。催化剂的重复性实验表明, Ce/Ti O2在使用较长的时间下仍保持较高的催化活性, 因而具有较高的稳定性。
4.通过电荷转移机制推论:Ce的掺杂主要是激发受束缚的电子, 提高了Ti O2表面电子-空穴对的分离速度, 提升了Ti O2对O2的吸附能力和速率, 光生电子-空穴复合减少使其复合率下降, 从而使Ce/Ti O2光催化降解浮选捕收剂苯甲羟肟酸的速率增加。
参考文献

