介孔CeO2的化学沉淀法合成及表征
宋晓岚, 江 楠, 曲 鹏, 何 希, 杨海平, 邱冠周
(中南大学 资源加工与生物工程学院 无机材料系, 长沙 410083)
摘 要: 以硝酸铈(Ce(NO3)3・6H2O)、 碳酸铵((NH4)2 CO3 ・H2O)为原料, 十六烷基三甲基溴化铵(CTAB)为模板剂, 采用化学沉淀法合成了一系列具有不同孔径的介孔CeO2粉末, 使用X射线衍射(XRD)、 差示/热重(DSC/TG)、 BET孔性能测试、 透射电镜(TEM)及红外光谱(IR)分析等手段对合成产物进行了分析和表征, 探讨了CTAB与Ce的摩尔比、 反应温度、 焙烧温度和时间对孔径大小和比表面积的影响。 在CTAB与Ce的摩尔比为1∶1、 反应温度为80℃、 焙烧温度为300℃、 焙烧时间为1h条件下, 制得了比表面积为132m2/g的介孔CeO2。
关键词: 介孔氧化铈; 沉淀法; 比表面积 中图分类号: O614.33; TB383
文献标识码: A
Synthesis and characterization of mesoporous CeO2 via chemical precipitation method
SONG Xiao-lan, JIANG Nan, QU Peng, HE Xi,YANG Hai-pin, QIU Guan-zhou
(Department of Inorganic Materials, School of Resources Processing and Bioengineering,Central South University, Changsha 410083, China)
Abstract: Mesoporous CeO2 powders with different pore sizes were synthesized by chemical precipitation method with cerium nitrate and ammonium carbonate as raw materials and cetyltrimethyl ammonium bromide(CTAB)as templates. X-ray diffractometry (XRD), different scanning calorimetry/thermalgravimetry (DSC/TG), BET method, transmission electron microscopy (TEM) and infrared (IR) absorbance were used to analyze and characterize the products. The effects of some factors, such as the mole ratio of CTAB to Ce, reaction temperature, calcination temperature and calcination time, on porous size and specific surface area were investigated. Mesoporous CeO2 with specific surface area of 132m2/g was made under the condition as: the ratio of CTAB to Ce 1∶1, the reaction temperature 80℃, the calcination temperature 300℃ and the calcination time 1h.
Key words: mesoporous CeO2; precipitation method; specific surface area
根据国际纯粹和应用化学联合会(IUPAC)的定义, 孔径小于2nm的多孔材料称为微孔材料, 如沸石分子筛之类; 大于50nm的多孔材料称为大孔材料, 如多孔陶瓷、 气凝胶等; 介于两者之间(2~50nm)的多孔材料则称为介孔材料(mesoporous materials)[1]。 非硅组成的介孔材料的研究在过去短短的8年里取得了长足的进展, 大孔径、 高比表面积及高热稳定性的非硅介孔材料的合成已经为人们展示了其发展的巨大潜力以及在光、 电、 磁、 化学传感器等方面独特的应用前景, 同时也为多相催化、 吸附分离、 能量储存、 生物化学等领域开拓了新的研究方向[2-3]。 Devi等[4]的研究证实, 作为传感器材料TiO2的气敏性可以通过获得和控制介孔结构来提高。
CeO2是稀土家族中一种重要的氧化物, 在催化、 涂料、 照明、 超导体、 感应器等方面有许多应用。 CeO2属萤石结构, 结构中存在1/2的立方体空隙位置, 能成为离子快速扩散的通道而形成快离子导体, 使CeO2有着优越的储放氧功能及高温快速氧空位扩散能力而被广泛用于汽车尾气净化催化[5]、 氧敏材料[6]及电极材料[7], 在现代高科技领域有着很大的发展潜力。 介孔CeO2因具有特有的结构, 可使其催化活性和氧敏性能得到进一步改善。 目前国外对介孔CeO2的研究较为活跃, 合成介孔CeO2方法有有机/无机氢化物合成法[8]、 简单快速蒸发法[9-10]以及低温化学法[11]等。 但迄今为止, 在国内尚未见到介孔CeO2合成制备与性能研究的相关文献报道。
液相化学沉淀法由于其原料成本低、 制备过程对环境污染小、 工艺过程简单、 工业放大容易而备受关注。 本文作者以硝酸铈(Ce(NO3)3・6H2O)、 碳酸铵((NH4)2 CO3 ・H2O)为原料, 以十六烷基三甲基溴化铵(CTAB)为模板剂, 采用沉淀法合成了具有不同孔径的介孔CeO2, 运用XRD、 DSC/TG、 BET、 TEM、 IR等方法对合成产物进行了结构分析和表征, 并讨论了CTAB与Ce的摩尔比、 反应温度、 焙烧温度和时间等因素的影响。
1 实验
1.1 样品制备
按化学计量比将分析纯Ce(NO3)3・6H2O和(NH4)2 CO3 ・H2O溶于水, 配成溶液, 往硝酸铈溶液中加入一定量的阳离子型表面活性剂――十六烷基三甲基溴化铵(CTAB), 用超声波溶解分散, 得混合液, 将混合液和碳酸铵溶液在水浴中分别预热30min和10min后, 将碳酸铵溶液倒入装有混合液的烧杯中, 接着用一定浓度的NaOH溶液调节混合液pH值至9左右, 然后用电动搅拌器以800r/min速度恒温均匀搅拌10h, 使其充分反应, 所得前驱体经真空抽滤、 多次洗涤、 真空60℃干燥过夜、 焙烧后得到淡黄色粉末产品。 制备条件和样品编号如表1所示, 分别考察了CTAB与Ce的摩尔比、 反应温度、 焙烧温度和焙烧时间对合成产物的影响。
1.2 测试
用日本理学Rigaku的Dmax/350 X射线衍射仪表征前驱体和产物的晶相组成和结构(XRD), 扫描范围: 小角1°~10°及大角10°~90°; 用德国耐驰Netzsch STA 449C综合热分析仪进行前驱体的差示/热重分析(DSC/TG); 用美国的NOVA-1000孔分析仪测定产物的N2等温吸附曲线、 比表面积和孔径分布(BET); 用美国Nicolet公司的Mexus傅立叶红外光谱仪进行有机物的定性分析(FT-IR)。
表1 介孔CeO2的制备参数
Table 1 Preparation parameter of ceria samples

2 结果与讨论
2.1 前驱体的XRD和DSC/TG分析

图1 样品C14的前驱体的XRD谱
Fig.1 XRD patterns of precursor of sample C14
样品C14的前驱体XRD谱如图1所示, 可知样品C14的前驱体中除了含有水合碳酸铈外, 还含少量CeO2, 表明沉淀反应形成前驱体Ce2(CO3)3・H2O后在干燥过程中有少量Ce2(CO3)3・H2O分解并氧化产生CeO2。

图2 样品C14的前驱体的DSC/TG曲线
Fig.2 DSC/TG curves for precursor of sample C14
图2所示为样品C14的前驱体的DSC/TG分析结果。 由图可见, 在30~100℃之间DSC曲线的吸热峰对应的是样品中吸附水分的脱附, 相应TG曲线上有质量损失; 在250~300℃, DSC曲线出现明显吸热峰, 该处应是前驱体中Ce2(CO3)3・H2O的分解氧化峰[12], 其分解氧化可表示为
2Ce2(CO3)3・H2O+O2=4CeO2+6CO2↑+2H2O↑
相应TG曲线急剧下降, 质量损失达21.61%; 300℃之后TG曲线较平稳, 表明样品已分解完全。
2.2 产物的XRD表征
图3和4所示分别为样品C14的小角度XRD谱和大角度XRD谱。 由图3可见, 在1°~2°间出现了表明存在介孔结构的特征衍射峰, 说明样品C14是介孔CeO2。 从图4可看出, 具有介孔结构的样品C14出现了CeO2立方萤石结构的特征峰, 表明产物C14是结晶良好的具有立方萤石型结构的单相CeO2(JCPDS: 34-394)。 图4中所显示的皆是C14的CeO2 特征峰; 结合图1和图2, 知道前驱体中的Ce2(CO3)3・H2O焙烧后完全转变为CeO2。

图3 样品C14的小角度XRD谱
Fig.3 Small angle XRD patterns of sample C14

图4 样品C14的XRD谱
Fig.4 XRD patterns of sample C14
2.3 产物的BET分析
图5(a)所示表明, 样品C14的N2吸附-脱附等温曲线属于IUPAC分类中的Ⅳ型, 是典型的介孔物质吸附曲线。 在液氮温度下, 样品的吸附量随N2相对压力p/p0 (p为压力, p0为饱和蒸汽压)的变化呈以下几个阶段: 1)低压段(0〈p/p0〈0.4), 样品N2吸附随着相对压力的上升增长平缓, 等温线较平坦, 而且吸附与脱附线基本重合, 此时N2分子以单层到多层吸附于孔内表面, 在壁上形成薄膜; 2)中等压力段(0.4〈p/p0〈0.9), 在p/p0=0.4处, 吸附线与脱附线开始分支不重叠, 出现滞后回环。 在这一阶段过程中未出现孔壁多层吸附和孔腔的毛细凝聚的明显分界, 即吸附曲线比较平滑, 无明显突跃部分, 表明介孔CeO2的孔径存在着一定的分布范围; 3) 高分压段(0.9〈p/p0〈1), 发生的是颗粒外表面的多分子层吸附; 在p/p0=0.93时候出现了突跃, 这来源于颗粒间的孔隙所造成的毛细管凝聚。
图5(b)所示为样品C14的孔径分布图。 从图中可看出, 样品C14的孔径主要分布在2~10nm范围内, 即样品孔结构中占主导地位的是介孔。 根据BJH法算得的平均孔径是3.27nm。
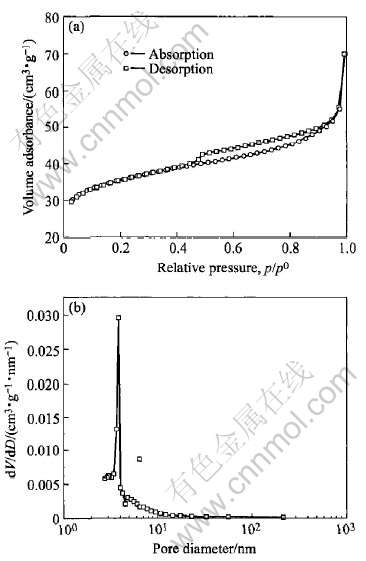
图5 样品C14的N2吸/脱附等温曲线(a)及孔径分布图(b)
Fig.5 N2 adsorption/desorption isotherm curve(a) and pore size distribution(b) of sample C14
2.4 产物的TEM分析

图6 样品C14的TEM照片
Fig.6 TEM image of sample C14

图7 样品C14焙烧前后的红外吸收光谱
Fig.7 FT-IR spectra of sample C14 before and after calcination
图6所示为样品C14的TEM照片。 从图中可以清晰看出分布在样品中孔道结构。 样品有序度不高, 孔道呈不规则分布, 而且孔径分布范围较大, 这与BET的分析完全吻合。
2.5 红外光谱分析
图7所示为样品C14经过300℃焙烧前后的红外吸收光谱。 图中3400cm-1附近强烈的羟基峰为样品中吸附的少量水所产生的振动峰; 1600cm-1区域出现的弱峰为样品中残留的模板剂中C―H的弯曲振动峰; 700cm-1区域出现的弱峰则为样品中残留的模板剂中C―H亚甲基的弯曲振动峰; 1300cm-1区域出现的峰是Ce―O―Ce的振动峰; 同时还有1000~1100cm-1区域出现的一系列弱峰, 这些峰的强度和最后制得的CeO2的比表面积的大小有关[8]。 由图7可见, 在1400~1600cm-1间, 焙烧后样品的振动峰尖锐程度下降, 说明了随着焙烧温度的升高, C―H 振动峰强度逐渐下降, 对应样品中的有机质逐渐减少, 与文献[13]结果相符。 最重要的是1300cm-1区域出现的振动峰在焙烧后峰形变大、 变缓, 说明形成Ce―O―Ce键, 生成CeO2。
2.6 介孔CeO2比表面积的影响因素
比表面积是介孔CeO2的性能参数, 直接影响其催化反应活性及氧敏性能[14]。 影响沉淀法合成介孔CeO2比表面积的因素很多。 本实验系统研究了前驱体合成过程中浓度配比、 沉淀反应温度以及前驱体热处理过程焙烧温度和焙烧时间对介孔CeO2比表面积的影响。
图8所示为CTAB与Ce摩尔比对介孔CeO2比表面积的影响。 结果表明, 随CTAB用量增加, 比表面积有增加的趋势, 当x(CTAB)∶x(Ce)=1∶1时, 介孔CeO2的比表面积达到95m2/g。 这是因为表面活性剂浓度增大, 将导致溶液中表面活性剂胶束和六方液晶相增多, 有利于介孔CeO2的形成。

图8 CTAB与Ce的摩尔比与介孔CeO2比表面积的关系
Fig.8 Variation of surface area with x(CTAB)/x(Ce)
介孔CeO2比表面积随反应温度变化的关系如图9所示, 图示结果显示宜采用较高的反应温度。 过低的反应温度将不利于高比表面积介孔CeO2的生成, 这是因为: 在沉淀反应中, 温度会对晶粒的生成和长大有一定影响。 当温度较低时, 过饱和度较大, 成核的速度快, 一般得到细小的颗粒, 但颗粒太小, 则难以过滤和洗涤, 容易团聚而形成更大的颗粒[15]; 升高温度则能使沉淀反应的反应常数增大, 反应速率加快, 同时也使布朗运动加速, 从而使质点间碰撞的频率增大。 因此, 在一定范围内提高反应温度能提高溶液中离子的反应活性, 有利于反应的充分进行。

图9 反应温度与介孔CeO2比表面积的关系
Fig.9 Variation of surface area with reaction temperature
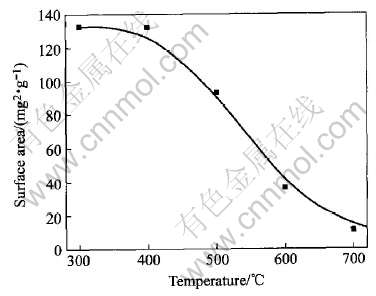
图10 碳酸铈的焙烧温度与CeO2比表面积的关系
Fig.10 Variation of surface area with calcination temperature

图11 碳酸铈的焙烧时间与CeO2比表面积的关系
Fig.11 Variation of surface area with calcination time
焙烧过程可以迅速除去混合在沉淀物碳酸铈中的模板剂, 同时沉淀物会发生脱水、 分解、 相转变、 烧结致密化和晶粒长大等一系列的变化, 研究焙烧条件有助于控制晶相结构和粉末粒径。 由图10可见, 随焙烧温度升高, 介孔CeO2粉末粒径变大, 导致比表面积的降低。 300℃焙烧时得到的介孔CeO2比表面积最大, 达到132m2/g。 而当焙烧温度从300℃提高到800℃, 比表面积急剧下降到20m2/g以下, 这是由于CeO2颗粒在高温烧结导致晶粒长大造成。
图11所示为CeO2比表面积随焙烧时间变化的关系图, 即太长的焙烧时间不利于介孔CeO2的生成。 这是因为, 前驱体焙烧过程将发生脱水、 分解并去除模板剂, 使CeO2产生多孔性。 焙烧时间太长, 会导致CeO2颗粒被烧结, 介孔结构被破坏, 造成孔径变小, 比表面积下降。 实验表明, 焙烧时间为1h最合适。
3 结论
1) 采用液相化学沉淀法, 以硝酸铈为铈源, 碳酸铵为沉淀剂, CTAB为模板剂, 在弱碱条件下, 通过控制反应条件和焙烧条件, 在CTAB与Ce的摩尔比为1∶1, 反应温度为80℃, 焙烧温度为300℃, 焙烧时间为1h的合成条件下, 制备出比表面积达132m2/g的介孔CeO2粉末, 其孔径范围2~10nm, 平均孔径3.27nm。
2) 在介孔CeO2合成过程中, 随模板剂浓度增大, 介孔CeO2比表面积增大; 而随焙烧温度升高, 焙烧时间延长, 所得到介孔CeO2的比表面积减小。
REFERENCES
[1]IUPAC. Manual of symbols and terminology[J] . Pure Appl Chem, 1972, 31: 578-638.
[2]Kishor M N, Masahiro F, Yuko T. Photocontrolled reversible release of guest molecules from coumarin-modified mesoporous silica[J]. Nature, 2003, 421: 350-353.
[3]Joo S H, Choi S J, Oh I, et al. Ordered nanoporous arrays of carbon supporting high dispersions of platinum nanoparticles[J]. Nature, 2001, 412: 169-172.
[4]Devi G S, Hyodo T, Shimizu Y, et al. Synthesis of mesoporous TiO2-based powders and their gas-sensing properties[J]. Sensors and Actuators B, 2002, 87: 122-129.
[5]Kaspar J, Fornasiero M, Graziani M. Use of CeO2-based oxides in the three-way catalysis[J]. Catalysis Today, 2000, 50: 285-298.
[6]Noriya I, Woosuck S, Norimitsu M, et al. Resistive oxygen gas sensors based on CeO2 fine powder prepared using mist pyrolysis[J]. Sensors and Actuators B, 2002, 87: 95-98.
[7]Toshiyuki M, John D, Wang Y R, et al. Influence of nanostructure on electrolytic properties in CeO2 based system[J]. Journal of Thermal Analysis and Calorimetry, 2002, 70: 309-319.
[8]Terribile D, Trovarelli A. The synthesis and characterization of mesoporous high-surface area ceria prepared using a hybrid organic/inorganic route[J]. Journal of Catalysis, 1998, 178: 299-308.
[9]Lundberg M, Cesa F. Mesoporous thin films of high-surface-area crystalline cerium dioxide[J]. Microporous and Mesoporous Materials, 2002, 54: 97-103.
[10]Lundberg M, Wallenberg L R. Crystallography and porosity effects of CO conversion on mesoporous CeO2[J]. Microporous and Mesoporous Materials, 2004, 69: 187-195.
[11]Levy C, Guizard C. Synthesis of ceria based ion conducting mesoporous membranes by soft-chemistry[J]. Separation and Purification Technology, 2003, 32: 327-333.
[12]张国栋. 材料研究与测试方法[M]. 北京: 冶金工业出版社, 2002: 154-159.
ZHANG Guo-dong. Research on Materials and Test Methods[M]. Beijing: Metallurgical Industry Press, 2002: 154-159.
[13]刘建红. 稀土醇盐及稀土氧化物介孔材料的合成及表征[D]. 北京: 北京化工大学, 2003: 28-34.
LIU Jian-hong. Synthesis and Characterization of Mesoporous Rare Alkoxide and Rare Oxide Materials [D]. Beijing: Beijing University of Chemical Technology, 2003: 28-34.
[14]张绍岩, 丁士文, 刘淑娟, 等. 均相沉淀法合成纳米ZnO及其光催化性能研究[J]. 化学学报, 2002, 60(7): 1225-1229.
ZHANG Shao-yan, DING Shi-wen, LIU Shu-juan, et al. Synthesis and photocatalytic property of nano ZnO[J]. Acta Chimica Sinica, 2002, 60(7): 1225-1229.
[15]肖楚民, 潘湛昌, 张环华, 等. 碳酸氢铵沉淀法制备二氧化铈超细粉体[J]. 矿冶工程, 2003, 23(1): 41-43.
XIAO Chu-min, PAN Zhan-chang, ZHANG Huan-hua, et al. Preparation of ultrafine powders CeO2 using precipitation method[J]. Mining and Metallurgical Engineering, 2003, 23(1): 41-43.
(编辑何学锋)
基金项目: 科技部国际科技合作项目(2005DFBA008); 国家自然科学基金项目资助(59925412)
收稿日期: 2006-04-28; 修订日期: 2006-07-17
通讯作者: 宋晓岚, 副教授; 电话: 0731-8877203; E-mail: xlsong@hnu.cn