���±�ţ�1004-0609(2008)06-1159-05
��TiCl4ͭ˿��������ˮ�ľ����¹���
����Ƽ1����ѧ��1��Ԭ��ά2�����˳�2
(1. ���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083��
2. ������ҵ�ɷ�����˾������ 563004)
ժ Ҫ������ͭ�������ﹲ������������ͭ˿��������ˮ���������е�ͭ�ͷ����������ˮ��Cu��V����Ч���ĸ���Ӱ�����ء�������������½����NaOH��ͭ˿��������ˮ��pHֵ����3.0~4.0����H2O2�ɽ����е�V4+������V5+���ٲ���Cu2+ʹCu��V��Ħ��������7.5~8.5��Ȼ���ټӼ��к�pHֵ��7.5~8.5����������20 min����ˣ���Һ��Cu��V��Ũ�Ⱦ�С��2.0 mg/L���ﵽ������ˮ�ۺ��ŷű��������к�Cu 45%~60%��V 11%~15 %�����кܸߵ��ۺϻ��ռ�ֵ��
�ؼ��ʣ�TiCl4��ͭ˿����ˮ�������ۺϻ���
��ͼ����ţ�TQ 134.1��TF 841 ���ױ�ʶ�룺A
New purification technique of wastewater in
removing vanadium from raw TiCl4 with copper wire
ZHANG Li-ping1, WANG Xue-wen1, YUAN Ji-wei2, GONG Shi-cheng2
(1. School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China;
2. Zunyi Titanium Industry Co. Ltd., Zunyi 563004, China)
Abstract��A coprecipitation process was used to purify the washing water and recover copper and vanadium. The factors affecting the purification were investigated. The results show that when the washing water is treated by adding sodium hydroxide to precondition the pH value to 3.0-4.0 under stirring, vanadium is oxidized from V4+ to V5+ with H2O2. The molar ratio of Cu to V is increased to 7.5-8.5 by adding Cu2+. The solution is neutralized to pH value of 7.5-8.5 with NaOH, then the solution is filtered after agitating for 20 min at room temperature. The filtrate is very clear with concentrations of V and Cu less than 2.0 mg/L, which meet with the National Standards of Integrated Discharged Wastewater. The contents of copper and vanadium in the filter residues are 45%~60% Cu and 11%~15% V, which is a good crude material for recovery of vanadium and copper.
Key words: TiCl4; copper wire; wastewater purification; comprehensive recovery
TiCl4�ǽ����Ȼ�ԭ�����������Ѽ��Ȼ������������Ѱ�ԭ�ϣ������ѹ�ҵ�ķ�չ��TiCl4�IJ���������[1-2]����������ʯ���������̼�Ȼ��õ��Ĵ�TiCl4�к��������ʣ�������Ҫ�������У�FeCl3��AlCl3��TiOCl2��SiCl4��VOCl3��Cl2��HCl��VCl4�ȡ���TiCl4����ͨ�������ᴿ��������ں����Ѽ��Ѱ��� ��[3-4]����TiCl4�е�SiCl4��Cl2��HCl�ȵͷе����ʿ���ͨ������ȥ����FeCl3��TiOCl2�ȸ߷е����ʱ�����������ܷ��룬��VOCl3��TiCl4������ѹ�ӽ���ֻ�ܲ��û�ѧ�������ѳ�����ѧ���������ڴ�TiCl4�м���һ�ֻ�ѧ����ʹ����VOCl3��ѡ���Ի�ԭ������������TiCl4�ķ�������������롣�������о������ڳ����Ļ�ѧ�Լ�����10�֣���ҵ�����г��õķ�����Ҫ�У�ͭ˿�����������۳�������������������л��������[5]��
Ŀǰ���ڱȽϳ���ij���������ͭ˿����������TiCl4ͭ˿�������Ļ������£���ͭ˿����ԭ������VOCl3��ԭ�ɲ�����TiCl4��VOCl2���÷�����Ч���ã���Ʒ����ʸߣ��������̼��������㣬ͭ�Բ�Ʒ��������Ⱦ��������ͬʱ����ȥ���л���ڳ��������У�ͭ˿�μӻ�ԭ��Ӧ�������ģ��γ�VOCl2��CuCl��������ͭ˿�����ʹ��һ��ʱ���ͭ˿�Ļ��Ա����С�����������½�����ˣ�Ϊ��ȷ��TiCl4�з����������꣬������ˮ��ϴͭ˿����ij������Իָ��仹ԭ����[6]����ϴ������CuCl��ˮ���Cu��CuCl2��TiCl4ˮ������TiO2�����ᣬVOCl2������ˮ����ת����VO2+����ϴͭ˿���õ��ķ�ˮpHֵΪ1.0~2.0�� ���ַ�ˮ�������ֳ�һ��ֻ����м�������������ˮ������������ˮ��Ϻ�һ��������ˮ�е�ͭ�ͷ������գ��������ͭ������Դ�˷ѣ����������ˮ�������Ѷȡ��������߲���ͭ ����������������ͭ˿��������ˮ�����������е�ͭ�ͷ�[7]��
1 ʵ��
1.1 ʵ��ԭ��
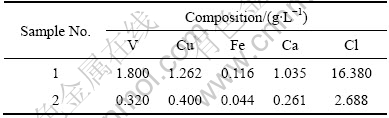
ʵ������ԭ��Ϊ�����ѳ���TiCl4ͭ˿��������ˮ������Ҫ�ɷ����ڱ�1����1��1�ŷ�ˮΪͭ˿��һ��ϴˮ��2�ŷ�ˮΪͭ˿������ϴˮ��1�ŷ�ˮ��pHֵΪ1.1��2�ŷ�ˮ��pHֵΪ1.8�����ַ�ˮ����dz��ɫ�����Ӽ��ˮ��pHֵ����3.0~5.0�����ǵ���ɫ�����ī��ɫ������V2O4�����������������������������������
��1 ͭ˿��������ˮ�Ļ�ѧ�ɷ�
Table 1 Composition of waste water formed by washing VOCl2 and CuCl adhered on copper-wire
1.2 ʵ���������Լ�
ʵ����Ҫ�������£����ͷ���Ƚ�����(CJJ-931,��̳�о���ʵ��������)��ԭ�����չ�����(AAnalyst100������)��pH��(Orion Model 410A������)��
ʵ�������Լ�Ϊ���������ơ�H2O2 (H2O2��30%)������ͭ���Լ���Ϊ��������
1.3 ʵ�鷽��
ʵ���жԷ�ˮ��Cu��V����Ч���ĸ������ؽ��п��죬ÿ����ȡ100 mLͭ˿��������ˮ����500 mL�ձ��У��Ƚ������һ������NaOH��ҺԤ��pHֵ��3.0~4.0����Һ��ɫ��dz��ɫ���ī��ɫ�����ż���H2O2��V4+������V5+����Һ����ɫ��Ϊ����ɫ��������Cu2+������Һ��Cu��VĦ����(ʵ����ڼ��Լ�����ͭ�����Ϊͭ˿������ϴˮ��������������ͭ�ĽᾧĸҺ)��Ȼ���ټӼ��к�ʹCu��V�ȳ������������ˣ�ȡ��������ʵ�鷢�֣���ҺpHֵ������5.0֮����Һ�п�ʼ�в���ɫ���������������Ӽ����Һ��pHֵ����7.0���ң����ó�����ˣ�ȡ��������Һ��������Cu��V�ĺ�����
1.4 ��������
ʵ����Ʒ�з������IJⶨ���÷����ı���������������������淋ζ�����ͭ�����ĸƵĺ�������ԭ�����շֹ��ȷ�������������Ũ�Ȳ�����������Һ�ζ����ζ�����Һ��pHֵ��pH�Ʋⶨ��
2 ���������
2.1 pHֵ����Һ��Cu��VŨ�ȵ�Ӱ��
��1�ŷ�ˮ�Ӽ�Ԥ��pHֵ��4.0���ټ�0.25 mL H2O2������Cu2+������Һ��Cu��V Ħ����Ϊ8.0�������²�ͬpHֵʱ�ⶨ��Һ��Cu��V��Ũ�ȣ�������2���С�
��2 ����pHֵ����Һ��Cu��VŨ�ȵ�Ӱ��
Table 2 Effect of precipitated pH value on concentrations of Cu and V in filtrate

�ɱ�2��֪�����ų���pHֵ���ߣ���Һ��Cu��V�������͡�������pHֵΪ4.3ʱ����Һ�л���Cu 375 mg/L����������ȫ��ҪʹCu2+��ȫ��������Һ��pH���������7.17���ϣ���ΪCu(OH)2������Ũ�Ȼ�KspΪ2.2��10-20[8]��������pHֵ������7.5ʱ����Һ��Cu��V��Ũ�Ⱦ�С��2.0 mg/L���ﵽ������ˮ�ۺ��ŷű�����ˮ�е�V4+�Ӽ��pHֵ�����ױ�H2O2������V5+������pHֵ�����ߣ�Cu2+��V5+�γ�ͭ��������(xCuO?yV2O5?zH2O)����[9]������Һ��pHֵ������7.5���ң���Һ�����ɵ�Cu(OH)2�ǻ�����������������Ч����ͭ��������γɹ�������ʵ�鷢�֣���ˮ���γɵ�ͭ���������̶���ѧ��ɣ�������������ԭ������ǣ���Һ��V5+��pHֵΪ7.5�����ж��ִ�����ʽ�� ��
�� ��
��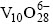 �ȣ���pHֵ��ͬʱ��V5+�ĸ��ִ�����ʽ�ı���Ҳ��ͬ[10-11]���кͷ�ˮ�ij�������Ϊ����ɫ������Ҫ��ѧ�ɷ����� ��3���ӱ�2��3���Կ��������Ʒ�ˮ��pHֵ7.5~8.5����������Һ��pHֵ��Cu��VŨ�ȿ�ֱ�Ӵﵽ������ˮ�ۺ��ŷű������˺�õ��ij�����������ɺ����õ����к�Cu(��������)45%~60%��V 11%~ 15%�������ۺϻ������á�
�ȣ���pHֵ��ͬʱ��V5+�ĸ��ִ�����ʽ�ı���Ҳ��ͬ[10-11]���кͷ�ˮ�ij�������Ϊ����ɫ������Ҫ��ѧ�ɷ����� ��3���ӱ�2��3���Կ��������Ʒ�ˮ��pHֵ7.5~8.5����������Һ��pHֵ��Cu��VŨ�ȿ�ֱ�Ӵﵽ������ˮ�ۺ��ŷű������˺�õ��ij�����������ɺ����õ����к�Cu(��������)45%~60%��V 11%~ 15%�������ۺϻ������á�
��3 ��ͬ����pHֵ�����µõ���������Ҫ�ɷ�
Table 3 Compositions of filter residues formed under different precipitated pH values

2.2 H2O2������Cu��V����Ч����Ӱ��
�����½�1�ŷ�ˮ�Ӽ�Ԥ����Һ��pHֵ��3.0���ټ���һ������H2O2��������Cu2+������Һ��Cu��VĦ����Ϊ8.0��Ȼ���ټӼ��к�����ҺpHֵΪ8.0������20 min����˵õ�H2O2������Cu��V����Ч����Ӱ�죬�����ͼ1��ʾ����ͼ��֪��δ��H2O2��������Һ��V��Ũ�Ƚӽ�200 mg/L��Cu��Ũ��Ҳ��50 mg/L���ϣ�Զ������ˮ�ۺ��ŷű�������H2O2����Һ��Cu��V��Ũ�����������͡���H2O2�ļ���������0.25 mL֮����Һ��Cu��V��Ũ�Ⱦ�С��2.0 mg/L���ﵽ���ҹ涨���ŷű����������������0.25 H2O2�ɽ�100 mL��ˮ�е�V4+��ȫ������V5+���ɱ�1���Եó���100 mL��1�ŷ�ˮ�е�V4+��ȫ����������H2O2������������0.2 mL��H2O2����Ч�����ʸߴ�80%���������Cl-��V4+������������ã���Ϊ��ʯú�ᷰ�������Һ�еͼ۷�������һ��ѡ������������������H2O2����Ч�����ʺܵ͡�

ͼ1 ˫��ˮ������Cu �� V������Ӱ��
Fig.1 Effects of addition of peroxide solution on precipitation of Cu and V
2.3 Cu��V��Ħ���ȶ���Һ��Cu��VŨ�ȵ�Ӱ��
ʵ�鷢�֣�ͭ˿��������ˮ�в���������Cu2+��Cu��V�ij����������������½�2�ŷ�ˮ�Ӽ�Ԥ����ҺpHֵ��3.5����0.10 mL H2O2������һ������Cu2+���ټӼ��к���pHֵ8.0����20 min����ˣ��õ�Cu��V��Ħ���ȶ���Һ��ʵ��������ͼ2���Կ���������Cu��VĦ���ȵ�������ҺCu��V��Ũ�����͡���ͭ˿������ϴˮ��Cu��VĦ����Ϊ1.0(����1)��������Cu2+��ֱ�������кͳ�������Һ��V��Ũ�Ƚӽ�80 mg/L��Cu��Ũ��Ҳ��5 mg/L���ϣ�δ�ﵽ���ҹ涨���ŷű�����ˮ��Cu��V��Ũ�ȶ���С��ֱ���к������γɳ������ˡ����������������Ը���Cu��V�ij���Ч��������Cu��V���ۺϻ��ղ�������Ӱ�졣������Cu2+��ʹCu��V��Ħ��������7.5~8.5���������кͳ������ˣ���Һ��V��Cu��Ũ�ȶ�С��2.0 mg/L���ﵽ��ҵ��ˮ���ŷű����ɴ˿���������Cu2+������V����������ģ�����Ҳ������Cu�����ij�������Ϊ��ʣ��Cu2+�γɵ������������Һ�о������á�Ȼ������������Cu��V��Ħ���ȣ���Һ��Cu��VŨ�ȷ����������ߣ���ΪCu��ʣ��Խ�࣬�к������ĵļ��Խ�࣬��ӵù�����п�����ɾֲ��������ʹͭ�����������ﷴ�ܣ�����Cu��V��Ħ����Ӧ������7.5~8.5��
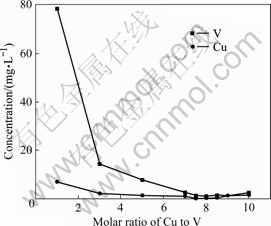
ͼ2 Cu��VĦ���ȶԳ�����Һ��Cu��VŨ�ȵ�Ӱ��
Fig.2 Effects of molar ratio of Cu to V on concentration of Cu and V in filtrate
2.4 ����ʱ���Cu��V����Ч����Ӱ��
�����½�1�ŷ�ˮ�Ӽ�Ԥ��pHֵ��4.0������0.25 mL H2O2������Cu2+������ҺCu��VĦ����Ϊ8.0���ټӼ��к���pHֵ8.0����������Ԥ��ʱ�����ˣ�����ʱ��Գ�����Һ��Cu��VŨ�ȵ�Ӱ�졣��ͼ3���Կ�����ͭ�������������γɵ��ٶȺܿ죬���кʹﵽ�յ��ٽ���20 min�Ժ�����Һ��Cu��V��Ũ�ȶ�����2.0 mg/L���ﵽ��ˮ�ŷŵ�Ҫ�����ӳ�����ʱ�䣬Cu��V��Ũ�ȱ仯������ˣ���H2O2������ķ�ˮ�ټӼ��к͵�pHֵ7.5~8.5����������20~30 min���ɹ��ˡ�
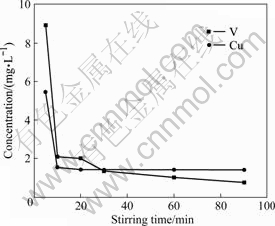
ͼ3 ����ʱ��Գ�����Һ��Cu��VŨ�ȵ�Ӱ��
Fig.3 Effects of stirring time on concentration of Cu and V in filtrate
2.5 �¶ȶ�Cu��VŨ�ȵ�Ӱ��
��1�ŷ�ˮ�Ӽ�Ԥ��pHֵ��4.0���ټ�0.25 mL H2O2��������Cu2+������ҺʹCu��VĦ����Ϊ8.0�� Ȼ���ټӼ��к���pHֵ8.0���ڲ�ͬ�¶��µõ���Cu��V���������ͼ4��ʾ��

ͼ4 �¶ȶԳ�����Һ��Cu��VŨ�ȵ�Ӱ��
Fig.4 Effects of temperature on concentration of Cu and V in filtrate
ͼ4��ʾ���¶ȶ���Һ��Cu�ij���Ӱ�첻����V��Ӱ��ܴ���Һ��40 �����£�������Һ��Cu��VŨ�ȶ�����2.0 mg/L���ﵽ�ŷű�����Һ�¶ȸ���40 �棬������Һ��V��Ũ�����¶�����Ѹ�������¶�����60 �棬��Һ��V��Ũ�Ƚӽ�60 mg/L��Զ������ˮ�ŷű���ʵ�鷢�֣������¶ȣ�����H2O2����Һ�в������������ࡣ������Ϊ��ˮ�е�Cu2+�Ƚ������Ӷ�H2O2�ķֽ��������[10]���¶�����H2O2�ķֽ��ٶȼӿ죬�Ӷ�����H2O2����Ч�����ʽ��ͣ���ˮ��V4+���������ף��Ӽ��кͺ�V4+������Cu2+����γ�ͭ�����������������ͭ˿��������ˮ�ľ���������ѡ���������½��С�
3 ����
1) ͭ˿��������ˮ����ͭ�������ﹲ����ר���������������ռ��������㣬�����ɱ��ͣ�������Һ��Cu��V��Ũ�ȼ���pHֵ����ֱ�Ӵﵽ��ҵ��ˮ�ŷű���
2) ͭ˿��������ˮ�������������������£�����Ӽ�Ԥ��pHֵ3.0~4.0��������������1.2~1.5��H2O2������������Һ��Cu��VĦ����7.5~8.5��Ȼ���ټӼ��к���pHֵΪ7.5~8.5��������20~30 min���ˡ�
3) ͭ˿��������ˮ����ͭ�������ﹲ���������������õ�������Cu��V�����ߣ����кܸߵ��ۺϻ������ü�ֵ��
REFERENCES
[1] ����, �ָ���, �� ��, �� ��, ���Ʒ�. 2005���й��ѹ�ҵ��չ����[J]. �ѹ�ҵ��չ, 2006, 23(2): 1-5.
WANG Xiang-dong, LU Fu-sheng, JIA Hong, HAO Bing, MA Yun-feng. Development report on titanium industry in 2005[J]. Titanium Industry Progress. 2006, 23(2): 1-5.
[2] �� ��, �� ��. �����⺣��������������״[J]. �ѹ�ҵ��չ, 2006(2): 7-14.
ZHANG Jian, WU Xian. Present status of manufacturing process for sponge titanium at home and abroad[J]. Development for Titanium Industry, 2006(2): 7-14.
[3] ������. �����Ѳ�ҵ�ķ�չս��[J]. �й���ɫ����ѧ��, 2006, 16(8): 50-53.
WENG Qi-Gan. Development strategy of sponge titanium industry[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(8): 50-53.
[4] �˹���. ȥ��TiCl4�з����ʸ��ַ����ıȽ�����[J]. ϡ�н���, 1993(3): 218-223.
DENG Guo-zhu. Appraised through comparison of diversified processes for the removal of vanadium from tetrachloride titanium[J]. Rare Metals, 1993(3): 218-223.
[5] XU Cong, YUAN Zhang-fu, WANG Xiao-qiang. Preparation of TiCl4 with the titanium slag containing magnesia and calcia in a combine fluidized bed[J]. Chinese J Chem Eng, 2006, 14(3): 281-288.
[6] Ī δ, �˹���, ����. ��ұ��[M]. ��2��. ����: ұ��ҵ������, 1998: 248-266.
MO Wei, DENG Guo-zhu, LUO Fang-cheng. Titanium metallurgy[M]. 2nd ed. Beijing: Metallurigical Industry Press, 1998: 248-266.
[7] ��ѧ��, ���˳�, �� ��, ����Ƽ. һ�ֺ�ͭ������ˮ�Ĵ�������. �й�ר��200710077748.1[P]. 2007-04-27.
WANG Xue-wen, GONG Shi-cheng, QIN Gang, ZHANG Li-ping. The treament of wastewater containing copper and vanadium. CN 200710077748.1[P]. 2007-04-27.
[8] DEAM J A. ���ϻ�ѧ�ֲ�[M]. ����: ��ѧ������, 2003.
DEAM J A. Langes hand book of chemistry[M]. Beijing: Science Press, 2003.
[9] ŷ����ף, ���̻�. ��м���-������������������ˮ[J]. ��������, 2002, 22(3): 165-168.
OUYANG Yu-zhu, WANG Ji-hui. Treatment of vanadium- containing wastewater by iron filling micoroelectrolysis- coprecipitation process[J]. Environmental Protection of Chemical Industry, 2002, 22(3): 165-168.
[10] ������, ��̸��. ���ⷰұ��[M]. ����: ұ��ҵ������, 1982: 120-159.
LIAO Shi-ming, BO Tan-lun. Foreign vanadium metallurgy[M]. Beijing: Metallurigical Industry Press, 1982: 120-159.
[11] ���ʶ�, �� �, ����ӱ. ��Ũ�Ⱥ�ͭ��ˮ�����������о�[J]. ��������, 2004(5): 280-281.
GUO Ren-dong, WU Hao, ZHANG Xiao-ying. The research on disposal of containing highly concentration copper[J]. Present Chemical, 2004(5): 280-281.
[12] ������. ʪ����ͭ�����е�Ӧ��[J]. ��ɫ����, 2002, 54(4): 81-85.
ZHANG Qi-xiu. The application in the field of copper hydrometallurgy[J]. Nonferrous Metals, 2002, 54(4): 81-85.
[13] ��𥻪, �� Ƽ, ����ȫ. �Ӻ�����ˮ�л���V2O5[J]. ��������, 1994(1): 36-38.
JIANG Fu-hua, ZHANG Ping, SHEN Zhao-quan. Recycled V2O5 from vanadium-containing wastewater[J]. Journal of Environment Protection, 1994(1): 36-38.
[14] Ԭ ��, ����Ԫ, ��С��, ������, �����, �� ��, �� ��, �� �, �� �. ʣ�������������ʯ������ϵȥ����ˮ�еĸ�����[J]. �й���ɫ����ѧ��, 2007, 17(5): 825-829.
YUAN Lin, CHAI Li-yuan, MIN Xiao-bo, WANG Yun-yan, SHU Yu-de, ZHOU Min, FANG Yan, WANG Pu, CHANG Hao. Removal of calcium ion from wastewater using waste activated sludge and artificial zeolites[J]. The Chinese Journal of Nonferrous Metals, 2007, 17(5): 825-829.
[15] ��־��. ʯ���кͷ������ؽ������ӵ����Է�ˮ[J]. ����ұ��, 2003, 23(6): 109-110.
LIU Zhi-gang. Lime neutralization processed acid wastewater containing heavy metal ions[J]. Jiangxi Metallurgy, 2003, 23(6): 109-11
������Ŀ�����Ҹ��¼����о���չ�ƻ�������Ŀ(2006AA03Z560)������ʡ�ܳ������ѧ����������Ŀ(06JJ1007)
�ո����ڣ�2007-10-10�������ڣ�2007-12-20
ͨѶ���ߣ���ѧ�ģ������ڣ��绰��0731-8830247��E-mail: wxwcsu@163.com
(�༭ ������)