DOI��10.19476/j.ysxb.1004.0609.2017.09.19
Mn������ҽ��Ti-Mo�Ͻ���֯����ѧ���ܵ�Ӱ��
�����壬����룬������
(������ҵ��ѧ ���Ͽ�ѧ�빤��ѧԺ������ 121001)
ժ Ҫ�����÷��Ժ���յ绡¯�Ʊ�Ti-8Mo-xMnϵ�кϽ��Կ���Mn�����Ӷ�����ҽ��Ti-Mo�Ͻ�����֯����ѧ���ܵ�Ӱ�졣�����������ԪTi-Mo�Ͻ���Ҫ��ϸС����״��������������ɣ�����1%Mn(��������)���ᾧ�Ħ������������Mn�ļ������ﵽ3%����ȫ�������������¡�������ѧ���Է��֣�����ȶ���Ti-8Mo-1Mn�Ͻ�����������з���Ӧ���յ��ĴӦ��ൽ�������������ת�䣬���ֳ���˫����������������Mn(1%��3%)��ߺϽ����ԣ��쳤����35%�����ߵ�53%��Mn�����ӵ�5%��7%�Ͻ�ǿ�ȵõ������ߣ�����ǿ�������856 MPa��ߵ�1201 MPa��ͬʱ�쳤��Ϊ22%�����к�Mn�Ͻ����Ӳ�ȶ��ϸߣ����Ϊ386HV������ԪTi-Mo�Ͻ��(251HV)1.65�����������Ti-8Mo-1Mn�Ͻ�ĵ���ģ����ߣ���150 GPa��������Mn�Ͻ�ĵ���ģ����76~87 GPa֮�䣬���˹����Ľӽ�����DZ����Ϊ����ҽ�ò��ϡ�
�ؼ���: Ti-Mo�Ͻ��̣�����֯����ѧ���ܣ��������
���±�ţ�1004-0609(2017)-09-1902-07�� ��ͼ����ţ�TG146.2��TG113.1��TG113.2�� ���ױ�־�룺A
����������ҽ�ý���������ȣ��Ѽ��ѺϽ����ھ��нϵ͵��ܶȡ��ߵı�ǿ�ȡ����õ���ʴ�Ժ����������Ե������ص㣬��˳�Ϊ������ơ������û����ؽ�����ҽ����������й㷺Ӧ�õĽ�������[1]��Ŀǰ, ���ٴ�ҽѧ��Ӧ�õ��Ѽ��ѺϽ���Ҫ�Ǵ�Ti(CP-Ti)��Ti-6Al-4V(TC4)�Ͻ𣬵����Ǿ��нϸߵĵ���ģ��(Լ110 GPa)��Զ�����˹�(3~20 GPa)�����ֲ�����壬�����Χ�Ĺ���������Ӧ�����Ρ�������ֲ������Χ���ֹ����գ���������ֲ��������ɶ�������ʹ������[2]�����⣬��TC4�Ͻ��������ļ����ķ����Ӻ������ӣ��ή��ϸ������Ӧ�ԣ�����ʹ�ô��ڰ�ȫ����[3]���о�����������ڹ����ѺϽ�ĸ������У��������������ṹ�Ħ��൯��ģ�����[2]����ˣ��о����ġ����и��͵���ģ���������������Ե���������ҽ�æ��ͻ����Ȧ����ѺϽ��ѳ�Ϊ���������о��ȵ�֮һ��
Ŀǰ���о��Ϳ�����ҽ�æ����ѺϽ���Ҫ��Ti-Nb[4]��Ti-Mo[5]��Ti-Ta[3]�ȶ�Ԫϵ, Ti-Mo-Nb[6]��Ti-Nb-Zr[7]��Ti-Nb-Ta[8] ����Ԫϵ��Ti-Nb-Ta-Zr[7]����Ԫϵ�Ͻ���Щ�Ͻ��ж�����Nb��Mo��Ta�Ȧ����ȶ�Ԫ�ء���Ȼ��ЩԪ�����ԣ������������ȶ���������ò�ǿ����˼����������ǵ��۵㶼�ܸߣ���Mo���۵�ߴ�2620 �棬���Ʊ�������������ѣ��γɵ���֯�ײ���ƫ����Ӱ����ѧ����ʴ���ܡ����⣬Nb��Mo��Ta��Ԫ�ض����ڹ��ص�ϡ��Ԫ�ء� ��ˣ������۵�ǿ�����ȶ�Ԫ��Fe��Mn����ȫ��һ���ִ���Nb��Mo��Ta��Ԫ���γɵĦ����ѺϽ���кܴ���о���������ֵ�����������о�������Ͻ���ҪΪTi-Fe[9]��Ti-Mn-Fe[1]��Ti-Sn-Cr [1]��Ti-Mo-Fe[10]��Ti-Mn[11]�ȡ�
Mn��ǿ�����ȶ�Ԫ�أ�����Ԧ�����нϴ�Ĺ���ǿ��ЧӦ[12]����Ϊ����������֯ȷ�ϵ�14������������Ԫ��֮һ����Mn��ά�������������³´�л������Ҫ���á������SANTOS��[11]��ҽ��Ti-Mn�Ͻ�Ľ��պ�ϸ�����������������w(Mn)��13%ʱ��Ti-Mn�Ͻ����������ϸ������ʣ���CP-Ti���൱��Ŀǰ��MnԪ�ؼ����ԪTi-Mo�Ͻ���о���δ���б��������������ڵ���Ti-8Mo�Ͻ�Ļ����ϣ��о�Mn��Ti-Mo�Ͻ�����֯����ѧ���ܵ�Ӱ�죬���ڿ������������Ħ���Ti-Mo-Mn��Ԫ����Mn��Ԫ����ҽ��Ti�Ͻ�
1 ʵ��
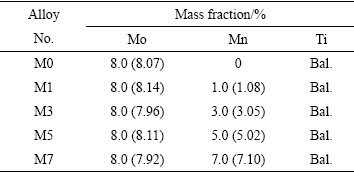
����Ƶ�ĸ�Ͻ�ΪTi-8Mo-xMn(���ΪTMM)(x=0��1��3��5��7(����������%)���ֱ���ΪM0��M1��M3��M5��M7)������Ti��Mo��Mn���������ڸߴ����������Ti�����������÷��Ժ���յ绡¯�������Ͻ�ijɷּ���1(����������������ɷ�)��Ϊʹ�Ͻɷ־��ȣ���������5�����ϡ�
��1 ����Ͻ������ɷֺ�ʵ�ʳɷ�
Table 1 Nominal and real chemical compositions of TMM alloys
Ϊ��æ��࣬�����Ͻ�ɷֵ�ĸ�Ͻ��й��ܴ��������Ƚ�ĸ�Ͻ��ȵ���������Ȼ����900 �����30 min�����ˮ�㣬�õ����ܴ�����ĺϽ�����ĥ�����и��õ�XRD�����༰������������������ĥ�������ͽ�ʴ�������ý��������۲�����֯�����õĸ�ʴ��Ϊ����ᡢ���ἰˮ�Ļ����Һ�������ΪV(HF):V(HNO3):V(H2O)=4:8:88���Ͻ����ṹ����D/max-2500X����������(Cu K������)���з�������CMT 5105 ������������������������ܲ��ԣ��õ��Ͻ�Ŀ���ǿ�Ȧ�b������ǿ�Ȧ�s���쳤�ʦġ�����ģ��E ����ѧ���ܡ����������ߴ���ͼ1 ��ʾ�������¶�Ϊ���£�ÿ�ֺϽ�������ظ�����4�Ρ�
2 ���������
2.1 �Ͻ����ṹ������֯
ͼ2��ʾΪ���ܴ�����ͬ��Mn����TMM�Ͻ��XRD�ס���ͼ2���Կ�����Ti-8Mo��Ԫ�Ͻ���Ҫ��HCP�������������ɣ�ͬʱ���м�������BCC ���ࡣ����ZHANG��[6]�����Ľ�������ơ�����ͬ���ǣ�Ti-8Mo�Ͻ�ȫ���ɦ�������ɣ�����������ڲ�ͬ�Ĺ����¶Ⱥ���ȴ�ٶ����¡�������Ϊб�����������壬ͨ���������������������ԪTi�Ͻ���Ti-Nb[4]��Ti-Fe[13]�ȵ�����Ԫ�غ�����Խϵ�ʱҲ���������ࡣ
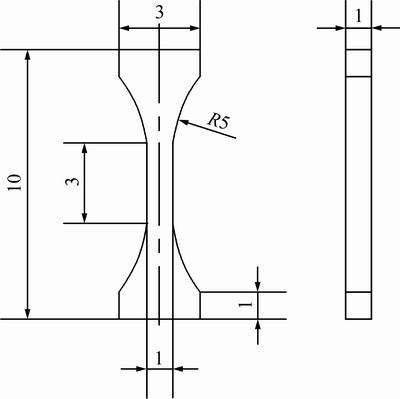
ͼ1 ��������ʾ��ͼ
Fig. 1 Schematic diagram of tensile specimen (Unit: mm)
Mn�ļ����Ti-8Mo�Ͻ����ṹ��Ӱ���������ġ�1%��Mn��ʹ�ô����Ħ��ౣ�������¡�����3%��Mn��ʹ�����Ͻ��Ϊ�����������Ħ��ࡣ��������Mn����5%��7%����Ϊ���ֻ࣬�Ǧ�������������ƫ�ƣ�����Mn������Ti����Ľ����Mnһֱ����Ϊ��ǿ�����ȶ�Ԫ�ء������һϵ�е�Ti-Mn�Ͻ���о��У�SANTOS��[11]���֣�����Ti-Mn�Ͻ𣬵�Mn������9.0%�����ȫ�����������¡�
ֵ��ע����ǣ���M1�Ͻ��г����˼������ľ�����������ṹ�Ħ������࣬����ͼ2�����ϽǵķŴ�ͼ�п��ø����������������Ti-Mo-Fe��Ԫ�Ͻ���Ҳ���ֹ�[10]����������Ӧ���������������֮���ڹ����ϵ���¡���ת��Ϊ����ɢ����䣬�������ȴ�ٶ�Ҳ�������������[12]����Ȼ�������������٣�����Ti�Ͻ����ѧ���������ǵ���ģ��Ӱ��ܴ����ں�����Ե���ѧ�����п�����ؿ�����
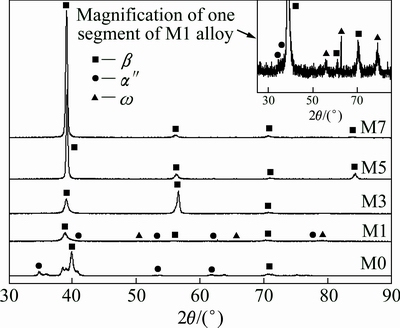
ͼ2 ��ͬ��Mn����TMM�Ͻ�XRD��
Fig. 2 XRD patterns of TMM alloys with different Mn contents
ͼ3��ʾΪTMM�Ͻ�Ĺ�ѧ����֯����ͼ3�ɼ���M0��Ԫ�Ͻ����֯��ҪΪϸС����״������(XRD����Ϊ������)(��ͼ3(a))������1%��Mnʹ�����Ͻ�ת��Ϊ���ᾧ�Ħ��࣬���������ɼ������⣬����������״�Ħ������ؾ�������(��ͼ3(b))����������Mn����������ʧ�����Ͻ�ȫ���ɵ��ᾧ�Ħ������(��ͼ3(c)��(d))(M7������֯ͼ��)��
ͼ4��ʾΪTMM�Ͻ��Ц���ľ���������ͼ4�ɼ�������Mn�������ӣ�����ľ�������֮��С����������Mn��ԭ�Ӱ뾶(0.131 nm)��Ti��(0.147 nm)С�ö࣬��Mnԭ��ȡ��Tiԭ���γ��û������壬����侧�����ļ�С��
2.2 �Ͻ����ѧ����
ͼ5��6��ʾ�ֱ�ΪTMM�Ͻ������µ�����Ӧ��-Ӧ�����ߺ��ɴ˵õ��ĺ�Mn��������ǿ�Ȧ�s������ǿ�Ȧ�b���쳤�ʦĵĹ�ϵ���ߡ���ͼ5�ɼ������кϽ���������߶���������-����-�ܱ�-���ѵĹ��̣�����ͬ���ǣ�M1�Ͻ�����ˡ�˫������(Double yielding)������841 MPa����������Ȼ����964 MPa�����ڶ�����������ͼ6�ɼ�������1%��Mn���Ͻ�Ħ�s����b����ֵ��������ߡ�Mn�����ӵ�3%����s����b�����½�����ֵ�������ӣ��ﵽ53%��֮������Mn���Ľ�һ�����ӣ�ǿ��ֵ������ӡ���Mn���ﵽ7%��s�ͦ�bֵ�ﵽ��ֱ�Ϊ1182 ��1201 MPa�����Ͻ�Ħ�ֵ�����½�����Mn��3%��53%�½���Mn��7%��22%��
������ѧ���ܽ����Ͻ���������ࡢ��������С������ء��ݱ�������Ti�Ͻ��������֦��࣬������(Athermal)����͵���(Isothermal)����[14]��ǰ��ͨ���Ӹ��¦�������ȴ�����µĴ��������γɣ�Ϊ����ɢת�䣬�����������ڹ��ܺ�ͨ������ʱЧ������������Ϊ��ɢת�䡣����֤�ݳ�ֱ�����Ti�Ͻ�Ĵ�������Ȧ������������С�������[15]��������������ࡢ������Դ�ʱ���ᵼ��Ti�Ͻ�����Լ��罵�ͣ���Ti-7.5Mo-1Fe�Ͻ�[10]���������������������Ϊ����ϸС�Ŀ���ʱ���������ͺϽ�����ԣ�������Ƶ�Ti-10Mo�Ͻ�[15]���ۺ�����XRD��(��ͼ2)��������֯(��ͼ3)��Ӧ��-Ӧ������(��ͼ5��6)�����������Ϊ��M1�Ͻ��еĦ������������Ҿ����ߴ��С��������ԺϽ������������ˡ��෴���úϽ���δ����Mn����ԪM0�Ͻ���ȣ�ǿ�Ⱥ����Զ��õ���ߡ�M1�Ͻ����õ��������ڳ����м������Ħ����⣬��Ҫ�ɦ�����ɡ�����Ϊ���������ṹ������ԪM0�Ͻ��е�б�����������������Ա���������ǿ[16]��M3ǿ�ȵ��½���������ʧ�йء�M5��M7�ĸ�ǿ������MnԪ�صĹ���ǿ��ЧӦ����ġ�

ͼ3 ��ͬ��Mn��TMM�Ͻ�Ĺ�ѧ����֯
Fig. 3 Optical micrographs of TMM alloys with different Mn contents
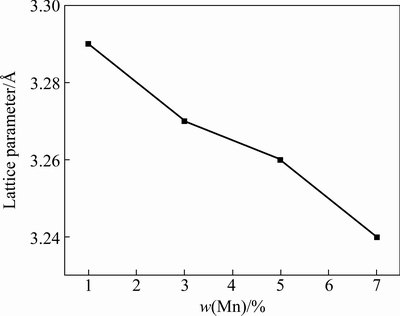
ͼ4 ����ľ������뺬Mn���Ĺ�ϵ
Fig. 4 Relationship between lattice parameters of �� phase and Mn content
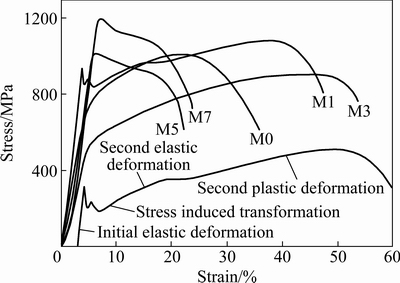
ͼ5 TMM�Ͻ��Ӧ��-Ӧ������
Fig. 5 Stress-strain curves of TMM alloys
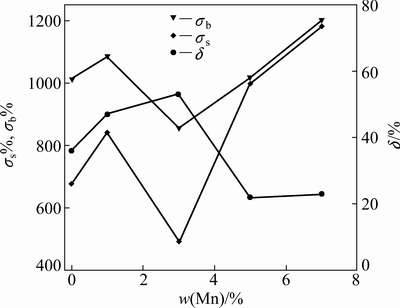
ͼ6 ���������뺬Mn���Ĺ�ϵ����
Fig. 6 Relationship between tensile properties and Mn content
M1�Ͻ�����Ķ��������������䲻ͬ�ı��λ����йء�������Ti�Ͻ�ı��λ�����ҪΪλ�����ơ�Ӧ���յ���������ת��(SIMT)�����ǵ����[16-18]��ȡ���ڦ�����ȶ��ԡ��������������ȶ�Ԫ���١�Ms��ӽ����£�����ȶ�ʱ���Ͻ��ܵ�Ӧ�����ã��ͻ��в��֦���ת��Ϊ�����ࡣ�������Ȱ�Ӧ���յ���������ת����У�Ȼ��λ�����ơ��������������ȶ�Ԫ�ضࡢMs�㴦�ڸ��£������ȶ���SIMT�����������ΰ�λ�����ƽ��С�Ti�Ͻ�����ƻ��������Ӧ������ʱ���ξͿ�����SIMT��ʽ���С�TAVARES��[19]��Ti-35Nb-0.35Si�Ͻ������ĶϿڸ�����X���䣬�۲쵽������ǰ��û�еĦ�������壬֤�������ȵĦ�������������о���������Ӧ�������µĦ���������ת�䡣���ڱ��о���M1�Ͻ��������������ȶ�Ԫ��(Mn)�����ͣ�����ȶ�������ʱ������ͨ��SIMT���η�ʽ������һ��������֮��������١����ݵļӹ�Ӳ�����������˦��� ���γɵ��Ѷȣ��̶���λ�����Ʒ�ʽ�����ڶ���������Ȼ�������ַ�ʽ���Ա��Σ�ֱ�����ѡ������ĺ�Mn�Ͻ�����Mn�����ߣ������ȶ������Ա���ֻ����λ�����Ʒ�ʽ���С�
ͼ7��ʾΪTMM�Ͻ����Ӳ�ȡ�����ģ����Mn�����Ĺ�ϵ����ͼ7�ɿ�������Ӳ�Ⱥ͵���ģ��������ͬ�ı仯���ơ�Ti-8Mo��Ԫ�Ͻ��Ӳ��ֵ��ͣ���Ϊ251HV������1%��Mn��Ӳ��ֵ������386HV�����65%����Mn���������ӵ�3%��Ӳ��ֵ��С��348HV��֮������Mn�����ӣ�Ӳ��ֵ�������ӣ�M1�ĵ���ģ����ߣ�Ϊ150 GPa��M3����ͣ�Ϊ76 GPa��M5��M7����M0���൱����ֵ��80~90 GPa֮�䡣

ͼ7 TMM�Ͻ����Ӳ�ȡ�����ģ����Mn�����Ĺ�ϵ
Fig. 7 Relationships among microhardness, elastic modulus and Mn content of TMM alloy
ע���Ti-8Mo-1Mn�Ͻ��Ӳ��ֵ�������Ҳ��ߡ���Ҳ��úϽ��к��еĦ����йء�����Ӳ������ࡣ�о���������Ti�Ͻ������е���(�������䡢���塢�¼�����)�У������Ӳ�����[5]����ʹ�ú������M1�Ͻ��Ӳ��ֵ�ﵽ�������MnԪ�ص�ǿ���ȶ���������ã���Mn������Ϊ3%ʱ��������ʧ��Ӳ��ֵ�½���֮��Ӳ��ֵ�������������MnԪ�ض�Ti����Ĺ���ǿ�����á�
������֪������ģ���Dz��ϵı������ܣ�ȡ����ԭ�Ӽ�Ľ����[17]�����ֽ��������ϵľ���ṹ��ԭ�Ӽ���йء������о���������Ti�Ͻ�ĸ������У�����ģ����˳���ɴ�С����Ϊ�ء����䡢���塢�£��������ߣ��µ����[18, 20-22]��ֻ��M1�Ͻ��к��Ц��࣬�ʸúϽ�ߵĵ���ģ����Ҫ�Ǵ���������Ħ�����ɵġ���Σ����������������Mn��MoԪ���ڦ����еĸ�����ʹ����Ms���½�������ģ������ [23]���ٴΣ�M1�ߵ�Eֵ����Mn������Ti�е�ЧӦ�йء���ͼ4��֪��Mnԭ�Ӽ��뵽Ti�����м�С�˾������͵�λ�����������λ�������ԽС��ԭ�Ӽ�Ľ������Խǿ��Eֵ��Խ��[24]������Mn�����ӵ�3%ʱ��������ʧ��ͬʱMn��MoԪ���ڦ����еĸ�������Ҳ��ʧ����ȻMn�����ӣ�Mn�Ĺ���ЧӦ���ӣ����Ȧ���Ե���ģ����Ӱ��ҪС�ö࣬�ʽ�ʣ�����M3�Ͻ�ĵ���ģ��������͡�֮������Mn�������ӣ�Mn�Ĺ���ЧӦ���ӣ�ԭ�Ӽ���������M5��M7�Ͻ��Eֵ��Ϊ�����ɴ˿��Կ�������Ti�Ͻ��У�����ṹ�Ե���ģ����Ӱ���ԭ�Ӽ��Ĵ�ö࣬�����Ǧ����Ӱ������༱�����ӵ���ģ��ֵ����ˣ�Ҫ��õ͵���ģ��������ҽ��Ti�Ͻ������Ʀ�����γɡ�
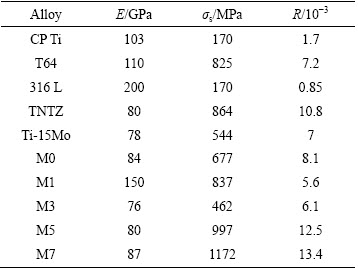
��ǰ����������������Ͼ��еĵ͵ĵ���ģ������Ϊ�����Ϻ��ع��ṩ����������������������Ӧ��ֵ��������ǿ���뵯��ģ���ı�ֵ(R)�Ǻ������������Ƿ������ڹǿƼ�������Ƶ�����ҽ�������һ��ʮ�����õIJ���[24]��RֵԽ�ߣ�����Խ����������ҽ������TMM�ͳ��õĽ�������ҽ�ò��ϵĦ�s��E��Rֵ���2��ʾ���ɱ�2�ɿ������봫ͳ������ҽ�ý�������CP-Ti[25]��316 L[25](�����)��ȣ����е�TMM�Ͻ�Ħ�s��Rֵ���ߣ���M1�Ͻ��⣬Eֵ���͡���T64(Ti-6Al-4V)[25]��Ti-15Mo�Ͻ�[6]��ȣ���Щ�Ͻ�ͬ��Eֵ�ͣ�����M5��M7�Ͻ��Rֵ���ߡ������ֺϽ��Rֵ������Ŀǰ����ҽ�æ��ͻ����Ȧ����ѺϽ��о����������������Ժ���ѧ���ܵ�TNTZ (Ti-29Nb-13Ta-5Zr)�Ͻ�[7]��ֵ���ߣ�ǰ�߷ֱ�Ϊ12.5��10-3��13.4��10-3������Ϊ10.8��10-3����ˣ�����ѧ�����ԽǶȣ�TMM�Ͻ�ȴ�ͳ������ҽ�ý������ϸ��ʺ����ڹǿƼ�������Ƶ�����ҽ������
��2 TMM�Ͻ��E����s��Rֵ
Table 2 Values of E, ��s and R of TMM alloys
3 ����
1) ��ԪTi-Mo�Ͻ���Ҫ��ϸС����״��������������ɡ�����ǿ�����ȶ�Ԫ��Mn�������˴���Ц������������1%Mnʹ�õ��ᾧ�Ħ�����ֱ����������������������������������������ࡣ��Mn�ļ������ﵽ3%����ȫ�������������¡�
2) ����ȶ���M1�Ͻ�����������з���Ӧ���յ��ĴӦ��ൽ�������������ת�䣬���ֳ���˫����������Mn����ߺ���ʧ��ת��Ϊ��һ������
3) ��������Mn(1%��3%)��ߺϽ����ԣ��쳤����35%�����ߵ�53%��Mn����ߵ�5%��7%�Ͻ�ǿ�ȵõ���ߣ�����ǿ����854 MPa��ߵ�1201 MPa��ͬʱ����22%���쳤�ʡ����к�Mn�Ͻ����Ӳ�Ⱥܸߣ����Ϊ386HV������ԪTi-Mo�Ͻ��1.65�����������M1�Ͻ�ĵ���ģ����ߣ���150 GPa��������Mn�Ͻ�ĵ���ģ��ֵ��76~87 GPa֮�䣬���˹����Ľӽ���
4) Mn����Ϊ5%��7%�Ͻ��RSMֵ(����ǿ���뵯��ģ���ı�ֵ)���ֹ㷺ʹ�õ�ҽ�úϽ���CP-Ti��Ti-6Al-4V�ߵö࣬��������������������ѧ�����Ե�Ҫ�����⣬Ti-Mo-Mnϵ�кϽ����۵�͡������������ײ���ƫ�����ɱ��͵��ŵ㡣
REFERENCES
[1] NIINOMI M, NAKAI M, HIEDA J. Development of new metallic alloys for biomedical applications[J]. Acta Biomaterialia, 2012, 8(11): 3888-3903.
[2] ����ѩ,�� ��,������,��Ǯ��,������,�� ��. ��Nb����Ti-Mo-Nb-Zr-Sn BCC�͵���ģ��������Ͻ�ijɷ����[J]. �й���ɫ����ѧ��, 2012, 22(12): 3378-3385.
LIU En-xue, WANG Qing, MA Ren-tao, CHA Qian-feng, JI Chun-jun, DONG Chuang. Composition design of BCC Ti-Mo-Nb-Zr-Sn solid solution alloy with low content Nb and modulus of elasticity[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(12): 3378-3385.
[3] ZHOU Y L, NIINOMI M, AKAHORI T. Effects of Ta content on Young's modulus and tensile properties of binary Ti-Ta alloys for biomedical applications[J]. Materials Science and Engineering A, 2004, 371(1/2): 283-290.
[4] GUO S, ZHANG J S, CHENG X N. A metastable ��-type Ti-Nb binary alloy with low modulus and high strength[J]. Journal of Alloys and Compounds, 2015, 644(25): 411-415.
[5] HO W F, JU C P, CHERN LIN J H. Structure and properties of cast binary Ti-Mo alloys[J]. Biomaterials, 1999, 20(7): 2115-2122.
[6] ZHANG L B, WANG K Z, XU L J, XIAO S L, CHEN Y Y. Effect of Nb addition on microstructure, mechanical properties and castability of ��-type Ti-Mo alloys[J]. Transactions of Nonferrous Metals Society of China, 2015,25(7): 2214-2220.
[7] ZHOU Y, LI Y X, YANG X J. Influence of Zr content on phase transformation, microstructure and mechanical properties of Ti75-xNb25Zrx (x=0-6) alloys[J]. Journal of Alloys and Compounds, 2009, 486(1/2): 628-632.
[8] ������,�� ��,�� �,�� ��,������. Ti-25Nb-25Ta�Ͻ���д��γ���ṹ�����ĵ������о�[J]. ������ѧ��,2014,33(5): 399-405.
WANG Guo-hui, SUN Wei, ZHAO Jie, CHEN Bin, HU Chang-qing. Electron microscopic study on the formation of shear bands and structural characteristics of Ti-25Nb-25Ta alloy[J]. Journal of Electron Microscopy, 2014, 33(5): 399-405.
[9] ������,· ��,�� ΰ,֧����, �� ��, ��ѡ��. ��ĩұ��Ti-Fe�Ͻ������֯����ѧ����[J].�����ȴ���ѧ��, 2016, 37(8): 36-40.
MENG Qing-yu, LU Xin, XU Wei, ZHI Ling-ling, CHEN Jun, QU Xuan-hui. Microstructure and mechanical properties of powder metallurgy Ti-Fe alloy[J]. Journal of Heat Treatment of Materials, 2016, 37(8): 36-40.
[10] LIN D J, LI CHERNN J H, JU C P. Structure and properties of Ti-7.5Mo-xFe alloys[J]. Biomaterials, 2002, 23(8): 1723-1730.
[11] SANTOS P F, NIINOMI M, CHO K. Microstructures, mechanical properties and cytotoxicity of low cost beta Ti-Mn alloys for biomedical applications[J]. Acta Biomaterialia, 2015, 26(15): 366-376.
[12] �� ��, ��Ⱥ��, Ī η. �ѵĽ���ѧ���ȴ���[M]. ������ұ��ҵ������, 2014: 16-74.
ZHANG Zhu, WANG Qun-jiao, MO Wei. Metallography and heat treatment of titanium[M]. Beijing: Metallurgical Industry Press, 2014: 16-74.
[13] HAGHIGHI S E��LU H B��JIAN G Y��CAO G H��HABIBI D. Effect of ���� martensite on the microstructure and mechanical properties of beta-type Ti-Fe-Ta alloys[J]. Materials and Design, 2015, 76(5): 47-54.
[14] CARDOSO F F, FERRANDINI P L, LOPES E S N. Ti�CMo alloys employed as biomaterials: Effects of composition and aging heat treatment on microstructure and mechanical behavior[J]. Journal of Mechanical Behavior of Biomedical Materials, 2014, 32(4): 31-38.
[15] ZHOU Y L, LUO D M. Microstructures and mechanical properties of Ti-Mo alloys cold-rolled and heat treated[J]. Materials Characterization, 2011, 62(10): 931-937.
[16] WILLIAMS J C, FONTAINE D, PATON N E. The �� phase as an unusual shear transformation[J]. Metallurgical Materials Transactions B, 1973, 4(10): 2701-2708.
[17] ZHANG D C, YANG S, WEI M, MAO Y F, TAN C G, LIN J G. Effect of Sn addition on the microstructure and superelasticity in Ti-Nb-Mo-Sn alloys[J]. Journal of Mechanical Behavior of Biomedical Materials, 2012, 13(13): 156-165.
[18] DING D, ZHANG D C, LUO Z C, TAN C G, ZHANG Y, LIN J G. Effects of Si addition on mechanical properties and superelasticity of Ti-7.5Nb-4Mo-2Sn shape memory alloy[J]. Materials and Design, 2014, 61(9): 146-149.
[19] TAVARES A M G, RAMOS W S, BLAS J C G. Influence of Si addition on the microstructure and mechanical properties of Ti�C35Nb alloy for applications in orthopedic implants[J]. Journal of Mechanical Behavior of Biomedical Materials, 2015, 51(11): 74-87.
[20] SOUZA S A, MANICARDI R B, FERRANDINI P L. Effect of the addition of Ta on microstructure and properties of Ti-Nb alloys[J]. Journal of Alloys and Compounds, 2010, 504(2): 330-340.
[21] ZHOU Y L, NIINOMI M, AKAHORI T. Decomposition of martensite ���� during aging treatments and resulting mechanical properties of Ti-Ta alloys[J]. Materials Science and Engineering A, 2004, 384(1/2): 92-101.
[22] FAN Z. On the Young��s moduli of Ti-6Al-4V alloys[J]. Scripta Metallurgica et Materialia, 1993, 29(11): 1427-1432.
[23] KIM H Y, HASHIMOTO S, KIM J I. Effect of Ta addition on shape memory behavior of Ti-22Nb alloy[J]. Materials Science and Engineering A, 2006, 417(1/2): 120-128.
[24] SONG Y, XU D S, YANG R, LI D, WU W T, GUO Z X. Theoretical study of the effects of alloying elements on the strength and modulus of-type bio-titanium alloys[J]. Materials Science and Engineering A, 1999, 260(1/2): 269-276.
[25] NIINOMI M. Mechanical properties of biomedical titanium alloys[J]. Materials Science and Engineering A, 1998, 243(1/2): 231-236.
Effect of manganese addition on microstructure and mechanical properties of Ti-Mo Biomedical alloys
WU Xiao-feng, YANG Hui-qi, WANG Chun-yu
(School of Materials Science and Engineering, Liaoning University of Technology, Jinzhou 121001, China)
Abstract: A series of Ti-8Mo-xMn alloys were fabricated by nonconsumable electrode vacuum arc furnace, the effect of Mn addition on the structure and mechanical properties of the alloy was investigated. The results indicate that ���� phase-dominated binary Ti-Mo alloy exhibits a fine, acicular martensitic structure. When 1% Mn (mass fraction) is added, most of equiaxed �� phase structure is retained. With Mn content increasing to 3% (mass fraction), entire �� phase is retained. Mn alloy with instability �� phase exhibits the two-stage yielding from stress-strain curves due to the stress-induced martensite transformation from �� to ���� during tensile deformation. Addition of a small amount of Mn (1% and 3 %) improves the plasticity of alloys, and the elongation increases from 35% to 53%. With Mn content increasing to 5% and 7% (mass fraction), the strength dramatically improves and tensile strength increases from 854 MPa to 1201 MPa, companied with 22% elongation. All the alloys with Mn exhibits the high microhardness, the highest is 386HV��which is 1.65 times than that of binary Ti-Mo alloy. The elastic modulus of Ti-8Mo-1Mn alloy with �� phase is the highest of all alloys 150 GPa. The elastic modulus of the other alloys with Mn are about 76~87 GPa, close to those of human skeletons. These alloys seem to have a great potential for use as an implant material.
Key words: Ti-Mo alloy; manganese; microstructure; mechanical property; biomaterial
Foundation item: Project (51104016) supported by Natural Science Foundation of China; Project (SKL-SPM-201204) supported by State Key Laboratory of New Technology for Comprehensive Utilization of Rare and Precious Metals, China
Received date: 2016-07-21; Accepted date: 2016-12-26
Corresponding author: WU Xiao-feng; Tel: +86-416-4199650; E-mail��hgd901@126.com
(�༭ ����)
������Ŀ��������Ȼ��ѧ����������Ŀ(51104016)��ϡ������ۺ������¼��������ص�ʵ���ҿ��ſ�������(SKL-SPM-201204)
�ո����ڣ�2016-07-21�������ڣ�2016-12-26
ͨ�����ߣ������壬���ڣ���ʿ���绰��0416-4199650��E-mail��hgd901@126.com