DOI:10.19476/j.ysxb.1004.0609.2019.12.17
高钙钢渣脱砷行为及机理
李 勇1, 2,祝 星1, 2,祁先进1, 2,魏永刚1, 2,李孔斋1, 2,胡建杭1, 2,王 华1, 2
(1. 昆明理工大学 省部共建复杂有色金属资源清洁利用国家重点实验室,昆明 650093;
2. 昆明理工大学 冶金与能源工程学院,昆明 650093)
摘 要:在分析高钙钢渣组成结构和浸出特性的基础上,开展高钙钢渣在溶液中除砷行为和机理。研究结果表明:高钙钢渣的主要成分为铁酸钙、硅酸二钙、硅酸三钙,其浸出液pH值为12.15,具有很强的碱性;随着钢渣粒径的变小或钢渣用量的增加,溶液中砷的去除率逐渐上升。钢渣粒径在48~75 μm时,对溶液中的As(Ⅲ)和As(Ⅴ)的去除量分别达到0.90 mg/g和0.93 mg/g;pH对钢渣的除砷率影响较小,经过反应后,对砷的固定率达到99%;高钙钢渣去除溶液中的砷离子受化学反应速率控制。当高钙钢渣与含砷溶液接触时,可对砷离子同时进行吸附和化学沉淀反应,形成较为稳定的钙和铁的砷酸盐和亚砷酸盐,实现溶液中砷离子的稳定化。含砷产物中砷的浸出毒性低于《危险废物鉴别标准GB 5085.3―2007》中规定的5 mg/L,产物属于一般固体废弃物。高钙钢渣适用于含砷酸性废水的无害化处置。
关键词:高钙钢渣;除砷;吸附
文章编号:1004-0609(2019)-12-2836-14 中图分类号:X758 文献标志码:A
砷(As)可通过岩石的风化和火山活动自然地释放到环境中[1],然而,其最主要的来源是矿物开采与冶炼、杀虫剂使用、化石燃料燃烧,特别是有色重金属冶炼排放出的大量含砷危废,已经造成了严重的水土污染和生态破坏[2-4]。砷对生态环境的破坏主要源于其在水溶液环境中的强迁移性。砷在水溶液中主要呈现出两种氧化态,即自然界发现的砷酸盐(As(Ⅴ))和亚砷酸盐(As(Ⅲ))的形态[5]。As(Ⅴ)的组成物在有氧环境中较常见,而As(Ⅲ)在无氧环境或冶炼废水中较常见,As(Ⅲ)比As(Ⅴ)具有更强的毒性[6]。在自然界的水体中As(Ⅴ)主要以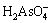 和
和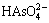 的形式存在,As(Ⅲ)主要以H3AsO3和
的形式存在,As(Ⅲ)主要以H3AsO3和 的形式存在,这取决于水溶液的pH值[1, 7]。鉴于水体中砷对于生态环境的巨大危害性,我国工业用水标准中砷含量需降低至0.5 mg/L,而饮用水含砷量需低于0.05 mg/L,欧盟和美国饮用水水质标准中规定砷含量为0.01 mg/L[1]。因此,水体除砷对于生态环境和饮用水安全具有十分重要的意义[8]。目前,中和沉淀法[9-10]、吸附法[11-12]、离子交换法[13-14]和膜分离法[15]等技术已应用于水体除砷,中和沉淀法是脱除高砷废水中砷的主要方法之一,而吸附法是常用的深度脱砷手段。中和沉淀法对As(Ⅲ)和As(Ⅴ)去除效果都较好,主要使用钙基沉淀剂或者碱性沉淀剂[16],但沉淀剂使用量大,可能导致二次危废排放,需辅以絮凝沉淀以达到深度净化。吸附法具有高效率、操作简单、再生潜力大等优点[17-19],适用于低浓度含砷水体处理,铁和铝的氧化物及其氢氧化物是水体除砷最常用的吸附剂[20-22],吸附剂成本和再生性能仍是该技术的关键。针对现有的除砷技术,迫切需要开发一种高效、低成本除砷技术[23-25]。
的形式存在,这取决于水溶液的pH值[1, 7]。鉴于水体中砷对于生态环境的巨大危害性,我国工业用水标准中砷含量需降低至0.5 mg/L,而饮用水含砷量需低于0.05 mg/L,欧盟和美国饮用水水质标准中规定砷含量为0.01 mg/L[1]。因此,水体除砷对于生态环境和饮用水安全具有十分重要的意义[8]。目前,中和沉淀法[9-10]、吸附法[11-12]、离子交换法[13-14]和膜分离法[15]等技术已应用于水体除砷,中和沉淀法是脱除高砷废水中砷的主要方法之一,而吸附法是常用的深度脱砷手段。中和沉淀法对As(Ⅲ)和As(Ⅴ)去除效果都较好,主要使用钙基沉淀剂或者碱性沉淀剂[16],但沉淀剂使用量大,可能导致二次危废排放,需辅以絮凝沉淀以达到深度净化。吸附法具有高效率、操作简单、再生潜力大等优点[17-19],适用于低浓度含砷水体处理,铁和铝的氧化物及其氢氧化物是水体除砷最常用的吸附剂[20-22],吸附剂成本和再生性能仍是该技术的关键。针对现有的除砷技术,迫切需要开发一种高效、低成本除砷技术[23-25]。
基于矿物吸附剂、农业或工业副产品吸附剂其低成本替代品已经在废水修复方面进行了研究[1, 26],钢渣年产量巨大,是工业副产品之一。钢渣主要由钙的氧化物和铁的氧化物组成,铁的氧化物可为As、Cr、P等阴离子提供吸附位点,钙的氧化物可以溶解于水体中,从而增加溶液的pH,促进重金属离子形成沉淀去除[27-28]。钢渣用于水体除砷的技术兼具中和沉淀和吸附优势,具备将砷吸附并进一步稳定化的技术特点。同时,钢渣也可作为重金属的吸附剂和沉淀剂[29-30]。现有利用钢渣去除水体中砷的研究仅关注砷的去除效率,而忽略了钢渣和水体中砷离子之间作用机理的研究[31-32]。此外,不同冶炼工艺或钢渣处理方法得到的钢渣组成和特性也不尽相同,需要进一步开展深入的研究。因此,开展高钙钢渣除砷技术的研究,有望用于有色重金属冶炼中含砷废水的处置或深度净化。本文研究了钢渣粒径、钢渣用量、pH值、时间对钢渣脱砷行为的影响规律,利用扫描电子显微镜-能量色散光谱仪(SEM-EDS)、X射线光电子能谱仪(XPS)对吸附砷后的钢渣其微观形貌特征和矿物学特征进行分析,揭示了钢渣除砷机理。借助浸出毒性(TCLP)实验,揭示了钢渣中砷的稳定性和迁移性。
1 实验
1.1 实验材料
实验中采用的高钙钢渣取自昆明钢铁有限公司,是炼钢过程产生的热态钢渣经过热焖和破碎磁选除铁之后得到的。钢渣经过再次破碎、研磨和筛分得到不同粒径的钢渣样品,密封存储、备用。
除砷实验中的亚砷酸钠(NaAsO2)、砷酸钠七水合物(NaH2AsO4・7H2O)、盐酸(HCl)、氢氧化钠(NaOH)等主要化学试剂,为分析纯(天津市申泰化学试剂公司)。在标准大气压下,用去离子水作为溶剂配置100 mg/L的亚砷酸钠溶液和砷酸钠溶液,配置2 mol/L的HCl和2 mol/L NaOH作为pH调整液。
1.2 材料表征
实验所用Autosorb-iQ-C全自动物理/化学吸附分析仪为美国Quantachrome仪器公司生产的ASIQC0004-3型,用来分析钢渣的比表面积。检测条件:测试孔隙度范围3.5~5000  ;比表面积>0.0005 m2/g,极限高真空1.33×10-8 Pa,-196 ℃,N2作为吸附等温线;X射线衍射仪为日本理学株式会社生产的Miniflex600型衍射仪,用来分析钢渣的物相成分,检测条件为:输出功率600 W,管电压40 kV,管电流15 mA,连续扫描Cu Kα射线,2θ扫描范围10°~80°;高分辨率电感耦合等离子体发射光谱仪(ICP)为德国生产的PQ 9000型,用来分析水体中As元素的含量,检测条件:波长范围160~900 nm,像素分辨率2 pm,光学分辨率3 pm,检测器分辨率2 pm,高光谱分辨率0.003nm,功率700~1700W;X射线光电子能谱仪(XPS)为美国赛默飞世尔科技公司生产的K-Alpha+型,用来分析反应前后钢渣表面的元素组成、结构和电子特征,检测条件为:分析室工作时的真空度为2×10-5 Pa,X光源为Al Kα源(Mono Al Kα),能量为1486.6 eV,6 mA×12 kV,束斑大小:400 μm;扫描模式为固定分析器能量(CAE)扫描,全谱扫描时通能为100 eV;窄谱扫描时通能为30 eV,扫描次数为5次,并以表面污染C 1s(284.8 eV)为标准进行能量校正。扫描电子显微镜(SEM)为荷兰FEI公司生产的Quanta 200型,用来分析反应前后钢渣的微观形貌,检测条件为:高真空6×10-4 Pa,低真空13~133 Pa,环境真空133~2600 Pa的条件下,加速电压为200~30000 V,放大倍数范围为25~200000倍,分辨率为3.5 nm,利用ETD探头和BSED探头进行检测,X射线能谱仪(EDS)是EDAX Genesis 2000型,仪谱的分辨率<131 eV,Peltier冷台:-5~50 ℃的参数下对样品进行检测。
;比表面积>0.0005 m2/g,极限高真空1.33×10-8 Pa,-196 ℃,N2作为吸附等温线;X射线衍射仪为日本理学株式会社生产的Miniflex600型衍射仪,用来分析钢渣的物相成分,检测条件为:输出功率600 W,管电压40 kV,管电流15 mA,连续扫描Cu Kα射线,2θ扫描范围10°~80°;高分辨率电感耦合等离子体发射光谱仪(ICP)为德国生产的PQ 9000型,用来分析水体中As元素的含量,检测条件:波长范围160~900 nm,像素分辨率2 pm,光学分辨率3 pm,检测器分辨率2 pm,高光谱分辨率0.003nm,功率700~1700W;X射线光电子能谱仪(XPS)为美国赛默飞世尔科技公司生产的K-Alpha+型,用来分析反应前后钢渣表面的元素组成、结构和电子特征,检测条件为:分析室工作时的真空度为2×10-5 Pa,X光源为Al Kα源(Mono Al Kα),能量为1486.6 eV,6 mA×12 kV,束斑大小:400 μm;扫描模式为固定分析器能量(CAE)扫描,全谱扫描时通能为100 eV;窄谱扫描时通能为30 eV,扫描次数为5次,并以表面污染C 1s(284.8 eV)为标准进行能量校正。扫描电子显微镜(SEM)为荷兰FEI公司生产的Quanta 200型,用来分析反应前后钢渣的微观形貌,检测条件为:高真空6×10-4 Pa,低真空13~133 Pa,环境真空133~2600 Pa的条件下,加速电压为200~30000 V,放大倍数范围为25~200000倍,分辨率为3.5 nm,利用ETD探头和BSED探头进行检测,X射线能谱仪(EDS)是EDAX Genesis 2000型,仪谱的分辨率<131 eV,Peltier冷台:-5~50 ℃的参数下对样品进行检测。
1.3 除砷实验
1.3.1 钢渣粒径对除砷的影响
将5 g粒径分别为380~830 μm、250~380 μm、180~250 μm、150~180 μm、75~150 μm、48~75 μm的钢渣分别放入pH为2.5±1、50 mL 100 mg/L的含砷溶液(As(Ⅲ)、As(Ⅴ))的锥形瓶中置于恒温水域振荡箱中,按180 r/min的转速震荡300 min,取出后用孔径为0.45 μm的微孔滤膜进行过滤,用ICP测量上清液中砷的浓度,对滤渣进行收集,干燥后进行密封保存。按式(1)对去除率进行计算,按式(2)对钢渣的吸附含量进行计算,每组实验设定3个平行样品。
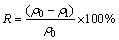 (1)
(1)
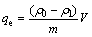 (2)
(2)
其中:R为去除率; 为水溶液中砷离子的初始浓度,mg/L;
为水溶液中砷离子的初始浓度,mg/L; 为用钢渣处理后水体中砷离子的浓度,mg/L;qe为钢渣的吸附含量,mg/g;V为砷溶液的体积,L;m为钢渣的含量,g。
为用钢渣处理后水体中砷离子的浓度,mg/L;qe为钢渣的吸附含量,mg/g;V为砷溶液的体积,L;m为钢渣的含量,g。
1.3.2 钢渣用量对除砷的影响
取75~150 μm的钢渣1、2、3、4、5、6、7 g,分别放入pH为1,50 mL 100 mg/L的含砷溶液的锥形瓶中,在室温条件下,以180 r/min的转速振荡300 min,取出后用孔径为0.45 μm的微孔滤膜进行过滤,用ICP测量上清液中砷的浓度,对滤渣进行收集,干燥后进行密封保存。按式(1)对去除率进行计算,按式(2)对钢渣的吸附含量进行计算,每组实验设定3个平行样。
1.3.3 pH值对钢渣除砷的影响
在不同pH条件下将75~150 μm、5 g的钢渣放入pH为1,50 mL 100 mg/L的含砷溶液中,在室温条件下,以180 r/min的转速振荡300 min,取出后用孔径为0.45 μm的微孔滤膜进行过滤,用ICP测量上清液中砷的浓度,对滤渣进行收集,干燥后进行密封保存。按公式(1)对去除率进行计算,按式(2)对钢渣的吸附含量进行计算,每组实验设定3个平行样品。
1.3.4 时间对钢渣除砷的影响
将75~150 μm、5 g的钢渣放入pH为1,50 mL 100 mg/L的含砷溶液中,在室温条件下,以180 r/min的转速分别振荡10、20、30、40、50、60、70、90、120、150、180、210、240、270和300 min。取出后用孔径为0.45 μm的微孔滤膜进行过滤,用ICP测量上清液中砷的浓度,对滤渣进行收集,干燥后进行密封保存。按式(1)对去除率进行计算,按式(2)对钢渣的吸附含量进行计算,每组实验设定3个平行样品。
1.4 毒性浸出实验
依据美国环保局推荐的《U.S.EPA Method 1311 Toxicity Characteristic Leaching Procedure (TCLP)》分析方法,对脱除砷后的钢渣进行毒性浸出测试,方法为:在1 L去离子水中加入5.7 mL的冰醋酸,将pH调节至2.88±0.05,制备浸提剂,然后将粒径为0.4~1.0 mm脱除砷后的钢渣与浸提剂以固液比为1:20进行混合,在恒温水浴振荡箱中以转速为180 r/min振荡18 h,完成后用硝酸清洗的过滤装置进行过滤,收集滤液,用ICP测量滤液中砷的浓度。
2 结果与讨论
2.1 钢渣的基本性质
比表面积测试显示48~75 μm的钢渣比表面积为2.245 m2/g,具有较为丰富的比表面积,利于与溶液中的砷离子接触[33]。采用XRF对钢渣化学组成进行分析,如表1所示。由表1可知,钢渣的主要化学组成是CaO、FexOy(铁氧化物)、SiO2、MgO,还含有少量在5%以下的P2O5、MnO、TiO2、V2O5、Al2O3等。根据钢渣的碱度w(CaO)/w(SiO2+P2O5)可知其值大约为3.2,根据MASON[34]提出的低碱度的钢渣值为小于1.8,中碱度的钢渣值为1.8~2.5之间,高碱度钢渣值为大于2.5,可知所选用的钢渣为高碱度钢渣。
表1 钢渣的化学组成
Table 1 Chemical composition of steel slags

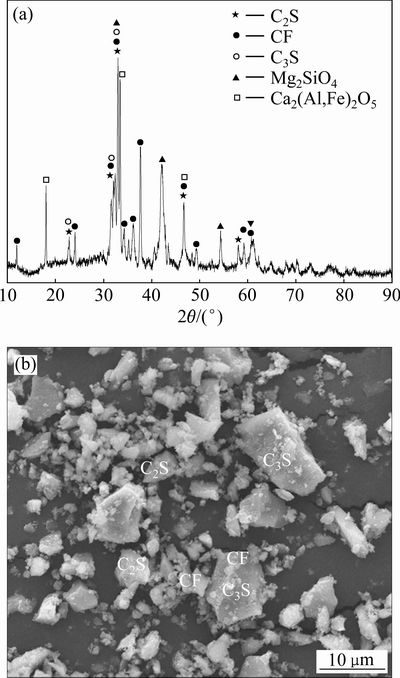
图1 钢渣的XRD谱和SEM像
Fig. 1 XRD pattern(a) and SEM image(b) of steel slag
利用XRD和SEM分析钢渣物相组成和微观形貌,如图1所示。由图1(a)可知,在2θ为22.83°、31.48°、32.91°、42.1°、46.5°和57.9°存在衍射峰,对应的物相为硅酸二钙(C2S);在2θ为11.9°、24.03°、32.05°、32.9°、34.28°、36.2°、37.6°、46.7°、49.2°、59.2°和60.7°存在的衍射峰对应的物相为铁酸钙(C2F);在2θ为32.3°和32.9°存在的衍射峰对应的物相为硅酸三钙(C3S);在2θ为32.99°、42.01°和54.3°存在的衍射峰对应的物相为镁橄榄石(Mg2SiO4),还在2θ为17.9°、33.4°和46.68°处发现了铁铝酸钙(Ca2(Al,Fe)2O5)的化合物,从峰强的大小和广度可以看出,其中以铁酸钙的物相最多,这与XRF元素分布相一致。图1(b)中钢渣SEM图显示较大块的钢渣多成板状和长条状,粒度大小不均,此为硅酸三钙(C3S);在其周围分布着圆形颗粒,其粒径较小,这些是硅酸二钙(C2S);同时可见,铁酸钙相(CF)在C3S、C2S晶体之间填充,形成连续的不规则形状[35-37]。
此外,按照《固体废物腐蚀性测定,GB/T 15555.12― 1995》对钢渣腐蚀性进行了测试,其浸出液pH值达到12.15,碱性较强,具有一定的腐蚀性,已十分接近《GB 5085.1―2007》中对腐蚀性危险废弃物的鉴别值12.5,其他重金属物质远低于危险废弃物鉴别标准。
钢渣富含钙和铁的氧化物的化学组成和强碱性的特点[38],决定了钢渣可以通过化学反应和吸附作用去除水体中的砷[1]。钢渣作为大宗固体废弃物,如能二次利用不仅为钢渣处置提供了途径,同时也降低了除砷成本。
2.2 钢渣脱砷行为
2.2.1 钢渣粒径对水溶液中砷脱除的影响
粒径对钢渣脱除水溶液中砷的影响如图2所示。随着钢渣粒径的减小,钢渣对As(Ⅲ)和As(Ⅴ)离子的去除率呈现上升趋势。粒径在75~150 μm范围,钢渣对As(Ⅲ)离子的去除率为85%,48~75 μm时达到最大(90%)。钢渣对As(Ⅴ)离子的去除效果比对As(Ⅲ)离子的去除效果好,在75~150 μm时,去除率为88%,48~75 μm时达到最大值(93%)。
钢渣粒径越小,比表面积越大,相应的表面能也越大,因而对砷离子的吸附量也越多,与含砷离子反应越充分[39-42]。在As(Ⅲ)离子去除过程中,粒径从380~830 μm减小至48~75 μm时,钢渣除砷量从0.45 mg/g增加至0.90 mg/g。对于As(Ⅴ)离子,除砷量相应的也从0.55 mg/g增加至0.93 mg/g,呈现出和As(Ⅲ)离子相同的递增趋势。
钢渣通过与砷离子发生物理吸附和化学沉淀从而达到脱除效果[41-43]。强碱性的钢渣在水溶液中,其碱性氧化物会发生溶解,达到中和沉淀效果[27]。钢渣对砷的脱除作用主要通过化学沉淀和配位体交换两种途径实现的,是一个化学吸附过程。钢渣中含有大量的钙铁氧化物,当与砷溶液混合后,其中的钙离子与溶液中的亚砷酸根离子和砷酸根容易形成非晶型的亚砷酸钙沉淀和砷酸钙沉淀。钢渣中的铁氧化物进入溶液后,其表面将结合配位水形成水合金属氧化物或氢氧化物,使钢渣界面上有大量―OH基团,砷酸根离子可以与铁离子的配位基进行交换而被吸附。
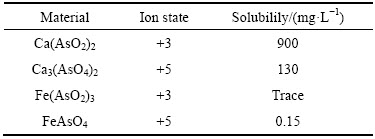
除砷后的钢渣浸出毒性实验结果显示,随着钢渣粒径减小,样品的浸出毒性降低。在As(Ⅲ)脱除实验中,除砷后粒径380~830 μm的钢渣中砷的浸出毒性为0.45 mg/L,而除砷后粒径48~75 μm钢渣中砷的浸出毒性降低至0.2mg/L,都低于《危险废物鉴别标准GB 5085.3―2007》规定的5 mg/L,属于一般固体废弃物。而在As(Ⅴ)离子去除中,除砷后钢渣的浸出毒性降至更低的值。结合表2工艺中砷化合物溶解度[44] (25 ℃)可以看出,砷的溶解度较低的原因是形成了亚砷酸铁和砷酸铁物质,因其溶解度相对较低,所以浸出毒性较低。
从图2中钢渣的吸附含量和钢渣对砷的固定比率的图中可以看出,钢渣的吸附量随着粒径的减少而增大,对浸出实验后的钢渣进行计算,固定在钢渣中砷含量的比率随粒径的减少而增大,并且As(Ⅴ)比As(Ⅲ)的固定比率相对较高,这与浸出毒性刚好相反,这是由于形成了更稳定的砷酸铁和亚砷酸铁及其衍生化合物(含砷化合物溶解度如表2所示)。
表2 工艺中砷化合物溶解度(25 ℃)
Table 2 Arsenic solubility in the process (25 ℃)
2.2.2 钢渣用量对水溶液中砷脱除的影响
采用75~150 μm的钢渣研究了钢渣用量对水溶液中砷的脱除影响,结果如图3所示。随着钢渣用量的增加,砷离子的去除率逐渐增大,当用量达到5 g时,溶液中As(Ⅲ)离子和As(Ⅴ)离子去除率达到96%左右。随着钢渣用量的增加,处理砷溶液后钢渣的浸出毒性呈现出缓慢的下降趋势,都低于危险废弃物排放标准规定的5 mg/L的值。在固定溶液中砷浓度一定的条件下,随着钢渣含量的增多,每克钢渣对As(Ⅲ)和As(Ⅴ)离子固定量呈现下降的趋势,但通过浸出实验后,稳定固定于钢渣中砷的比率较高,仅仅有少量的砷化物再次浸出进入溶液中。
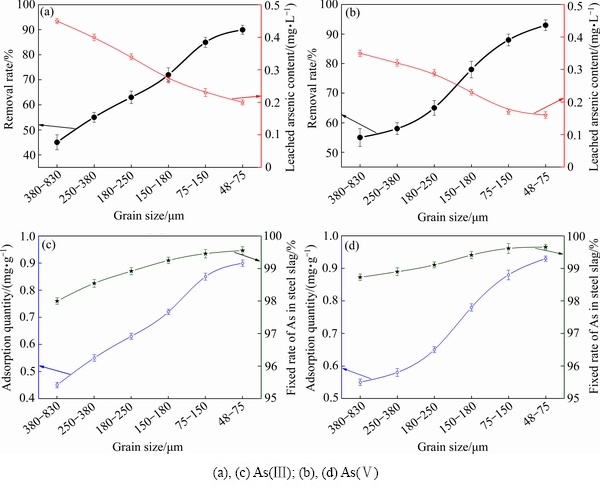
图2 粒径对钢渣脱除水溶液中砷的影响
Fig. 2 Effect of mesh number on As removal of steel slag in aqueous solution
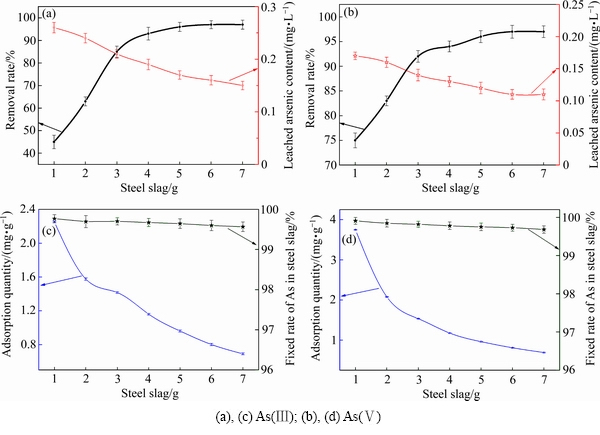
图3 用量对钢渣脱除水溶液中砷的影响
Fig. 3 Effect of dosage on As removal of steel slag in aqueous solution
钢渣除砷能力趋于饱和,相对应的钢渣除砷量减少。在溶液中砷离子浓度一定,钢渣用量较小时,吸附点位和反应点位对重金属离子浓度范围所造成的扩散、吸附反应的驱动力不明显。随着钢渣用量的增加,提供给溶液中砷离子有效点位增多,去除率也逐渐增加;当钢渣用量达到较高水平时,单位质量吸附和反应驱动力下降,并随反应点位逐渐接近饱和,驱动力明显下降,导致砷离子吸附量减少。
2.2.3 pH值对钢渣除砷的影响
水溶液的pH对钢渣除砷的影响如图4所示,强碱性的钢渣对水体的适应能力很强,在十分宽泛的pH范围(1~12)内对As(Ⅲ)和As(Ⅴ)都具有较高的去除率。砷离子的浸出毒性较低,随溶液的pH值变化很小。强碱性的钢渣引起水体中pH的变化,这样改变了砷离子的存在形态。砷离子的极化能力强,在pH较低的水溶液中对于As(Ⅲ)主要以H3AsO3形态存在,对于As(Ⅴ)主要以H3AsO4和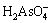 形态存在,当pH值升高时,对于As(Ⅲ)主要以
形态存在,当pH值升高时,对于As(Ⅲ)主要以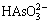 和
和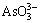 的形态存在,对于As(Ⅴ)主要以
的形态存在,对于As(Ⅴ)主要以 形态存在[7],以这样的形态存在更容易接近钢渣表面而被吸附,其次,溶液中H+与砷离子对钢渣表面吸附点位有着互相竞争关系,pH的增大可降低H+与砷离子的竞争作用,有利于砷的吸附。此外,因钢渣的主要成分为CaO、FexOy以及SiO2等组成的复合氧化物,pH值增大,会降低氧化物表面的正电位和能量,有利于
形态存在[7],以这样的形态存在更容易接近钢渣表面而被吸附,其次,溶液中H+与砷离子对钢渣表面吸附点位有着互相竞争关系,pH的增大可降低H+与砷离子的竞争作用,有利于砷的吸附。此外,因钢渣的主要成分为CaO、FexOy以及SiO2等组成的复合氧化物,pH值增大,会降低氧化物表面的正电位和能量,有利于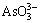 、
、 接近表面,在氧化物表面通过吸附和化学反应共同作用形成更稳定的产物。如图中的钢渣对砷的吸附量可以看出,其对As(Ⅲ)和As(Ⅴ)的吸附量处于一个相对稳定的值,且对As(Ⅴ)的吸附量比对As(Ⅲ)的吸附量更多,从钢渣对砷的固定比率可以看出,仅有少量的砷经过浸出毒性实验后再次进入到溶液中,固定比率处于较高的水平。
接近表面,在氧化物表面通过吸附和化学反应共同作用形成更稳定的产物。如图中的钢渣对砷的吸附量可以看出,其对As(Ⅲ)和As(Ⅴ)的吸附量处于一个相对稳定的值,且对As(Ⅴ)的吸附量比对As(Ⅲ)的吸附量更多,从钢渣对砷的固定比率可以看出,仅有少量的砷经过浸出毒性实验后再次进入到溶液中,固定比率处于较高的水平。
2.2.4 钢渣除砷动力学分析
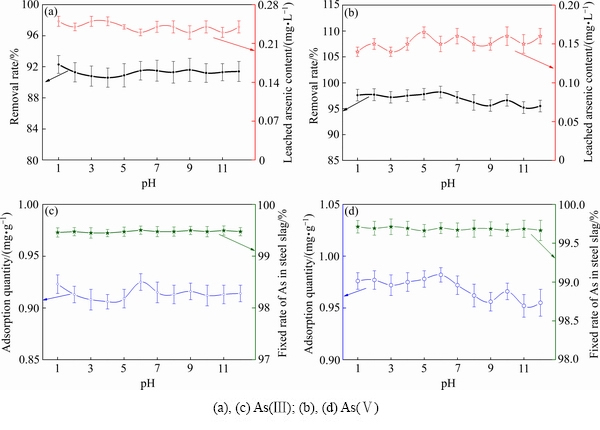
图4 pH值对钢渣脱除水溶液中砷的影响
Fig. 4 Effect of pH on As removal of steel slag in aqueous solution
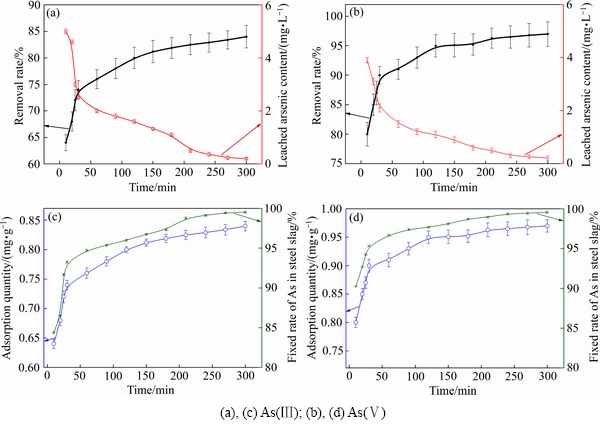
图5 时间对钢渣脱除水溶液中砷的影响
Fig. 5 Effect of times on As removal of steel slag in aqueous solution
时间对钢渣脱除水溶液中砷的影响如图5所示,随着时间的延长,钢渣对As(Ⅲ)离子和As(Ⅴ)离子的去除效率表现出相似的趋势,在初期时,砷离子的去除率随时间显著上升,吸附曲线较为陡直,在后期时,砷离子去除率随时间延长变化缓慢,曲线较为平缓,最终达到吸附平衡状态,显示出“快速吸附,缓慢平衡”规律。砷的浸出毒性值可以看出,钢渣与水溶液中的砷离子接触时间越长,浸出毒性越小,这主要是因为在较短的时间内,钢渣对砷离子主要是通过吸附作用,从而达到去除目的,随着时间的增加,通过化学反应去除砷的量不断增加,形成的物质更加稳定,所以浸出毒性较低。As(Ⅲ)离子和As(Ⅴ)离子的浸出毒性规律相同。钢渣对砷离子的吸附含量也随时间的延长而增加,钢渣对砷离子的固定率随着时间的延长呈递增的趋势,并且反应后形成的物质更加稳定。
采用吸附动力学的方法研究时间对钢渣脱除水溶液中砷的影响,采用准二级(PSO)模型来描述吸附动力学,动力学模型的数学表达式方程(3)给出如下:
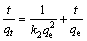 (3)
(3)
其中:qe代表的是钢渣在平衡时的吸附能力,mg/g;qt代表的是钢渣在对应时间(min)的吸附能力,mg/g;k2是相关吸附速率常数,g/(mg・min)。
从图5可以观察到在吸附反应开始后的十几分钟内,动力学过程慢慢接近饱和,这是由于细小颗粒的钢渣表面存在大量的吸附点。通过PSO模型分析,此时速率控制是主要的限制步骤,这意味着吸附过程是由于化学吸附作用和物理吸附作用引起的,这些现象涉及吸附剂和被吸附物电子之间的相互作用。钢渣吸附行为与单纯吸附剂不同在于吸附和化学沉淀反应同时发生,及时将砷离子进行化学稳定化,这些详细细节在2.3部分将予以讨论和解释。由PSO模型推导出的相应的速率参数如表3所示。
表3 PSO模型获得的吸附动力学的吸附速率参数
Table 3 Adsorption rate parameters for adsorption kinetics obtained from PSO model
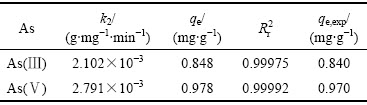
从图6中可以看出,线性回归系数较高( ≈ 0.999),说明了这个模型适合As(Ⅲ)离子和As(Ⅴ)离子的研究,初始浓度为100 mg/L时,平衡时仅检测出含有较低浓度的砷,说明可以利用钢渣去除水体中的砷,以达到处理污染水体的目的。
≈ 0.999),说明了这个模型适合As(Ⅲ)离子和As(Ⅴ)离子的研究,初始浓度为100 mg/L时,平衡时仅检测出含有较低浓度的砷,说明可以利用钢渣去除水体中的砷,以达到处理污染水体的目的。
2.3 钢渣脱砷机理分析
为揭示钢渣在酸性含砷溶液中的除砷机理,本文利用铜冶炼含砷酸性废水作为含砷水体,利用SEM、EDS和XPS研究除砷后钢渣的微观形貌、元素组成和价态分布演变规律,探索钢渣脱砷机理。铜冶炼含砷酸性废水含砷量为12530 mg/L,pH值为1,主要含有砷、硫酸及少量的其他重金属。
图7所示为脱砷后钢渣的SEM像,从图7中可以看出,钢渣粒径分布相对均匀,有长条的棒状物和很多小颗粒堆叠在一起的团聚物,这与原始钢渣形貌(见图1(b))有较大差异。还含有一些小颗粒分布在棒状物的附近,团聚物是由小颗粒堆叠在长条状的棒状物形成的。元素面扫描结果显示Ca、Fe和As分布均匀,这说明钢渣在强酸性条件下脱除砷是通过钢渣的溶解和与砷离子的再次反应,从而达到脱除水体中砷的目的。
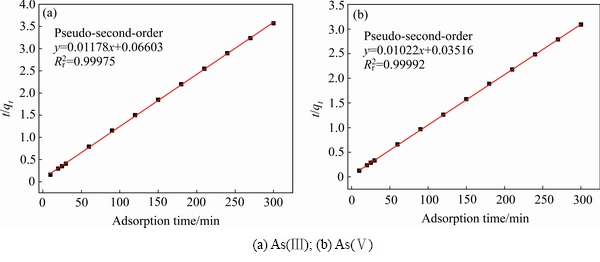
图6 钢渣吸附砷的准二级吸附动力学
Fig. 6 PSO adsorption kinetics of arsenic adsorption on steel slag
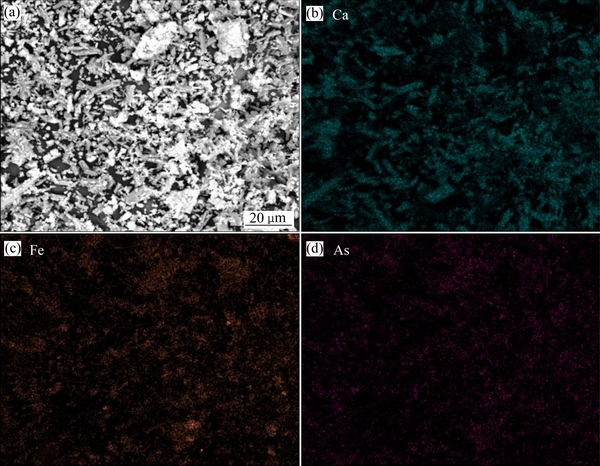
图7 除砷后钢渣的SEM像及元素面扫描分布
Fig. 7 SEM image(a) and element map scanning distributions for steel slag after treatment of contaminated acid solution
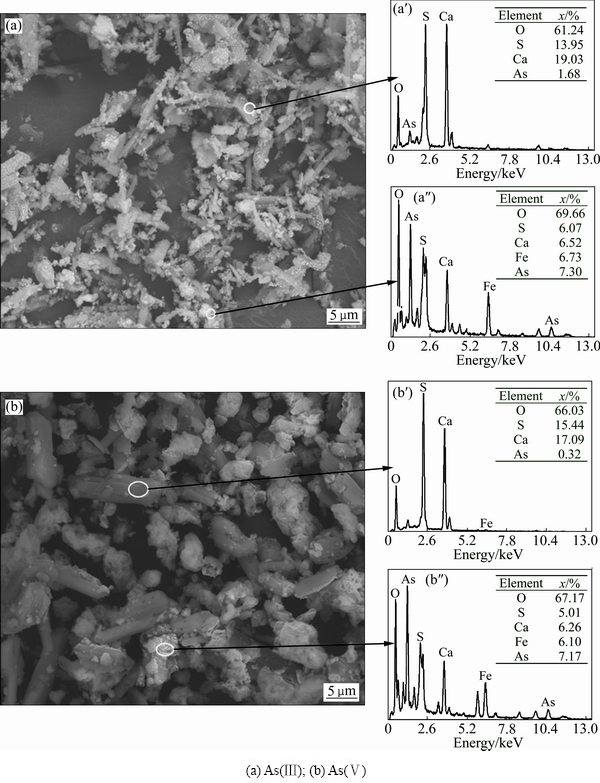
图8 钢渣去除含砷污酸的SEM像和EDS谱
Fig. 8 SEM images((a), (b)) and EDS spectra of steel slag removal of arsenic-containing waste acid
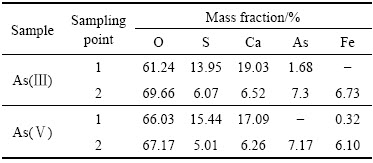
图8所示为钢渣去除含砷污酸的SEM像和EDS谱,表4所列为其EDS能谱分析。图8(a)中钢渣去除了含As(Ⅲ)离子的污酸,从EDS图中可以看出,长条形的棒状物的原子组成为O(61.24%)、S(13.95%)、Ca(19.03%)、As(1.68%),对其进行物质成分计算分析,发现是由CaSO4和Ca3(AsO3)2组成;而小颗粒的团聚物原子组成为O(69.66%)、S(6.07%)、Ca(6.52%)、Fe(6.73%)、As(7.30%),由SEM像可以看出,长条形的棒状物出现少量的砷含量是因为其表层负载有少量的小颗粒,对其进行物相成分计算分析,发现是由CaSO4、FeAsO3和Ca3(AsO3)2。图8(b)所示为钢渣去除含As(Ⅴ)离子的污酸,同样,也对其中的长条状的棒状物和小颗粒的团聚物进行组成分析。发现长条状的棒状物原子组成为O(66.03%)、S(15.44%)、Ca(17.09%)、Fe(0.32%),对其进行物相成分计算分析,发现是由CaSO4、Ca3(AsO4)2和少量的FeAsO4;小颗粒的团聚物原子组成为O(67.17%)、S(5.01%)、Ca(6.26%)、Fe(6.10%)、As(7.17%),对其进行物质成分计算分析,发现是由CaSO4、FeAsO4和Ca3(AsO4)2。其中长条状的棒状物可以清晰看见没有负载小颗粒,从而没有检测到砷的含量,主要物质成分为硫酸钙的化合物,小颗粒的团聚物因为负载于长条形的棒状物上,所以检测含有钙元素的存在。
可验证钢渣在酸性含砷水体中发生了如下反应:
第一步,氧化亚铁和氧化钙的溶解反应,并且在高钙钢渣所形成的局部过碱条件下,亚铁被游离氧或活性氧进一步氧化成三价铁[45]。
铁和钙氧化物溶解:
FeO(s)+2H+(aq)=Fe2+(aq)+H2O(l) (4)
CaO(s)+2H+(aq)=Ca2+(aq)+H2O(l) (5)
CaO(s)+H2O(l)=Ca2+(aq)+2OH-(aq) (6)
Fe2+(aq)+2OH-(aq)=Fe(OH)2(s) (7)
6Fe(OH)2(s)+O2(aq)=2Fe3O4(s)+6H2O(l) (8)
4Fe3O4(s)+O2(aq)+18H2O(l)=12Fe(OH)3(s) (9)
Fe(OH)3(s)+3H+(aq)= Fe3+(aq)+3H2O(l) (10)
第二步,As(Ⅲ)和As(Ⅴ)化学吸附及沉淀:
Fe3+(aq)+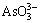 (aq)=FeAsO3(s) (11)
(aq)=FeAsO3(s) (11)
Ca2+(aq)+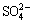 (aq)=CaSO4(s) (12)
(aq)=CaSO4(s) (12)
3Ca2+(aq)+2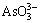 (aq)=Ca3(AsO3)2(s) (13)
(aq)=Ca3(AsO3)2(s) (13)
Fe3+(aq)+ (aq)=FeAsO4(s) (14)
(aq)=FeAsO4(s) (14)
3Ca2+(aq)+2 (aq)=Ca3(AsO4)2(s) (15)
(aq)=Ca3(AsO4)2(s) (15)
表4 钢渣的EDS分析
Table 4 EDS analysis of steel slag
为进一步获得脱砷后钢渣的表面信息,对脱砷后的钢渣进行XPS分析。图9所示为钢渣脱除As(Ⅲ)和As(Ⅴ)后的XPS谱。钢渣在280 eV、532 eV、347 eV中观察到的结合能分别为C 1s、O 1s、Ca 2p3/2元素。另外,在102.08 eV、152.08 eV、624.08 eV、712.08 eV附近发现了额外峰分别对应Si 2p、S 2p、Mn 2p、Fe 2p3/2。在图9(a)和(b)中还出现对应砷元素的As 3d峰。
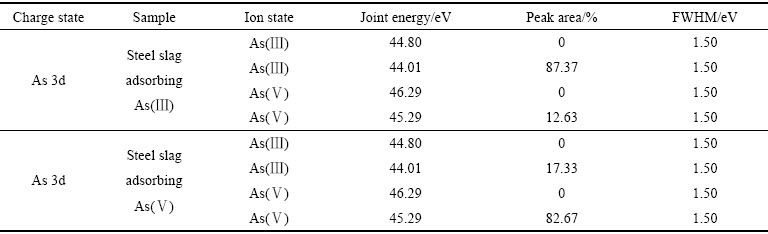
图9(c)所示为钢渣脱除水体中As(Ⅲ)离子后的As 3d XPS图谱,在42~48 eV可见两个较高的峰,源于As(Ⅲ)离子的主峰和分裂峰,而另两个强度较低的矮峰,对应为As(Ⅴ)离子的主峰和分裂峰。经过拟合之后,结果如表5所示,其中As(Ⅲ)离子的峰面积占87.37%,As(Ⅴ)离子的峰面积占12.63%。图9(d)所示为钢渣脱除水体中As(Ⅴ)离子后的As 3d XPS谱。主要对应As(Ⅴ)特征谱峰,其中As(Ⅴ)离子的峰面积占82.67%,除砷后钢渣中出现了As(Ⅴ)和As(Ⅲ)并存现象,可能是源于钢渣与砷离子(砷酸或亚砷酸离子)之间的氧化还原反应,Fe和Mn价态变化也会引起As氧化还原。
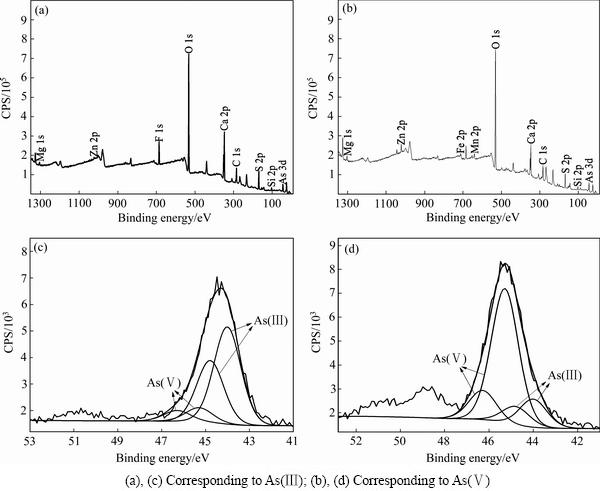
图9 钢渣去除砷的XPS谱
Fig. 9 As 3d XPS spectra of arsenic removed by steel slag
表5 As的结合能和相对含量
Table 5 As 3d binding energy and relative content
3 结论
1) 高钙钢渣主要成分为铁酸钙、硅酸二钙、硅酸三钙,还含有少量的硅酸镁和铁铝酸钙,其浸出液的pH值为12.15,碱性较强,具有一定的腐蚀性,略低于《GB 5085.1―2007》中对腐蚀性危险废弃物的鉴别值12.5。
2) 钢渣粒径和用量对除砷效率影响较大,水体除砷率随着粒径减小或钢渣用量增加而增加。钢渣粒径在48~75 μm之间时,钢渣在As(Ⅲ)和As(Ⅴ)水体中除砷量分别达到0.90 mg/g和0.93 mg/g。钢渣吸附除砷受pH值影响较小,在1~12的pH范围内,钢渣吸附的砷能够稳定固定于钢渣中,砷的固定率达到99%。动力学分析显示钢渣吸附行为受化学沉淀反应速率控制,吸附和化学沉淀同时发生,可及时将砷离子稳定化。
3) 高钙钢渣通过化学吸附和中和沉淀作用实现水体中砷离子脱除,钢渣中以CaO为主的碱性氧化物使水溶液呈碱性,钢渣中铁氧化物可加速砷离子吸附及后续沉淀,形成较为稳定的钙和铁的砷酸盐及亚砷酸盐,这些含砷颗粒附着于钢渣表面,达到稳定化作用。除砷钢渣中砷主要以原水体中As(Ⅲ)和As(Ⅴ)形态存在。反应后的钢渣经过毒性浸出实验,砷的浸出毒性低于《危险废物鉴别标准GB 5085.3―2007》规定的5 mg/L,属于一般固体废弃物。
REFERENCES
[1] OH C, RHEE S, OH M, PARK J. Removal characteristics of As(Ⅲ) and As(Ⅴ) from acidic aqueous solution by steel making slag[J]. Journal of Hazardous Materials, 2012, 213/214: 147-155.
[2] LI Xun, ZHU Xing, QI Xian-jin, LI Kong-zhai, WEI Yong-gang, WANG Hua, HU Jian-hang, HUI Xing-huan, ZHANG Xin. Pyrolysis of arsenic-bearing gypsum sludge being substituted for calcium flux in smelting process[J]. Journal of Analytical & Applied Pyrolysis, 2018, 130: 19-28.
[3] 赵占冲, 史谊峰, 祝 星, 祁先进, 王晓武, 尤开云, 王 华. 含砷石膏渣还原分解行为及砷迁移规律[J]. 中国有色金属学报, 2017, 27(1): 187-197.
ZHAO Zhan-chong, SHI Yi-feng, ZHU Xing, QI Xian-jin, WANG Xiao-wu, YOU Kai-yun, WANG Hua. Reductive decomposition behavior of arsenic bearing gypsum sludge with coal and arsenic migration rule[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(1): 187-197.
[4] 沈 忱, 闵小波, 史美清, 周波生, 赵宗文, 李辕成, 张 纯. 砷滤饼的铜砷分离[J]. 中国有色金属学报, 2017, 27(2): 356-362.
SHEN Chen, MIN Xiao-bo, SHI Mei-qing, ZHOU Bo-sheng, ZHAO Zong-wen, LI Yuan-cheng, ZHANG Chun. Separation of copper and arsenic in arsenic filtration cake[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(2): 356-362.
[5] YANG Jin-qin, CHAI Li-yuan, LI Qing-zhu, SHU Yu-de. Redox behavior and chemical species of arsenic in acidic aqueous system[J]. Transactions of Nonferrous Metals Society of China, 2017, 27(9): 2063-2072.
[6] WANG Jia-ning, ZENG Xian-chun, ZHU Xian-bin, CHEN Xiao-ming, ZENG Xin, MU Yao, YANG Ye, WANG Yan-xin. Sulfate enhances the dissimilatory arsenate-respiring prokaryotes-mediated mobilization, reduction and release of insoluble arsenic and iron from the arsenic-rich sediments into groundwater[J]. Journal of Hazardous Materials, 2017, 339: 409-417.
[7] BULUT G, YENIAL U, EMIROGLU E, SIRKECI A A. Arsenic removal from aqueous solution using pyrite[J]. Journal of Cleaner Production, 2014, 84(1): 526-532.
[8] JIANG Guo-min, PENG Bing, CHAI Li-yuan, WANG Qing-wei, SHI Mei-qing, WANG Yun-yan, LIU Hui. Cascade sulfidation and separation of copper and arsenic from acidic wastewater via gas-liquid reaction[J]. Transactions of Nonferrous Metals Society of China, 2017, 27(4): 925-931.
[9] KLERK R J D, FELDMANN T, DAENZER R, DEMOPOULOS G P. Continuous circuit coprecipitation of arsenic(Ⅴ) with ferric iron by lime neutralization: The effect of circuit staging, co-ions and equilibration pH on long-term arsenic retention[J]. Hydrometallurgy, 2015, 151: 42-50.
[10] CUI Jie, DU Ya-guan, XIAO Hong-xia, YI Qiu-shi, DU Dong-yu. A new process of continuous three-stage co-precipitation of arsenic with ferrous iron and lime[J]. Hydrometallurgy, 2014, 146(4): 169-174.
[11] SAIZ J, BRINGAS E, ORTIZ I. Functionalized magnetic nanoparticles as new adsorption materials for arsenic removal from polluted waters[J]. Journal of Chemical Technology & Biotechnology, 2014, 89(6): 909-918.
[12] CHEN Ou-po, LIN Yu-jung, CAO Wen-zhi, CHANG Chang-tang. Arsenic removal with phosphorene and adsorption in solution[J]. Materials Letters, 2017, 190: 280-282.
[13] LAATIKAINEN M, SILLANPAA M, SAINIO T. Comparison of ion exchange process configurations for arsenic removal from natural waters[J]. Desalination & Water Treatment, 2016, 57(29): 13770-13781.
[14] TANDORN S, ARQUEROPANYO O A, NAKSATA W, SOOKSAMITI P. Preparation of anion exchange resin loaded with ferric oxide for arsenic(Ⅴ) removal from aqueous solution[J]. International Journal of Environmental Science & Development, 2017, 8(6): 399-403.
[15] SANCHEZ J, BUTTER B, CHAVEZ S, RIFFO L, BASAEZ L, RIVAS B. Quaternized hydroxyethyl cellulose ethoxylate and membrane separation techniques for arsenic removal[J]. Desalination & Water Treatment, 2016, 57(52): 25161-25169.
[16] WANG Yong-liang, LV Cui-cui, XIAO Li, FU Guo-yan, LIU Ya, YE Shu-feng, CHEN Yun-fa. Arsenic removal from alkaline leaching solution using Fe(Ⅲ) precipitation[J]. Environmental Technology, 2018, 2: 1479-1487.
[17] ARANDA P R, LLORENS I, PERINO E, VITO I D, RABA J. Removal of arsenic(Ⅴ) ions from aqueous media by adsorption on multiwall carbon nanotubes thin film using XRF technique[J]. Environmental Nanotechnology Monitoring & Management, 2016, 5: 21-26.
[18] GONG Xu-jin, LI Wei-guang, ZHANG Duo-ying, FAN Wen-biao, ZHANG Xin-ran. Adsorption of arsenic from micro-polluted water by an innovative coal-based mesoporous activated carbon in the presence of co-existing ions[J]. International Biodeterioration & Biodegradation, 2015, 102: 256-264.
[19] CHAMMUI Y, SOOKSAMITI P, NAKSATA W, ARQUEROPANYO O. Kinetic and mechanism of arsenic ions removal by adsorption on leonardite char as low cost adsorbent material[J]. Journal of the Chilean Chemical Society, 2014, 59(1): 2378-2381.
[20] GILES D E, MOHAPATRA M, ISSA T B, ANAND S, SINGH P. Iron and aluminium based adsorption strategies for removing arsenic from water[J]. Journal of Environmental Management, 2011, 92(12): 3011-3022.
[21] KUMARPS, FLORES R Q, SJOSTEDT C, ONNBY L. Arsenic adsorption by iron-aluminium hydroxide coated onto macroporous supports: Insights from X-ray absorption spectroscopy and comparison with granular ferric hydroxides[J]. Journal of Hazardous Materials, 2015, 302: 166-174.
[22] MAJI S, GHOSH A, GUPTA K, GHOSH A, GHORAI U, SANTRA A, SASIKUMAR P, GHOSH U G. Efficiency evaluation of arsenic(Ⅲ) adsorption of novel graphene oxide@iron-aluminium oxide composite for the contaminated water purification[J]. Separation & Purification Technology, 2018, 197: 388-400.
[23] BAIG S A, SHENG Tian-tian, HU Yun-jun, XU Jiang, XU Xin-hua. Arsenic removal from natural water using low cost granulated adsorbents: A review[J]. CLEAN-Soil, Air, Water, 2015, 43(1): 13-26.
[24] CHIBAN M, ZERBET M, CARJA G, SINAN F. Application of low-cost adsorbents for arsenic removal: A review[J]. Journal of Environmental Chemistry & Ecotoxicology, 2012, 4: 91-102.
[25] ROY P, MONDAL N K, BHATTACHARYA S, DAS B, DAS K. Removal of arsenic(Ⅲ) and arsenic(Ⅴ) on chemically modified low-cost adsorbent: Batch and column operations[J]. Applied Water Science, 2013, 3(1): 293-309.
[26] 杨丽韫, 陈 军, 袁 鹏, 白 皓, 李 宏. 钢渣去除废水中重金属离子的研究综述[J]. 钢铁, 2017, 52(8): 1-9.
YANG Li-yun, CHEN Jun, YUAN Peng, BAI Hao, LI Hong. Research review of heavy metal ions removal from waste water by steelmaking slag[J]. Iron and Steel, 2017, 52(8): 1-9.
[27] OH C T, RHEE S S, IGARASHI T, KON H J, LEE W T, PARK J B . Sorption characteristics of arsenic on furnace slag by adsorption isotherm and kinetic sorption experiments[J]. Journal of the Korean Geotechnical Society, 2010, 26(9): 37-45.
[28] TRANG T T T, YANG C M, SHEN S, LE M H. Research on survey and assessment of the conditions affecting arsenic adsorption and removal by steel slag in water[J]. Angewandte Chemie, 2015, 15(3): 4516-4519.
[29] CHAKRABORTY A, SENGUPTA A, BHADU M K, PANDEY A, MONDAL A. Efficient removal of arsenic(Ⅴ) from water using steel-making slag[J]. Water Environment Research A Research Publication of the Water Environment Federation, 2014, 86(6): 524-531.
[30] SHI W, LI H, LIAO G, PEI G, LIN Y. Carbon steel slag and stainless steel slag for removal of arsenic from stimulant and real groundwater[J]. International Journal of Environmental Science & Technology, 2018, 15: 2337-2348.
[31] AHN J S, CHON C M, MOON H S, KIM K W. Arsenic removal using steel manufacturing byproducts as permeable reactive materials in mine tailing containment systems[J]. Water Research, 2003, 37(10): 2478-2488.
[32] 杨长明, 陈氏秋张, 沈 烁. 钢渣对水溶液中砷的吸附动力学和热力学特性试验[J]. 净水技术, 2015, 34(2): 83-89.
YANG Chang-ming, TRAN Thi-thu-trang, SHEN Shuo. Experiment of characteristics of adsorption kinetics and thermodynamics for arsenic (As) removal by steel slag[J]. Water Purification Technology, 2015, 34(2): 83-89.
[33] 姚景相, 陶珍东, 刘 鹏. 钢渣比表面积和掺入量对水泥性能的影响[J]. 水泥工程, 2008, 20(1): 23-26.
YAO Jing-xiang, TAO Zhen-dong, LIU Peng. Influences of specific area and amount of steel slag on cement performance[J]. Cement Engineering, 2008, 20(1): 23-26.
[34] MASON B. The constitution of some open-heart slag[J]. J Iron Steel Inst, 1994, 11: 69-80.
[35] 孟华栋, 刘 浏, 布焕存. 不同碱度钢渣的高温热闷粉化性能研究[J]. 环境工程, 2014, 32(6): 105-108.
MENG Hua-dong, LIU Liu, BU Huan-cun. Research on the autoclave powder property of steel slag with different basicity at high temperature[J]. Environmental Engineering, 2014, 32(6): 105-108.
[36] 赵计辉, 王栋民, 阎培渝. 转炉热焖钢渣矿物学特征的研究[C]// 中国硅酸盐学会. 中国硅酸盐学会固废分会成立大会第一届固废处理与生态环境材料学术交流会论文集: 2015年卷. 北京: 1994~2019中国学术期刊电子出版社, 2015: 239.
ZHAO Ji-hui, WANG Dong-min, YAN Pei-yu. Mineral characteristics of converter hot stew steel slag[C]// The Chinese Ceramic Society. Proceedings of the 1st Academic Conference on Solid Waste Disposal and Ecological and Environmental Materials: 2015 Volume. Beijing: 1994-2019 China Academic Journal Electronic Publishing House, 2015: 239.
[37] 张玉柱, 雷云波, 李俊国, 邢宏伟, 韩志杰, 龙 跃. 钢渣矿相组成及其显微形貌分析[J]. 冶金分析, 2011, 31(9): 11-17.
ZHANG Yu-zhu, LEI Yun-bo, LI Jun-guo, XIAN Hong-wei, HAN Zhi-jie, LONG Yue. Analysis of mineralogical composition in steel slag and its microstructure[J]. Metallurgical Analysis, 2011, 31(9): 11-17.
[38] SARKAR C, BASU J K, SAMANTA A N. Removal of Ni2+ ion from waste water by geopolymeric adsorbent derived from LD slag[J]. Journal of Water Process Engineering, 2017, 17: 237-244.
[39] STYLIANOU M A, INGLEZAKIS V J, MOUSTAKAS K G, MALAMIS S P, LOIZIDOU M D. Removal of Cu(Ⅱ) in fixed bed and batch reactors using natural zeolite and exfoliated vermiculite as adsorbents[J]. Desalination, 2007, 215(1): 133-142.
[40] 李灿华, 张勋利. 钢渣在废水处理中的应用[J]. 中国废钢铁, 2009(1): 40-43.
LI Can-hua, ZHANG Xun-li. Application of steel-slag in wastewater treatment[J]. Iron & Steel Scrap of China, 2009(1): 40-43.
[41] 朱跃刚, 陈仁民, 李灿华, 朱成林. 钢渣吸附剂在废水处理中的应用[J]. 武钢技术, 2007, 45(3): 35-38.
ZHU Yue-gang, CHEN Ren-min, LI Can-hua, ZHU Cheng-lin. Application of steel-slag adsorbent in wastewater treatment[J]. Wisco Technology, 2007, 45(3): 35-38.
[42] 朱跃刚, 程 勇, 李灿华. 钢渣吸附剂的研制[J]. 中国废钢铁, 2007(6): 30-34.
ZHU Yue-jin, CHENG Yong, LI Can-hua. Development of steel slag adsorbent[J]. Iron & Steel Scrap of China, 2007(6): 30-34.
[43] 董晓丹, 王 涛. 钢渣在污水处理及生态治理中的应用[J]. 炼钢, 2006, 22(2): 57-61.
DONG Xiao-dan, WANG Tao. Application of the steel-making slag in waste water treatment and ecology control[J]. Steelmaking, 2006, 22(2): 57-61.
[44] 廖天鹏, 祝 星, 祁先进, 王 华, 史谊峰, 刘春侠. 铜污泥中重金属形态分布及浸出毒性分析[J]. 化工进展, 2014, 33(3): 762-768.
LIAO Tian-peng, ZHU Xing, QI Xian-jin, WANG Hua, SHI Yi-feng, LIU Chun-xia. Chemical speciation of heavy metals and leaching toxicity analysis of sludge in copper metallurgy plant[J]. Chemical Industry and Engineering Progress, 2014, 33(3): 762-768.
[45] PETTINATO M, MUKHERJEE D, ANDREOLI S, MINARDI E R, CALABRO V, CURCIO S, CHAKRABORTY S. Industrial waste―An economical approach for adsorption of heavy metals from ground water[J]. American Journal of Engineering and Applied Sciences, 2015, 8(1): 48-56.
Behavior and mechanism of arsenic removal by high-calcium steel slag
LI Yong1, 2, ZHU Xing1, 2, QI Xian-jin1, 2, WEI Yong-gang1, 2, LI Kong-zhai1, 2, HU Jian-hang1, 2, WANG Hua1, 2
(1. State Key Laboratory of Complex Nonferrous Metal Resources Clean Utilization, Kunming University of Science and Technology, Kunming 650093, China;
2. Faculty of Metallurgical and Energy Engineering, Kunming University of Science and Technology, Kunming 650093, China)
Abstract: Based on the analysis of the composition and leaching characteristics of high-calcium steel slag, the research on the removal of arsenic from the solution using high-calcium steel slag was carried out, and the arsenic removal mechanism was also explored. The high-calcium steel slag is composed of calcium ferrite, dicalcium silicate and tricalcium silicate following with pH value of 12.15 in the leaching corrosion test, revealing strong alkalinity. With the decrease of slag particle size or the increase of slag dosage, the arsenic removal rate increases gradually. When the particle size of steel slag is in the range of 48-75 μm, the removal amounts of As(Ⅲ) and As(Ⅴ) in the solution reach 0.90 mg/g and 0.93 mg/g, respectively. The pH value has slight influence on the arsenic removal rate. The arsenic fixation rate reaches 99% for arsenic-enriched steel slag after reaction. It is found that the arsenic removal in the solution using high-calcium steel slag is controlled by the chemical reaction rate. When high-calcium steel slag contacts with arsenic-containing solution, arsenic ions can be adsorbed and precipitated simultaneously to form relatively stable arsenates and arsenites of calcium and iron for the removal and stabilization of arsenic ions in the solution. The leaching toxicity of arsenic in arsenic-containing steel slag is lower than 5 mg/L, specified in the “identification standard for hazardous wastes GB 5085.3―2007”, and the products are general solid wastes. The high-calcium steel slag is suitable for the harmless disposal of arsenic-containing acid wastewater.
Key words: high calcium steel slag; arsenic removal; adsorption
Foundation item: Project(51764036) supported by the National Natural Science Foundation of China
Received date: 2018-09-26; Accepted date: 2019-05-20
Corresponding author: ZHU Xing; Tel: +86-871-65153405; E-mail: zhuxing2010@hotmail.com
(编辑 龙怀中)
基金项目:国家自然科学基金资助项目(51764036)
收稿日期:2018-09-26;修订日期:2019-05-20
通信作者:祝 星,副教授,博士;电话:0871-65153405;E-mail:zhuxing2010@hotmail.com