嗜酸氧化亚铁硫杆菌亚铁氧化系统研究进展
来源期刊:中国有色金属学报2006年第7期
论文作者:张成桂 夏金兰 邱冠周
文章页码:1239 - 1249
关键词:亚铁氧化系统; 嗜酸氧化亚铁硫杆菌; 电子传递; rus操纵子
Key words:Fe2+ oxidation system; Acidithiobacillus ferrooxidans; electron transfer; rus operon
摘 要:嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans)是目前研究得最多的浸矿细菌, 其能量代谢途径复杂多样。 在有氧条件下, A. ferrooxidans以氧化Fe2+、 H2或(和)各种还原性硫化物提供能量来生长, 在亚铁氧化系统中, A. ferrooxidans的各种菌株氧化亚铁后产生的电子经大致相同的传递途径传递给最终电子受体O2, 但是最初电子受体可能有所不同。 讨论了A. ferrooxidans亚铁氧化系统中电子顺电势梯度传递的各个电子传递载体的组成, 基因结构和特征以及可能的相互作用机制; 同时, 介绍了A. ferrooxidans生长过程中, 少量电子经细胞色素bc1复合体逆电势梯度传递、 参与还原力NAD(P)H的生成和CO2固定过程中可能存在的电子传递模式, 以及A. ferrooxidans在不同生长基质中生长时rus操纵子的转录调控模式。
Abstract: Acidithiobacillus ferrooxidans, one kind of the best studied bioleaching microorganisms, has a complex diversity of energy metabolic pathways. Under aerobic conditions, A. ferrooxidans grows with energy from oxidation of Fe2+, H2 or/and various reductive sulfides, and the electrons released by oxidation of Fe2+ are transferred through a similar electron transport chain to the final electron acceptor O2, though the first electron acceptor may be different from one strain to another stain of A. ferrooxidans. The gene structures and gene feature of electron carriers, and the possible mechanism of the interactions between the electron carriers in the downhill flow of electron transfer during ferrous oxidation were investigated, and the possible electron transfer model for a few of electrons transported through bc1 complex by way of uphill flow of electron transfer for production of the reductive product NAD(P)H for CO2 fixation during the growth of A. ferrooxidans, as well as the transcript regulation mechanism of rus operon of A. ferrooxidans growing in different media were introduced.
基金信息:国家重点基础研究发展计划资助项目
文章编号: 1004-0609(2006)07-1239-11
张成桂, 夏金兰, 邱冠周
(中南大学 资源加工与生物工程学院, 长沙 410083)
摘 要: 嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans)是目前研究得最多的浸矿细菌, 其能量代谢途径复杂多样。 在有氧条件下, A. ferrooxidans以氧化Fe2+、 H2或(和)各种还原性硫化物提供能量来生长, 在亚铁氧化系统中, A. ferrooxidans的各种菌株氧化亚铁后产生的电子经大致相同的传递途径传递给最终电子受体O2, 但是最初电子受体可能有所不同。 讨论了A. ferrooxidans亚铁氧化系统中电子顺电势梯度传递的各个电子传递载体的组成, 基因结构和特征以及可能的相互作用机制; 同时, 介绍了A. ferrooxidans生长过程中, 少量电子经细胞色素bc1复合体逆电势梯度传递、 参与还原力NAD(P)H的生成和CO2固定过程中可能存在的电子传递模式, 以及A. ferrooxidans在不同生长基质中生长时rus操纵子的转录调控模式。
关键词: 亚铁氧化系统; 嗜酸氧化亚铁硫杆菌; 电子传递; rus操纵子
中图分类号: Q936 文献标识码: A
ZHANG Cheng-gui, XIA Jin-lan, QIU Guan-zhou
(School of Resources Processing and Bioengineering, Central South University,
Changsha 410083, China)
Abstract: Acidithiobacillus ferrooxidans, one kind of the best studied bioleaching microorganisms, has a complex diversity of energy metabolic pathways. Under aerobic conditions, A. ferrooxidans grows with energy from oxidation of Fe2+, H2 or/and various reductive sulfides, and the electrons released by oxidation of Fe2+ are transferred through a similar electron transport chain to the final electron acceptor O2, though the first electron acceptor may be different from one strain to another stain of A. ferrooxidans. The gene structures and gene feature of electron carriers, and the possible mechanism of the interactions between the electron carriers in the downhill flow of electron transfer during ferrous oxidation were investigated, and the possible electron transfer model for a few of electrons transported through bc1 complex by way of uphill flow of electron transfer for production of the reductive product NAD(P)H for CO2 fixation during the growth of A. ferrooxidans, as well as the transcript regulation mechanism of rus operon of A. ferrooxidans growing in different media were introduced.
Key words: Fe2+ oxidation system; Acidithiobacillus ferrooxidans; electron transfer; rus operon
嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans: A. ferrooxidans)是一种硫杆菌属化能自养菌, 属于革兰氏阴性细菌, 好氧嗜酸, 主要生长在pH=1~3的环境中, 是迄今已报道的20多种浸矿细菌中研究得最多的浸矿细菌。 A. ferrooxidans在有氧条件下依靠Fe2+、 各种还原性硫化物以及H2氧化来提供能量生长。 在无氧条件下, 能[CM(22]以Fe3+或以S为电子受体、 H2为电子供体, 或以[CM)] Fe3+为电子受体、 含还原性硫化合物为电子供体提供能量的情况下生长[1-6]。 这些现象说明 A. ferrooxidans能量代谢途径的多样性和复杂性。
A. ferrooxidans在Fe2+基质中生长时, Fe2+被快速氧化成Fe3+提供电子。 在pH 2.0时, 电对Fe2+/Fe3+的电位为0.77V, 稍低于pH 7.0时电对O2/H2O的0.82V, 表明O2 能够在有质子(H+)的情况下作为电子受体被Fe2+还原成H2O, 所以生活在极端酸性环境中的A. ferrooxidans能够利用Fe2+氧化提供电子而作为生长的能量物质; 1mol Fe2+氧化释放1mol电子, 大量的Fe2+氧化后放出的电子才能满足少量细菌细胞的生长。 目前, 人们通过对亚铁氧化系统中的多种功能组分的分离纯化和分子生物学方面的研究, 对亚铁氧化系统中的关键酶及其分子生物学作用途径有了较深入的了解, 认为亚铁氧化后大部分的电子顺电势梯度传递给O2, 同时少量电子逆电势梯度传递, 产生还原力NAD(P)H参与CO2的固定和有氧代谢。 图1所示为基于已有研究推演出的可能的亚铁氧化系统电子传递模式[7, 8]。 如图1所示, 可能的电子顺电势梯度传递途径为: Fe2+→Cyc2→Rus→Cyc1→Cyt c氧化酶→O2 或Fe2+→Iro→Cytc→Rus→Cyc1→Cyt c氧化酶→O2; 可能的电子逆电势梯度传递途径为: Fe2+→Rus→CycA→Cyt bc1复合体和NADH-Q还原酶。 对于不同 A. ferrooxidans菌株, 亚铁氧化系统中的电子载体可能不同, 这反映了A. ferrooxidans与环境相适应的遗传多样性。 另外, 有关电子载体相关操纵子的表达调控研究也是近年来的热点, 其中顺电势梯度传递途径Cyc2→Rus→ Cyc1→Cyt c氧化酶→O2中的电子传递体的表达操纵子rus研究得最多。 如图2所示, rus操纵子由cyc2、 cyc1、 orf、 coxB、 coxA、 coxC、 coxD和rus 8个基因以及2个上游启动子PⅠ、 [CM(22]PⅡ和一个位于coxD和rus基因间的内部启动子Prus所组成, 这8个基因的编码产物分别为Cyc2、 Cyc1、 功能未知蛋白(ORF)、 细胞色素c氧化酶的4个亚基(Ⅱ、 Ⅰ、 Ⅲ、 Ⅳ)和Rus[9]。 本文作者拟对近几年有关A. ferrooxidans亚铁氧化系统的电子传递载体及重要操纵子rus的表达调控的研究进展进行综述。
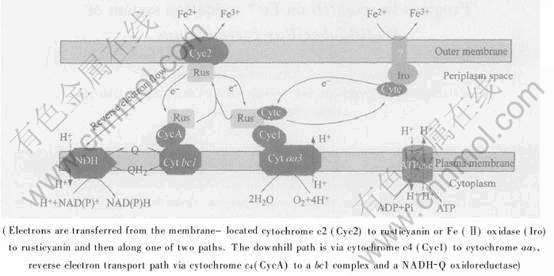
图1 A. ferrooxidans亚铁氧化系统电子传递模式简图
Fig.1 Model of electron transport pathway of iron oxidation of A. ferrooxidans
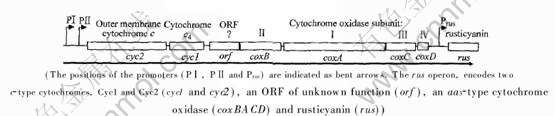
图2 rus操纵子的结构模型
Fig.2 Structural model of rus operon, each gene shown by an open box
1 顺电势梯度电子传递载体
1.1 外膜细胞色素c蛋白Cyc2
Yarzábal等[10]认为由cyc2基因编码的一种外膜细胞色素c类蛋白Cyc2(分子量为22kDa)可能是A. ferrooxidans电子传递链中的第一个电子受体候选者(如图1所示), 因为Cyc2能将细胞外Fe2+氧化后释放的电子经过外膜到达质膜上的细胞色素氧化酶这个过程串成为一个整体模式, 同时编码Cyc2的cyc2基因是rus操纵子中的第一个被转录翻译的基因(如图2所示)。 由于在细胞质(pH约为6)和细胞周质(pH值约为3.5)环境中, Fe2+高度自氧化成Fe3+, Fe3+容易转变为不溶物, 因而游离Fe2+氧化难以在细胞内环境中进行, 而应该在pH 1~2的细胞外环境中进行。 A. ferrooxidans细胞表面覆盖有与细胞外多聚物中葡萄糖酸结合的多聚Fe复合物, Ingledew等[11]推断该多聚Fe复合物将电子从膜外传递给下一个位于细胞周质中的电子受体。 关于Fe2+氧化后电子的最初受体候选者的推论还有很多[12-15], 但只有Cyc2位于细胞外膜上[10], 具备最初电子受体的环境条件。 在其他种类的微生物, 如Desulfovibrio vulgaris, Geobacter sulfurreducens, Shewanella putrefaciens 和 Shewanella frigidimarina等的细胞外膜上也存在细胞色素c类蛋白, 这些细胞色素蛋白和可溶性金属离子或矿石相互作用, 参与能量代谢[16, 17]。 在S. putrefaciens中的两种外膜细胞色素c类蛋白, 甚至具有金属还原酶的活性[17]。 Cyc2的功能可能与此类似。 尽管Cyc2作为Fe2+氧化后的最初电子受体推论好像十分合理, 但是还是不能排除是否还有从细胞内分泌出的蛋白质参与细胞外电子传递。
1.2 Fe(Ⅱ)氧化酶
Fe(Ⅱ)氧化酶 (Iron oxidase: Iro)也被认为可能在A. ferrooxidans电子传递链中充当Fe2+氧化后的最初电子受体。 如图1所示, Iro将来自Fe2+氧化释放的电子经过水溶性细胞色素c和铜蓝蛋白(Rus)将电子传递给下一个电子传递体Cyc1(一种与细胞色素aa3复合体偶联的细胞色素c4蛋白)。 Yamanaka等 [12] 以A. ferrooxidans Fe-1作研究对象, 发现Iro在将电子传递给水溶性细胞色素c552(s)的过程中, 需要Rus的参与以保持Iro的稳定性; 在没有Rus的酸性Fe2+溶液中, 细胞色素c552(s)虽然也能快速接受Iro的电子转变成还原态, 但在其后的自氧化过程中将导致Iro解聚失活[18]。 Iro最先是由Kusano等[19]从 A. ferrooxidans Fe-1中分离而来, 是由8~10个分子量为6kDa的亚基组成的同聚体。 iro基因的开放阅读框(ORF)中包含有273个核苷酸, Southern杂交验证iro基因在细菌基因组中为单一拷贝, Nothern杂交时在0.6kb和0.45kb处各出现一个杂交信号, 虽然为什么出现两个杂交信号的原因还没有确证, 但由此却可以肯定iro基因是独立于其他基因而单独转录的。 对N末端氨基酸残基序列与蛋白质数据库中的序列比对结果表明, Iro是HiPIPs ( high-redox potential ion-sulfur proteins)家族中的新成员[19]。 HiPIPs在紫色光合细菌中广泛存在, 每个亚基含有4Fe-4S族。 HiPIPs和Iro都含有7个最保守的氨基酸残基, 其中4个Cys充当4Fe-4S的配位基, 另外三个保守的残基分别为Tyr、 Phe和Gly、 Tyr和Phe与4Fe-4S相互作用, Gly则在HiPIPs亚基的正确折叠中起重要作用。 iro基因具有与E. coli σ70所识别的启动子相似的序列: -10位的TACAAT和-35位的GCTGGC。 Bruscella等[20]研究发现从A. ferrooxidans ATCC33020中克隆的iro基因能在E.coli中高效表达, 表达产物能分泌到E. coli细胞周质空间(pH约为6)。 他们通过对表达产物的研究认为Iro拥有HiPIP的全部特征, 并发现该Iro蛋白在E. coli中的表达依赖Tat系统, 因为在E. coli ΔtatC突变体细胞周质中检测不到该蛋白产物。
虽然定位在周质空间的Iro被推定为Fe2+氧化后电子传递的最初电子受体, 也被认为是HiPIPs中的新成员, 但是有一些观察和现象与此相矛盾。 首先, HiPIPs一般出现在光合细菌中, 它在两个膜整合蛋白复合体之间传递电子, 即在细胞色素bc1复合体到光合反应中心或末端细胞色素氧化酶之间传递电子[21, 22], 其次, 在很多A. ferrooxidans菌株中都没有检测到Fe(Ⅱ)氧化酶的存在[9]。
尽管关于A. ferrooxidans的Iro的报道很多, 但是目前关于Iro和Fe2+之间的的具体作用机制还不甚清楚。 Bruscella等[20]报道iro基因在A. ferrooxidans ATCC23270和A. ferrooxidans ATCC-33020的基因组中坐落位点与iro基因在A. ferrooxidansFe-1和A. ferrooxidans BRGM中的不同, 在A. ferrooxidans ATCC 23270和A. ferrooxidans ATCC 33020中, iro基因不是坐落在purA操纵子(腺苷酸基琥珀酸合成酶操纵子)下游, 而是在petC2操纵子(细胞色素bc1复合体纵子)下游, 编码一个类细胞色素c1蛋白。 即Iro蛋白也可能与光合细菌中HiPIP功能一样, 在细胞色素bc1复合体到末端细胞色素氧化酶之间传递电子, 而在硫氧化系统中发挥重要的作用。 另外, Giudici-Orticoni等[13]从A. ferrooxidans ATCC23270中纯化了一种含有细胞色素c类蛋白并能在Fe2+存在的情况下迅速还原Rus的酶, 他们称该酶为Iron-Rus细胞色素氧化还原蛋白, 该蛋白中的细胞色素c类蛋白和Rus紧密结合在一起, 并有别于细胞色素c552(s), 可能是膜结合的细胞色素c552(m)或c550(m), 他们认为Iron-Rus细胞色素氧化还原蛋白可能就是使Fe2+氧化的第一个组分。
1.3 铜蓝蛋白
如图1所示, 铜蓝蛋白(Rus)作为电子传递链中可游动的电子传递体, 它一方面将电子从Cyc2顺电势梯度传递给细胞色素aa3复合体偶联细胞色素c4蛋白(Cyc1); 另一方面, 它将电子从Cyc2逆电势梯度传递给另一种与细胞色素bc1复合体偶联的细胞色素c4蛋白(CycA)。
铜蓝蛋白(Rus)是rus基因编码的一种水溶性铜结合蛋白, 分子量为16kDa。 rus基因位于rus操纵子的最下游, 在基因组中为单拷贝基因, 能单独转录或/和其他基因共转录[9]。 从不同 A. ferrooxidans菌株中分离的Rus, 其氨基酸序列的差别小于10%[23], 其铜离子配位基包括Cys(138)、 His(143)、 Met(148)和His(85) 4个氨基酸, 其中His(85)后面紧联Ser[24]。 这与Amicyanin和Plastocyanin等铜蛋白的His后紧联Asn不同, 如Amicyanin中是His(47)-Asn(48), Plastocyanin中是His(39)-Asn(40)。
Rus的氧化还原电位在pH 3.2时为0.68V, 相对其他铜蛋白来说电位较高。 Cu-N(His85)的距离在Rus氧化态和还原态时是不同的, 而其它铜蛋白没有发生变化; Cu-S(Met148)的距离相对于其他铜蛋白的Cu-S(Met)距离较短而致使Cu离子在Rus蛋白中被包裹得更紧更深, 也许是由于这两个因素的原因, 导致Rus氧化还原电位较高[25]。
最初发现Rus时, 人们认为它是Fe2+氧化后的直接电子受体, 但后来的体外研究表明, 从Fe2+到Rus的电子传递速率太低, 这与Fe2+氧化后电子在A. ferrooxidans体内的快速传递相矛盾[12]。 说明在电子传递到Rus过程中, 一定有中间电子载体存在, 这意味着Rus拓宽了电子传递途径。 目前在其它革兰氏阴性细菌中没有发现有Rus的存在, 氧化亚铁钩端螺旋菌在Fe2+基质中生长时也没有痕量的Rus的表达。
Rus在以Fe2+基质中生长的A. ferrooxidans细胞体内大量表达, 约占细胞蛋白总量的5%[26], 说明Rus在A. ferrooxidans代谢中具有重要的生物学功能。 大量Rus存在于细胞周质可以很有效的收集外膜上电子受体(可能是Cyc2蛋白)上的电子, 使外膜上的电子受体总是保持在氧化状态以便随时随地地接受Fe2+氧化后释放的电子, 同时最大速率地驱动Fe2+氧化。 如果其他因素(如O2的浓度, 抑制剂的存在)变化影响电子传递的速率, Rus调节电子下传速率, 同时也保持外膜上电子受体的氧化状态。 这使Rus既能作为从外膜电子载体上收集电子的电子储存库, 也是往下分流电子的电子传递通道。 这似乎也是对于以低能量物质为生长基质的A. ferrooxidans细菌高效利用能量供自己生长的有效方式。
A. ferrooxidans中Rus的表达量与生长基质和生长周期有关。 在Fe2+基质中, rus基因在整个生长过程中都表达, 因为Rus蛋白在对数生长期和稳定期内一直存在。 但是以S为培养基质, rus基因和Rus的表达主要是在对数前期内, 表达量相对于以Fe2+为基质中的要少, 进入对数中后期表达量逐渐减少, 直至消失; 把从S基质稳定期内的细菌接种到新鲜的S培养基质培养液中, 接种后最初的8h后免疫印迹杂交没有信号产生, 进入对数生长前期Rus表达量上升, 从无到有说明Rus是重新合成的[27]。 令人惊讶的是在无氧条件下(H2/Fe3+), 免疫印迹杂交也显现出Rus杂交信号, 将无氧条件下生长的细菌转入有氧条件下Fe2+生长基质中, 细菌在开始生长时并没有Fe2+氧化能力, 经过一段时间的适应, 氧化Fe2+的能力才恢复, Blake等[28]推测在无氧条件下检测到的Rus可能只是Rus的原形式, 因为其原蛋白中没有铜的存在, Fe2+和氧气可能在Rus活性的回复中起到了十分重要的作用。 Ramírez等[29]研究发现A. ferrooxidans在以不含Fe的金属硫化物(ZnS, CuS)为培养基质的生长过程中也表达Rus。 但Rus在硫氧化系统中的作用及其调节机制还没有文献阐述。
1.4 细胞色素c
在Fe2+基质中生长的A. ferrooxidans细胞体内, 细胞色素c含量可占到细菌蛋白质总量的10%, 它在Fe2+氧化后的电子传递过程中发挥十分重要的作用。 对A. ferrooxidans ATCC 23270基因组序列分析发现, A. ferrooxidans可能含有11个编码细胞色素c的基因。 相对于以Fe2+为基质, A. ferrooxidans以S0为基质生长时的细胞色素c的种类和总量一般明显较少。 Yarzábal等[30]发现有一种细胞色素c只在S0基质生长条件下表达, 有3种细胞色素c只在Fe2+基质生长条件下特异表达, 还有的细胞色素c在两种培养基质条件下都能表达, 这表明不管是Fe2+氧化还是S0氧化, 细胞色素c都参与了其中的反应过程; 同时也表明在不同的培养基质条件下, 不同的能源物质作为电子供体时能调节不同种类的细胞色素c参与相关的生物化学反应, 使A. ferrooxidans表现出不同的环境适应性。 相对于S0, 等摩尔的Fe2+氧化后将电子传递到O2的过程中产生的能量少得多, 同时, 由于A. ferrooxidans在Fe2+基质生长的过程中, 需要细胞色素bc1通过逆电势梯度传递电子参与NAD(P)H的反应[7, 31], 因此Fe2+氧化需要更多或高浓度的电子传递组分(如细胞色素c)来驱动其氧化的发生, 才能满足A. ferrooxidans生长过程中能量的需求。
Cabrejos 等[32]针对缺失Fe2+氧化活性但保留有S0氧化活性的A. ferrooxidans ATCC23270突变菌株进行研究时发现, 突变菌株细胞体内的细胞色素c合成系统不能正常工作。 似乎A. ferrooxidans在S0氧化过程可以不需要细胞色素c。 但是更多证据表明这是错误的, 因为在S0基质上生长的A. ferrooxidans体内通常包含有很多种类的细胞色素c, 几乎所有有关A. ferrooxidans S0氧化的文献都认为细胞色素c是其呼吸链中的组分之一。
在无氧和以Fe3+作为电子受体的条件下, A. ferrooxidans在生长过程中能被诱导超量表达一种耐酸细胞色素c, 其分子量为28kDa, 氧化还原电位势在pH 2.0时为0.56V。 如, 当A. ferrooxidans细菌从有氧条件下(Fe2+/O2体系)转入到无氧条件下(H2/Fe3+体系)生长时, 该耐酸细胞色素c的表达量显著增加。 值得注意的是, 在S0/Fe3+、 Fe2+/O2、 H2/O2或H2/S0等体系中, A. ferrooxidans也高水平表达耐酸细胞色素c [6]。 序列分析发现, 无氧条件下和有氧条件下表达的细胞色素c的氨基酸序列相似性不大, 由此, Ohmura等[6]认为这是由于它们分别和Fe3+还原和Fe2+氧化相关联, 即执行不同的氧化还原的功能的缘故。
1.5 Cyc1-细胞色素c氧化酶偶联细胞色素c4蛋白
Cyc1是由cyc1基因编码的一种c4型细胞色素蛋白, 它负责将电子从Rus传递给细胞色素c氧化酶(如图1所示)。 A. ferrooxidans ATCC33020菌株中, cyc1基因的ORF为585bp。 在该ORF上游, 存在两个可能的转录起始位点, 表达的Cyc1分子量为21kDa, 包含两个亚铁血红素结合区域[9, 33]。 氨基酸序列比对分析发现, 该细胞色素c与从A. ferrooxidans BRGM[34]菌株中分离的膜结合细胞色素c552(m)在分子量大小和序列方面相似性极高, 与从A. ferrooxidans Fe-1[28]菌株中分离的21kDa的膜结合细胞色素c552(m)在N末端的同源性为84%, 其中72%的氨基酸残基相同。 Cyc1中有一段序列在A. ferrooxidans Fe-1 细胞色素c552(m)中存在, 然而在A. ferrooxidans Fe-1 细胞色素c552(s)中没有, 以及Cyc1氨基酸序列与从Azotobacter vinelandii, Pseudomonas aeruginosa, Pseudomonas stutzeri 和 Pseudomonas nautica 617中分离的细胞色素c4的序列高度相似, 因此Cyc1被认为是c4型的膜结合细胞色素c552(m)。 也有证据认为14kDa的外膜结合水可溶性细胞色素c552(s)是由Cyc1修饰或加工的产物, 两者在N末端的同源性为95.3%, 其中67.9 %的氨基酸残基相同, 但是c552(s)只有单一的亚铁血红素结合域, 而且c552(s)只是存在于很少的A. ferrooxidans菌株中, 并不是普遍存在[35, 36]。
1.6 细胞色素c氧化酶
细胞色素c氧化酶是电子传递链上的终端酶, 它承担着细胞色素c到O2的电子传递功能, 催化O2还原为H2O, 并与质子泵功能相偶联(如图1所示)。
细胞色素c氧化酶是含血红素/铜终端氧化酶大家族的成员之一。 大多数需氧细菌血红素/铜终端酶中都含有3个核心亚基, 其中亚基I最保守, 它含有与两个血红素基团和一个Cu(CuB)离子配位的组氨酸。 亚基II也非常保守, 含有双核CuA中心, 接受细胞色素c上的电子。 1999年Harrenga等[37]研究发表了Paracoccus denitrificans含4个亚基的细胞色素c氧化酶完善的三维晶体结构, 该研究结果为细胞色素c氧化酶结构功能分析和其催化反应机理的阐述, 提供了更详细更可靠的直接证据。
Kai等[38, 39] 较详细地研究了A. ferrooxidans 33020细胞色素c氧化酶的表达、 结构与酶特征, 结果表明A. ferrooxidans 33020细胞色素c氧化酶含有4个亚基Ⅰ-Ⅳ(coxB、 coxA、 coxC、 coxD), 分别由基因coxA、 coxB、 coxC、 coxD编码。 亚基Ⅰ (CoxA)最保守, 由627个氨基酸组成, 分子量为60kDa, 拥有与两个血红素基团和一个铜离子配位的组氨酸、 两个高度疏水区域和一个12次跨膜螺旋核心区。 亚铁血红素和CuB所在的核心区域虽然镶嵌在膜脂双分子层中, 但更趋向于膜脂外侧, 这就解释了细胞色素c氧化酶为何在与细胞周质所处的pH环境大致相符的pH 3.5时氧化活性最大。 亚基Ⅱ (CoxB)起初由254个氨基酸组成, 当去掉由51个氨基酸组成的N末端信号肽后, 便形成有功能的细胞色素c氧化酶亚基Ⅱ, 该亚基的N末端的两个跨膜区将其锚定在膜上, C末端有保守芳香氨基酸序列(145-WKWTFSY-151)[9]。 细胞色素氧化酶亚基Ⅱ含有混价态的双核CuA中心[2(Cu-S)], 其配位氨基酸为H181、 C222、 C226、 H230和M233, 对CuA起稳定作用的氨基酸为W145 和 D178, 还有3个高度保守的氨基酸残基 (Q144、 D178和D193)和细胞色素c相互作用。 亚基Ⅲ (CoxC)由183个氨基酸残基组成, 分子量为20kDa, 有5个跨膜螺旋整合在细胞膜中。 亚基Ⅳ (CoxD)只有64个氨基酸残基, 分子量为7kDa, 是只有一个跨膜螺旋的小蛋白, 不同细菌细胞色素c氧化酶的亚基Ⅳ序列不同, 因而它是细菌细胞色素c氧化酶中保守性最差、 变异度较高的一个蛋白质。 十分有趣的是, A. ferrooxidans在系统进化树的分类中属于变形杆菌, 但是CoxA、 CoxB和CoxC的氨基酸残基序列却和蓝细菌(Synechococcus vulcanus、 Synechocystis sp.和Anabaena sp.)中细胞色素c氧化酶同源性更高, 然而核苷酸的序列比对的结果却与此相反[17]。
从细胞色素c到细胞色素c氧化酶的电子传递以及在细胞色素c氧化酶中的后续电子传递过程一直是人们所关注的问题。 快速动力学研究证明, CuA是接受来自细胞色素c上电子的初始受体, 二者间复合物的形成是它们间反应的限速步骤[40], CuB双核中心位于其跨膜疏水区内, 是O2键合位点, 当一分子O2被还原时, 除了4个质子消耗于H2O的形成外, 还有4个质子被跨膜泵出。 细胞色素c氧化酶的质子泵功能与电子传递性质密切偶联, 在大多数条件下质子泵控制整个反应的活性。 Iwata等[41]根据Paracoccus denitrificans晶体结构中存在2个极性空腔, 提出了D-通道和K-通道两种可能的质子传递途径, 其中D-通道是泵出质子的通道, K-通道是底物质子的通道。 后来的蛋白质残基的突变研究结果也支持这两种质子通道的存在[42]。 尽管Thermus thermophilus细胞色素c氧化酶的氨基酸残基序列和Paracoccus denitrificans的相差较远, 但从其晶体结构中却能辨别出K-通道和D-通道的存在, D-通道和K-通道可能是细菌所共有的质子传递途径。
2 逆电势梯度电子传递载体
电子逆向传递经过细胞色素bc1复合体和NADH-Q还原酶, 产生导致CO2固定和有氧代谢所需的还原力NAD(P)H[7] (见图1)。
Brasseur等 [43] 研究证明了在Fe2+基质中, A. ferrooxidans ATCC19859的细胞色素bc1复合体只在电子的逆向传递中起作用, 而在电子的顺电势梯度的下传中没有功能。 但在硫基质氧化系统中, 细胞色素bc1复合体在顺电势梯度的电子传递中起作用。 这与对A. ferrooxidans ATCC23270基因组序列分析所得到的结论相符合, 该结论表明在其基因组中存在两个独立的编码细胞色素bc1复合体的操纵子信息, 分别负责编码相关功能的细胞色素bc1复合体 [43, 44]。
Levican等[45]阐述了参与电子逆向传递的pet操纵子和与之相邻的res操纵子。 其中res操纵子由resB, resC和hyp2组成, resB和resC分别编码ResB和ResC蛋白, 它们可能在两个亚铁血红素细胞色素c4和细胞色素c1的成熟过程中起着分子伴侣的作用。 pet操纵子位于resB基因上游, 由cycA、 sdrA、 petA、 petB和petC组成, 其中cycA基因编码含两个铁血红素的c4型细胞色素蛋白CycA, sdrA基因编码核糖醇/葡萄糖脱氢酶家族中的一条短链, petA基因编码细胞色素b, petB基因编码Rieske蛋白-Fe-S还原酶, petC基因编码细胞色素c1。 在Fe2+氧化系统中, cyc1编码的细胞色素c552从Rus将电子传递给末端细胞色素aa3复合体; 在pet操纵子中, cycA编码的CycA可能也有相似的功能, 即在电子的逆电势梯度传递过程中, CycA从Rus将电子传递给细胞色素bc1复合体。
在Fe2+基质中生长的A. ferrooxidans, 由于必需有亚铁氧化的电子(大约是Fe2+氧化释放出电子的5%)用于产生NAD(P)H, 以满足其细胞固定CO2和参与有氧代谢所需要的还原力。 但由于电对Fe2+/Fe3+在pH 2.0时的电位为0.77V, 低于电对NAD+/NADH在pH 7.0时的电位-0.32V, 因此为了产生NAD(P)H, 便需要能量推动电子从Fe2+逆流到NAD+。 Ingledew等[46]推测逆流电子所需的能量主要来自膜内外之间的质子势。 Matin等[47] 观察到在pH值为3的环境中, A. acidophilus所需的绝大部分氧气吸收可被KCN或NaN3所抑制, 导致质子势下降, 但仍然存在35mV的质子势。 在低浓度KCN的存在下, Elbehti等[7]研究结果表明加入ATP能够加速电子经细胞色素bc1复合体和NADH-Q复合体的传递速度。 这里ATP的水解维持低质子势的存在, 同时提供能量加速电子的逆向传递。 Shoji 等[48]发现在A. novellas中ATP能够调节二聚体的细胞色素c氧化酶活性。 Elbehti等[7, 49] 认为A. ferrooxidans细胞内电子逆电势梯度和顺电势梯度的传递由ATP/ADP的比值调节, 当ATP/ADP的比值小时, Fe2+氧化生成的电子传递至细胞色素c氧化酶产生质子势, 来合成ATP, 生长的细胞不断利用ATP。 但是当ATP/ADP接近或超过某一阈值时, ATP调节细胞色素c氧化酶活性使其活性下降, ATP水解产生化学质子势, 这种能量用于电子逆电势梯度传递产生NAD(P)H。
3 rus操纵子转录调控模式
A. ferrooxidans能在极端酸性的有氧和无氧条件下生存和利用多种能量, 说明它有其独特的环境适应机制, 但目前关于A. ferrooxidans在无氧条件下的能量代谢以及电子传递过程中的氧化还原反应还没有明晰的轮廓, 大多数研究集中在Fe2+和S0基质中有氧代谢生长下的rus操纵子的表达及其调控。
如图2所示, rus操纵子在第一个顺反子cyc2上游存在两个启动子(PⅠ、 PⅡ), 而且在coxD和rus之间还有一个内部启动子(Prus)。 这些启动子和E. coli σ70所识别的启动子序列相类似。 在一个操纵子中存在三个启动子, 可能与细胞在不同选择压力下的环境适应性相关, 也意味着这些基因的表达调控机制较复杂。 由于有内部启动子的存在, rus基因的表达和其他基因的表达在某种环境下不同步[50]。
在蛋白质水平上, 在S0基质生长的 A. ferrooxidans在稳定期内没有Rus、 CoxB和Cyc1等蛋白的存在, 但是把稳定期的细菌接种到新的含S0基质培养液中, 在接种最初的8h用免疫印迹的方法没有检测到Rus的存在, 而在大约经过一天后, 细菌进入对数生长期, 测到了细菌细胞体内的Rus、 CoxB和Cyc1的清晰条带, 说明细胞重新合成了Rus等蛋白; 进入对数生长中后期后, 细胞体内Rus, CoxB和Cyc1含量不断减少, 直至消失。 但是, 在Fe2+基质生长的细胞中的Rus、 CoxB和Cyc1在对数生长期以及进入稳定期后都一直稳定地存在[51]。 Ramírez等[29]发现A. ferrooxidans ATCC19859在Fe2+、 S0和硫化物基质中生长时蛋白质的表达存在差异, 其中Rus在含硫化合物中表达下调而在Fe2+基质中表达上调。
在转录水平上, rus基因的转录量在细菌生长的对数前中期远远高于细菌生长的稳定期(在稳定期rus几乎没有转录); 相对于S0基质, Fe2+基质明显给出较高的细胞内rus、 cyc1和coxB的转录量。
Yarzábal等[51]通过比较分析在Fe2+、 S0基质生长的细胞中的rus操纵子的各个基因表达情况, 发现rus操纵子的表达不是组成性表达, 而是转录水平上可调节性的表达, 不同的能量基质启动不同的启动子。 他们利用引物延伸方法检测发现, 在Fe2+基质对数生长期的细胞内PI、 PII和Prus三个启动子同时起始转录, 但各自的强度不一样, PI相对较弱, Prus最强; 在S0基质中生长的细菌细胞只有PI和Prus在对数生长前期起始转录, 其中PI在对数生长前期起始转录量较Fe2+生长环境中的还强烈(见图3)。
从以上分析可知, 相对于S0基质, Fe2+基质能使其中生长的细胞的rus操纵子的基因表达量较高; 当从S0基质中转入到Fe2+中生长的细胞, rus操纵子中各个蛋白质快速表达, 当从Fe2+基质中转入到S0中生长的细胞, rus操纵子中各个蛋白质水平快速减少直至消失; 在(Fe2++S0)基质中生长的细胞, 在前段时间, rus操纵子中各个蛋白质快速表达达到最大值, 在Fe2+被完全氧化后, 其量又快速减少。 即Fe2+优先S0被A. ferrooxidans利用。 也就是说, rus操纵子的表达被Fe2+正调控, 但S0对rus操纵子没有抑制作用。 图3中的模型进一步说明了这种关系。
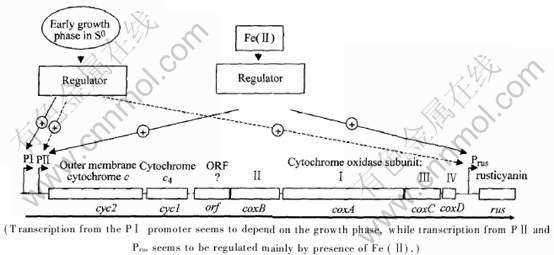
图3 rus操纵子转录调控模式
Fig.3 Model of transcriptional and post-transcriptional regulation of rus operon
A. ferrooxidans在(Fe2++S0)基质中生长, 环境的pH值是先稍微变大, 然后因为S0的氧化产生H2SO4而变小。 rus操纵子中的各个蛋白质的表达是和环境pH值的变化相联系吗? Amaro等[52]报道在 A. ferrooxidans中有一些依赖pH的蛋白质存在, 把稳定期细菌 (此时环境的pH值为1) 接种到新的含S0基质新鲜培养液中(pH为3.5), Rus重新合成; 在Fe2+、 (Fe2++S0)基质中都是pH值先变大, Rus等的合成量也加大。 似乎表明rus操纵子中的各个蛋白质表达的水平与pH值的上升呈相关性; 然而, 把A. ferrooxidans从pH 1.5转移到pH 3.5的环境中, SDS-PAGE显示除了有一个36kDa 的外膜蛋白增加外, 蛋白质条带谱没有其他明显变化。 Yarzábal等[51]推测rus操纵子在S0基质中的表达变化可能和环境中的营养成份的变化相关; 另外, S0对rus操纵子没有抑制作用, 但随着S0的氧化, 其氧化产物是否抑制rus操纵子中蛋白质的表达等, 还有待进一步的研究。
4 结论
目前对于A. ferrooxidans在分子遗传学和基因工程方面的深入研究正在进行之中, 对A. ferrooxidans ATCC33270基因组测序的工作已经完成。 随着研究的不断深入, 人们将通过研究A. ferrooxidans对环境的适应机制, 比较研究不同环境中A. ferrooxidans转录图谱和蛋白质图谱, 揭示出A. ferrooxidans的代谢调控机制; 通过建立A. ferrooxidans突变体库来研究A. ferrooxidans基因组中重要性状或功能基因, 阐明这些功能基因的表达与调控机制的相互关系。 有理由相信, 关于A. ferrooxidans的生理、 遗传及能量代谢机制方面的研究将使人们更好的了解A. ferrooxidans, 以便有目的地改造A. ferrooxidans, 培育出各种符合工业要求的优良的改良A. ferrooxidans菌株来为工业浸矿服务。
REFERENCES
[1]Brock T D, Gustafson J. Ferric iron reduction by sulfur-and iron-oxidizing bacteria[J]. Applied and Environmental Microbiology, 1976, 32: 567-571.
[2]Pronk J T, de Bruyn J C, Bos P, et al. Anaerobic growth of Thiobacillus ferrooxidans[J]. Applied and Environmental Microbiology, 1992, 58: 2227-2230.
[3]Pronk J T, Liem K, Bos P, et al. Energy transduction by anaerobic ferric iron respiration in Thiobacillus ferrooxidans[J]. Applied and Environmental Microbiology, 1991, 57: 2063-2068.
[4]Das A, Mishra A K, Roy P. Anaerobic growth on elemental sulfur using dissimilar iron reduction by autotrophic Thiobacillus ferrooxidans[J]. FEMS Microbiology Letters, 1992, 97: 167-172.
[5]Drobner E, Huber H, Stetter K O. Thiobacillus ferrooxidans, a facultative hydrogen oxidizer[J]. Applied and Environmental Microbiology, 1990, 56: 2922-2923.
[6]Ohmura N, Sasaki K, Matsumoto N, et al. Anaerobic Respiration Using Fe3+, S0, and H2 in the Chemolithoautotrophic Bacterium Acidithiobacillus ferrooxidans[J]. Journal of Bacteriology, 2002, 184: 2081-2087.
[7]Elbehti A, Brasseur G, Lemesle-Meunier D. First evidence for existence of an uphill electron transfer through the bc1 and NADH-Q oxidoreductase complexes of the acidophilic obligate chemolithotrophic ferrous ion-oxidizing bacterium Thiobacillus ferrooxidans[J]. Journal of Bacteriology, 2000, 182: 3602-3606.
[8]Rawlings D E. Characteristics and adaptability of iron- and sulfur-oxidizing microorganisms used for the recovery of metals from minerals and their concentrates[EB/OL]. http://www.microbialcellfactories.com/content/4/1/13.
[9]Appia-Ayme C, Guiliani N, Ratouchniak J, et al. Characterization of an operon encoding two c-type cytochromes, an aa3-type cytochrome oxidase, and rusticyanin in thiobacillus ferrooxidans ATCC 33020[J]. Applied and Environmental Microbiology, 1999, 65(11): 4781-4787.
[10]Yarzábal A, Brasseur G, Ratouchniak J, et al. The high-molecular-weight cytochrome c Cyc2 of Acidithiobacillus ferrooxidans is an outer membrane protein[J]. The Journal of Bacteriology, 2002, 184: 313-317.
[11]Ingledew W J, Cox J C, Halling P J. A proposed mechanism for energy conservation during Fe2+ oxidation by Thiobacillus ferrooxidans: chemiosmotic coupling to net H+ influx[J]. FEMS Microbiology Letters, 1977, 2: 193-197.
[12]Rawlings D E. The molecular genetics of thiobacillus ferrooxidans and other mesophilic, acidophilic, chemolithotrophic, iron- or sulfur-oxidizing bacteria[J]. Hydrometallurgy, 2001, 59: 2-3.
[13]Giudici-Orticoni M T, Guerlesquin F, Bruschi M, et al. Interaction-induced redox switch in the electron transfer complex rusticyanin-cytochrome c4[J]. Journal of Biological Chemistry, 1999, 274(43): 30365-30369.
[14]Blake R C, Shute E A. Respiratory enzymes of Thiobacillus ferrooxidans. kinetic properties of an acid-stable iron: rusticyanin oxidoreductase[J]. Biochemistry, 1994, 33: 9220-9228.
[15]Fry I V, Lazaroff N, Packer L. Sulfate-dependent iron oxidation by Thiobacillus ferrooxidans: characterization of a new EPR detectable electron transport component on the reducing side of rusticyanin[J]. Biochimica et Biophysica Acta, 1986, 246: 650-654.
[16]Beliaev A S, Saffarini D, McLaughlin J, et al. MtrC, an outer membrane decahaem c-cytochrome required for metal reduction in Shewanella putrefaciens MR-1[J]. Molecular microbiology, 2001, 39: 722-730.
[17]Myers C R, Myers J M. Role for outer membrane cytochromes OmcA and OmcB of Shewanella putrefaciens MR-1 in reduction of manganese dioxide[J]. Applied and Environmental Microbiology, 2001, 67: 260-269.
[18]Yamanaka T, Fukumori Y, Yano T, et al. Enzymatic mechanisms in the dehydrogenation of ferrous ions by Thiobacillus ferrooxidans[A]. Diversity of Environmental Biogeochemistry[C]. Amsterdam, Netherlands: Elsevier, 1991. 267-273.
[19]Kusano T, Takeshima T, Sugawara K, et al. Molecular cloning of the gene encoding Thiobacillus ferrooxidans Fe(Ⅱ) oxidase[J]. Journal of Biological Chemistry, 1992, 267: 11242-11247.
[20]Bruscella P, Cassagnaud L, Ratouchniak J, et al. The HiPIP from the acidophilic Acidithiobacillus ferrooxidans is correctly processed and translocated in Escherichia coli, in spite of the periplasm pH difference between these two micro-organisms[J]. Microbiology, 2005, 151(5): 1421-1431.
[21]Bonora P, Principi I, Monti B, et al. On the role of high-potential iron-sulfur proteins and cytochromes in the respiratory chain of two facultative phototrophs[J]. Biochimica et Biophysica Acta. 1999, 14(10): 51-60.
[22]Menin L, Gaillard J, Parot P, et al. Role of HiPIP as electron donor to the RC-bound cytochrome in photosynthetic purple bacteria[J]. Photosynthesis Research, 1998, 55: 343-348.
[23]Bengrine A, Guiliani N, Appia-Ayme C, et al. Sequence and expression of the rusticyanin structural gene from Thiobacillus ferrooxidans ATCC33020 strain[J]. Biochimica et Biophysica Acta, 1998, 1443: 99-112.
[24]Casimiro D R, Toy-Palmer A, Blake R C, et al. Gene synthesis, high-level expression, and mutagenesis of Thiobacillusferrooxidans rusticyanin: His85 is a ligand to the blue copper center[J]. Biochemistry, 1995, 34: 6640-6648.
[25]Nunzi F, Guerlesquin F, Shepard W, et al. Active site geometry in the high oxido-reduction potential rusticyanin from Thiobacillus ferrooxidans. 1994, 203: 1655-1662.
[26]Cox J C, Boxer D H. The purification and some properties of rusticyanin, a blue copper protein involved in iron (Ⅱ) oxidation from Thiobacillus ferrooxidans[J]. The Journal of Bacteriology, 1978, 174: 497-502.
[27]Yarzábal A, Duquesne K, Bonnefoy V. Rusticyanin gene expression of Acidithiobacillus ferrooxidans ATCC 33020 in sulfur- and in ferrous iron media[J]. Hydrometallurgy, 2003, 71: 107-114.
[28]Blake R C, Sasaki K. Ohmura N. Does aporusticyanin mediate the adhesion of Thiobacillus ferrooxidans to pyrite? [J]. Hydrometallurgy, 2001, 59: 357-372.
[29]Ramírez P, Guiliani N, Valenzuela L, et al. Differential protein expression during growth of acidithiobacillus ferrooxidans on ferrous iron, sulfur compounds, or metal sulfides[J]. Applied and Environmental Microbiology, 2004, 70(8): 4491-4498.
[30]Yarzábal A, Brasseur G, Bonnefoy V. Cytochromes c of Acidithiobacillus ferrooxidans[J]. FEMS Microbiology Letters, 2002, 209: 189-195.
[31]Brasseur G, Levican G, Bonnefoy V, et al. Apparent redundancy of electron transfer pathways via bc1 complexes and terminal oxidases in the extremophilic chemolithoautotrophic Acidithiobacillus ferrooxidans[J]. Biochimica et Biophysica Acta, 2004, 1656(2-3): 114-26.
[32]Cabrejos M E, Zhao H L, Guacucano M, et al. IST1 insertional inactivation of the resB gene: implications for phenotypic switching in Thiobacillus ferrooxidans[J] . FEMS Microbiology Letters, 1999, 175: 223-229.
[33]Appia-Ayme C, Bengrine A, Cavazza C, et al. Characterization and expression of the co-transcribed cyc1 and cyc2 genes encoding the cytochrome c4 (c552) and a high-molecular-mass cytochrome c from Thiobacillus ferrooxidans ATCC 33020[J]. FEMS Microbiology Letters, 1998, 167: 171-177.
[34]Elbehti A, Asso M, Guigliarelli B, et al . Characterization of the three membrane bound metallo enzymes required to postulate the existence of a bc-type complex in T. ferrooxidans[A]. Biomine, The Australian Mineral Foundation[C], 1997. PB2.1-PB2.9.
[35]Yamanaka T, Fukumori Y. Molecular aspects of the electron transfer system which participates in the oxidation of ferrous ion by Thiobacillus ferrooxidans[J]. FEMS Microbiology Review, 1995, 17: 401-413.
[36]Mansch R, Sand W. Acid-stable cytochromes in ferrous ion oxidizing cell-free preparations from Thiobacillus ferrooxidans[J]. FEMS Microbiology Letters, 1992, 92: 83-88.
[37]Harrenga A, Michel H. The cytochrome c oxidase from Paracoccus denitrificans does not change the metal center ligation upon reduction[J]. Journal of Biological Chemistry, 1999, 274: 33296-33299.
[38]Kai M, Yano T, Fukumori Y, et al. Cytochrome oxidase of an acidophilic iron-oxidizing bacterium, Thiobacillus ferrooxidans, functions at pH 3.5[J]. Biochemical and Biophysical Research Communications, 1989, 2: 839-843.
[39]Kai M, Yano T, Tamegai H, et al. Thiobacillus ferrooxidans cytochrome c oxidase: purification, and molecular and enzymatic features[J]. Journal of Biological Chemistry, 1992, 112: 816-821.
[40]Antalis T M, Palmer G. Kinetic characterization of the interaction between cytochrome oxidase and cytochrome c[J] . Journal of Biological Chemistry, 1982, 257: 6194-6206.
[41]Iwata S, Ostermeier C, Ludwig B, et al. Structure at 2.8 resolution of cytochrome c oxidase from Paracoccus denitrificans[J]. Nature, 1995, 376: 660-669.
[42]Konstantinov A A, Siletsky S, Mitchell D, et al. The roles of the two proton input channels in cytochrome c oxidase from Rhodobacter sphaeroides probed by the effects of site-directed mutations on time-resolved electrogenic intraprotein proton transfer[J]. Proceedings of the National Academy of Sciences, 1997, 94: 9085-9090.
[43]Brasseur G, Bruscella P, Bonnefoy V, et al. The bc1 complex of the iron-grown acidophilic chemolithotrophic bacterium Acidithiobacillus ferrooxidans functions in the reverse but not in the forward direction. Is there a second bc1 complex?[J]. Biochimica et Biophysica Acta, 2002, 1555: 37-43.
[44]Brassuer G, Levican G, Bonnefoy V, et al. Apparent redundancy of electron transfer pathways via bc1complexes and terminal oxidases in the extremely acidophilic chemoautotrophic Acidithiobacillus ferrooxidans[J]. Biochimica et Biophysica Acta, 2004, 1656: 114-126.
[45]Levican G, Bruscella P, Guacucano M, et al. Characterization of the petI and res operons of Acidithiobacillus ferrooxidans[J]. The Journal of Bacteriology, 2002, 184: 1498-1501.
[46]Ingledew W J. T. ferrooxidans, the bioenergetics of an acidophilic chemolithotrophic bacteria[J]. Biochimica et Biophysica Acta, 1982, 683: 89-117.
[47]Matin A, Wilson B, Zychlinsky E, et al. Proton motive force and the physiological basis of delta pH maintenance in Thiobacillus acidophilus[J]. The Journal of Bacteriology, 1982, 150: 582-591.
[48]Shoji K, Tanigawa M, Hori K, et al. The effects of several nucleotides on the molecular state and catalytic activity of Thiobacillus novellus cytochrome c oxidase ATP affects the oxidase uniquely[J]. The Journal of Bacteriology, 1999, 264: 960-964.
[49]Elbehti A, Nitschke W, Tron P, et al. Redox components of cytochrome bc-type enzymes in acidophilic prokaryotes (Ⅰ): characterization of the cytochrome bc1-type complex of the acidophilic ferrous ion-oxidizing bacterium Thiobacillus ferrooxidans[J]. The Journal of Biological Chemistry, 1999, 274(24): 16760-16765.
[50]Yarzábal A, Duquesne K, Bonnefoy V. Rusticyanin gene expression of Acidithiobacillus ferrooxidans ATCC33020 strain in sulfur- and in ferrous iron-media[J]. Hydrometallurgy, 2003, 71: 107-114.
[51]Yarzábal A, Appia-Ayme C, Ratouchniak J, et al. Regulation of the expression of the Acidithiobacillus ferrooxidans rus operon encoding two cytochromes c, a cytochrome oxidase and rusticyanin[J]. Microbiology, 2004, 150: 2113-2123.
[52]Amaro A M, Chamorro D, Seeger M, et al. Effect of external pH perturbations on in vivo protein synthesis by the acidophilic bacterium Thiobacillus ferrooxidans[J]. The Journal of Bacteriology, 1991, 173: 910-915.
(编辑何学锋)
基金项目: 国家重点基础研究发展计划资助项目(2004CB619201)
收稿日期: 2006-01-20; 修订日期: 2006-05-29
通讯作者: 夏金兰, 教授, 博士; 电话: 0731-8836944; E-mail: jlxia@mail.csu.edu.cn

