Leucobacter对Cr(Ⅵ)的还原及其还原产物的成分分析
朱文杰,龙怀中,杨志辉,柴立元
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
摘 要:考察Leucobacter spp. Ch1的细胞在生长状态和休眠状态对六价铬的还原;运用SEM和TEM对还原前后Leucobacter的形态进行观察,并利用EDAX和EPR分析还原产物的成分。研究结果表明:在好氧条件下,生长的细菌还原250 mg/L Cr(Ⅵ) 需5 h,细胞悬液需45 min;在厌氧条件下,休眠细胞还原能力较强,而接种于培养基的细菌无还原能力;还原反应的产物主要附着在细菌的末端,表明反应发生于细胞表面;反应产物中Cr的含量为28.2%,表明三价铬以Cr(OH)3沉淀的形式存在。
关键词:Leucobacter;六价铬;还原;产物
中图分类号:X172 文献标识码:A 文章编号:1672-7207(2008)03-0443-05
Bio-reduction of Cr(Ⅵ) by Leucobacter and element analysis of
reduction products
ZHU Wen-jie, LONG Huai-zhong, YANG Zhi-hui, CHAI Li-yuan
(School of Metallurgical Scinence and Engineering, Central South University, Changsha 410083, China)
Abstract: Chromate reduction ability of Leucobacter spp. Ch1 was studied with its growing cells and resting cells. SEM and TEM were used to observe the shape of bacterial cell before and after Cr(Ⅵ) reduction. EDAX and EPR were employed to determine the composition of the reduction products. The results show that it takes 5 h to reduce 250 mg/L Cr(Ⅵ) with growing cells and 45 min with resting cells under aerobic conditions. Effective reduction ability is also found in resting cells rather than in growing cells under anaerobic conditions. Reaction product adheres to the terminal of bacterial cells, which indicates that chromate reduction takes place on the surface of Ch1 cells. Reduction product contains 28.2% of Cr and it is determined as trivalent chromium in the form of Cr(OH)3 precipitate.
Key words: Leucobacter; hexavalent chromium; reduction; product
铬盐是一种用途广泛的工业原料,同时又是一种危险的重金属污染物,在自然条件下最为稳定的形态是三价铬和六价铬。其中六价铬的氧化性很强,对生物具有毒性、诱变性以及致癌作用[1];三价铬则毒性小,并且在pH值高于5时以Cr(OH)3沉淀的形式存在[2]。因此,目前治理六价铬污染的方法主要是将Cr(Ⅵ) 还原为无毒的Cr(Ⅲ)。
生活在受铬污染环境中的微生物往往具有还原六价铬的能力。1977年,第1株具有铬还原能力的假单胞菌被发现[3],此后研究者们从自然界中分离出数十种铬还原功能菌,如Arthrobacter[4],Bacillus[5],Enterobacter[6]和Escherichia[7]等。铬还原菌可以在生长过程中还原六价铬,但在研究过程中,经常利用休眠状态的细菌细胞还原六价铬,以实现将生长代谢等生理活动与细菌的还原功能分开,消除其对还原作用的影响[8-9]。作为一种防御机制,细菌还原六价铬的行为具有治理和修复铬污染的潜力。但是,目前所报道的铬还原菌的还原能力普遍较低,阻碍了生物还原法在实际应用中的发展[10-11]。
Leucobacter spp. Ch1是一种新的高效六价铬还原菌,分离自高盐、高碱、高铬的铬渣堆放场。在此,本文作者研究该菌在生长过程中以及休眠状态下对Cr(Ⅵ) 的还原,观察还原前后该菌的形态变化,并利用X射线能谱(EDAX)和电子顺磁共振(EPR)分析确定还原产物的成分。
1 实验方法
1.1 菌种鉴定及培养条件
研究用菌种为从长沙铬盐厂铬渣污染土壤中分离的六价铬还原功能菌,鉴定为白色杆菌属(Leucobacter)的一种,命名为Ch1。该菌16S rDNA序列已经提交到Genbank,序列登录号为EF 362778。将细菌的DNA序列与GenBank数据库中已有的16SrDNA序列进行相似性比较分析。用ClustalX进行序列比对后采用Mega3.1软件进行系统发育分析。
Leucobacter生长于LB培养基中,其中:蛋白胨10 g;NaCl 10 g;酵母浸膏5 g;葡萄糖4 g;H2O 1 L,调节pH值至9.0。
1.2 六价铬的生物还原
1.2.1 生长细菌还原Cr(Ⅵ)
向LB培养基中加入K2Cr2O4溶液使其中Cr(Ⅵ)的质量浓度为250 mg/L,接种对数期Ch1菌培养物至细菌初始浓度2.4×108 个/mL。用1 mol/L的NaOH调节培养液的pH值至9.0,置于30 ℃恒温摇床中培养,考察其中六价铬浓度的变化。
1.2.2 休眠细胞还原Cr(Ⅵ)
取对数期末期Ch1菌培养物,在4 ℃时以6 000 r/min转速离心30 min。弃上清液,沉淀用pH值为9.0的Tris-HCl缓冲液重悬制成细菌细胞悬液。细胞浓度为2.4×109 个/mL,Cr(Ⅵ) 初始浓度为250 mg/L。于30 ℃恒温培养箱中进行好氧反应,考察其中六价铬浓度的变化[12]。
1.3 分析检测方法
采用二苯碳酰二肼分光光度法[13]测定溶液中Cr(Ⅵ)浓度。
还原前后细菌形貌用扫描电镜(SEM,JEOL JSM-6360LV)和透射电镜(TEM,JEM-1230)分别进行观察并拍照。
反应中生成蓝灰色沉淀,在真空抽滤装置中用去离子水冲洗4遍,除去沉淀中可溶性物质,于120 ℃烘干8 h,用X射线能谱仪(EDAX,Finder 1000)分析其元素组成。
取少量上述烘干的沉淀样品置于电子顺磁共振仪(Bruker 200D-SRC EPR spectrometer)的谐振腔内于室温下进行分析。微波频率为9.53 GHz,功率为5 mW,时间间隔为200 ms,中心磁感应强度为0.41 T,扫宽为0.80 T。
2 结果与讨论
2.1 Ch1菌系统发育分析
通过与Genbank中的数据进行比对,发现Ch1菌和白色杆菌属(Leucobacter spp.)有很高的同源性。其中,与菌株 Leucobacter aridicollis str. L9的序列同源性最高,达到97.39%,另有其他5个种的同源性均大于 97%。因此,可以确定,菌株CRB 1是 Leucobacter菌属的1种。根据细菌16S rRNA序列以及同源性分析,绘制系统发育进化树,如图1所示,其中数字表示菌株同源性概率。目前,报道的无色杆菌属的9个种,在发育地位上分为2个亚组,而Leucobacter sp. CRB 1 位于Leucobacter 菌属的分枝之上,但又与其他菌种有一定进化距离,因此,推测该菌是白色杆菌属的一个新种。

图1 基于Ch1菌16S rRNA序列的系统发育树
Fig.1 Phylogenetic tree based on 16S rDNA sequences of strain Ch1
2.2 细菌Leucobacter spp. Ch1还原Cr(Ⅵ)
分别在好氧和厌氧条件下用Ch1菌还原Cr(Ⅵ)。按10%接种量接种到含铬的LB培养基中,结果如图2所示。在好氧条件下,生长的Leucobacter 5 h内还原250 mg/L Cr(Ⅵ),而厌氧条件下Cr(Ⅵ)的浓度没有明显减少,还原反应不能进行。在pH值为9.0的休眠细胞悬液中,还原反应在厌氧、好氧条件下均可进行,好氧条件下的反应速率比厌氧条件下的反应速率高,还原250 mg/L Cr(Ⅵ)仅需45 min。这说明Ch1菌铬还原酶还原作用的进行并不需要氧气,J. McLean等[14]分离的Pseudomonad (CRB 5)既可以在无氧条件下也可以在有氧条件下还原低浓度Cr(Ⅵ)。
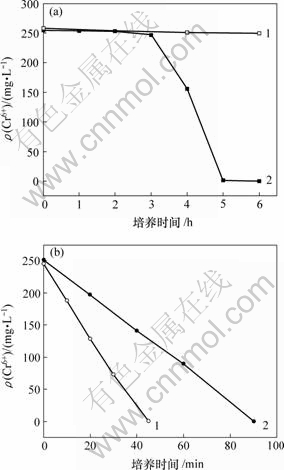
(a) 生长细胞;(b) 休眠细胞
1—好氧条件下;2—厌氧条件下
图 2 生长细菌及休眠细胞对Cr(Ⅵ)还原的影响
Fig.2 Influence of growing cells and resting cells on Cr(Ⅵ) reduction
2.3 细菌的生长
接种2% Ch1菌液到LB培养基,考察Leucobacter在好氧以及厌氧条件下的生长情况,其生长曲线如图3所示。其中:D600是波长为600 nm时的光密度。

1—好氧条件下;2—厌氧条件下
图3 Ch1菌的生长曲线
Fig.3 Growth curves of bacterial strain Ch1
由图3可知,Ch1菌是好氧细菌,在通气条件下细菌生长旺盛,对数期为20 h;而厌氧条件下细菌生长非常缓慢。氧气缺乏抑制了细菌的生长,导致细菌浓度过低,进而影响了Ch1菌的铬还原功能。
2.4 Leucobacter还原Cr(Ⅵ)前后的形貌观察
Leucobacter还原Cr(Ⅵ)前后的形貌进行扫描电镜(SEM)观察,细菌长度为1~3 ?m,直径为0.3~0.5 ?m。未经过还原反应的细菌表面粗糙,呈细颗粒状,其表面鞭毛隐约可见(图4(a))。还原反应后的细菌形态和无铬培养的细菌细胞有很大区别,如图4(b)所示。细菌的末端黏附大团无定形物质,该物质在无铬培养的细胞上是不存在的,初步推测该物质为六价铬还原产物的沉淀物。
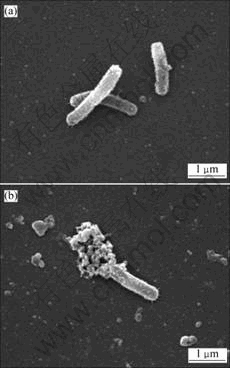
(a) 反应前;(b) 反应后
图4 还原反应前、后Ch1菌扫描电镜像
Fig.4 SEM images of strain Ch1 before and after chromate reduction
在放大倍数为20 000的透射电镜下发现,反应前细菌表面无附着物,内部有空腔或者囊泡结构,推测菌体内黑点为细菌的遗传物质(图5(a))。还原后细胞的切片截面如图5(b)所示,可以看到在细胞表明围绕着一圈深色物质,该物质相对分子质量较大,因此,可以判断该物质和扫描电镜照片中细胞末端无定形物质一样,为还原反应的产物。

(a) 反应前;(b) 反应后
图5 还原反应前后Ch1菌TEM 像
Fig.5 TEM images of strain Ch1 before and after chromate reduction
T. L. Daulton等在研究中也观察到类似的现象[15]。电镜结果表明,还原生成的产物存在于细胞体外,说明细菌的六价铬还原酶位于细胞膜之上。推测在还原过程中,细胞膜上的铬还原酶将所接触到的Cr(Ⅵ)催化还原为Cr(Ⅲ),并在碱性条件下生成Cr(OH)3沉淀。Ch1菌的菌体周生鞭毛,并具有很强的活动能力,在细菌向前游动过程中,鞭毛不停地向后摆动,随即将细胞表面生成的三价铬沉淀推动到细菌的末端,最后累积成大团的无定形物质。
2.5 反应产物的能谱分析
在Ch1菌还原六价铬的过程中,反应体系的颜色由初始的黄绿色变为蓝灰色,并生成大量沉淀产物。用X射线能谱(EDAX)对反应产物进行元素分析,结果如图6所示。可见,产物中含量最多的是O,占沉淀总质量的35.7%;其次是Cr,占28.2%;C占24.5%,其中,C和O是细菌的菌体成分,因此,还原产物应为含铬化合物。
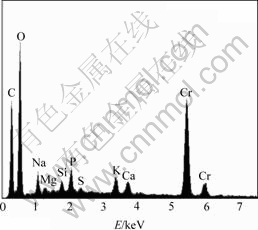
图6 还原产物的X射线能谱
Fig.6 EDAX spectrum of reduction product
2.6 还原产物的电子顺磁共振分析
由于通过EDAX分析不能判断元素的价态,故对还原产物进行电子顺磁共振(EPR)检测,同时,以分析纯的CrCl3 和 K2Cr2O7粉末为标准样作为对照。在EPR谱图中(如图7所示),由于六价铬离子是逆磁性物质,故未显示任何信号;CrCl3的标样则显示了强大的信号;还原产物的信号也比较强烈,其中心位置和谱线形状与CrCl3标样的结果非常吻合,据此断定还原产生的沉淀物质的主要成分就是三价铬。三价铬在pH>5的环境中以氢氧化物的形式存在[2],因此,确定Leucobacter spp. Ch1菌将溶液中的Cr(Ⅵ)还原为Cr(Ⅲ),并生成了Cr(OH)3沉淀。

1—CrCl3标样;2—反应产物;3—K2Cr2O7标样
图7 还原产物电子顺磁共振谱
Fig.7 EPR spectra of reduction product
3 结 论
a. Leucobacter spp. Ch1是一种高效六价铬还原菌:在好氧条件下,生长的细菌还原250 mg/L Cr(Ⅵ)需5 h,而细胞悬液还原250 mg/L Cr(Ⅵ)仅需45 min。该菌的生长需要氧气,在厌氧条件下细菌生长受到抑制,影响其还原性能。
b. 还原反应后有大团产物附着于细菌末端及表面,表明反应发生在Leucobacter细胞的表面。
c. 还原反应的产物中含有大量铬,其价态为三价,反应产物为以沉淀形式存在的Cr(OH)3。
参考文献:
[1] Petrilli F L, Flora S D. Toxicity and mutagenicity of hexavalent chromium on Salmonella typhimurium[J]. Applied and Environmental Microbiology, 1977, 33(4): 805-809.
[2] Rai D, Sass B M, Moore D A. Lung cancer among workers in chromium chemical production[J]. Inorganic Chemistry, 1987, 26: 345-349.
[3] Romanenko V I, Korenkov V N. A pure culture of bacteria utilizing chromates and bichromates as hydrogen acceptors in growth under anaerobic conditions[J]. Microbiologica, 1977, 46: 414-417.
[4] Asatiani N V, Abuladze M K, Kartvelishvili T M, et al. Effect of Chromium(Ⅵ) Action on Arthrobacter oxydans[J]. Current Microbiology, 2004, 49(5): 321-326.
[5] LIU Yun-guo, XU Wei-hua, ZENG Guang-ming, et al. Cr(Ⅵ) reduction by Bacillus sp. isolated from chromium landfill[J]. Process Biochemistry, 2006, 41(9): 1981-1986.
[6] Wang P C, Tsukasa M, Kohya K, et al. Isolation and characterization of an Enterobacter cloacae strain that reduces hexavalent chromium under anaerobic conditions[J]. Applied and Environmental Microbiology, 1989, 55: 1665-1669.
[7] Wang Y T, Shen H. Modeling Cr(Ⅵ) reduction by pure bacterial cultures[J]. Water Research, 1997, 31: 727-732.
[8] Thacker U, Patrikh R, Shouche Y, et al. Reduction of chromate by cell-free extract of Brucella sp. isolated from Cr(Ⅵ) contaminated sites [J]. Bioresource Technology, 2007, 98(8): 1541-1547.
[9] Viamajala S, Smith W A, San R K, et al. Isolation and characterization of Cr(Ⅵ) reducing Cellulomonas spp. from subsurface soils: Implications for long-term chromate reduction[J]. Bioresource Technology, 2007, 98(3): 612-622.
[10] Jeyasingh J, Philip L. Bioremediation of chromium contaminated soil: optimization of operating parameters under laboratory conditions[J]. Journal of Hazardous Materials, 2005, 118(1/3): 113-120.
[11] Ganguli A, Tripathi A K. Bioremediation of toxic chromium from electroplating effluent by chromate-reducing Pseudomonas aeruginosa A2Chr in two bioreactors[J]. Applied Microbiology and Biotechnology, 2002, 58(3): 416-420.
[12] Mabbett A N, Macaskie L E. A novel isolate of Desulfovibrio sp. with enhanced ability to reduce Cr(Ⅵ)[J]. Biotechnology Letters, 2001, 23(9): 683-687.
[13] 魏复盛. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社, 2002: 346.
WEI Fu-sheng. Monitoring analysis methods of water and waste water[M]. 4th ed. Beijing: Press of Environment Science of China, 2002: 346.
[14] McLean J, Beveridge T J. Chromate reduction by a Pseudomonad isolated from a site contaminated with chromated copper arsenate[J]. Applied and Environmental Microbiology, 2001, 67(3): 1076-1084.
[15] Daulton T L, Little B J, Jones-Meehan, et al. Microbial reduction of chromium from the hexavalent to divalent state[J]. Geochimica et Cosmochimica Acta, 2007, 71(3): 556-565.
收稿日期:2007-08-26;修回日期:2007-10-07
基金项目:国家自然科学基金资助项目(20477059);国家高技术研究发展计划(863)项目(2006AA06Z374)
通信作者:柴立元(1966-),男,江西万年人,教授,从事重金属废水、废渣处理与资源化、矿冶环境生物技术的研究;电话:0731-8836921;E-mail: lychai@mail.csu.edu.cn