DOI:10.19476/j.ysxb.1004.0609.2019.12.20
Cu2+胁迫对Acidithiobacillus ferrooxidans亚铁氧化代谢及胞外电子传递影响
仉丽娟1,吴 平1,王志杰1,周文博2,周洪波2
(1. 南京工业大学 生物与制药工程学院,南京 211816;
2. 中南大学 资源加工与生物工程学院生物冶金教育部重点实验室,长沙 410083)
摘 要:为了查明Cu2+胁迫影响Acidithiobacillus ferrooxidans(At. ferrooxidans)亚铁氧化代谢机制,本研究设计了由低到高Cu2+浓度(0~25 g/L)胁迫环境,利用邻菲啰啉分光光度法、实时荧光定量PCR和循环伏安法等分析手段分别探究了不同Cu2+浓度胁迫下At. ferrooxidans亚铁氧化率、亚铁氧化电子传递链rus operon相关基因表达及胞外电子传递的响应情况。结果表明:Cu2+胁迫浓度由0 g/L增加至25 g/L时,At. ferrooxidans菌亚铁氧化活性显著降低(25 g/L Cu2+,对应下24 h亚铁氧化抑制率约为50%),rus operon相关基因表达显著下调(尤其是细胞内膜蛋白编码基因Cyc1和细胞色素c氧化酶编码基因CoxBACD分别下调12.4倍和4~6倍),Fe2+氧化胞外传递电子能力也降低(循环伏安曲线还原峰值29.0 μA(对照组,0 g/L Cu2+)和26.5 μA(25 g/L Cu2+))。综上所述,高浓度Cu2+胁迫引起At. ferrooxidans菌亚铁氧化代谢Rus operon相关基因表达显著下调,造成胞外电子传递速率降低,最终导致At. ferrooxidans菌亚铁氧化率降低。
关键词:Acidithiobacillus ferrooxidans;重金属胁迫;亚铁氧化代谢;胞外电子传递
文章编号:1004-0609(2019)-12-2868-09 中图分类号:Q939.97 文献标志码:A
Acidithiobacillus ferrooxidans(At. ferrooxidans),极端嗜酸化能自养菌,是目前生物浸出相关报道中研究较多的极端嗜酸微生物菌种之一,其参与的生物浸出过程主要通过氧化亚铁或还原态硫生成氧化剂Fe3+或浸出剂H2SO4实现贫矿/尾矿、电镀污泥、电子电器废弃物、城市污泥等中重金属无害化、资源化[1-7]。随着生物浸出进行,大量溶出的重金属对At. ferrooxidans生长及代谢产生一定影响,尤其是高浓度重金属环境甚至导致微生物代谢停滞或死亡[8-10]。At. ferrooxidans等嗜酸微生物通常对不同重金属离子呈现出一定抗性,从而有利于其在极端环境中生长和浸出效率维持。已有研究结果表明,At. ferrooxidans菌株对Cu2+最大耐受浓度(Maximum tolerated concentrations)在0.6~19 g/L之 间[8-9];At. ferrooxidans耐受Cu2+毒性主要通过表达大量铜抗性相关基因,如CopA1Af、CopA2Af和CopBA等CopA efflux ATPases, Cus efflux systems、CusCBA1AfRND system和CusF1Af,CusF2Af和CopCAf等CusFcopper chaperones等,平衡细胞内Cu2+浓度[11-12]。
Fe3+是生物浸出过程中主要的氧化剂,其存在促进了硫化物等难溶态中重金属的释放[13]。Fe3+主要通过At. ferrooxidans生物氧化循环再生,进而保证生物浸出过程持续高效进行[14]。但伴随浸出体系中重金属不断溶出,At. ferrooxidans亚铁氧化代谢能力受到抑制,且溶出重金属浓度越高,抑制作用越显著[8, 10]。CRISTOBAL等[11]对At. ferrooxidans ATCC 53993进行长期连续耐受Cu2+驯化,提高了该菌株抗Cu2+毒性能力;发现于40 mmol/L Cu2+胁迫条件下,驯化后的菌株中与亚铁氧化代谢相关的rus operon上不同蛋白表达上调。此外,驯化后的At. ferrooxidans生物浸提重金属效率提高[15]。
综上可见,At. ferrooxidans通过表达不同铜抗性相关基因抵抗极端胁迫环境,但重金属耐受性在同种At. ferrooxidans不同菌株之间存在差异,且微生物耐受重金属能力显著影响生物亚铁氧化效率,进而影响浸出过程。因此,在利用At. ferrooxidans生物浸出黄铜矿、废覆铜板渣等含铜固废之前,获得高耐受Cu2+毒性菌株,并开展处理对象或浸出液中Cu2+胁迫对该功能菌株亚铁氧化代谢影响研究,将为之后浸出试验研究和后续工程推广应用提供更多理论支持和指导,具有重要理论和实际意义。目前已有研究报到主要关注较低重金属胁迫浓度(<100 mmol/L Cu2+)对At. ferrooxidans亚铁氧化速率影响[7-9],但是At. ferrooxidans在生物浸出过中通常面临更高浓度的Cu2+胁迫环境(>100 mmol/L Cu2+),而且在高浓度重金属胁迫下At. ferrooxidans亚铁氧化特性存在何种变化还不清楚。此外,有关高浓度重金属胁迫(Cu2+)对At. ferrooxidans亚铁氧化代谢传递途径相关基因rus operon表达和胞外电子传递情况影响也鲜有报道。
因此,本研究首先通过分离、驯化获得高耐受重金属毒性的At. ferrooxidans,并针对该株At. ferrooxidans菌开展了由低到高Cu2+浓度胁迫下(0~25 g/L)该微生物亚铁氧化代谢率和胞外电子传递(循环伏安法)响应研究,同时结合实时荧光定量PCR技术探究高浓度Cu2+胁迫对At. ferrooxidans菌亚铁氧化代谢电子传递途径(Rus operon)相关基因表达的影响,最终旨在探明Cu2+胁迫对At. ferrooxidans亚铁氧化代谢性能的影响机制。
1 实验
1.1 菌种及培养条件
本实验所用菌种At. ferrooxidans由本实验室自电镀工业园处理废水池中分离,并保存。At. ferrooxidans纯菌釆用改进的基本盐培养基((NH4)2SO4, 3.0 g/L;KCl, 0.1 g/L; K2HPO4,0.5 g/L; MgSO4·7H2O, 0.5 g/L;Ca(NO3)2,0.01 g/L)中添加44.7 g/L FeSO4·7H2O作为能源,逐步添加1%~10%综合电镀污泥,于初始pH 1.8±0.05、(30±2) ℃、180 r/min条件下逐步连续驯化培养,最终驯化获得耐受多种重金属能力的高活性菌株。获得的At. ferrooxidans菌种连续活化培养以保持其高活性,并用于后续研究。
1.2 不同Cu2+胁迫浓度对At. ferrooxidans亚铁氧化活性影响
按10%(V/V)接种量将处于对数生长期的At. ferrooxidans接入新鲜无菌0K基本盐培养基中(最终菌浓约为2×107 cells/mL),加入4.5 g/L Fe2+作为能源,用浓硫酸调节初始pH至1.8±0.05,于(30±2) ℃、180 r/min摇床中培养至亚铁氧化殆尽。然后在摇瓶中加入不同浓度的Cu2+重金属进行胁迫实验,同时加入4.5 g/L Fe2+作为能源,培养过程中外加50%(体积分数)硫酸控制体系pH不超过2.0±0.05。其中Cu2+胁迫浓度分别选取3、5、7、10、15、20、25 g/L,以不添加Cu2+胁迫的实验组作为对照组。每隔2 h取样,监测不同胁迫浓度条件下总铁、亚铁、体系氧化还原电位(Oxidation-reduction potential,ORP)等相关理化参数随时间的变化。每个实验组进行3个平行实验,结果为平均值±标准误差(SD)。
亚铁氧化抑制率(Inhibition efficiencyh),即在固定培养时间内(24 h),相比于对照实验组(Control without Cu2+),胁迫实验组亚铁氧化抑制率

 。其中,C为对照组亚铁氧化量;A为胁迫实验组亚铁氧化量。
。其中,C为对照组亚铁氧化量;A为胁迫实验组亚铁氧化量。
1.3 Cu2+胁迫下At. ferrooxidans亚铁氧化电子传递链Rus operon相关基因表达情况
收集不同Cu2+浓度(0、7.0和25.0 g/L)胁迫下培养4、9和24 h的菌体:先用过滤除去黄钾铁矾等沉淀,将滤液低温4 ℃下12000 r/min离心15 min,将收集的菌体用pH 2.0的灭菌基本营养盐中清洗2~3次,最终将获得的菌体即刻开展RNA提取实验。
细菌总RNA提取按照Omega公司提供的Bacterial RNA Kit操作手册进行。提取的RNA分别通过1%琼脂糖凝胶电泳和Nanodrop ND-1000 Spectrophotometer检测仪检测RNA完整性、纯度及浓度。将完整、无杂质污染的RNA按照TOYOBO公司提供的ReverTra Ace qPCR RT Master Mix with gDNA Remover(Code No.FSQ-301)试剂盒说明进行RNA反转录合成cDNA。
ND-1000 Spectrophotometer检测仪检测RNA完整性、纯度及浓度。将完整、无杂质污染的RNA按照TOYOBO公司提供的ReverTra Ace qPCR RT Master Mix with gDNA Remover(Code No.FSQ-301)试剂盒说明进行RNA反转录合成cDNA。
常规PCR反应在T-Gradient Thermoblock PCR仪(Biometra,Gottingen,Gemnany)中进行。Quantitative PCR反应所用仪器为iCycleriQ Real-time PCR detection system (Bio-Rad Laboratories, Inc., Hercules, USA)。rus operon相关基因(Cyc2、Cyc1、CoxB、CoxA、CoxC、CoxD、Rus、Orf)特异性引物参照CARLOS等的报道[16],同时以alaS作为内参基因[17]。具体Quantitative PCR操作步骤按照Carlos等[16]报道方法。所有实验采用3组平行对照,以不加cDNA模板作为空白对照。具体目的基因差异表达分析方法参照2-△△ct法[18],计算公式为:1) 靶基因改变倍数(fold change)= 2-△△Ct;2) △△Ct=(Ct1-Ct2)experiment-(Ct1-Ct2)control。其中,Ct1为目的基因达到阈值时扩增循环数;Ct2为内参基因达到阈值时扩增循环数。
1.4 Cu2+浓度胁迫下At. ferrooxidans亚铁氧化胞外电子传递研究
按10%的接种量将处于对数生长期的At. ferrooxidans接入新鲜无菌基本盐培养基中(菌浓约为2×107 cells/mL),加入4.5 g/L Fe2+作为能源,用浓硫酸调节培养基初始pH至1.8±0.05,于(30±2) ℃、180 r/min摇床中培养至亚铁氧化殆尽。此时添加亚铁氧化抑制率约为50%的Cu2+浓度(25.0 g/L)进行胁迫并培养24 h,将培养菌液真空抽滤除去铁矾等沉淀物,过滤菌液12000 r/min,15 min收集菌体,用pH 2.0的灭菌0K培养基清洗2~3次至获得沉淀菌体为无色,最终溶于0K培养基中,将获得的高浓度菌液进行后续电化学实验。
取定量的菌液滴加至2.5 cm×1 cm×0.2 cm的ITO导电玻璃表面,均匀涂抹开形成1 cm×1 cm的菌斑,室温下晾干,然后添加等体积的Nafion溶液覆盖至菌斑表面,室温下晾干,制成“微生物电极”后进行循环伏安测试。测试选用可换膜H型电解槽(CH2010-S,天津艾达)作为循环伏安测试反应槽,单池容量为250 mL,膜选用质子交换膜Nafion 117(杜邦,全氟磺酸离子膜N117);电化学体系为120 mL,电解液为pH 2.0的基本盐培养基,对电极为Pt电极(1.0 cm×1.0 cm),参比电极为Ag/AgCl,扫描范围为-0.5~0.8 V,扫描速度为20 mV/S。将体系的3个电极接入电化学测试系统,其中工作电极和参比电极放置在同一侧电解槽中并尽量靠近但不直接接触,通过电化学综合测试系统(PARSTAT4000,美国普林斯顿)向工作电极施加恒定变化的电压,实时监测电流响应和时间关系。实验中,分别以无粘附At. ferrooxidans菌体的ITO导电玻璃和不添加Cu2+胁迫的作为实验对照组进行循环伏安测试。
1.5 分析方法
培养体系氧化还原电位(ORP,Oxidation-reduction potential)选用Pt (vs Ag/AgCl)电极测定。pH采用pH复合电极来测定。微生物数量通过血球计数板直接计数。溶液中总Fe和Fe2+浓度通过邻菲啰啉分光光度法测定(HJ/T 345-2007)。
2 结果与讨论
2.1 Cu2+胁迫对At. ferrooxidans亚铁氧化活性影响
通过改变培养基中Cu2+浓度,研究Cu2+胁迫对At. ferrooxidans菌亚铁氧化活性的影响,结果如图1所示。
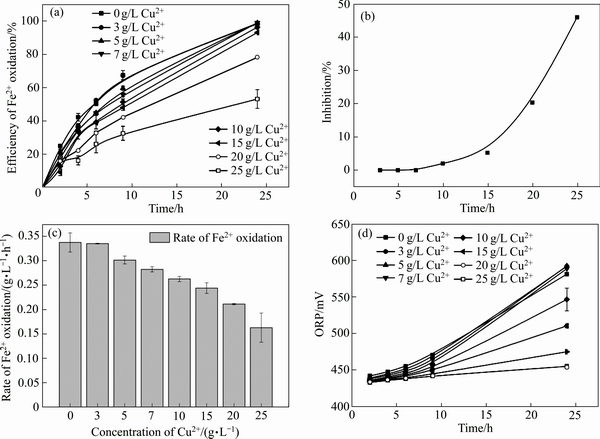
图1 Cu2+胁迫对At. ferrooxidans菌亚铁氧化率、24 h亚铁氧化抑制率、对数期亚铁氧化速率和体系氧化还原电位的影响
Fig. 1 Effects of Cu2+ on variations of ferrous oxidation activity(a), inhibition efficiency of ferrous oxidation in 24 h(b), rate of ferrous oxidation during logarithmic stage(c) and oxidation-reduction potential(ORP)(d)
Cu2+浓度由低到高胁迫下,体系亚铁氧化随时间变化结果表明(见图1(a)):培养体系中添加Cu2+胁迫对At. ferrooxidans菌亚铁氧化活性有抑制作用;且添加Cu2+浓度越高,抑制作用越显著。比较不同实验组经过24 h培养后的亚铁氧化率发现(见图1(a)),对照组和胁迫实验组(ρCu2+≤15 g/L)体系亚铁氧化率超过93%,表明At. ferrooxidans在Cu2+≤15 g/L条件下,24 h内亚铁氧化效率受到抑制作用不显著,其对应的亚铁氧化抑制率不超过7%(见图1(b))。但当Cu2+胁迫浓度增加至20 g/L和25 g/L,亚铁氧化率(24 h)分别降至78.3%和53%(见图1(a));即Cu2+胁迫浓度≥20 g/L时,微生物亚铁氧化活性受到显著抑制,对应的亚铁氧化抑制率( )分别为21.7%和46.8%(见图1(b))。对数生长期内,At. ferrooxidans以恒定的速度氧化亚铁(见图1(a))。而该期间内亚铁氧化速率随Cu2+胁迫浓度增加而降低,即当Cu2+胁迫浓度由0 g/L增加至25 g/L时,亚铁氧化速率由0.34 g/(L·h)降低至0.16 g/(L·h)(见图1(c))。
)分别为21.7%和46.8%(见图1(b))。对数生长期内,At. ferrooxidans以恒定的速度氧化亚铁(见图1(a))。而该期间内亚铁氧化速率随Cu2+胁迫浓度增加而降低,即当Cu2+胁迫浓度由0 g/L增加至25 g/L时,亚铁氧化速率由0.34 g/(L·h)降低至0.16 g/(L·h)(见图1(c))。
根据Nernst方程[19-20],体系氧化还原电位主要由Fe3+/Fe2+摩尔比值决定。当体系中Fe2+不断被At. ferrooxidans氧化,Fe3+浓度逐渐升高,因此体系氧化还原电位也呈逐渐上升趋势(见图1(d));但随着添加Cu2+胁迫浓度的升高,亚铁氧化速率降低(见图1(c)),造成体系氧化还原电位值上升出现延滞现象,尤其是Cu2+胁迫浓度≥20 g/L(见图1(d))。
2.2 Cu2+胁迫对At. ferrooxidans亚铁氧化电子传递链rus operon相关基因表达影响
At. ferrooxidans氧化Fe2+获得能源,并将产生的电子通过“downhill”途径传递给高氧化还原电势对(O2/H2O)。“downhill”电子传递途径相关蛋白编码基因为rus operon,公认电子传递途径为:Fe2+在At. ferrooxidans表面发生氧化并将产生的电子依次传递给外膜蛋白cytochrome c (Cyc2)→周质空间铜蓝蛋白rusticyanin RcY (Rus)→周质空间蛋白二聚体cytochrome c4 (Cyc1)→内膜蛋白aa3型细胞色素c氧化酶(CoxBACD)→Cytoplasmic O2[17, 21-23]。At. ferrooxidans在pH 2.0酸性条件下完成1 mol亚铁电子顺势传递产生32.99 kJ能量,并贮存于ATP中,以维持其正常生长。
为了进一步阐明Cu2+胁迫导致At. ferrooxidans亚铁氧化活性降低原因,研究利用Real-time quantitative PCR探究Cu2+胁迫下At. ferrooxidans亚铁氧化电子传递链rus operon相关基因表达情况,结果如图2~5所示。
图2所示为不同Cu2+浓度胁迫下,Cyc2基因随时间表达变化情况。Cyc2基因编码细胞外膜蛋白,该蛋白是Fe2+氧化电子传递链上第一个电子受体[22]。与对照组相比,Cu2+添加抑制了Cyc2基因表达:添加7 g/L Cu2+胁迫下,Cyc2表达略微下调;当添加25 g/L Cu2+胁迫时,胁迫时间越长,对Cyc2基因转录抑制作用越显著,Cyc2基因表达最高下调4.9倍。
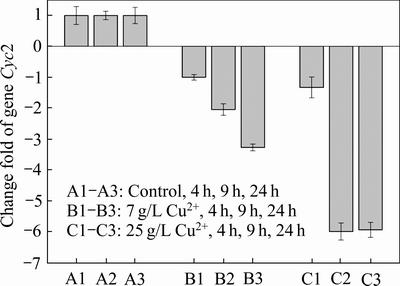
图2 与对照组相比,编码细胞外膜蛋白Cyc2基因在不同Cu2+浓度胁迫下的表达情况
Fig. 2 Expression of gene Cyc2 under stress of Cu2+
Fe2+氧化电子传递是蛋白与蛋白之间相互作用,如Cyc2编码的外膜蛋白将接受的电子按序传递给周质空间铜蓝蛋白(Rus)→cytochrome c4(Cyc1)。Cu2+胁迫下这两个周质空间蛋白的基因表达情况如图3所示。无论在低浓度(7 g/L)还是高浓度(25 g/L)Cu2+胁迫下,Rus表达略微下调,变化不显著(见图3(a))。与Rus表达不同,Cyc1在25 g/L Cu2+高浓度胁迫下表达显著下调,最高下调12.4倍(见图3(b))。
基因CoxBACD编码aa3型细胞色素氧化酶的四个不同亚基,该酶位于细胞内膜,在Fe2+氧化中起到重要作用,因为其从Cyc1获得电子并将电子传递给最终受体O2[21-22]。图4显示了Cu2+胁迫下细胞色素氧化酶4个不同亚基基因表达情况。结果显示:Cu2+刺激下,细胞色素氧化酶CoxBACD 4个亚基基因表达下调。高浓度25 g/L Cu2+胁迫培养24 h后,CoxBACD 4个亚基基因表达下调4~6倍。基因Orf表达的蛋白参与亚铁氧化电子传递,溶于周质空间。定量分析Orf基因表达结果显示(见图5):在两种Cu2+胁迫下,Orf表达下调情况相近,最高下调3.6~3.9倍,且与时间相关。
综上所述,Cu2+胁迫下(尤其是25 g/L高浓度Cu2+条件下),At. ferrooxidans中与亚铁氧化电子传递链编码蛋白相关的Rus operon基因表达降低,其中细胞内膜蛋白编码基因Cyc1和细胞色素c氧化酶编码基因CoxBACD表达显著降低,因而推断这两种基因(Cyc1和CoxBACD)编码的蛋白可能是亚铁氧化电子传递链途径中的限速酶。LIU等[24]通过构建含Rus基因的基因工程菌At. ferrooxidans,同样提出Cyc1或CoxBACD基因表达的产物酶可能是亚铁氧化电子传递途径限速酶。由此,本研究结果与LIU等研究结果相一致。
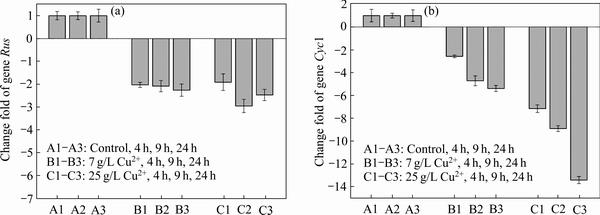
图3 与对照组相比基因Rus和Cyc1在Cu2+浓度胁迫下的表达情况
Fig. 3 Expression of genes Rus(a)和Cyc1(b) under stress of Cu2+
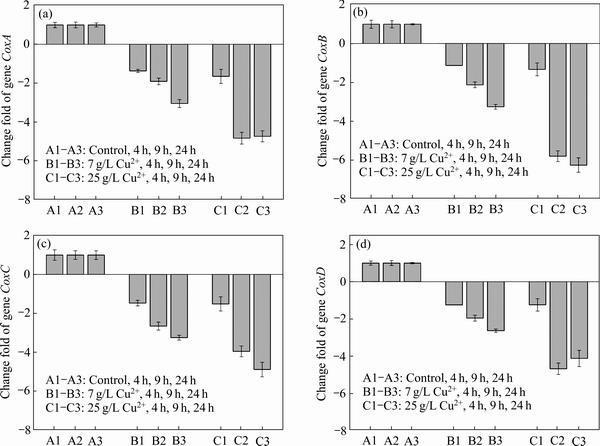
图4 与对照组相比编码细胞内膜蛋白Cyc aa3 4个不同亚基的基因CoxABCD在Cu2+浓度胁迫下表达情况(CoxA, CoxB, CoxC, CoxD)
Fig. 4 Expression of genes CoxA(a), CoxB(b), CoxC(c), CoxD(d) under stress of Cu2+
2.3 Cu2+胁迫对At. ferrooxidans胞外电子传递影响
鉴于At. ferrooxidans自身特有的亚铁氧化电子传递链系统(“downhill”途径),利用线性循环伏安电化学法研究At. ferrooxidans在Cu2+胁迫下胞外电子传递情况,如图6所示。

图5 与对照组相比,基因Orf在Cu2+浓度胁迫下表达情况
Fig. 5 Expression of gene Orf under stress of Cu2+
图6(a)所示为无Cu2+重金属胁迫培养下At. ferrooxidans菌体线性循环伏安曲线。Abiotic control曲线为工作电极表面(无粘附At. ferrooxidans菌体)线性循环伏安曲线(见图6(a)),结果显示电流在0 μA附近且无明显氧化/还原峰,表明工作电极表面不存在其他氧化还原电对,不影响At. ferrooxidans菌循环伏安测定。对照组At. ferrooxidans菌微生物电极在0.8~-0.5~ 0.8 V(vs Ag/AgCl)循环扫描范围内,由0.8 V开始向负极(-0.5 V)扫描,起初无阴极还原电流,当阴极电势低于0.4V时,开始缓慢出现还原电流,即还原反应开始,进一步降低还原电势至180 mV左右时,出现最大还原峰(约为29 μA),此时还原反应速率达到最大。在-0.5 V左右出现另一个还原峰,此时可能出现析氢现象;之后开始正向扫描(-0.5~0.8 V),正向扫描中无明显阳极峰出现。由此可知,At. ferrooxidans胞外电子传递电化学反应不可逆。依据CARBAJOSA等[25]研究结果可知:At. ferrooxidans在无任何电子传递中间体条件下能够直接从电极表面获得电子产能,实现高效培养。结合At. ferrooxidans固有的Rus operon电子传递链[22]可得,阴极电子直接被外膜蛋白Cytochrome c接纳,Cytochrome c被还原,然后进一步通过电子传递链上的其他蛋白传递电子,完成传递过程。CASTELLE等[22]报道指出纯化的At. ferrooxidans细胞外膜上的Cytochrome c氧化还原电势为560 mV,是目前已知最高氧化还原电势的细胞色素c。综上所述,微生物电极还原峰可能主要由Cytochrome c得到阴极电子并传递而还原产生,且该微生物电极电化学反应不可逆。

图6 At. ferrooxidans菌循环伏安曲线
Fig. 6 Cyclic voltammetry of At. ferrooxidans
图6(b)所示为在25 g/L Cu2+胁迫培养24 h后At. ferrooxidans菌线性循环伏安曲线图。与对照组相似,在0.8~-0.5 V反向扫描过程中在180 mV附近出现还原峰,可推测在此还原峰发生Cytochrome c还原反应,还原峰对应的峰电流值为26.5 μA,低于对照组还原峰电流值(29.0 μA)。循环伏安曲线氧化还原电流峰值可表示在给定条件下该氧化还原反应进行速率[26]。因而,在相同细胞数下,未经过重金属胁迫的At. ferrooxidans发生的还原反应速度最快,获得电子的能力最强,其对应的亚铁氧化能力也最强,高于Cu2+重金属胁迫实验组,与前述结果一致(见图1)。由此推断出,重金属胁迫培养导致了At. ferrooxidans胞外电子传递能力降低。
3 结论
1) Cu2+胁迫对At. ferrooxidans菌亚铁氧化活性有抑制作用:Cu2+胁迫浓度越高,对At. ferrooxidans菌亚铁氧化活性抑制作用越显著。本研究驯化获得的At. ferrooxidans菌能够耐受25 g/L Cu2+,对应下亚铁氧化抑制率( ,24 h)约为50%。
,24 h)约为50%。
2) Cu2+胁迫抑制了At. ferrooxidans菌亚铁氧化代谢Rus operon相关基因的表达,尤其是细胞内膜蛋白编码基因Cyc1和细胞色素c氧化酶编码基因CoxBACD。因而,Cu2+胁迫下,At. ferrooxidans亚铁氧化电子传递链限速酶可能与Cyc1和CoxBACD基因编码的细胞内膜蛋白和细胞内膜蛋白细胞色素色素c氧化酶有关。
3) 与对照组相比,经过高浓度Cu2+胁迫培养的At. ferrooxidans胞外传递电子能力降低。
4) 高浓度Cu2+胁迫引起At. ferrooxidans菌亚铁氧化代谢Rus operon相关基因的表达显著下调,造成胞外电子传递速率降低,最终导致At. ferrooxidans菌亚铁氧化活性降低。
REFERENCES
[1] MARRA A, CESARO A, RENE E R, BELGIORNO V, LENS P N L. Bioleaching of metals from WEEE shredding dust[J]. Journal of Environmental Management, 2018, 210: 180-190.
[2] YANG Yuan-kun, CHEN Shu, LI Shi-cheng, CHEN Meng-jun, CHEN Hai-yan, LIU Bi-jun. Bioleaching waste printed circuit boards by Acidithiobacillus ferrooxidans and its kinetics aspect[J]. Journal of Biotechnology, 2014, 173: 24-30.
[3] UMESH J, HONG H. Extraction of silver from spent silver oxide-zinc button cells by using Acidithiobacillus ferrooxidans culture supernatant[J]. Journal of Cleaner Production, 2013, 44: 39-44.
[4] HONG Hocheng, SU Cheer, JADHAV U U. Bioleaching of metals from steel slag by Acidithiobacillus thiooxidans culture supernatant [J]. Chemosphere, 2014, 117: 652-657.
[5] Park Jeonghyun, Han Yosep, Lee Eunseong, Choi Uikyu, Yoo Kyungkeun, Song Youngsoo, Kim Hyunjung. Bioleaching of highly concentrated arsenic mine tailings by Acidithiobacillus ferrooxidans[J]. Separation and Purification Technology, 2014, 133: 291-296.
[6] 仉丽娟, 周洪波, 康 鑫, 陈岩贽, 周文根, 史美玉, 周文博, 温 勇, 王 炜, 刘晓文. 嗜酸铁氧化微生物富集物高效浸提废覆铜板分选残渣中的铜[J]. 中国有色金属学报, 2015, 25(10): 2936-2944.
ZHANG Li-juan, ZHOU Hong-bo, KANG Xin, CHEN Yan-zhi, ZHOU Wen-gen, SHI Mei-yu, ZHOU Wen-bo, WEN Yong, WANG Wei, LIU Xiao-wen. High extraction of copper from flotationtailings of waste copper-clad laminates by an acidophilic iron-oxidizing enrichment[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(10): 2936-2944.
[7] 林 海, 林丽娟, 董颖博. 用氧化亚铁硫杆菌从废印刷线路板中浸出铜[J]. 湿法冶金, 2019, 38(2): 104-109.
LIN Hai, LIN Li-juan, DONG Yin-bo. Bioleaching of copper waste printed circuit boards by Acidithiobacillus ferrooxidans[J]. Hydrometallurgy of China, 2019, 38(2): 104-109.
[8] CABRERA G, GOMEZ J M, CANTERO D. Influence of heavy metals on growth and ferrous sulphate oxidation by Acidithiobacillus ferrooxidans in pure and mixed cultures[J]. Process Biochemistry, 2005, 40(8): 2683-2687.
[9] 叶茂友, 严苹方, 孙水裕, 韩大建, 庄圣炜, 郑 莉, 黄绍松. 铜离子浓度对嗜酸性氧化亚铁硫杆菌生长特性和生长动力学的影响[J]. 中国有色金属学报, 2016, 26(10): 2238-2245.
YE Mao-you, YAN Ping-fang, SUN Shui-yu, HAN Da-jian, ZHUANG Sheng-wei, ZHENG Li, HUANG Shao-song. Effect of copper ion concentration on growth activity and kinetics of Acidithiobacillus ferrooxidans[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(10): 2238-2245.
[10] CABRERA G, GOMEZ J M, CANTERO D. Kinetic study of ferrous sulphate oxidation of Acidithiobacillus ferrooxidans in the presence of heavy metal ions[J]. Enzyme and Microbial Technology, 2005, 36(2/3): 301-306.
[11] MARTINEZ-BUSSENIUS C, NAVARRO C A, ORELLANA L, PARADELA A, JEREZ C A. Global response of Acidithiobacillus ferrooxidans ATCC 53993 to high concentrations of copper: A quantitative proteomics approach[J]. Journal of Proteomics, 2016, 145: 37-45.
[12] ALMARCEGUI R J, NAVARRO C A, PARADELA A, ALBAR J P, von BERNATH D, JEREZ C A. Response to copper of Acidithiobacillus ferrooxidans ATCC 23270 grown in elemental sulfur[J]. Research in Microbiology, 2014, 165(9): 761-772.
[13] ROHWERDER T, GEHRKE T, KINZLER K, SAND W. Bioleaching review part A: Progress in bioleaching: fundamentals and mechanisms of bacterial metal sulfide oxidation[J]. Applied Microbiology and Biotechnology, 2003, 63(3): 239-248.
[14] LIU Huan, LU Xian-cai, ZHANG Li-juan, XIANG Wan-li, ZHU Xiang-yu, LI Juan, WANG Xiao-lin, LU Jian-jun, WANG Ru-cheng. Collaborative effects of Acidithiobacillus ferrooxidansand ferrous ions on the oxidation of chalcopyrite[J]. Chemical Geology, 2018, 493: 109-120.
[15] FATEMEH P, MOHAMMAD M S. Enhancement of copper, nickel, and gallium recovery from LED waste by adaptation of Acidithiobacillus ferrooxidans[J]. Waste Management, 2018, 79: 98-108.
[16] CARLOS C, REIS F C, VICENTINI R, MADUREIRA D J, OTTOBONI L M. The rus operon genes are differentially regulated when Acidithiobacillus ferrooxidans LR is kept in contact with metal sulfides[J]. Current Microbiology, 2008, 57(4): 375-380.
[17] YARZA’BAL A, APPIA-AYME C, RATOUCHNIAK J, BONNEFOY V. Regulation of the expression of the Acidithiobacillus ferrooxidans rus operon encoding two cytochromes c, a cytochrome oxidase and rusticyanin[J]. Microbiology, 2004, 150: 2113-2123.
[18] LIVAK K J, SCHMITTGEN T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T)) method[J]. Methods, 2001, 25(4): 402-408.
[19] AHMADI A, SCHAFFIE M, MANAFI Z, RANJBAR M. Electrochemical bioleaching of high grade chalcopyrite flotation concentrates in a stirred bioreactor[J]. Hydrometallurgy, 2010, 104(1): 99-105.
[20] DE GC, OLIVER D J, PESIC B M. Effect of heavy metals on the ferrous iron oxidizing ability of Thiobacillus ferrooxidans[J]. Hydrometallurgy, 1997, 44: 53-63.
[21] QUATRINI R, APPIA-AYME C, DENIS Y, JEDLICKI E, HOLMES D S, BONNEFOY V. Extending the models for iron and sulfur oxidation in the extreme acidophile Acidithiobacillus ferrooxidans[J]. BMC Genomics, 2009, 10: 394-412.
[22] CASTELLE C, GUIRAL M, MALARTE G, LEDGHAM F, LEROY G, BRUGNA M, GIUDICI-ORTICONI M T. A new iron-oxidizing/O2-reducing supercomplex spanning both inner and outer membranes, isolated from the extreme acidophile Acidithiobacillus ferrooxidans[J]. Journal of Biological Chemistry, 2008, 283(38): 25803-25811.
[23] 尹华群, 刘征华, 刘学端. 冶金微生物的铁硫代谢多样性及其与矿物的相互作用[J]. 微生物学报, 2018, 58(4): 560-572.
YIN Hua-qun, LIU Zheng-hua, LIU XUe-duan. Diversity of iron and sulfur metabolism in bioleaching microorganisms and their interaction with minerals[J]. Acta Microbiologica Sinica, 2018, 58(4): 560-572.
[24] LIU Wu, LIN Jian-qun, PANG Xin, CUI Shuang, MI Shuang, LIN Jian-qiang. Overexpression of rusticyanin in Acidithiobacillus ferrooxidans ATCC19859 increased Fe(II) oxidation activity[J]. Current Microbiology, 2011, 62(1): 320-324.
[25] CARBAJOSA S, MALKI M, CAILLARD R, LOPEZ M F, PALOMARES F J, MARTIN-GAGO J A, RODRIGUEZ N, AMILS R, FERNANDEZ V M, DE LACEY A L. Electrochemical growth of Acidithiobacillus ferrooxidans on a graphite electrode for obtaining a biocathode for direct electrocatalytic reduction of oxygen[J]. Biosensors & Bioelectronics, 2010, 26(2): 877-888.
[26] 贾 铮, 戴长松, 陈 玲. 电化学测量方法[M]. 北京: 化学工业出版社, 2013: 137-139.
JIA Zheng, DAI Chang-song, CHEN Ling. Electrochemical methods[M]. Beijing: Chemical Industry Press, 2013: 137-139.
Effects of Cu2+ stress on ferrous oxidation metabolism and extracellular electron transfer of Acidithiobacillus ferrooxidans
ZHANG Li-juan1, WU Ping1, WANG Zhi-jie1, ZHOU Wen-bo2, ZHOU Hong-bo2
(1. Faculty of Biotechnology and Pharmaceutical Engineering, Nanjing University of Technology, Nanjing 211816, China;
2. Key Laboratory of Biometallurgy, Ministry of Education, School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China)
Abstract: The effects of Cu2+ stress (0-25 g/L) on the ferrous oxidation efficiency, expression of Rus operon genes and extracellular electron transfer of Acidithiobacillus ferrooxidans(At. ferrooxidans) were investigated by using phenanthroline spectrophotometry, real-time quantitative PCR and cyclic voltammetry. The obtained results indicate that the increased concentrations of Cu2+ stress from 0 g/L to 25 g/L inhibit the ferrous oxidation activity of At. ferrooxidans. Under the stress of 25 g/L Cu2+, the 24 h ferrous oxidation inhibition efficiency is about 50% in comparison to the control (0 g/L Cu2+). The high concentration of Cu2+ stress also decreases the transcriptional levels of Rus operon genes. Especially, Cyc1 and CoxBACD are decreased by 12.4 fold and 4-6 fold, respectively. Meanwhile, the decreased rate of extracelluler electron transfer in At. ferrooxidans under the stress of 25 g/L Cu2+ (26.5 μA) is found in comparison to that in the control (0 g/L Cu2+, 29.0 μA). In conclusion, the high concentration of Cu2+ stress results in the down-regulated expression of Rus operon genes related to Fe2+ oxidation, afterwards inhibiting the electron transport from Fe2+ oxidation, and finally leading to a decrease in the rate of ferrous oxidation.
Key words: Acidithiobacillus ferrooxidans; metal stress; ferrous oxidation metabolism; extracellular electron transfer
Foundation item: Project(18KJB450001) supported by the University Natural Science Research Project of Jiangsu Province, China; Project(1701136B) supported by the Jiangsu Province Postdoctoral Research Fund, China; Project (2018M632298) supported by the Postdoctoral Research Fund of China
Received date: 2018-12-20; Accepted date: 2019-05-14
Corresponding author: ZHANG Li-juan; Tel: +86-18913005292; E-mail: lijuan_zhang@njtech.edu.cn
(编辑 龙怀中)
基金项目:江苏省高等学校自然科学研究面上项目(18KJB450001);江苏省博士后科研资助计划项目(1701136B);中国博士后科学基金资助项目(2018M632298);
收稿日期:2018-12-20;修订日期:2019-05-14
通信作者:仉丽娟,助理研究员,博士;电话:18913005292;E-mail:lijuan_zhang@njtech.edu.cn