��ѹ�����´�ʯú����ȡ�����������Ĺ���
��F͢��κ�ƣ�����֣���־�ң����˱���
(����������ѧ ұ������Դ����ѧԺ������ ������650093)
ժ Ҫ���Թ���ij��ʯú���м�ѹ����ᷰʵ���о�����ѹ���������¿��켸����Ҫ���ضԷ������ʵ�Ӱ�졣�õ�����Ѽ�������Ϊ����Ӧʱ��3 h����������Ũ��200 g/L�������¶�180 �棬����ת��580 r/min���ڴ������£���������(��������)Ϊ76%��������������ʵ�����������������ʿɴ�90%���ϡ�����Һ����������ա���ԭ������pH��Ԥ���������ܼ���ȡ�ķ����ܹ���Ч�ط��������������ȡ�ʿɴ�98.1%��������Ϊ99.14%���ð�ˮ��������Һ�еķ���������(��۷����)��550 ������3 h���ɲ�������Ϊ99% V2O5��ȫ���̷�������Ϊ85%���ҡ�
�ؼ��ʣ�����ʯú����ѹ������ܼ���ȡ
��ͼ����ţ�TF841.3 ���ױ�־�룺A ���±�ţ�1672-7207(2010)04-1268-08
Technics for vanadium pentoxide extraction from black shale in pressure field
LI Min-ting, WEI Chang, LI Cun-xiong, DENG Zhi-gan, LI Xing-bin, FAN Gang
(Faculty of Metallurgical and Energy Engineering, Kunming University of Science and Technology,
Kunming 650093, China)
Abstract: The extraction of vanadium from black shale in Guizhou was investigated by pressure acid leaching. The effects of main factors on leach recovery were investigated in pressure field. Optimum parameters for the leaching of vanadium for one-step leaching are: reaction time of 3 h, sulfuric acid concentration of 200 g/L, leaching temperature of 180 �� and stirring speed of 580 r/min. Under these conditions, about 76% vanadium is recovered. A two-step countercurrent leaching process is developed, and the vanadium recovery of 90% is obtained. Vanadium in the leachate is efficiently separated and enriched by solvent extraction after several preprocesses namely. The extraction and stripping yields of vanadium are 98.1% and 99.41%, respectively. Ammonia is employed to precipitate vanadium in the stripping liquor, subsequently and then the precipitates (ammonium poly-vanadate) are calcined at 550 �� for 3 h to produce 99% V2O5. The overall yield of vanadium through all process stages is about 85%.
Key words: vanadium; black shale; pressure acid leaching; solvent extraction
��Ȼ���к����е����ķ����ڣ�ͨ�������ڷ��Ѵ��������ο�̼���ࡢʯú��ʯ�ͻ������˷���ͼط���ȿ��С�ʯú���ҹ������Ѵ���������һ����Ҫ������Դ���㷺�ֲ������ϡ����ݡ����ϡ��㽭�����������������ࡢ�½���ʡ(��)��ʯú�и���Ľ����ͷǽ���Ԫ����60���֣��й�ҵ���ü�ֵ��Ʒλ�ϸߵ���20���֣���V��Mo��Ag��Y��Ga��Se�ȣ��ʱ���Ϊ��һ�ֵ�Ʒλ��������ӿ��ҹ�ʯú����Ϊ6l8.8��108 t�����к���1.18��108 t��ռ�ҹ�V2O5�ܴ�����87%[1]����ʯú����ȡ���Ĵ�ͳ�������ƻ����ա�ˮ��(��������)���������������������������˵���Ը���ʯú����н�ǿ����Ӧ�ԣ�ȱ���Ƿ������ʽϵ�(ͨ����50%)���Ի�����Ⱦ�����ء����Ż�����������ͻ��������������ȡ�ޡ�һЩ�о���Ϊ����߷������ʺͼ��ỷ����������ʯú�ᷰ�����˴������о���֣������[2]���÷ֶ��ܽⷨ��ȡʯú�е����������������ø�ѡȥ��ʯú�д�̼������ϡ����������ܽ��������еķ���Ȼ��������������ν�ȡ���������з���ʹ�ַ�ת����Һ�У�����Һ������������Һ����Һ����������֬������һ����ȡ���ɻ�ô���(��������)��97.0%��������������Ʒ������������85%���ϡ�³����[3]���á������P204��ȡ�����ᷴ��ȡ����ˮ�����������ƾ������������̴���������ʯú����ȡ����������������ʵ�������£���������Һ���Խ���ʯú��Լ80%�ķ�����P204��TBP�Ļǻ�ú����Һ��ȡ��������Һ����ȡ�ɵõ��ϴ�������������Һ���پ���ˮ�������Ƚ⣬�ɵõ�������98%���ϵľ�����Ʒ���ù�����1996�����ҹ���������ʵ���˹�ҵ�����������⣬��Ժ��Ƹߵ�ʯú��Դ��½֥����[4]��������������һϡ��������գ�ŷ������[5]����������������һϡ��������գ������µ�[6]�����˸ƻ����ա�������գ���𥻪��[7]����øƻ����ա����������������������ʯú�����Ѵ������⣬�����ᷰ��ԭ����Ҫ��ʯ��ҵ�����ɻҡ�ʯ�ͽ�������ͷϴ����ȣ����õķ�����Ҫ�б��ա����[8-9]���������[10-11]��ֱ�����[12]���������Թ���ij�غ���ʯú������3���ᷰʵ�鷽�����о�[13]�����������ա���ѹ�������ѹ�������ѹ������������������ǰ2�ַ������õķ�������С��60%�����ڱ��չ��̲������µIJ�������ķ���������������·������ʵͣ���ˣ��������߲��ü�ѹ������ܼ���ȡ�ķ�����ʯú����ȡ�������������÷�����ͳ�ı��չ������Cl2��HCl���к����壬���жԻ����Ѻõ��ص㣻ͬʱ���ڽϸߵ��¶Ⱥ�����£�����ʱ���������̣���3~4 h������ѹ���ͨ����Ҫ16~20 h���������նԷ�Ӧ�豸�IJ���Ҫ��ϸ�(������ʣ�ͨ��Ϊ�Ѳ�)���������ɱ����ƻ����չ��յĵͣ��ȳ�ѹ������Ըߡ�
1 ʵ��
1.1 ԭ�����Լ�����
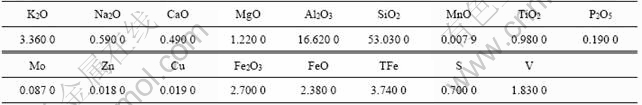
ʵ��ԭ����������ij�أ���Ҫ�Ļ�ѧ�ɷ����1��ʾ��ɨ��羵�������������ͼ1��ʾ��
��ͼ1��֪������Ҫ�ֲ����������������������ĸ������У��������ķ����������ܹ������ο����С�
1.2 ʯú�з��ĸ���״̬
ʯú�Ŀ�����ɸ��Ӷ�䣬��ɢϸ�����ĸ���״̬����̬���ֶ���ԡ����������������֣��ɷ�Ϊ3��[14]�������������������������ĸ��ͺ������ܹ�������(�����ʯ��ʯ��ʯ��)����2��ʾΪʵ���ÿ����������༰��̬���������
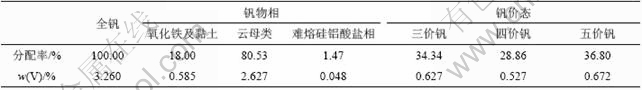
�ӱ�2���Կ���������Ҫ������ͬ����ʽ��������ĸ�����ⲿ�ֵķ�(V2O5)����Ϊ2.627%��ռ�ܷ�80.53%����Σ���������ʽ���������������������ʣ�༫�����ķ�������ͬ����ʽ���������ܹ������ο����С�
����ʯúԭ����һ��ֻ�����۷����ļ۷����ڣ����ٷ��ֶ��۷�����۷������˸���ط�ʯú���ļ۷������������۷������⣬���ֵ���ʯú�з����������۷�Ϊ��[15-16]���ӱ�2�ɿ�����ʵ���ÿ�����3�ּ�̬�ķ�������������۷�������ߣ���������۷�����������[15]���о�����нϴ������һ��˵��ʯú�з�����״̬�ĸ��ӺͶ�䡣ʯú���и�̬�ķ�����Խ�ߣ����ڷ��Ľ���Խ��������Ϸ������������֪�����۷����ļ۷���Ҫ��������ͬ����ʽ��������ĸ�����У���۷�����������ʽ����������������������С�
��1 ԭ�ϵĻ�ѧ�ɷ�(��������)
Table 1 Chemical composition of black shale sample %
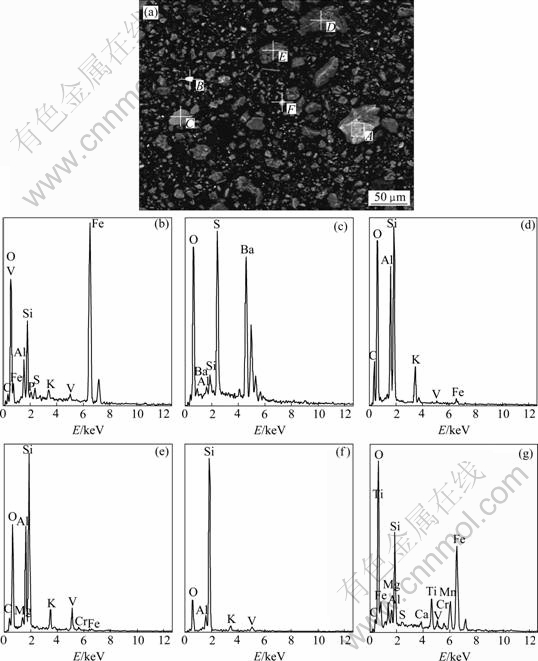
(a) ʯú��SEM��(b) A�����ף�(c) B�����ף�(d) C�����ף�(e) D�����ף�(f) E�����ף�(g) F������
ͼ1 ʯú��ɨ��羵�����������
Fig.1 SEM image and EDS patterns of black shale sample
1.3 ʵ�鷽��
��ʯ������С��0.074 mm�Ŀ���ռ85%(��������)����ȡ��ԭ��200 g������һ��ʵ���������е����������ϼ��뷴Ӧ����ʼ�������£�����Ԥ���¶Ⱥ�ʼ��ʱ��ͬʱ���ѹ��ͨ�����������½�����ȡ���������Ͻ���Һ�̷��룬���������еķ����������㷰�����ʡ���ѹ���������£����췴Ӧʱ�䡢��������Ũ�ȡ���Ӧ�¶ȡ�����ת�١����Ӽ�FeSO4����Ũ�ȶԷ������ʵ�Ӱ�죬ͬʱ���������������� ʵ�顣
�������������õ��Ģ�ν���Һ����������ա���ԭ������pH��Ԥ��������P204Ϊ��ȡ������6��������ȡ������H2SO4Ϊ���ͼ�����5�����ͣ�����Һ��60 ������1 h���ð�ˮΪ����������90 ����г������������ϴ�Ӻ���550 �����ռ��ɵõ���״V2O5��
��2 ʵ���ÿ����������༰��̬�������
Table 2 Phase and valence state of vanadium in used sample
2 ���������
2.1 ��ѹ���ʵ��
�̶�ʵ������Ϊ����ʯ������С��0.074 mm�Ŀ���ռ85%������������ѹ��Ϊ1.2 MPa��Һ�̱�Ϊ 1.2 mL/g��
2.1.1 ��Ӧʱ��Է������ʵ�Ӱ��
�ڽ����¶�Ϊ180 �桢Һ�̱�Ϊ1.2 mL/g����������Ũ��Ϊ200 g/L�������£�������Ӧʱ��Է������ʵ�Ӱ����ͼ2��ʾ����ͼ2�ɿ��������ŷ�Ӧʱ����ӳ�����������Ѹ����ߣ���3 h�ﵽ���ֵ��Ϊ75.79%���˺����ӳ�����ʱ�䣬�����ʻ������䣬��ԭ���д���һ���о����ں��������н���ʱ��ɿ�����3 h��
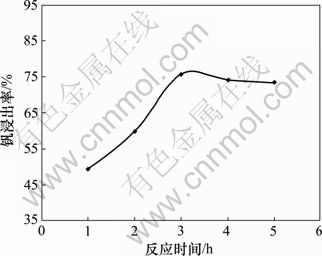
ͼ2 ��Ӧʱ��Է������ʵ�Ӱ��
Fig.2 Effect of reaction time on leach recovery of vanadium
2.1.2 ��������Ũ�ȶԷ������ʵ�Ӱ��
�ڽ����¶�Ϊ180 �桢Һ�̱�Ϊ1.2 mL/g����Ӧʱ��Ϊ3 h�������£���������Ũ�ȶԷ������ʵ�Ӱ����ͼ3��ʾ����ͼ3��֪��������������Ũ�ȵ����ӣ���������Ѹ����ߣ�����������Ũ�ȴ�200 g/L���ӵ�330 g/Lʱ�����������������Ʊ�û�������74.23%���ӵ�78.24%�������4%��ͬʱ�����ڳ�ʼ��������Ũ��Խ�ߣ�����Һ�еIJ�����������Ũ��ҲԽ�ߣ�����������Ũ��Ϊ330 g/Lʱ��������������Ũ��Ҳ�ﵽ65 g/L������������ⲿ�����ᣬ�ͻ����Ӻ�����Һ�к����е��Լ���������ˣ���������Ũ��Ϊ200 g/L��Ϊ���ʡ�

ͼ3 ��������Ũ�ȶԷ������ʵ�Ӱ��
Fig.3 Effect of H2SO4 concentration on leach recovery of vanadium
2.1.3 ��Ӧ�¶ȶԷ������ʵ�Ӱ��
��Һ�̱�Ϊ1.2 mL/g����������Ũ��Ϊ200 g/L����Ӧʱ��Ϊ3 h�������£������¶ȶԷ������ʵ�Ӱ����ͼ4��ʾ����ͼ4��֪����Ӧ�¶ȶԷ�������������Ӱ�죬�������ʴ�120 ��ʱ��40.68%���ӵ�180 ���75.30%��������34.38%���������ѧ��Ӧ�����Ƿ������ܽ����ʵ���Ҫ���Ʋ��衣��Ӧ�������£�V2O3+O2+2H+��2VO2++H2O+3e��V2O4+4H+��2VO2++ 2H2O��V2O5+2H+��2VO2++H2O�����ں���ʵ���н����¶�ѡΪ180 �档
2.1.4 ����ת�ٶԷ������ʵ�Ӱ��
�ڽ����¶�Ϊ180 �桢Һ�̱�Ϊ1.2 mL/g����Ӧʱ��Ϊ3 h����������Ũ��Ϊ200 g/L�������£�����ת�ٶԷ������ʵ�Ӱ����ͼ5��ʾ����ͼ5�ɿ������ڽ���ת��Ϊ100~500 r/min��Χ�ڣ��������������ת�����Ӷ��������ӣ���41.0%���ӵ�73.8%��������32.8%���˺������ӽ���ת�٣��������ʻ������䡣�����������ת�����ӵ�500 r/min����ʱ�����������ҺĤ�߽��ﵽһ����Сֵ����ʱ������ת�ٶԷ������ʵ�Ӱ�챻������������Ӧ�����ʿ��Ʋ���ת��ΪҺĤ���ƻ�ѧ��Ӧ���ƣ��������жϹ��̵Ļ��������һ����ʵ���о���Ϊ��ȷ���㹻�Ľ���ת�٣��ں��������н���ת���Կ�����580 r/min��

ͼ4 ��Ӧ�¶ȶԷ������ʵ�Ӱ��
Fig.4 Effect of temperature on leach recovery of vanadium

ͼ5 ����ת�ٶԷ������ʵ�Ӱ��
Fig.5 Effect of stirring speed on leach recovery of vanadium
2.1.5 ���Ӽ�����Ũ�ȶԷ������ʵ�Ӱ��
Ϊ�������Һ�����Ĵ������ʣ�����������Ӧ�Ķ���ѧ����������Fe3+���Դ����������ã��Եͼ۷������������ڽ����¶�Ϊ180 �桢Һ�̱�Ϊ1.2 mL/g����������Ũ��Ϊ200 g/L����Ӧʱ��Ϊ3 h�������£����첻ͬFeSO4����Ũ�ȶԷ������ʵ�Ӱ�죬�����ͼ6��ʾ����ͼ6�ɼ���FeSO4����Ũ��Ϊ6.6 g/Lʱ���������Ѵ�75.2%����û�м���FeSO4ʱ�����5%���˺�������FeSO4����Ũ�ȣ��������ʻ���������ߡ���������ԭ����Fe����Ϊ3.74%���ڽ�����Ӧ�����У�һ���ֵ�Fe���ܳ������˴����������ã����FeSO4����Ũ�ȶԷ�������û������Ӱ�졣

ͼ6 FeSO4����Ũ�ȶԷ������ʵ�Ӱ��
Fig.6 Effect of FeSO4 concentration on leach recovery of vanadium
���������������õ���ѹ��ղ������£���Ӧʱ��Ϊ3 h����������Ũ��Ϊ200 g/L����Ӧ�¶�Ϊ180 �棬����ת��Ϊ300 r/min�����Ӽ�����Ũ��Ϊ6.6 g/L���ڴ������½�����3��ƽ��ʵ�飬�������ʷֱ�Ϊ75.23%, 76.4%��76.79%��ƽ��ֵΪ76%���ҡ�
2.1.6 ������������
Ϊ�˽�һ����߷�������ͬʱ������ϵ�¶ȣ��Խ������̽����Ż����������������������ķ�������������ʵ����5�ε�Ԫʵ����ɡ���Ԫʵ���������¡�
��Σ���Ӧʱ��Ϊ3 h����������Ũ��Ϊ200 g/L����Ӧ�¶�Ϊ150 �棬Һ�̱�Ϊ1.2 mL/g�����Ӽ�����Ũ��Ϊ6.6 g/L��
��Σ���Ӧʱ��Ϊ4 h����������Ũ��Ϊ330 g/L����Ӧ�¶�Ϊ150 �棬Һ�̱�Ϊ1.2 mL/g�����Ӽ�����Ũ��Ϊ6.6 g/L��
��κ͢�ν���ת�پ�Ϊ580 r/min����ѹ��Ϊ1.2 MPa��ʵ�������3��ʾ��
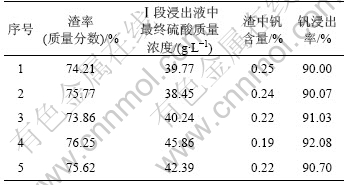
�ӱ�3�ɿ���������������������������Ԫʵ��ķ������ʾ���90.00%���ϣ��Ȣ�ν����Ľ�����76.00%�����14.00%��ʵ�黹������ԭ������Ҫ���ʽ����Ľ����ʣ������ͼ7��ʾ����ͼ7�ɼ����������Խ�����ѡ���Խϲԭ���е����ʽ�������ͬ�̶ȵر��ܳ������У�75%���ҵ�Mg������Һ�����������Fe��Al2O3��K2O��Na2O��CaO����������30%~60%֮�䡣����ԭ���е�SiO2�����ﵽ53.03%�����н϶�����ԵĹ豻�ܳ����������ϵĹ��˴����������ѡ�ʵ����������ԭ����SiO2���������ܳ���SiO2�����ʽ�Ϊ0.7%��
��3 ������������ʵ����
Table 3 Experimental results of two-step countercurrent leaching
2.1.7 �������ı���
������ɨ��羵��������������ͼ8��ʾ���Ա�ͼ1��ͼ8��֪��������������������ԭ�������������������ĸ������еķ��ѻ����ϱ��ܳ���
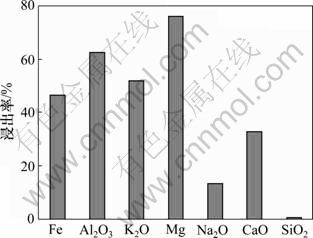
ͼ7 ԭ������Ҫ���ʽ����Ľ�����
Fig.7 Leaching recovery of main metal impurity in material
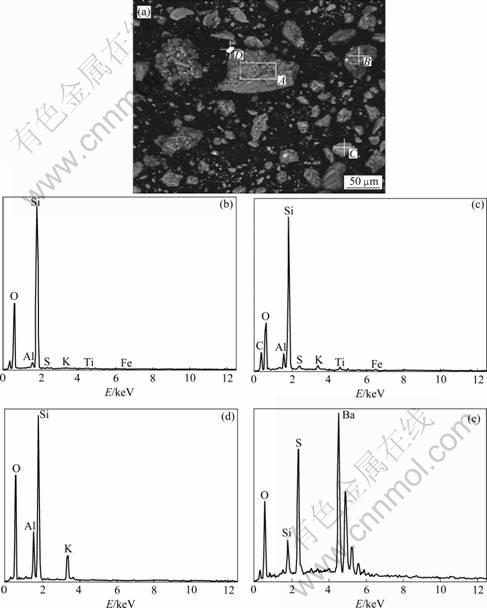
(a) ��������SEM��(b) A�����ף�(c) B�����ף�(d) C�����ף�(e) D������
ͼ8 ����������ɨ��羵������������
Fig.8 SEM image and EDS patterns of leach residue
2.2 ����Һ����ȡ��
����Һ����ȡ����ֱ����������[17]��ֱ�ӳ�����ԭ�����[18]���ܼ���ȡ[19-21]�������ܼ���ȡ�ķ�������ҺΪ������������ʵ��õ��Ģ�ν���Һ���仯ѧ�ɷּ���4��
��4 ��ν���Һ����Ҫ�ɷ�(����Ũ��)
Table 4 Main compositions in �� leachate g/L

��ǰ���������������Խ�����ѡ���Խϲԭ�����������ʽ�������ͬ�̶ȵر��ܳ����ӱ�4�ɼ�����Һ�����ʺ����ϸߣ������ں�������Һ����ȡV2O5��ͬʱ����Һ����Ƚϸߣ�����ȡ֮ǰ��Ҫ����Һ����Ԥ������
2.2.1 ��ҺԤ����
����Һ�к��д����IJ���H2SO4������������ⲿ�����ᣬ�������к��Լ���������ʹ�����ɱ����ߡ���������ϵ�л������������о�[21]�����ڽ���Һ�в��轺����(�轺�������ɢ����Ĥ)����ˣ����IJ�����ɢ�����������ⲿ��H2SO4�����������H2SO4������Ϊ85%����������Ϊ96%���������ʽ��������ʾ���90%���ϣ���������Һ(��Һ)��H2SO4����Ũ��Ϊ6.5 g/L���ҡ��������Ϊ��һ���ð�ˮ����pHʱ��ʡ�˰�ˮ������ͬʱ�����H2SO4�����ʣ�����ճɱ��͡�����ʵ����õ���ȡ��(P204)����ȡ����ͬʱ������ȡ���������ӣ��Ӷ�������ȡ��ʹ��Ч�ʵ͡���Ʒ���ʺ����ߣ���ˣ�����ȡ֮ǰ�����뽫���������ӻ�ԭ�ɶ��������ӡ�ʹ��Na2SO3Ϊ��ԭ����������Ϊ��ѧ��Ӧ����������1����Fe3+�Ļ�ԭ�ʿɴ�98.20%��
2.2.2 ��Һ�з�����ȡ������ȡ
ǰ����ȡʵ����������10% P204+5% TBP+85% (��������)�ǻ�ú����ϵ�Է��нϺõ���ȡЧ��������ȡ�����Ϊ10% P204+5% TBP+85%�ǻ�ú�͡��л�����ˮ�������Ϊ1?1�����¡���ʼˮ��pHΪ2.3��ʱ��Ϊ10 min�������£�����6����ȡ������ȡ��98.1%���ڷ��ͼ�H2SO4����Ũ��Ϊ160 g/L���л�����ˮ�������Ϊ5?1~8?1�����¡�ʱ��Ϊ15 min�������£�����5�����ͣ����ķ���ȡ�ʿɴ�99.14%������Һ��V2O5����Ũ��Ϊ75.0~84.0 g/L��Fe����Ũ��Ϊ0.5~0.8 g/L�������������Ч���Ϻá�
2.2.3 ���ij���������
���۲��ú����ᷰ������������ð�ˮ�������������Һ�еķ������ڷ���Һ�еķ������ļ۷�����ʽ���ڵģ���ˣ��ڳ���֮����뽫����������۷���������Ϊ200 g/L��NaClO3��Һ�����¶�Ϊ60 ��������1 h������¶����ߵ�90 �棬�����������Һ�м���18%��ˮ����������֤NH4+����۷������ʵ����ȴ���3������V2O5��pHΪ2.0���ҵ��ܽ����С����ˣ�������ʼpH������2.0����������Ϊ98.2%���Եõ��ĺ������ϴ�ӡ������550 ���Ƚ�3 h���ɵõ���V2O5��ĩ��V2O5��Ʒ���ȴ���99%��ȫ����V2O5������Ϊ85%���ҡ�
2.3 �����������Ļ�������
��ѹ�����´�ʯú����ȡ�����������Ĺ������̰�����ѹ�������ҺԤ��������ԭ���ܼ���ȡ�����͡������������ȹ��̣��乤��������ͼ9��ʾ��
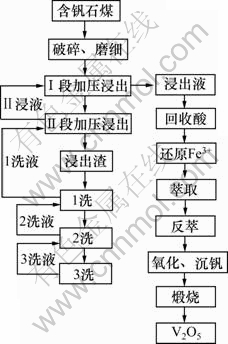
ͼ9 ��ѹ�����´�ʯú����ȡV2O5�Ĺ�������ͼ
Fig.9 Flow sheet for extraction of V2O5 from black shale under pressure field
3 ����
(1) �о��˽������̸���Ҫ���ضԷ������ʵ�Ӱ�죬�õ���ѹ��ղ������£���Ӧʱ��Ϊ3 h����������Ũ��Ϊ200 g/L����Ӧ�¶�Ϊ180 �棬����ת��Ϊ580 r/min�����Ӽ�����Ũ��Ϊ6.6 g/L���ڴ������·������ʿɴ�76%�������������������������ʿɴ�90%���ϡ�
(2) ����85%ú��+10% P204+5% TBP����ȡ��ϵ���ܹ��ܺõط����������������ȡ�ʺͷ���ȡ�ʷֱ�Ϊ98.1%��99.41%��ȫ���̷������ʿɴ�85%���ҡ�
�ο����ף�
[1] ������. ʯú�ᷰ�о���չ���������������г�״��[J]. ������ɫ����, 2006, 22(1): 16-20.
BIN Zhi-yong. Progress of the research on extraction of vanadium pentoxide from black shale and the market of the V2O5[J]. Hunan Nonferrous Metals, 2006, 22(1): 16-20.
[2] ֣����, ��ѧ��, ��С��, ��. ʪ����ȡʯú�з����¹����о�[J]. ��̶��ѧ��Ȼ��ѧѧ��, 2003, 25(1): 43-45.
ZHENG Xiang-ming, TIAN Xue-da, ZHANG Xiao-yun, et al. Extraction of vanadium pentoxide from stone coal with a wet chemical separation method[J]. Natural Science Journal of Xiangtan University, 2003, 25(1): 43-45.
[3] ³����. ���ᷨ��ʯú����ȡ�����������������о��빤ҵʵ��[J]. ʪ��ұ��, 2002, 21(4): 175-183.
LU Zhao-ling. Investigation and industrial practice on extraction of V2O5 from black shale containing vanadium by acid process[J]. Hydrometallurgy of China, 2002, 21(4): 175-183.
[4] ½֥��, �ܰ���, ������, ��. ʯú�������� ���� ϡ����Һ�����ᷰ�����о�[J]. ϡ�н���, 1994, 18(5): 321-327.
LU Zhi-hua, ZHOU Bang-na, YU Zhong-xing, et al. Craft sthdy on extracting vanadium form black shale by means of oxidation roasting: Diluted alkali solution[J]. Chinese Journal of Rare Metals, 1994, 18(5): 321-327.
[5] ŷ������, л����, ������. ʯú���α�����ȡ�ᷰ����dz��[J]. ú̿�ӹ����ۺ�����, 1993(1): 11-13.
OUYANG Chang-lun, XIE Xiang-lan, TENG Dai-ming. A process analysis of extracting vanadium from black shale by no salt-roasting, extracting[J]. Coal Processing & Comprehensive Utilization, 1993(1): 11-13.
[6] ������, ŷ����ף, ���徲, ��. ����ʯú���α�����������������������յ��о�[J]. ��ѧ����, 2001, 42(3): 117-119.
ZOU Xiao-yong, OUYANG Yu-zhu, PENG Qing-jing, et al. Study on the process of producing vanadium pentoxide from bone coal vanadium mine by no-salt-roasting and acid leaching[J]. Chemical World, 2001, 42(3): 117-119.
[7] ��𥻪, ��Ƽ, ����ȫ. ʯú���ᷰ������Ⱦ�¹���[J]. ��ѧ����, 1992, 33(12): 538-540.
JIANG Fu-hua, ZHANG Ping, SHEN Zhao-quan. A new craft characterized by no pollution on extracting vanadium from black shale[J]. Chemical World, 1992, 33(12): 538-540.
[8] Holloway, P C, Etsell, T H. Process for the complete utilization of oil sands fly ash[J]. Canadian Metallurgical Quarterly, 2005, 45(1): 25-32.
[9] Shelwit H, Alibrahim M. Extraction of sulfur and vanadium from petroleum coke by means of salt-roasting treatment[J]. Fuel, 2006, 85(5/6): 878-880.
[10] Mishra D, Kim D J, Ralph D E, et al. Bioleaching of vanadium rich spent refinery catalysts using sulfur oxidizing lithotrophs[J]. Hydrometallurgy, 2007, 88(4): 202-209.
[11] Mishra D, Kim D J, Ralph D E, et al. Bioleaching of spent hydro-processing catalyst using acidophilic bacteria and its kinetics aspect[J]. Journal of Hazardous Materials, 2008, 152(3): 1082-1091.
[12] Navarro R, Guzman J, Saucedo I, et al. Vanandium recovery from oil fly by leaching, precipitation and solvent extraction process[J]. Waste Management, 2007, 2(3): 425-438.
[13] ��F͢, κ��, ����, ��. ʯú��ѹ����ᷰ̽�������о�[J]. ϡ�н���, 2007, S31: 28-31.
LI Min-ting, WEI Chang, FAN Gang, et al. The pathbreaking experimentation study on extracting vanadium from stone-coal by acid leaching with oxygen pressure[J]. Chinese Journal of Rare Metals, 2007, S31: 28-31.
[14] Ф�Ķ�. ��������ʯú�Ŀ���ѧ��ʪ���ᷰ�о�[J]. ��ɫ����, 2007, 59(3): 85-90.
XIAO Wen-ding. Mineralogy of stoI/e coal from Shanglin of Guangxi and vanadium extraction with hydrometallurgical process[J]. Nonferrous Metals, 2007, 59(3): 85-90.
[15] ������. ʯú�з��ļ�̬��������ɶ��ᷰ���յ�ָ������[J]. ú̿�ӹ����ۺ�����, 1989(5): 5-8.
XU Guo-zhen. Guidance function of vanadium valence and material composition in black shale to extracting vanadium process[J]. Coal Processing & Comprehensive Utilization, 1989(5): 5-8.
[16] ������, ������, �����. ������ɽʯú�ս�����뷰ת�����о�[J]. �ִ�����, 1993, 7(1): 109-117.
XU Guo-zhen, ZHANG Xiu-rong, YIN Guang-heng. Sintering of black shale and the transformation of vanadium in Yushan Jiangxi province[J]. Geoscience, 1993, 7(1): 109-117.
[17] Sandra IVtolo, Maurizia Seggiani. Recovery of vanadium from heavy oil and Orimulsion fly ashes[J]. Hydrometallurgy, 2007, 57(2): 141-149.
[18] Lozano L J, Juan D. Technical note leaching of vanadium from spent sulphuric acid catalysts[J]. Minerals Engineering, 2001, 14(5): 543-546.
[19] Olazabal M A, Fernandez M M, Madariaga L A, et al. Selective extraction of vanadium(��) from solution containing molybdenum(��) by ammonium salts dissolved in toluene[J]. Solvent Extraction and Ion Exchange, 1992, 10(4): 623-635.
[20] Zhang P W, Inoue K, Yoshizuka K, et al. Extraction and selective stripping of molybdenum(��) and vanadium(��) from sulfuric acid solution containing aluminum(��), cobalt(��), nickel(��) and iron(��) by LIX63 in Exxsol D80[J]. Hydrometallurgy, 1996, 41(1): 45-53.
[21] Jeong J, Kim M S. Recovery of H2SO4 from waste acid solution by a diffusion dialysis method[J]. Journal of Hazardous Materials, 2005, 124(1/3): 230-232.
�ո����ڣ�2009-08-18�������ڣ�2009-11-04
������Ŀ�����Ҹ����о���չ�ƻ�(��863���ƻ�)��Ŀ(2006AA06Z130)������ʡ�Ƽ���֧����Ŀ(2007GA010)������������ѧ���㲩ʿѧλ������������������Ŀ(2008��)
ͨ�����ߣ�κ��(1962-)���У����������ˣ����ڣ���ʿ�о�����ʦ������ʪ��ұ���о����绰��0871-5188819��E-mail: weichang2008@sina.com
(�༭ �°���)