DOI: 10.11817/j.ysxb.1004.0609.2020-39554
�������̿�ֽ����������̼�����ѧ
�� �֣��� �֣��� �ɣ�Ҧ ¶�����ľ٣��� ϼ
(�Ĵ���ѧ �����뻷��ѧԺ �����������̼����о����ģ��ɶ� 610065)
ժ Ҫ�������̿�������һ�����ʹ�����Ⱦ����Эͬ����Դ��������������������г�����MnSO4�⣬�������ɸ�����MnS2O6��Ӱ������Һ����Դ�����á�������MnO2��Ϊԭ�ϣ��о��������̽��е�Ũ��MnS2O6��ǿ���ֽ���̣�������MnS2O6Ũ�ȡ���Ӧʱ�䡢��Ӧ�¶ȡ�����Ũ�Ⱥ��̿�Ͷ�����ȹؼ���Ӧ������MnS2O6�ֽ��Ӱ�졣����MnO2��ǿ�������ֽ�MnS2O6�����˶���ѧ���������������MnO2��ǿ�������ֽ�MnS2O6�ı��۷�Ӧ����Ϊ2����Ӧ���Ϊ74.8 kJ/mol�����ڻ�ѧ��Ӧ���ƹ��̡�
�ؼ��ʣ��̿���������������(MnS2O6)��MnO2�������ֽ⣻����ѧ
���±�ţ�1004-0609(2020)-10-2475-07���� ��ͼ����ţ�X506��TQ031.7���� ���ױ�־�룺A
�����������ڴ�����Ⱦ���Ƶ������̿����������Դ�������õ��˿��ٷ�չ[1-4]������Ҫ������������SO2��MnO2ͨ��������ԭ��Ӧ����MnSO4��ʵ��������SO2���ѳ���ͬʱ��ʵ���̿��������ֵĽ�������Ӧ������ʽ(1)��(2)��ʾ��Ȼ���������̿�����Ӧ���̽�����һ��������ĸ���������������(MnS2O6)(��ʽ(3))��
MnO2+SO2��MnSO4 (1)
SO2+0.5O2+H2O��H2SO4 (2)
MnO2+2SO2��MnS2O6 (3)
����Һ��MnS2O6�Ĵ��ڶ�����Һ����Դ�����þ��о��Ӱ�죬�����������̲�Ʒʱ���ᾧ�����Ʒ�����²�Ʒ���Ƚ��͡�����ɫ�ȱ����������⡣����������������������ʱ��MnS2O6�Ĵ��ڶԵ���ϰ�����������ã��о������������Һ��MnS2O6��Ũ�ȸ���5 g/Lʱ����ʵ�ֵ���ϰ�[5-6]����ˣ����������̿�����Һ��MnS2O6Ũ�ȶ�����Һ����Դ������������Ҫ��
MnS2O6�����������SO2�IJ���ȫ�����������һ���Ļ�ѧ���ȶ��ԣ���ǿ������������MnS2O6����ͨ���绯��Ӧ�ֽ�ΪMnSO4��SO2��
MnS2O6��MnSO4+SO2 (4)
���о�����[7]�����������Ҳ�ɱ�ֱ��������������(��ʽ(5))��
MnS2O6+H2O+Oxidant��MnSO4+H2SO4 (5)
��ά���[7]�����̿�����ͬ����������βҺ�����������̷ֽ����Խ������о������������MnS2O6�ֽ�������H2SO4Ũ�ȡ�MnS2O6Ũ�Ⱥ��¶ȵ����߶�������MnSO4Ũ�ȵ��������С�����ǣ����о���ʹ�õ��Ǹ߳�ʼŨ��MnS2O6(Լ34 g/L)����Һ��������MnS2O6��ʼŨ�Ƚϵ�(��10 g/L)�������μӿ�MnS2O6�����ֽⲢʵ�������ȥ�����о����ʼ�������
MnO2��������һ����������������������ȻMnO2���ڸ�Ч����ȥ��MnS2O6��������ؽ��ͼ����ɱ���Ȼ����Ŀǰ����MnO2���ر��ǹ��ں�MnO2������MnS2O6���о�����[8-9]���йض���ѧ���о��Ծ��ѷ�����ˣ����о�����ȻMnO2��Ϊ��������ϵͳ�о���MnS2O6��ͬ��ʼŨ�ȡ���Ӧ�¶ȡ���Ӧʱ�䡢����Ũ�ȺͿ��Ͷ�����ȹ��ղ�����MnO2�����ֽ�MnS2O6���ܵ�Ӱ�죬���Ը÷�Ӧ���̵ķ�Ӧ����ѧ������ȫ�����������Ϊ�����̿��������Ĺ��̻��ƹ�Ӧ���ṩ����֧�֡�
1 ʵ��
1.1 ��Ҫ���ϡ��Լ�������
��Ҫ���ϡ��Լ�����MnS2O6���̿�����Һ���ɿ������Խ����̽�������������ϵͳ�Ƶá���������MnO2����Լ�������ɷַ������������ȫ�̺���Ϊ40.35%�����������Ҫ�Ԧ�-MnO2��̬���ڡ�ʵ��������õ���H2SO4��I2��Na2S2O3��5H2O��MnSO4��H2O��CH3COOH�Լ���Ϊ���������ɳɶ�������ѧƷ����˾������ʹ��ǰ������ǰ������ʵ���о����������豸��Ҫ��AUY120�ͷ�����ƽ��DL-101S�ͼ���ʽ���¼��ȴ�����������DL-1�͵�������¯��G-100S�ͳ�������ϴ����
1.2 ʵ�鷽��
1.2.1 MnS2O6�ֽ�
��������Һ��MnS2O6��ʼŨ�ȴ���15000 mg/L��ʵ��ʱͨ��ϡ�ʹ����õ��趨Ũ�ȵĺ�MnS2O6����Һ��Ϊ��֤��Һ����ͳһ��ϡ�ͺ�Һͨ������MnSO4��H2O����Mn2+Ũ��һ�£�ϡ�������ڵ��ڽ�ҺpH��
ȡ50 mL��MnS2O6����Һ����100 mL��ƿ�У�Ȼ�����һ���������ᣬ������Ⱥ���ƿѸ��ת���������������ˮԡ�С�Ѹ�ټ���ָ������MnO2��Ȼ���ܷ⣬�ں���ˮԡ��200 r/min�������������·�Ӧ����Ӧһ��ʱ���ȡ������ӦҺ�����ˣ��ⶨ��Һ��MnS2O6��ʣ��Ũ�ȡ�MnS2O6�ֽ��ʰ�ʽ(6)��ʾ���м��㣺
 (6)
(6)
ʽ�У� ΪMnS2O6�ķֽ���(%)��
ΪMnS2O6�ķֽ���(%)�� ��
�� ΪMnS2O6�ij�ʼ��ʣ��Ũ��(mg/L)��
ΪMnS2O6�ij�ʼ��ʣ��Ũ��(mg/L)��
1.2.2 MnS2O6Ũ�Ȳⶨ
��������-�������ⶨ��Ʒ��MnS2O6Ũ��[10]������Ϊ��������Ʒ���������ȣ���Ʒ��MnS2O6���ȷֽ�����SO2����N2Ϊ��������ҺΪ����Һ������Ϊָʾ����������Ʒ�ֽ������SO2������Һ��Na2S2O3����Һ�ζ���ͬʱ���հ���ʵ�顣MnS2O6��Ũ�ȼ�����ʽ(7)��ʾ��
 (7)
(7)
ʽ�У� ΪMnS2O6Ũ��(mg/L)��VΪ����������ƿ�е�����(mL)��
ΪMnS2O6Ũ��(mg/L)��VΪ����������ƿ�е�����(mL)��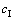 �����ҺŨ��(mol/L)��V0Ϊ�հ���������������Ʊ���Һ(mL)��V1Ϊ��Ʒ�ζ���������Ʊ���Һ���(mL)��cΪ��������Ʊ���ҺŨ��(mol/L)��VrΪ��ӦҺȡ�����(mL)��
�����ҺŨ��(mol/L)��V0Ϊ�հ���������������Ʊ���Һ(mL)��V1Ϊ��Ʒ�ζ���������Ʊ���Һ���(mL)��cΪ��������Ʊ���ҺŨ��(mol/L)��VrΪ��ӦҺȡ�����(mL)��
2 ���������
2.1 MnO2��ֽ�MnS2O6�����о�
2.1.1 ��ʼŨ�ȶ�MnS2O6�ֽ��Ӱ��
���Ƴ�ʼŨ�ȷֱ�Ϊ4000��6000��8000��10000��12000 mg/L�ĺ�MnS2O6������Һ���ֱ�ȡ50 mL��100 mL��ƿ��Ȼ�����μ���10.0 g��MnO2������Ũ��Ϊ1.4 mol/L����90 ����������·�Ӧ����ͬMnS2O6��ʼŨ����MnS2O6ʣ��Ũ����ʱ��ı仯��ͼ1��ʾ��

ͼ1 ��ͬ��ʼŨ����MnS2O6Ũ����ʱ��ı仯���
Fig. 1 MnS2O6 concentration varied with reaction time under different initial concentrations of MnS2O6
��ͼ1��֪���ڲ�ͬ��ʼŨ���£�MnS2O6���ֳ�����ķֽ��ѧ��Ϊ���ڳ�ʼ��30 min�ڷ�Ӧ���ʽϿ죬MnS2O6Ũ��Ѹ�ٽ��ͣ�Ȼ�����ŷ�Ӧʱ����ӳ�������������Ϊ���ŷ�Ӧ���̵ij�������Һ��H+�����Ļ�Ӱ���̿����ĵ縺��[11]��MnS2O6�������ֽ����ʼ���������MnS2O6��ʼŨ�ȵ�����MnS2O6�ķֽ�Ч�����ͣ���MnS2O6�ľ�������ȥ���������ߡ�������Ϊ��Ũ�������·�Ӧ�Ĵ��ʶ����������MnS2O6���ӿ��Բ��뵽�ֽⷴӦ�С����ֽ��ʵĽ�����Ҫ��������������Ӧ������ͬ�������£���ʼ��Ӧ����������������Ч���뷴Ӧ�IJ��֡�
2.1.2 ����Ũ�ȶ�MnS2O6�ֽ��Ӱ��
����MnS2O6��ʼŨ��Ϊ8000 mg/L�ĺ�MnS2O6������Һ���ֱ�ȡ50 mL��100 mL��ƿ�в�����10.0 g��MnO2��Ȼ��ֱ����1.0��1.2��1.4��1.6��1.8 mol/L�����ᣬ��90 ����·�Ӧ����ͬ����Ũ����MnS2O6Ũ����ʱ��ı仯��ͼ2��ʾ����������Ũ�ȵ�����MnS2O6�ķֽ��������ߣ�������Ũ����1.0 mol/L������1.8 mol/Lʱ��MnS2O6�ķֽ�����56.7%������82.9%��������ΪMnO2��������������ҺpHֵ������أ�����Ũ������ʹMnO2�ı�������������ǿ������ǿ����MnS2O6�����ֽ�[11-12]��ͬʱ����pH��Ӧ�����»�����Ч����MnS2O6���Էֽ���̣���;�����MnS2O6�������ֽ����ʡ�
2.1.3 ��Ӧ�¶ȶ�MnS2O6�ֽ��Ӱ��
����MnS2O6��ʼŨ��Ϊ8000 mg/L�ĺ�MnS2O6������Һ���ֱ�ȡ50 mL��100 mL��ƿ�У�����10.0 gMnO2���1.4 mol/L���ᣬ��60��70��80��90��100 ����ºʹ��������·�Ӧ����ͬ��Ӧ�¶���MnS2O6ʣ��Ũ����ʱ��ı仯��ͼ3��ʾ����ͼ3��֪�����ŷ�Ӧ�¶ȵ����ߣ�MnS2O6��ʣ��Ũ�����½������¶ȵ���80 ��ʱ��MnS2O6�ķֽ������淴Ӧ�¶ȵ����߱仯����������Ӧ�¶ȸ���80 ��ʱ��MnS2O6�ֽ����ʿ������ߡ�������ΪMnS2O6�ķֽ���һ�����ȷ�Ӧ�������¶������ڼ���MnS2O6�ķֽ⡣���⣬�ϸߵķ�Ӧ�¶�Ҳ������ǿ��MnO2������Ӧ���̺ͷ�Ӧ����[11]�����߹�ͬ����ʵ��MnS2O6�ֽ�Ч�ʵ�������

ͼ2 ��ͬ����Ũ����MnS2O6Ũ����ʱ��ı仯���
Fig. 2 MnS2O6 concentration varied with reaction time under different H2SO4 contents

ͼ3 ��ͬ�¶���MnS2O6Ũ����ʱ��ı仯���
Fig. 3 MnS2O6 concentration varied with reaction time at different temperatures
2.1.4 MnO2��Ͷ������MnS2O6�ֽ��Ӱ��
����MnS2O6��ʼŨ��Ϊ8000 mg/L�ĺ�MnS2O6������Һ��ȡ50 mL����100 mL��ƿ�У��ֱ����0��5.0��7.5��10.0��12.5��15.0 g��MnO2��Ȼ���ټ���1.8 mol/L��Ũ���ᣬ��90 ����£��������跴Ӧ����ͬMnO2��Ͷ����ʱMnS2O6��ʣ��Ũ����ʱ��ı仯��ͼ4��ʾ����ͼ4��֪����Ͷ��MnO2��ʱMnS2O6�ķֽ���ֻ��55.5%������MnO2��Ͷ���������ӣ�MnS2O6�ķֽ���Ҳ���������ƣ���MnO2���Ͷ������MnS2O6�ķֽ�����Ӱ���Ϊ������Ͷ��������10 g��MnS2O6�ķֽ�����80.0%�������ֲ��䡣MnO2��Ͷ������Ӱ���С��������Ͷ��������Զ����������Ҫ������ʱMnS2O6�ķֽ����Ϊ��ѧ��Ӧ���ƣ���ˣ�����MnO2���Ͷ������MnS2O6��Ӱ���Ϊ����

ͼ4 ��ͬMnO2��Ͷ����MnS2O6Ũ����ʱ��ı仯
Fig. 4 MnS2O6 concentration varied with reaction time under different MnO2 ore dosages
2.2 MnS2O6�ֽ��ѧ�о�
2.2.1 ����ѧģ��
��Ӧ����ѧ�����˷�Ӧ�����з�Ӧ��ķ�Ӧ���ʣ���һ���ʾ����˹���Ӧ��ʱ��Ӧװ�õ�ͣ��ʱ����豸�ߴ磬���ڴ��ģ���������Ҫ��ʵ�����塣Ϊ���õ��˽�MnO2��ֽ�MnS2O6��Ӧ�����Լ�MnS2O6��ʼŨ�ȡ�����Ũ�ȡ�MnO2��Ͷ�������¶ȵ����ضԷ�Ӧ���ʵ�Ӱ�죬��Ӧ����ѧ�о�������Ҫ��
MnO2��ֽ�MnS2O6�ķ�Ӧ���ʷ��̿�����ָ������ģ�ͱ�ʾ��
 (8)
(8)
ʽ�У�tΪ��Ӧʱ��(min)�� ΪMnS2O6��Ũ��(mg/L)��k1Ϊ��Ӧ���ʳ�����nΪMnS2O6�ı��ַ�Ӧ������
ΪMnS2O6��Ũ��(mg/L)��k1Ϊ��Ӧ���ʳ�����nΪMnS2O6�ı��ַ�Ӧ������
����MnS2O6�ĺ����仯�ܵ�������Ӧ������Ӱ�죬��ʽ(8)���Ը�дΪ��ʽ(9)����ʽ[13-14]��
 (9)
(9)
����
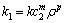 (10)
(10)
ʽ�У� Ϊ����Ũ��(mol/L)��
Ϊ����Ũ��(mol/L)�� ΪMnO2��Ͷ����(g/L)��mΪ����ı��ַ�Ӧ������pΪMnO2�ı��ַ�Ӧ������
ΪMnO2��Ͷ����(g/L)��mΪ����ı��ַ�Ӧ������pΪMnO2�ı��ַ�Ӧ������
2.2.2 �ֽ��ѧ�о�

ͼ5 ��ͬMnS2O6Ũ����MnS2O6�ķֽ��ѧ
Fig. 5 MnS2O6 decomposition kinetics at different initial MnS2O6 concentrations
��1 ��ͬMnS2O6��ʼŨ����MnS2O6�ֽ��ѧ���ϵ��
Table 1 Kinetic correlation coefficient of MnS2O6 decomposition under different initial concentrations

����ʽ(8)��������С���˷���ϴ���ͼ1��ʾ���ݣ������ͼ5��ʾ�����ϵ������1����n=2ʱ��ʽ(8)���ԽϺõ�������ͬMnS2O6��ʼŨ����MnS2O6�ֽ������ (
( ��ʾMnS2O6��ʼŨ��)��t���ԽϺá���n=2����ʽ(9)���ֿ��Եõ�
��ʾMnS2O6��ʼŨ��)��t���ԽϺá���n=2����ʽ(9)���ֿ��Եõ�
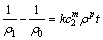 (11)
(11)
����ʽ(11)�Բ�ͬ����Ũ����MnS2O6�ķֽ������д����������ͼ6��ʾ�����ʳ����������ϵ������2����ͬ����Ũ���£� ��t���нϺõ���������ԣ���ʽ(10)����ȡ�����ɵ�
��t���нϺõ���������ԣ���ʽ(10)����ȡ�����ɵ�
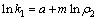 (12)
(12)
��ʽ(12)�Բ�ͬ����Ũ���µ����ʳ���k1���д������ó����ϵʽΪ
 (13)
(13)

ͼ6 ��ͬ����Ũ����MnS2O6�ķֽ��ѧ
Fig. 6 Decomposition kinetics of MnS2O6 at different H2SO4 contents
��2 ��ͬ����Ũ����MnS2O6�ֽ��ѧ�����ʳ��������ϵ��
Table 2 Rate constants and kinetics correlation coefficients of MnS2O6 decomposition under different acid contents

��ˣ��õ����������̷ֽⷴӦ����ѧ����ʽ������ı��۷�Ӧ����Ϊ1.89��
�Բ�ͬMnO2��Ͷ����ʵ������ʽ(11)�����������ͼ7��ʾ�����ʳ��������ϵ������3���ڲ�ͬMnO2��Ͷ���£� ��t��������ԽϺã���ʽ(10)ȡ�����ɵ�
��t��������ԽϺã���ʽ(10)ȡ�����ɵ�
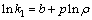 (14)
(14)
����ʽ(14)�Բ�ͬMnO2��Ͷ�����µ����ʳ���k1���д����õ����ϵʽΪ
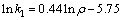 (15)
(15)
�ɴ˿ɵö���ѧ����ʽ��MnO2��ı��۷�Ӧ����Ϊ0.44��

ͼ7 ��ͬMnO2��Ͷ������MnS2O6�ķֽ��ѧ
Fig. 7 Decomposition kinetics of MnS2O6 with different MnO2 ore dosages
��3 ��ͬMnO2��Ͷ������MnS2O6�ֽ��ѧ�����ʳ��������ϵ��
Table 3 Rate constants and correlation coefficients of decomposition kinetics of MnS2O6 under different MnO2 ore dosages
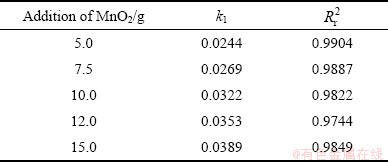
�Բ�ͬ�¶���MnS2O6�ķֽ�����ʽ(11)������������ͼ8��ʾ�����ʳ��������ϵ������4����ͬ�¶��� ��t��������ԽϺã����ʳ���k1Ϊ0.0016(60 ��)��0.0030(70 ��)��0.0042(80 ��)��0.0143(90 ��)��0.0278(100 ��)�����ݰ�������˹����ʽ��
��t��������ԽϺã����ʳ���k1Ϊ0.0016(60 ��)��0.0030(70 ��)��0.0042(80 ��)��0.0143(90 ��)��0.0278(100 ��)�����ݰ�������˹����ʽ��
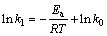 (16)
(16)
ʽ�У�EaΪ��Ӧ���ۻ��(kJ/mol)��RΪĦ�����峣��(8.314 J/(mol��K))��TΪ��Ӧ�¶�(K)��
����ʽ(16)�Բ�ͬ�¶��µ����ʳ���k1���д����ó������Թ�ϵʽΪ
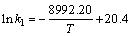 (17)
(17)
�Ƚ�ʽ(16)��ʽ(17)���������MnO2��ֽ�MnS2O6�ķ�Ӧ���Ϊ74.8 kJ/mol�����о�֤������Ӧ���ӵ���ɢ���С��20.0 kJ/mol��������ײ���л�ѧ��Ӧ�Ļ��һ����40~400 kJ/mol֮��[15]���ɴ�˵��MnO2���MnS2O6�ķֽ����ڻ�ѧ��Ӧ���ƣ��¶�����ٽ�MnO2����MnS2O6�ķ�Ӧ��

ͼ8 ��ͬ�¶���MnS2O6�ķֽ��ѧ
Fig. 8 Decomposition kinetics of MnS2O6 at different temperatures
��4 ��ͬ�¶���MnS2O6�ֽ��ѧ�����ʳ��������ϵ��
Table 4 Rate constants and kinetics correlation coefficients of MnS2O6 decomposition at different temperatures

3 ����
1) ��MnS2O6��ʼŨ�Ƚϵ������£���߷�Ӧ�¶ȡ�����Ũ���Լ�һ����Χ������MnO2��Ͷ�������ɼӿ�MnS2O6�������ֽ⣬���MnS2O6Ũ�ȷֽ��ʽ��͡�
2) MnO2��ǿ�������ֽ��У�MnS2O6�ı��ּ���Ϊ2����Ӧ���Ϊ74.8 kJ/mol�����ڻ�ѧ��Ӧ���ƹ��̡�����ʵ���п�ͨ������Һ�������Ũ�ȡ������Լ�Ͷ��һ������MnO2�����ʵ���̿�����������нϵ�Ũ��MnS2O6��ȥ����
REFERENCES
[1] ������, ���ľ�. ���̿��ѳ�������SO2���о���չ[J]. �й���ҵ, 2001, 19(2): 10-12.
ZHU Xiao-fan, JIANG Wen-ju. Process and study on removal of SO2 in flue gas with pytolusite[J]. China��s Manganeses Industry, 2001, 19(2): 10-12.
[2] SUN Wei-yi, DING Sang-lan, ZENG Shan-shan, SU Shi-jun, JIANG Wen-ju. Simultaneous absorption of NOx and SO2 from flue gas with pyrolusite slurry combined with gas-phase oxidation of NO using ozone[J]. Journal of hazardous materials, 2011, 192(1): 124-130.
[3] SUN Wei-yi, SU Shi-jun, WANG Qing-yuan, DING Sang-lan. Lab-scale circulation process of electrolytic manganese production with low-grade pyrolusite leaching by SO2[J]. Hydrometallurgy, 2013, 133: 118-125.
[4] QU Bing, HU Wen-li, DENG Lin, SUN Wei-yi, DING Sang-lan, GAN Zhi-wei, SU Shi-jun. Simultaneous determination of dithionate and sulfate in leaching solution from SO2-leaching pyrolusite by ion chromatography[J]. Energy &Fuels, 2016, 30(10): 8561-8566.
[5] WARD C B. Hydrometallurgical processing of manganese containing materials: The United States, US7951282[P]. 2011-05-19.
[6] YOU Zhi-xiong, LI Guang-hui, ZHANG Yuan-bo, PENG Zhi-wei, JIANG Tao. Extraction of manganese from iron rich MnO2 ores via selective sulfation roasting with SO2 followed by water leaching[J]. Hydrometallurgy, 2015, 156: 225-231.
[7] ��ά��, ���˾�, ��ɣ�, ���ľ�, �� Ө. ���̿�����ͬ����������βҺ�����������̷ֽ����Ե��о�[J]. �Ĵ���ѧѧ��(���̿�ѧ��), 2011, 43(3):166-170.
SUN Wei-yi, SU Shi-jun, DING San-lan, JIANG Wen-ju, XU Ying. Study on the decomposition characteristics of MnS2O6 in the tail liquid of simultaneous desulfurization and denitrification of soft manganese pulp flue gas[J]. Journal of Sichuan University (Engineering Science), 2011, 43(3): 166-170.
[8] QU Bing, DENG Lin, DENG Biao, HE Ke-jie, LIAO Bing, SU Shi-jun. Oxidation kinetics of dithionate compound in the leaching process of manganese dioxide with manganese dithionate[J]. Reaction Kinetics, Mechanisms and Catalysis, 2018, 123(2): 743-755.
[9] �½�ΰ, ͯ�ŷ�, ��־��, �ߴ���. ��MnSO4��Һ��MnS2O6��ȥ�������о�[J]. ��������ѧ��, 2011(1): 177-180.
CHEN Jian-wei, TONG Zhang-fa, CHEN Zhi-chuan, GAO Da-ming. Study on conditions for removing MnS2O6 from MnSO4 solution[J]. Chinese Journal of Environmental Engineering, 2011(1): 177-180.
[10] SOFFER N. The determination of dithionate, sulphite and sulphate in manganese leach liquors[J]. Analyst, 1961, 86(1029): 843-849.
[11] ������. �������̿�ʯ����������ˮʵ���о�[D]. �Ϸ�: �Ϸʹ�ҵ��ѧ, 2007.
SONG Yin-xian. Study on oxidation of coking wastewater by manganese oxide mineral[D]. Hefei: Hefei University of Technology, 2007.
[12] FURLANI, PAGNANELLI. Reductive acid leaching of manganese dioxide with glucose: Identification of oxidation derivatives of glucose[J]. Hydrometallurgy, 2006, 81(3): 234-240.
[13] �����, ������, ������, ������, �����, ŷ������, �ں���. �������������̿���������еķֽ��ѧ[J]. �й���ɫ����ѧ��, 2016, 26(6): 1303-1310.
WANG Yu-hong, LEI Zuo-min, QU Xin-ke, HUANG Li-ying, HOU Jia-min, OUYANG Qiu-lin, LI Hai-feng. Oxidative breakdown kinetics of glucose in process of leaching manganese oxide ore[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(6): 1303-1310.
[14] �ބ���. ���̿��������⽹��ɫ�ط�Ӧ���̵��о�[D]. ����: ������ѧ, 2009.
CUI Qing-yan. Study on reaction process of caramel oxidative degradation using pyrolusite as a oxidant[D]. Nanning: Guangxi University, 2009.
[15] ������, ���ӿ�, �� ��. ������ѧ:����ѧ���绯ѧ�����漰���廯ѧ[M]. �人: �人��ѧ������, 2003.
LIN Zhi-xin, AN Cong-jun, LIU Yi. Physical chemistry: Kinetics, electrochemistry, surface and colloidal chemistry[M]. Wuhan: Wuhan University Press, 2003.
Decomposition of manganous dithionate with natural MnO2 ore and kinetics study
DING Lin, YANG Lin, WANG Cheng, YAO Lu, JIANG Wen-ju, JIANG Xia
(College of Architecture and Environment, National Engineering Research Center for Flue Gas Desulfurization, Sichuan University, Chengdu 610065, China)
Abstract: Manganese oxide desulfurization is a new desulfurization technology and coupled with the resource utilization of sulfur simultaneous. However, the desulfurization process has an inevitable byproduct, the manganese dithionate (MnS2O6), which affect the following resource utilization. In this study, the natural manganese oxide ore (��-MnO2) strengthened low concentration MnS2O6 decomposition was carefully studied. The effects of operation conditions, including the original MnS2O6 concentration, reaction time, temperature, slurry acidity and manganese ore addition on decomposition of MnS2O6 were discussed, and the kinetics was also analyzed based on these results. The results show that the apparent reaction order of MnS2O6 with natural MnO2 ore is 2, and the activation energy is 74.8 kJ/mol, which is a typically chemical reaction control process.
Key words: manganese oxide ore desulfurization; manganese dithionate (MnS2O6); natural MnO2 ore; oxidation decomposition; kinetics
Foundation item: Project(2018YFC0213405) supported by the National Key Research and Development Program of China
Received date: 2019-09-20; Accepted date: 2020-07-20
Corresponding author: YANG Lin; Tel: +86-28-85403016; E-mail: andyyiyin@scu.edu.cn, evanlinyang@sina.com
(�༭ ������)
������Ŀ�������ص��з��ƻ�������Ŀ(2018YFC0213405)
�ո����ڣ�2019-09-20�������ڣ�2020-07-20
ͨ�����ߣ��� �֣����о�Ա����ʿ���绰��028-85403016��E-mail��andyyiyin@scu.edu.cn, evanlinyang@sina.com